





2022版《导与练》高考化学二轮复习 区间六 电解质溶液课件PPT
展开
这是一份2022版《导与练》高考化学二轮复习 区间六 电解质溶液课件PPT,共54页。PPT课件主要包含了命题点1,水的电离与溶液酸碱性,命题点2,命题点3,命题点4,命题点5,考情分析与预测,知能点1,知能点2,知能点3等内容,欢迎下载使用。
NO.1 “品”高考考情——考什么?怎么考?精准备考!
2.(2021·浙江6月选考,19)某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。下列说法正确的是( )A.25 ℃时,若测得0.01 ml·L-1 NaR溶液pH=7,则HR是弱酸B.25 ℃时,若测得0.01 ml·L-1 HR溶液pH>2且 pHc(X-)>c(OH-)>c(H+)B.三种一元弱酸的电离常数:Ka(HX)>Ka(HY)>Ka(HZ)C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
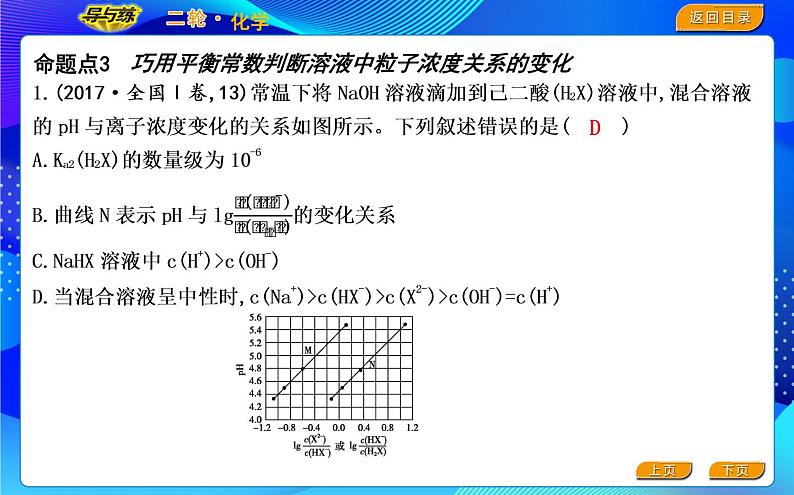
巧用平衡常数判断溶液中粒子浓度关系的变化
结合图像判断溶液中粒子浓度的关系
2.(2019·全国Ⅰ卷,11)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10-3 ,Ka2=3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2-的导电能力之和大于HA-的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
沉淀溶解平衡的图像分析及其计算
1.(2021·全国乙卷,13)HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水解。实验发现,298 K时c2(M+)~c(H+)为线性关系,如下图中实线所示。下列叙述错误的是( )A.溶液pH=4时,c(M+)c(R+)或c(Y+)+c(R+)=c(Z-)+c(X-)的选项,前者一般属于离子浓度大小比较类题型,可以根据水解程度、电离程度相对大小解决,有些也可以根据电荷守恒结合酸碱性分析,后者一般考查的是“三个守恒”。2.对于酸碱混合型(一弱一强)的离子浓度大小排序问题可用“三点分析法”进行分析。三点分别为:(1)半中点:一元酸、碱弱的一方反应掉50%或二元弱酸被中和掉50%。(2)中性点:溶液整体显中性时溶液中既有弱酸、碱剩余,又有生成的含弱离子的盐存在。
(3)中和点:酸、碱按照方程式化学计量数比恰好完全中和的点。例:CH3COOH与NaOH中和过程。
②中性点:因为显中性,所以有c(H+)=c(OH-),根据电荷守恒有c(CH3COO-)=c(Na+),同时中性溶液中常温下c(H+)=c(OH-)=10-7ml·L-1,浓度极低,所以最后排序为c(CH3COO-)=c(Na+)>c(H+)=c(OH-)。
③中和点:是醋酸被完全中和的点,此时溶液是CH3COONa溶液,由于CH3COO-水解,所以有c(Na+)>c(CH3COO-),由于水解显碱性,所以有 c(OH-)>c(H+),由于醋酸根水解程度较小,所以有c(CH3COO-)>c(OH-),最终排序为c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。一般题目经常考的就是这几个点的粒子浓度比较,其他点较少考查,如有考查可以根据上述三点综合分析。注意:二元弱酸与一元强碱反应可以根据“一级中和点”“二级中和点”类似进行分析,比如H2C2O4与NaOH反应,一级中和时溶质为NaHC2O4,二级中和时溶质为Na2C2O4。再如二元弱酸正盐与一元强酸反应可以根据“一级反应点”“二级反应点”类似分析,比如Na2C2O4与HCl反应,一级反应点溶质为NaHC2O4和NaCl(1∶1),二级反应点溶质为H2C2O4和NaCl(1∶2)等等。
3.电解质溶液类题目涉及图像坐标为对数时:要“化对为指”,即把对数(或负对数)坐标化为指数坐标来考虑,要注意负对数化为指数坐标后,沿坐标轴方向坐标值是减小的。例:(2018·全国Ⅲ卷,12)如图1是原题图像,如图2是“化对为指”后图像
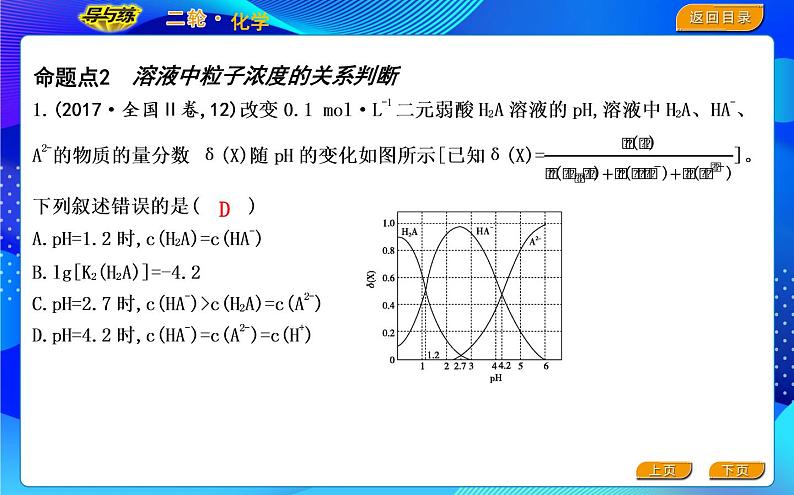
4.电解质溶液类题目涉及K计算的图像通常均根据“交点”或“有坐标值的点”进行计算:例(2017·全国Ⅱ卷,12)
NO.3 “练”关键能力——考什么,练什么,实现精练!
1.(2021·浙江高三模拟)25 ℃时,下列说法正确的是( )A.H2A溶液与NaOH溶液按物质的量1∶1恰好完全反应时,溶液酸碱性无法判断B.可溶性正盐BA溶液呈中性,可以推测BA对水的电离没有影响C.醋酸的电离度:pH=3的醋酸溶液大于pH=4的醋酸溶液D.pH=2的HCl和pH=12的Ba(OH)2溶液等体积混合后,溶液显碱性
解析 H2A溶液与NaOH溶液按物质的量1∶1恰好完全反应后,生成的是NaHA,但是H2A的电离常数不知道,所以该溶液酸碱性无法判断,A正确;可溶性正盐BA溶液呈中性,只能说明HA和BOH的电离常数相同,但是如果都是弱酸、弱碱,且电离常数相同,则BA的阴、阳离子水解程度相同,促进水的电离,B错误;醋酸是弱电解质,稀释促进电离,稀释后溶液的pH增大,pH越大说明越稀,醋酸的电离程度越大,C错误;pH=2的HCl和pH=12的Ba(OH)2 溶液中,氢离子和氢氧根离子浓度相同,等体积混合后,溶液显中性,D错误。
2.(2021·天津南开中学高三三模)常温下,下列说法正确的是( )
溶液中粒子浓度关系判断
[思维建模] 此类题解题模式是①读图:如果有对数或负对数,则需要“化对为指”;若有倒数坐标,则把坐标“正过来”;②分析各选项内容:若为离子浓度大小比较类型选项,则首先分析溶液成分,然后根据电离、水解程度以及“三个守恒规律”进行分析;若为涉及K的计算,通常根据图像中“交点”或“有坐标值的点”来进行计算;若涉及“中和反应问题或数量级计算问题”,则根据上述“知能点4”技巧进行分析。
相关课件
这是一份高考化学二轮复习专题7电解质溶液(含解析)课件PPT,共60页。PPT课件主要包含了对点集训,电解质溶液图像分析等内容,欢迎下载使用。
这是一份2022版《导与练》高考化学二轮复习 区间一 化学与STSE 化学与传统文化课件PPT,共52页。PPT课件主要包含了考情纵览按图索题,命题点1,社会环境,命题点2,化学与生产生活,命题点3,化学与传统文化,考情分析与预测,知能点1,传统文化与化学史等内容,欢迎下载使用。
这是一份2022版《导与练》高考化学二轮复习 区间五 电化学课件PPT,共58页。PPT课件主要包含了命题点1,新型化学电源,命题点2,命题点3,命题点4,命题点5,金属的腐蚀与防护,命题点6,考情分析与预测,知能点1等内容,欢迎下载使用。








