





2022年高考总复习 化学 模块1 第三单元 第1节 原子结构 元素周期表课件PPT
展开
这是一份2022年高考总复习 化学 模块1 第三单元 第1节 原子结构 元素周期表课件PPT,共58页。PPT课件主要包含了半导体等内容,欢迎下载使用。
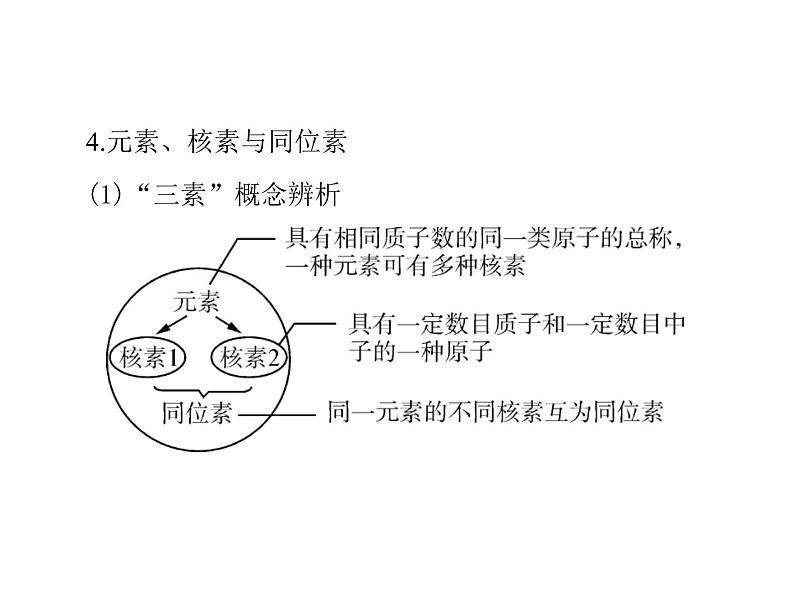
考点一1.构成原子的微粒及作用
(1)原子中:质子数(Z)=核电荷数=__________;(2)质量数(A)=________(Z)+________(N);(3)阳离子的核外电子数=质子数-__________;(4)阴离子的核外电子数=质子数+__________。
4.元素、核素与同位素(1)“三素”概念辨析
(2)同位素的特征①相同存在形态的同位素,化学性质________________,
物理性质______。
②天然存在的同一元素各核素所占的原子百分数一般
(3)常见的重要核素及其应用
[ 自主测评 ]1.易错易混辨析(正确的画“√”,错误的画“×”)。(1)一种元素可以有多种核素,也可能只有一种核素,有多
少种核素就有多少种原子(
(4)一种核素只有一种质量数(
(5)质量数就是元素的相对原子质量(
(6)质子数相同的微粒不一定都属于同一种元素(
(5)× (6)√
2.【深度思考】H、D、T 形成的氢气分子有____________;H、D、T 与 16O、17O 可形成的水分子有______种;其中相对分子质量相同的有__________________;这些水分子的物理性质____;化学性质______________________________。
以同位素为核心的概念辨析
1.(2020年石家庄模拟)230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是( ) A.Th元素的质量数是232 B.Th元素的相对原子质量是231 C.232Th转化成233U是化学变化 D.230Th和232Th的化学性质相同
解析:Th有质量数为230、232的两种同位素,因此无法确定Th的质量数,A错误;不知230Th与232Th的丰度,无法确定Th的相对原子质量,B错误;化学变化过程中原子种类不变,而232Th转化为233U是原子种类发生变化,C错误;230Th与232Th互为同位素,二者化学性质相同,D正确。
解析:A 正确;同位素是同种元素不同种原子间互称,B正确;同素异形体是同一元素的不同单质,C 错误;D 正确,相对分子质量都是 20。答案:C
(1)同位素的“六同三不同”
原子中各种微粒数目之间的关系及计算
3.(2020 年扬州模拟)科学家制造出的第 112 号元素 ,其原
子的质量数为 277。关于该元素的下列叙述中正确的是(A.其原子核内中子数和质子数都是 112B.其原子核内中子数为 122,核外电子数为 112C.其原子质量是 12C 原子质量的 227 倍D.其原子质量与 12C 原子质量之比为 277∶12
解析:该原子的中子数为 277-112=165,A、B 错误;原子的质量之比等于其相对原子质量之比,约等于原子的质量数之比,C 错误,D 正确。
[归纳提升] 求一定质量的某物质中粒子数的思维模板
指定粒子的物质的量粒子数
2.原子或离子结构示意图
3.核外电子排布与元素性质的关系
(1)金属元素原子的最外层电子数一般小于 4,较易_______电子,形成阳离子,表现出__________性,在化合物中显正化
(2)非金属元素原子的最外层电子数一般大于或等于 4,较易________电子,活泼非金属原子易形成阴离子,在化合物中
(3)稀有气体元素的原子最外层为 8 电子(氦为 2 电子)稳定结构,不易失去或得到电子,通常表现为 0 价。
[ 自主测评 ]1.易错易混辨析(正确的画“√”,错误的画“×”)。(1)元素原子的多样性是由构成原子的质子和中子数目引
(2)元素的化学性质主要取决于元素原子的最外层电子数
(3)原子核外电子中,最外层上的电子能量最高((4)当最外层上的电子数变为 4 个时即达稳定结构(
(5)硫离子的结构示意图:
(6)117 号元素 Ts 的同位素原子具有相同的电子数(
答案:(1)a 为氢元素;b 为硫元素;c 为氯元素;d 为钾元
(2)a 为氢元素;b 为氧元素;c 为硫元素;d 为钙元素
1.(2020年鞍山模拟)短周期元素 X 和 Y,元素 X 原子的最外层电子数为 a,次外层电子数为 b;元素 Y 原子的 M 层电子数为(a-b),L 层电子数为(a+b)。则 X、Y 两元素形成的化合
物可能具有的性质是(A.和水反应C.和氢氧化钠反应
B.和硫酸反应D.和氯气反应
解析:根据 Y 原子的 L 层电子数为(a+b),M 层电子数为(a-b),知 a+b=8,再根据 X 原子次外层电子数为 b,可知 b=2,则 a=6,进而确定 X 为氧(O),Y 为硅(Si)。两元素形成SiO2,SiO2 为酸性氧化物,可与 NaOH 反应。
A.K+的结构示意图:
2.(2020 年山东三模)火药制备是我国古代闻名世界的化学工艺,原理为 2KNO3+S+3C===K2S+N2↑+3CO2↑。下列表
示反应中相关微粒的化学用语正确的是(B.K2S 的电子式:C.CO2 的结构式为:O==C==OD.16O2与18O3 互为同位素
解析:A 项,K 元素的核电荷数为19,质子数为19,核外电子数为 19,K+表示失去最外层一个电子,K+核外还有 18 个
电子,各层电子数分别为2、8、8,K+的结构示意图为
1~20 号元素原子核外电子排布的特点与规
(4)电子层数与最外层电子数相等的原子:H、Be、Al;最外层电子数是电子层数 2 倍的原子:He、C、S;最外层电子数是电子层数 3 倍的原子:O。
(5)次外层电子数是最外层电子数 2 倍的原子:Li、Si。(6)内层电子总数是最外层电子数 2 倍的原子:Li、P。
等电子粒子的判断和应用
4.(2019 年淄博模拟)已知 A、B、C、D 是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
(1)如果 A、B、C、D 均是 10 电子的粒子,请写出 A、D
的电子式:A______________;D______________。
(2)如果 A 和 C 是 18 电子的粒子,B 和 D 是 10 电子的粒
①A 与 B 在溶液中反应的离子方程式为 _________________________________________________________________。②根据上述离子方程式,可以判断 C 与 B 结合质子的能力大小是_________________(用化学式或离子符号表示)。
(2)①HS-+OH-===S2-+H2O或H2S+OH-===HS-+H2O ②OH->S2-或OH->HS-
(1)“10 电子”微粒
(2)“18 电子”微粒
(3)记忆其他等电子微粒
1.原子序数:按照元素在周期表中的顺序给元素编号,称之为________,__________=核电荷数=质子数=核外电子数。
(1)周期:把__________相同的元素,按______________的
顺序,从左至右排成的横行。
(2)族:把_____________相同的元素,按_____________的
顺序,从上至下排成的纵行。
4.元素周期表中的特殊位置
①分界线:沿着元素周期表中__________________与____________________的交界处画一条虚线,即为金属元素区
和非金属元素区的分界线。
②各区位置:分界线左下方为____________,分界线右上方为______________。③分界线附近元素的性质:既表现__________的性质,又
表现____________的性质。
(2)过渡元素:元素周期表中部从__________族 10 个纵列
共六十多种元素,这些元素都是金属元素。
(3)镧系:元素周期表第六周期中,57 号元素镧到 71 号元素镥共 15 种元素。(4)锕系:元素周期表第七周期中,89 号元素锕到 103 号元素铹共 15 种元素。(5)超铀元素:在锕系元素中 92 号元素铀(U)以后的各种元素。
5.元素周期表的三大应用(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供了线索。
探矿(地球化学元素的分布与它们在元素周期表中的位置
关系对其有指导意义)、研制农药材料等。
[ 自主测评 ]1.易错易混辨析(正确的画“√”,错误的画“×”)。(1)原子的电子层数一定等于周期数,原子的最外层电子数
(2)ⅠA 族全是碱金属,ⅦA 族全是非金属((3)元素周期表中的每一格均表示一种元素(
(4)原子的最外层有 1 个或 2 个电子,则可能是ⅠA、ⅡA
族元素,也可能是副族、Ⅷ族元素或 0 族元素氦(
(5)同一周期,ⅡA 族与ⅢA 族的原子序数差一定为 1(
(6)原子及离子的核外电子层数等于该元素所在的周期数
均表示了元素在元素周期表中的相应
(5)× (6)×
2.【深度思考】(2020 年南京月考)如图为元素周期表中五种元素的相对位置。若 B 的原子序数为 a,则这五种元素的核电荷数之和可能为________。
答案:5a 或 5a+10 或 5a+14
这两种元素的说法错误的是(
元素周期表的结构与位置推导
1.(2020 年正定模拟)国际理论与应用化学联合会已正式确定了第 114 号和第 116 号元素的名称缩写为 Fl、Lv。下列有关
A.两种元素位于同一周期B.116 号元素位于第ⅥA 族C.两种元素都是活泼的非金属元素D.114 号元素的原子半径比 116 号元素的原子半径大
解析:第 114 号元素和第 116 号元素分别处于第七周期ⅣA族和ⅥA 族,均为金属元素,A、B 正确,C 错误;依据同周期原子半径递变规律判断 114 号元素的原子半径比 116 号元素的原子半径大,D 正确。
2.结合如图所示元素周期表,回答下列问题:(1)表中所列元素,属于长周期元素的有______(填字母,下同),属于主族元素的有__________;g 元素位于第________周期________族;i 元素位于第________周期________族。(2)f 元素位于第________周期________族。
(1)“0 族”法确定元素位置①熟记 0 族元素的相应周期数和原子序数
②确定主族元素在周期表中位置的方法:原子序数-最邻
近的稀有气体元素的原子序数=ΔZ。
若ΔZ0,则在该稀有气体元素下一周期,族序数为ΔZ
①原子序数是奇数的主族元素,其所在主族序数必为奇数。②原子序数是偶数的主族元素,其所在主族序数必为偶数。
元素周期表原子序数的定量关系
3.(2020年淄博实验中学月考)下列各图为元素周期表的一
部分,表中的数字为原子序数,其中 M 为 37 的是(
4.(2019 年运城模拟)元素周期表中的前 4 周期,两两相邻的 5 种元素如图所示,若 B 元素的核电荷数为 a。下列说法正
A.B、D 的原子序数之差可能为 2B.E、B 的原子序数之差可能是 8、18 或 32C.5 种元素的核电荷数之和为 5a+10D.A、E 的原子序数之差可能是 7
解析:由题中所给 5 种元素的位置关系可以看出 D 一定不是第一周期元素(因为如果 D 是第一周期元素,则 D 一定属于元素周期表最左边的第ⅠA 族元素或最右边的 0 族元素),所以A 错误;由题意可知 5 种元素在前 4 周期,所以 D、B、E 分别为第二、三、四周期的元素,由元素周期表的结构可知 5 种元素一定在过渡元素右边,所以 D、E 的原子序数分别为 a-8、a+18,A、C 的原子序数分别为 a-1、a+1,即只有 C 正确。
[归纳提升] 元素周期表中元素原子序数的序差规律(1)同周期ⅡA 族与ⅢA 族元素的原子序数之差有以下三种情况:第2、3 周期(短周期)相差1,第4、5 周期相差11,第6、7 周期相差25。
(2)相邻周期,同一主族元素的原子序数可能相差2、8、18、32。若 A、B 是同主族相邻周期元素,A、B 所在周期分别有
m 和 n 种元素。如图:
当 A、B 在ⅠA 或ⅡA 族时,y=x+m。A、B 在ⅢA~0
2.(2020 年浙江选考)下列说法正确的是(
A.35Cl和37Cl是两种不同的元素 B.单晶硅和石英互为同素异形体 C.HCOOH和HOCH2CHO互为同系物 D.H与Na在元素周期表中处于同一主族
相关课件
这是一份化学人教版 (2019)第四章 物质结构 元素周期律第一节 原子结构与元素周期表完美版课件ppt,共23页。PPT课件主要包含了原子的构成,原子核外电子排布,本节重点,本节难点,原子结构的探索历程,原子核,核外电子,带1个单位正电荷,不带电,带1个单位负电荷等内容,欢迎下载使用。
这是一份高考化学一轮总复习优化设计 第五单元 第1节 原子结构 元素周期表课件PPT,共60页。PPT课件主要包含了必备知识自主预诊,核电荷数,质子数,中子数,核燃料,测定一些文物的年代,自我诊断,关键能力考向突破,答案BD,pdf等内容,欢迎下载使用。
这是一份2022年高考总复习 化学 模块1 第三单元 高考素能提升五 元素推断题的分类突破课件PPT,共18页。PPT课件主要包含了解题模板,考向1,结构与位置互推,模板应用,答案B,考向2,性质与位置互推,说法正确的是,考向3等内容,欢迎下载使用。









