



(通用版)高考化学一轮复习讲练测第18讲 原电池 化学电源(精讲)(2份打包,解析版+原卷版,可预览)
展开【考情分析】
原电池的内容是高考的常考知识点之一,常以选择题的形式考查原电池的工作原理,如判断电极反应式和电池反应方程式的正误,电子或阴阳离子的移向,及依据电极反应式判断电极及电解质溶液中的现象;以填空题的形式考查新型原电池电极反应式和电池反应式的书写。
【核心素养分析】
1.变化观念与平衡思想:认识原电池反应的本质是自发的氧化还原反应;能多角度、动态地分析原电池中物质的变化及能量的转换。
2.证据推理与模型认知:能利用典型的原电池装置,分析原电池原理,建立解答原电池问题的思维模型,并利用模型揭示其本质及规律。
3.科学态度与社会责任:具有可持续发展意识和绿色化学观念,能对与原电池有关的社会热点问题做出正确的价值判断与分析。
【网络构建】
【知识梳理】
智能点一 原电池的工作原理及应用
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是自发进行的氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:
①电解质溶液;
②两电极直接或间接接触;
③两电极插入电解质溶液中。
3.工作原理
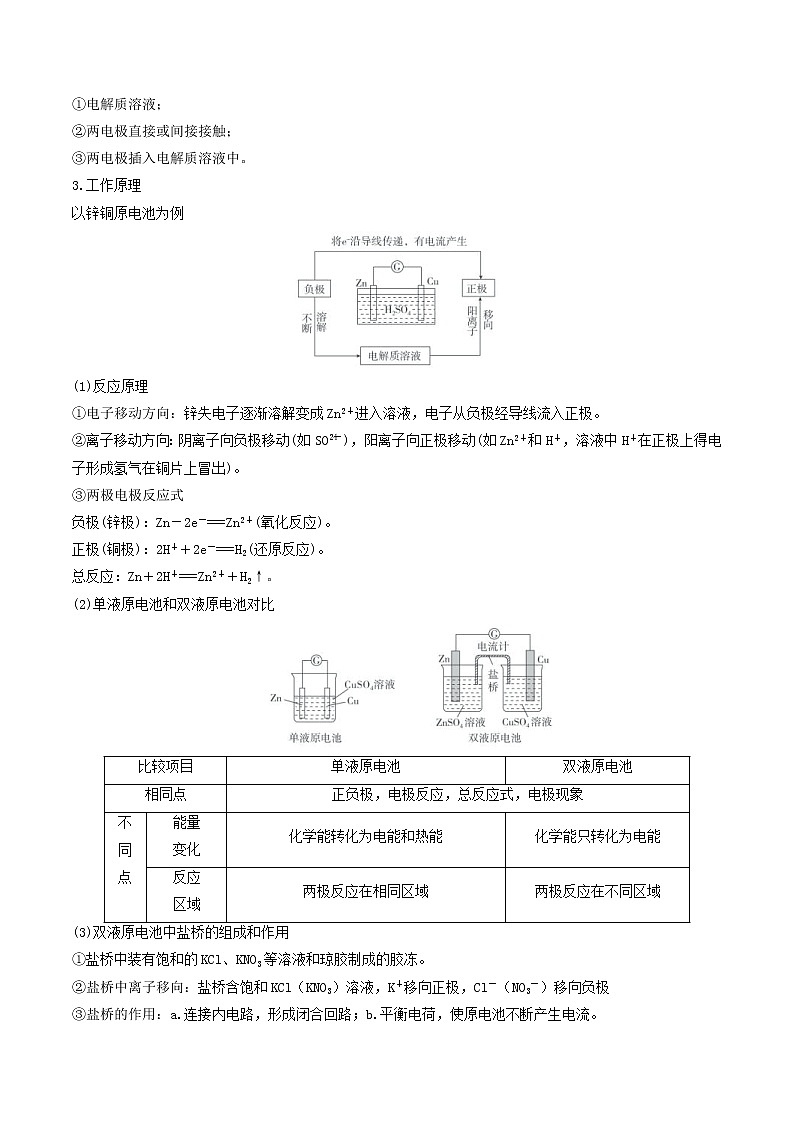
以锌铜原电池为例
(1)反应原理
①电子移动方向:锌失电子逐渐溶解变成Zn2+进入溶液,电子从负极经导线流入正极。
②离子移动方向:阴离子向负极移动(如SOeq \\al(2-,4)),阳离子向正极移动(如Zn2+和H+,溶液中H+在正极上得电子形成氢气在铜片上冒出)。
③两极电极反应式
负极(锌极):Zn-2e-===Zn2+(氧化反应)。
正极(铜极):2H++2e-===H2(还原反应)。
总反应:Zn+2H+===Zn2++H2↑。
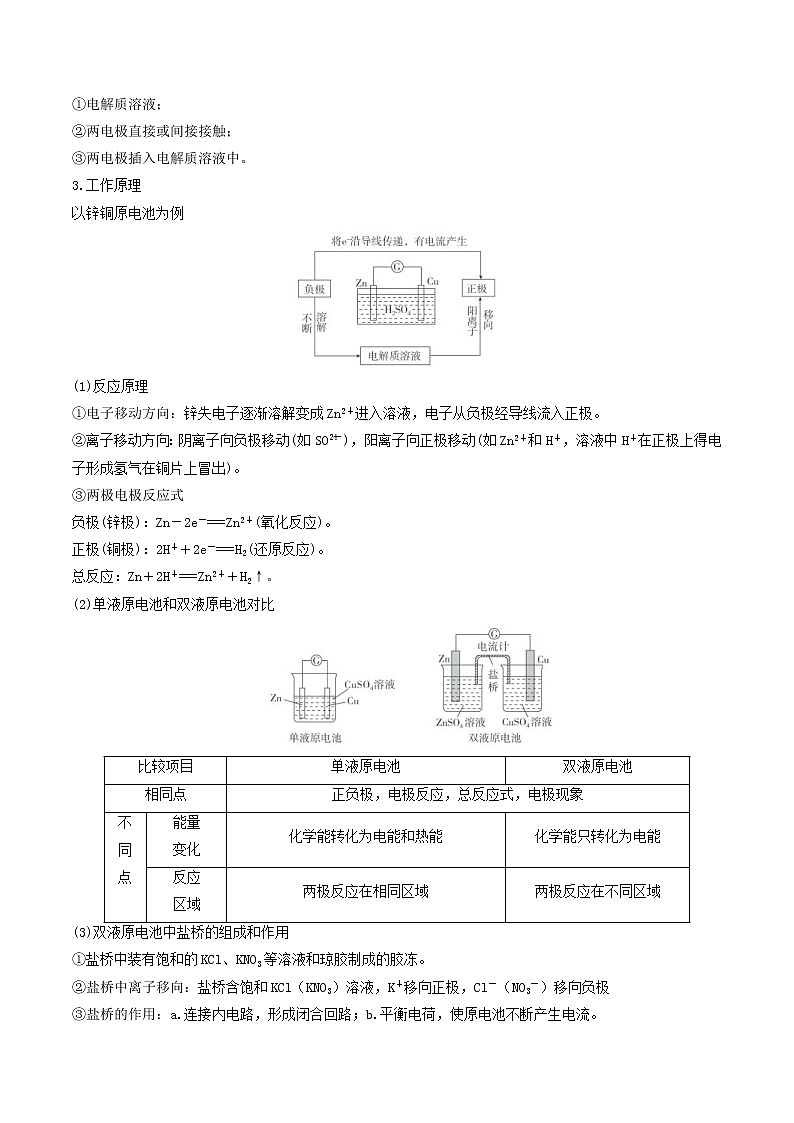
(2)单液原电池和双液原电池对比
(3)双液原电池中盐桥的组成和作用
①盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻。
②盐桥中离子移向:盐桥含饱和KCl(KNO3)溶液,K+移向正极,Cl-(NO3-)移向负极
③盐桥的作用:a.连接内电路,形成闭合回路;b.平衡电荷,使原电池不断产生电流。
4.原电池原理的应用
(1)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属(或非金属)。
(2)加快化学反应速率:一个自发进行的氧化还原反应,形成原电池时会使反应速率增大。如在Zn与稀硫酸反应时加入少量CuSO4溶液构成原电池,反应速率增大。
(3)用于金属的防护:使被保护的金属制品作原电池正极而得到保护。如要保护一个铁质的输水管道或钢铁桥梁等,可用导线将其与一块锌块相连,使锌作原电池的负极。
(4)设计制作化学电源
①拆分反应:将氧化还原反应分成两个半反应。
②选择电极材料:将还原剂(一般为比较活泼的金属)作负极,活泼性比负极弱的金属或非金属导体作正极。如果还原剂不是金属而是其它还原性物质,可选择惰性电极——石墨棒、铂片作负极。
③构成闭合回路:电解质溶液一般要能够与负极发生反应,或者电解质溶液中溶解的其他物质能与负极发生反应(如溶解于溶液中的空气)。如果两个半反应分别在两个容器进行(中间连接盐桥),则两个容器中的电解质溶液应含有与电极材料相同的金属的阳离子。
④画装置图:结合要求及反应特点,画出原电池装置图,标出电极材料名称、正负极、电解质溶液等。
智能点二 常见化学电源及工作原理
1.化学电源的优点和优劣判断标准
(1)相对其他能源,电池的优点是能量转换效率较高,供能稳定可靠,形状、大小可根据需要设计,使用方便等。
(2)判断电池优劣的标准是电池单位质量或单位体积所能输出的比能量或比功率及可储存时间的长短。
2.日常生活中的几种电池
(1)碱性锌锰干电池——一次电池
正极反应:2MnO2+2H2O+2e-===2MnOOH+2OH-;
负极反应:Zn+2OH--2e-===Zn(OH)2;
总反应:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。
(2)银锌电池——一次电池
负极反应:Zn+2OH--2e-===Zn(OH)2;
正极反应:Ag2O+H2O+2e-===2Ag+2OH-;
总反应:Zn+Ag2O+H2O===Zn(OH)2+2Ag。
(3)锂电池——一次电池
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为8Li+3SOCl2===6LiCl+Li2SO3+2S。
①负极材料为锂,电极反应为8Li-8e-===8Li+。
②正极的电极反应为3SOCl2+8e-===2S+SOeq \\al(2-,3)+6Cl-。
(4)二次电池(可充电电池):放电后能充电复原继续使用
铅蓄电池是最常见的二次电池,负极材料是Pb,正极材料是PbO2。
①放电时的反应
a.负极反应:Pb+SOeq \\al(2-,4)-2e-===PbSO4;
b.正极反应:PbO2+4H++SOeq \\al(2-,4)+2e-===PbSO4+2H2O;
c.总反应:Pb+PbO2+2H2SO4===2PbSO4+2H2O。
②充电时的反应
a.阴极反应:PbSO4+2e-===Pb+SOeq \\al(2-,4);
b.阳极反应:PbSO4+2H2O-2e-===PbO2+4H++SOeq \\al(2-,4);
c.总反应:2PbSO4+2H2O===Pb+PbO2+2H2SO4。
注:可逆电池的充、放电不能理解为可逆反应。
3.图解二次电池的充放电
4.二次电池的充放电规律
(1)充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电子,可简记为负接负后作阴极,正接正后作阳极。
(2)工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
5.“高效、环境友好”的燃料电池
(1)氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
(2)甲烷燃料电池
①酸性介质(如H2SO4)或传导质子(H+)固体介质
总反应式:CH4+2O2===CO2+2H2O。
负极反应式:CH4-8e-+2H2O===CO2+8H+。
正极反应式:2O2+8e-+8H+===4H2O。
②碱性介质(如KOH)
总反应式:CH4+2O2+2OH-===COeq \\al(2-,3)+3H2O。
负极反应式:CH4-8e-+10OH-===COeq \\al(2-,3)+7H2O。
正极反应式:2O2+8e-+4H2O===8OH-。
③熔融盐介质(如K2CO3)
总反应式:CH4+2O2===CO2+2H2O。
负极反应式:CH4-8e-+4CO32-===5CO2+2H2O。
正极反应式:2O2+8e-+4CO2===4CO32-。
④用能传导氧离子(O2-)的固体作介质
总反应式:CH4+2O2===CO2+2H2O。
负极反应式:CH4-8e-+4O2-===CO2+2H2O。
正极反应式:2O2+8e-===4O2-。
(3)解答燃料电池题目的思维模型
(4)解答燃料电池题目的几个关键点
①要注意介质是什么?是电解质溶液还是熔融盐或氧化物。
②通入负极的物质为燃料,通入正极的物质为氧气。
③通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
6.化学电源中电极反应式书写的一般方法
(1)明确两极的反应物;
(2)明确直接产物:根据负极氧化、正极还原,明确两极的直接产物;
(3)确定最终产物:根据介质环境和共存原则,找出参与的介质粒子,确定最终产物;
(4)配平:根据电荷守恒、原子守恒配平电极反应式。
注意:①H+在碱性环境中不存在;②O2-在水溶液中不存在,在酸性环境中结合H+,生成H2O,在中性或碱性环境结合H2O,生成OH-;③若已知总反应式时,可先写出较易书写的一极的电极反应式,然后在电子守恒的基础上,总反应式减去较易写出的一极的电极反应式,即得到较难写出的另一极的电极反应式。
【典例剖析】
高频考点1 考查原电池原理
例1. (2020·陕西榆林一模)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图所示。下列说法正确的是( )
A.b电极反应式为O2+2H2O+4e-===4OH-
B.溶液中OH-向电极b移动
C.NH3的还原产物为N2
D.电流方向:由a经外电路到b
【变式训练】(2020·河北唐山模拟)根据下图,下列判断中正确的是( )
A.烧杯a中的溶液pH降低
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
高频考点2 考查原电池正、负极的判断
例2.分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
【变式训练】观察如图所示装置,可发现电流计指针偏转,M棒变粗,N棒变细。表中所列的M、N、P对应物质可构成该装置的是
A.AB.BC.CD.D
高频考点3 考查原电池原理的应用
例3.A、B、C、D都是金属,把C浸入A的硫酸盐溶液中,C的表面有A析出;A与D组成原电池时,A质量减少;B与D构成原电池时,电子是从D经导线流向B。A、B、C、D四种金属的活动性顺序为
A.A>B>C>DB.A>C>D>BC.C>A>D>BD.C>D>B>A
【变式训练1】现有A、B、C、D四种金属片:①把A、B用导线连接后同时浸入稀硫酸中,B表面逐渐溶解;②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C
根据上述情况,下列说法中正确的是
A.在①中,金属片B发生还原反应
B.在②中,金属片C作正极
C.上述四种金属的活动性由强到弱的顺序是:A>B>C>D
D.如果把B、D用导线连接后同时漫入稀硫酸中,则金属片D上有气泡产生
【变式训练2】(加快氧化还原反应速率)把适合题意的图像填在横线上(用A、B、C、D表示)
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是________。
(2)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是________。
(3)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图像是________。
高频考点4 考查可充电电池(二次电池)
例4.(2020·新课标Ⅰ)科学家近年发明了一种新型Zn−CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为 SKIPIF 1 < 0
B. 放电时,1 ml CO2转化为HCOOH,转移的电子数为2 ml
C. 充电时,电池总反应为 SKIPIF 1 < 0
D. 充电时,正极溶液中OH−浓度升高
【变式训练】“天宫一号”飞行器在太空工作期间必须有源源不断的电源供应。其供电原理是:白天太阳能帆板发电,将一部分电量直接供给天宫一号,另一部分电量储存在镍氢电池里,供黑夜时使用。如图为镍氢电池构造示意图(氢化物电极为储氢金属,可看做H2直接参加反应)。下列说法正确的是
A.充电时阴极区电解质溶液pH降低
B.充电时阳极反应为Ni(OH)2-e-+OH-=NiOOH+H2O
C.放电时NiOOH在电极上发生氧化反应
D.在使用过程中此电池要不断补充水
高频考点5 考查新型电源(新型燃料电池)
例5.(2021·内蒙古高三一模)一种钌(Ru)基配合物光敏染料敏化太阳能电池,其工作原理如图所示。下列说法错误的是
A.电池工作时,将太阳能转化为电能
B.X电极为电池的负极
C.Y电极发生的电极反应为 SKIPIF 1 < 0 +2e-=3I-
D.当电池工作从开始到结束时,电解质溶液中I-和 SKIPIF 1 < 0 的浓度分别会发生很大变化
【变式训练】(2021·吉林松原市实验高级中学高三月考)由于化石燃料的长期大量消耗,传统能源逐渐枯竭,而人类对能源的需求量越来越高,氢能源和化学电源的开发与利用成为全球发展的重要问题。科学家利用氨硼烷设计成原电池装置如图所示,该电池在常温下即可工作,总反应为 SKIPIF 1 < 0 。下列说法错误的是
A.b室为该原电池的正极区
B.a室发生的电极反应式为 SKIPIF 1 < 0
C.放电过程中, SKIPIF 1 < 0 通过质子交换膜由b室移向a室
D.其他条件不变,向 SKIPIF 1 < 0 溶液中加入适量硫酸能增大电流强度
比较项目
单液原电池
双液原电池
相同点
正负极,电极反应,总反应式,电极现象
不
同
点
能量
变化
化学能转化为电能和热能
化学能只转化为电能
反应
区域
两极反应在相同区域
两极反应在不同区域
种类
酸性
碱性
负极反应式
2H2-4e-===4H+
2H2+4OH--4e-===4H2O
正极反应式
O2+4e-+4H+===2H2O
O2+2H2O+4e-===4OH-
电池总反应式
2H2+O2===2H2O
备注
燃料电池的电极不参与反应,有很强的催化活性,起导电作用
选项
M
N
P
A
锌
铜
稀硫酸
B
铜
铁
稀盐酸
C
银
锌
硝酸银溶液
D
锌
铁
硝酸铁溶液
(通用版)高考化学一轮复习讲练测第18讲 原电池 化学电源(精练)(2份打包,解析版+原卷版,可预览): 这是一份(通用版)高考化学一轮复习讲练测第18讲 原电池 化学电源(精练)(2份打包,解析版+原卷版,可预览),文件包含通用版高考化学一轮复习讲练测第18讲原电池化学电源精练解析版doc、通用版高考化学一轮复习讲练测第18讲原电池化学电源精练原卷版doc等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
(通用版)高考化学一轮复习讲练测第17讲 化学能与热能(精讲)(2份打包,解析版+原卷版,可预览): 这是一份(通用版)高考化学一轮复习讲练测第17讲 化学能与热能(精讲)(2份打包,解析版+原卷版,可预览),文件包含通用版高考化学一轮复习讲练测第17讲化学能与热能精讲解析版doc、通用版高考化学一轮复习讲练测第17讲化学能与热能精讲原卷版doc等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
(通用版)高考化学一轮复习讲练测第15讲 原子结构 化学键(精讲)(2份打包,解析版+原卷版,可预览): 这是一份(通用版)高考化学一轮复习讲练测第15讲 原子结构 化学键(精讲)(2份打包,解析版+原卷版,可预览),文件包含通用版高考化学一轮复习讲练测第15讲原子结构化学键精讲解析版doc、通用版高考化学一轮复习讲练测第15讲原子结构化学键精讲原卷版doc等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。












