






所属成套资源:全套人教版九年级化学下册教学习题课件
人教版九年级化学下册第十单元课件合集共9套
展开
这是一份人教版九年级化学下册第十单元课件合集共9套,共60页。
人教版九年级化学下册第十单元课件合集共9套
第十单元 酸和碱
课题1 常见的酸和碱第1课时 常见的酸
提示:点击 进入习题
答案显示
C
见习题
D
见习题
见习题
见习题
B
见习题
B
D
B
D
B
C
A
1.石蕊、酚酞等溶液叫做______________,石蕊溶液遇酸溶液变成________色,遇碱溶液变成________色;酚酞溶液遇酸溶液________,遇碱溶液__________。
酸碱指示剂
红
蓝
不变色
变成红色
2.【2022•柳州】化学课中老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是( )A.水 B.稀盐酸C.氨水 D.氯化钠溶液
C
3.向某一无色溶液中滴加少许无色酚酞溶液,溶液变红色。若向此无色溶液中滴加少许紫色石蕊溶液,则溶液呈现的颜色为( )A.无色 B.紫色 C.红色 D.蓝色
D
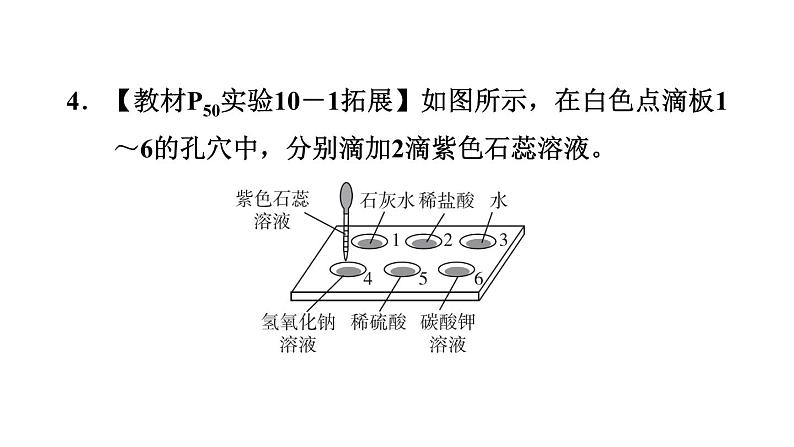
4.【教材P50实验10-1拓展】如图所示,在白色点滴板1~6的孔穴中,分别滴加2滴紫色石蕊溶液。
(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显________(填“酸性”或“碱性”)。(2)溶液变为红色的孔穴有________(填孔穴序号,下同)。(3)作为空白对照实验的孔穴是________。(4)孔穴4中溶液变为________色,若向孔穴4中滴加稀硫酸,溶液变成紫色,说明溶液由_______性变成中性。
碱性
2、5
3
蓝
碱
5.浓盐酸是______色,有________气味的液体,打开盛浓盐酸的试剂瓶瓶塞,在瓶口会看到________,说明浓盐酸具有挥发性。人的胃液中含有________,可帮助消化。
无
刺激性
白雾
盐酸
6.浓硫酸是________色,黏稠的液体,不易挥发。浓硫酸具有的特性:①吸水性,常作________剂;②腐蚀性,能使木材、纸张等________而变黑。③浓硫酸溶于水放出大量的热,所以稀释浓硫酸时应把________沿器壁慢慢注入______中,并用________不断搅拌。
无
干燥
炭化
浓硫酸
水
玻璃棒
7.如图所示,已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会( )A.左端下沉B.右端下沉C.仍平衡D.无法判断
B
8.【教材P53实验10-3改编】如图所示是稀释浓硫酸实验的示意图。(1)写出图中a、b两种仪器的名称:a.________,b.________。(2)b容器所盛的试剂是_______(填“水”或“浓硫酸”)。(3)稀释时,若两种试剂添加顺序颠倒,将会发生_________________的后果。
玻璃棒
量筒
浓硫酸
液滴溅出伤人
(4)取用浓硫酸后要立即塞上瓶塞,原因是____________________________________________。
防止浓硫酸吸收空气中的水分使溶质质量分数变小
9.【2022•云南】天宫课堂中,宇航员通过实验呈现了“奥运五环”,实验中使用了指示剂——溴百里酚蓝,溴百里酚蓝溶液在不同环境中的显色情况如下:
下列溶液能使绿色溴百里酚蓝溶液变为黄色的是( )A.氯化钠溶液 B.醋酸溶液C.氢氧化钾溶液 D.碳酸钠溶液
B
10.【2022•南京二模】用酒精和水浸泡蝴蝶兰花得到紫色溶液,该溶液遇酸性溶液显红色,遇碱性溶液显黄色。下列说法不正确的是( )A.蝴蝶兰花的溶液与酸作用显红色的本质是与酸溶液中的H+反应B.蝴蝶兰花的溶液可用作酸碱指示剂C.将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色D.能使蝴蝶兰花的溶液显黄色的一定是碱的溶液
【点拨】蝴蝶兰花的溶液与酸作用显红色是化学变化,其本质是与酸溶液中的H+反应,故A选项说法正确;因为蝴蝶兰花的溶液遇酸碱性溶液会显示不同颜色,因此可作指示剂,故B选项说法正确;氯化钠的溶液呈中性,不会使指示剂变色,故C选项说法正确;能使蝴蝶兰花的溶液变黄色的是碱性溶液,但不一定是碱的溶液,故D选项说法错误。
【答案】D
11.【2022•长沙】“酸”对我们来说一定不陌生。下列说法正确的是( )A.稀盐酸不能用于除铁锈B.浓硫酸具有腐蚀性C.浓盐酸没有挥发性D.稀盐酸能使无色酚酞溶液变红
【点拨】点拨:铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁和水,稀盐酸能用于除铁锈,故A说法错误;浓硫酸具有强烈的腐蚀性,故B说法正确;浓盐酸具有挥发性,故C说法错误;稀盐酸显酸性,不能使无色酚酞溶液变红,故D说法错误。
【答案】B
12.下列关于盐酸和硫酸的说法中,不正确的是( )A.都能使紫色石蕊溶液变红B.都可用于金属除锈C.它们的浓溶液都必须密封保存D.它们的浓溶液都可作干燥剂
D
13.下列关于两瓶敞口存放一段时间的浓盐酸和浓硫酸的说法中,正确的是( )A.溶液质量都变小B.溶质质量分数都变小C.溶剂质量都变大D.瓶口都有白雾
【点拨】浓盐酸具有挥发性,溶质质量减小,溶剂质量不变,溶液质量减小,溶质质量分数变小;浓硫酸具有吸水性,能吸收空气中的水分,溶质质量不变,溶剂的质量变大,溶液质量增加,溶质质量分数变小;浓盐酸具有挥发性,挥发出的氯化氢与空气中的水蒸气结合成盐酸小液滴,形成白雾,浓硫酸不具有挥发性,不能形成白雾。
【答案】B
14.【中考•扬州】硫酸是一种重要的工业原料,下列说法不正确的是( )A.浓硫酸可用于干燥O2B.浓硫酸可使纸张炭化C.稀释浓硫酸时,应将水慢慢注入浓硫酸中D.稀硫酸可用于金属表面除锈
C
15.下列有关实验现象的描述正确的是( )A.柠檬酸使无色酚酞溶液不变色B.氢氧化钠溶液遇酚酞溶液变红C.浓盐酸敞口放置时瓶口有白色的烟雾D.浸有紫色石蕊的干燥小花放入二氧化碳气体中,小花变红
第十单元 酸和碱
课题1 常见的酸和碱第2课时 酸的化学性质
提示:点击 进入习题
答案显示
A
见习题
A
见习题
C
C
见习题
A
B
D
见习题
B
1.酸与金属反应的基本反应类型是________反应。这类反应的条件是:①所用金属必须是在金属活动性顺序里__________的金属;②所用的酸必须是无强氧化性的酸,常用______________。另外还要注意铁与该类酸反应时生成物中铁元素一定显______价。
置换
位于氢前
稀盐酸、稀硫酸
+2
2.下列物质不能由金属和酸反应直接制得的是( ) A.AgCl B.FeCl2 C.MgCl2 D.AlCl3
【点拨】银在金属活动性顺序中排在氢后,不能直接与稀盐酸反应制得氯化银。
A
3.【中考•淄博】手机的某些部件里含有Mg、Al、Cu、Ag等金属,将废旧手机的部件粉碎并浸入足量稀硫酸中,充分反应后,所得溶液中含有的金属离子是( )A.Mg2+、Al3+ B.Cu2+、Ag+C.Al3+、Cu2+ D.Mg2+、Ag+
A
4.实验时,李华把一枚生锈的铁钉放入足量的稀盐酸中,过一会儿,他看到的现象是___________________________;发生反应的化学方程式为___________________________;过一段时间,他又看到铁钉表面有气泡产生,该反应的化学方程式为_______________________________。
铁锈逐渐消失,溶液变成黄色
Fe2O3+6HCl===2FeCl3+3H2O
Fe+2HCl===FeCl2+H2↑
他又将铝片放入足量的稀盐酸中,奇怪的是开始无明显现象,过一段时间后才看到有气泡冒出,试用学过的知识解释原因:_______________________________,______________________________(用化学方程式表示)。
Al2O3+6HCl===2AlCl3+3H2O
2Al+6HCl===2AlCl3+3H2↑
5.用稀盐酸浸泡生锈的铁钉,较短时间内,铁钉表面有大量气泡冒出,溶液呈黄色,下列说法错误的是( )A.若将盐酸换成稀硫酸,能观察到几乎相同的现象B.溶液中除氢离子、氯离子外,还会增加亚铁离子、铁离子C.因为盐酸易挥发,故液面上方只有氯化氢气体D.除锈时不宜将铁钉长时间浸泡,一段时间后应取出并冲洗
C
6.【2022•泰州】硫酸是重要的化工原料。下列有关硫酸的说法错误的是( )A.浓硫酸具有吸水性B.稀硫酸能与锌反应制取氢气C.稀释浓硫酸时温度降低D.稀硫酸可用于金属表面除锈
C
7.【2021·甘南】利用以下装置对酸的化学性质进行探究。
(1)标号为①的仪器名称是__________。(2)实验Ⅰ中,在点滴板的a、b穴中滴入酸溶液后,溶液变红的是____(填“a”或“b”)。使用点滴板的优点之一是_____________________________________________。(3)实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂X的名称是____________。
试管
a
节约试剂(合理即可)
澄清石灰水
(4)实验Ⅲ中,在仪器①、②中均可观察到的现象是____________、____________。仪器②中发生反应的化学方程式是________________________________。
固体逐渐溶解
得到黄色溶液
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
8.【2022•湘潭】下列不能与稀盐酸反应的物质是( )A.银 B.氧化铜 C.碳酸钠 D.氢氧化钾
A
9.试管内壁附着的下列物质不能用稀盐酸浸泡而除去的是( )A.盛石灰水后残留的白色固体B.用氢气还原氧化铜留下的红色固体C.探究铁生锈条件后留下的红棕色固体D.硫酸铜溶液与氢氧化钠溶液反应后留下的蓝色固体
【点拨】用氢气还原氧化铜留下的红色固体是铜,铜不能与稀盐酸反应,故不能用稀盐酸浸泡而除去,B选项符合题意。
【答案】B
10.【2021·贵港】现有一包金属粉末,可能由Al、Mg、Zn、Fe、Ag中的一种或几种组成。取该样品2.4 g,向其中加入100 g一定溶质质量分数的稀硫酸,恰好完全反应,产生0.2 g H2,溶液呈无色,无固体剩余。则下列结论正确的是( )A.该样品的组成仅有两种可能B.所用稀硫酸的溶质质量分数为19.6%C.该样品中一定含有MgD.所得溶液中溶质的总质量为12 g
由上述分析可知,该样品中不一定含有Mg,C选项说法不正确;反应生成0.2 g氢气,说明参加反应的硫酸根的质量是9.6 g,则无色溶液中溶质总质量为9.6 g+2.4 g=12 g,D选项说法正确。
【答案】D
11.A、B、C、D、E是常见的五种物质。已知C是人体胃液中可帮助消化的物质,D是大理石的主要成分,其相互关系如图所示,“—”表示相连物质间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。
(1)写出下列物质的化学式:C________,E________。(2)写出下列反应的化学方程式。①C与D的反应:_________________________________;②C转化为B的反应:_________________________________________________________________,
HCl
CaO
CaCO3+2HCl===CaCl2+CO2↑+H2O
CuO+2HCl===CuCl2+H2O(合理即可)
③C转化为A的反应:_______________________________,该反应属于__________(填基本反应类型)反应;④C与E的反应:_______________________________;B与E的反应是________(填“吸热”或“放热”)反应。(3)上述反应中的分解反应有________个。
Zn+2HCl===ZnCl2+H2↑(合理即可)
置换
CaO+2HCl===CaCl2+H2O
放热
2
12.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊溶液B.若d是Cu(OH)2固体,则X一定是稀硫酸C.若X是稀硫酸,则c可能是单质D.若b是Fe2O3,则黄色溶液可能是硫酸铁
【点拨】酸能使紫色石蕊变红色,因此若X是稀硫酸,则a可能是紫色石蕊溶液,A正确;若d是Cu(OH)2固体,则X不一定是稀硫酸,还可能是稀盐酸等,B错误;铁和稀硫酸反应生成硫酸亚铁和氢气,c可能是单质,C正确;b是Fe2O3,则黄色溶液可能是硫酸铁,稀硫酸和氧化铁反应生成硫酸铁和水,D正确。
【答案】B
第十单元 酸和碱
课题1 常见的酸和碱第3课时 常见的碱
提示:点击 进入习题
答案显示
见习题
见习题
B
B
见习题
C
D
见习题
见习题
B
D
A
D
见习题
C
1.氢氧化钠是一种白色固体,________溶于水,溶于水时________热,在空气中易潮解,可作________剂,有强烈腐蚀性,俗称_______、_______、________。
易
放
干燥
火碱
烧碱
苛性钠
2.氢氧化钙是一种白色粉末,______溶于水,其溶解度随着温度的升高而________,俗称__________、________,其水溶液俗称________。
微
减小
消石灰
熟石灰
石灰水
3.【2021•邵阳】下列关于氢氧化钠的描述中错误的是( )A.对皮肤有强烈的腐蚀作用B.其水溶液能使石蕊溶液变红C.能去除油污,可作炉具清洁剂D.易溶于水,溶解时放出热量
【点拨】紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,氢氧化钠溶液显碱性,其水溶液能使石蕊溶液变蓝,B错误。
B
4.【中考·郴州】下列关于Ca(OH)2的说法错误的是( )A.微溶于水,水溶液呈碱性B.能与酸反应,可用于治疗胃酸过多C.与CuSO4溶液按一定比例混合,可配制波尔多液D.澄清溶液可用来检验CO2
【点拨】氢氧化钙能与酸反应,但氢氧化钙具有腐蚀性,不能用于治疗胃酸过多,故B选项错误。
B
5.(1) 氢氧化钠应________保存,因为_______________________________,写出氢氧化钠变质的化学方程式____________________________。工业上常用氢氧化钠溶液吸收二氧化硫,以减少空气污染,写出反应的化学方程式:__________________________。(2)熟石灰是常见的碱,在生产中有很多用途。①由生石灰制取熟石灰的化学方程式为_______________________________________;
密封
NaOH易吸收空气中的H2O和CO2
2NaOH+CO2===Na2CO3+H2O
2NaOH+SO2===Na2SO3+H2O
CaO+H2O===Ca(OH)2
②用石灰砂浆抹墙,墙面逐渐变得坚硬,反应的化学方程式为_______________________________;③除上述用途外,再举出一个应用熟石灰的实例:______________________________;
Ca(OH)2+CO2===CaCO3+H2O
改良酸性土壤(合理即可)
6.下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是( )A.浓盐酸 B.浓硫酸 C.石灰水 D.烧碱溶液
【点拨】浓盐酸易挥发,导致溶液的质量减小,但未发生化学变化,A错误;浓硫酸易吸水,导致溶液的质量增大,B错误;石灰水与空气中的二氧化碳反应生成碳酸钙沉淀和水,因发生化学变化导致溶液的质量减小,C正确;烧碱溶液与二氧化碳反应生成碳酸钠和水,溶液质量增加,D错误。
【答案】C
7.【中考•泸州】下列物质不能与NaOH溶液反应的是( )A.二氧化碳 B.硝酸C.硫酸铜 D.氢氧化铁
D
8.【2021•绍兴】物质的溶解度不同,用途也不同。下表是几种物质的溶解度(20 ℃),请据表回答:
(1)实验中一般用氢氧化钠溶液吸收二氧化碳,而不用澄清石灰水来吸收二氧化碳,主要原因是氢氧化钙________于水,吸收效果不好。(2)实验中一般用澄清石灰水检验二氧化碳,但是根据上表可知能使澄清石灰水变浑浊的不一定是二氧化碳,也可能是二氧化硫,请用化学方程式说明__________________________________________。
微溶
SO2+Ca(OH)2===CaSO3↓+H2O
(3)20 ℃时,饱和氢氧化钠溶液的溶质质量分数为________(精确到0.1%)。
52.2%
9.碱溶液的化学性质相似,写出下列反应的化学方程式。(1)氢氧化钾久置在空气中变质_______________________________。(2)二氧化碳通入氢氧化钡溶液中,溶液变浑浊_______________________________。(3)氢氧化锂(LiOH)溶液也能吸收二氧化碳气体_______________________________。
2KOH+CO2===K2CO3+H2O
CO2+Ba(OH)2===BaCO3↓+H2O
2LiOH+CO2===Li2CO3+H2O
10.【2022•盘锦】下列关于氢氧化钠的描述中错误的是( )A.易与空气中成分反应而变质B.蚊虫叮咬后涂抹NaOH溶液减轻痛痒C.能去除油污,可作炉具清洁剂D.NaOH水溶液能使紫色石蕊溶液变蓝
【点拨】氢氧化钠易与空气中的二氧化碳反应生成碳酸钠而变质,故A说法正确;蚊虫叮咬后不能涂抹NaOH溶液减轻痛痒,因为氢氧化钠溶液具有强烈的腐蚀性,故B说法错误;氢氧化钠能与油脂反应,能去除油污,可作炉具清洁剂,故C说法正确;NaOH水溶液显碱性,能使紫色石蕊溶液变蓝,故D说法正确。
【答案】B
11.合理的实验设计往往可以让我们得出准确的结论,以下实验设计不能证明CO2与NaOH溶液发生了化学反应的是( )
D
12.某同学总结的Ca(OH)2的化学性质如图所示。下列说法错误的是( ) A.甲一定是碳酸盐 B.Ca(OH)2俗称熟石灰 C.反应③可用于检验某种温室气体 D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
【点拨】甲不一定是碳酸盐,也可能是硫酸铜等盐,故A选项错误。
【答案】A
13.物质性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体 ②有腐蚀性 ③能与空气中的二氧化碳反应 ④易溶于水,溶解时放热 ⑤易吸收水分而潮解。实验室中必须将它密封保存的主要原因是( )A.①② B.①② C.②③④ D.③⑤
D
14.现有盐酸、氢氧化钠溶液、氢氧化钙溶液三瓶失去标签的药品,为了鉴别它们,分别将其编号为A、B、C,并进行如下实验,请根据实验现象回答下列问题:实验一:用三支试管分别取A、B、C三种样品少许,向其中通入气体a,只有B中产生白色沉淀,A、C无明显现象;实验二:用两支试管分别取A、C溶液少许,向其中滴加无色溶液b,A中溶液变红,C中无明显现象。
(1)气体a的化学式为______,溶液b的名称是_________。(2)写出三种溶液溶质的化学式:A____________、B__________________、C____________________。(3)写出实验一中产生白色沉淀的化学方程式____________________________________________。(4)在本实验中,如果将实验一和实验二的顺序颠倒,能否达到实验目的?__________________________。
CO2
酚酞溶液
NaOH
Ca(OH)2
HCl
Ca(OH)2+CO2===CaCO3↓+H2O
能达到实验目的
15.【2022·吉林】下列关于NaOH和Ca(OH)2的用途中,说法错误的是( )A.用Ca(OH)2制波尔多液B.用Ca(OH)2改良酸性土壤C.用NaOH溶液检验CO2D.用NaOH固体干燥某些气体
【点拨】可用Ca(OH)2、CuSO4配制农药波尔多液,故A说法正确;Ca(OH)2显碱性,可用于改良酸性土壤,故B说法正确;二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,无明显现象,不能用NaOH溶液检验CO2,故C说法错误;氢氧化钠具有吸水性,可用NaOH固体干燥某些气体,故D说法正确。
【答案】C
第十单元 酸和碱
课题2 酸和碱的中和反应第1课时 中和反应
提示:点击 进入习题
答案显示
A
见习题
见习题
见习题
见习题
C
A
D
见习题
C
1.由________离子和________离子组成的化合物叫做盐,如__________、___________________等都是盐。NH4Cl、NH4NO3等虽然不含金属离子(含有NH4+),也属于盐,因此盐的组成中__________(填“一定”或“不一定”)含有金属元素。
金属
酸根
NaCl
CuSO4(合理即可)
不一定
2.【2022·自贡】分类是化学学习和研究的重要方法之一。下列物质分类错误的是( )A.氧化物:SO2、CuO、KMnO4B.酸:HCl、H2SO4、HNO3C.碱:NaOH、Ca(OH)2、NH3·H2OD.盐:NH4Cl、AgNO3、BaSO4
A
3.________和________作用生成盐和水的反应叫做中和反应。中和反应的实质是________中的________和________中的________结合生成水。注意:中和反应的反应物一定是________和________,生成物是盐和水,但有盐和水生成的反应________(填“一定”或“不一定”)是中和反应。
酸
碱
酸溶液
H+
碱溶液
OH-
酸
碱
不一定
4.【教材P60实验10-8拓展】氢氧化钠与稀盐酸反应观察不到明显现象,为了确定反应是否发生,丽丽小组同学设计了如图1所示的实验探究方案。 请回答下列问题:(1)标号仪器的名称:①__________,②__________。
滴瓶
烧杯
(2)玻璃棒在实验中的作用及目的是_____________________。(3)当观察到烧杯中溶液颜色__________________时,说明酸碱恰好完全中和。(4)该实验过程中发生反应的化学方程式为__________________________。
搅拌,使反应物充分接触
由红色变成无色
NaOH+HCl===NaCl+H2O
(5)仿照填写图2圆圈内的空白,其反应的实质是_________________________。
H+和OH-结合成H2O
Na+ Cl- H2O
5.中和反应在实际中的应用:(1)农业生产中常用__________改良酸性土壤。(2)工业上常用________来中和硫酸厂的污水,反应的化学方程式为_________________________________。(3)医疗上:①常用含氢氧化铝的药片治疗胃酸过多症,反应的化学方程式为_______________________________;②可用牙膏、肥皂水等_____性物质中和蚊虫叮咬后留在皮肤中的蚁酸。
熟石灰
熟石灰
Ca(OH)2+H2SO4===CaSO4+2H2O
Al(OH)3+3HCl===AlCl3+3H2O
碱
6.【2021•百色】下列实际应用中,不是利用中和反应原理的是( )A.用熟石灰改良酸性土壤B.用稀硫酸处理印染厂的碱性废水C.用含碳酸氢钠的药物治疗胃酸过多D.用稀氨水涂抹在蚊虫叮咬处(分泌出蚁酸)止痒
C
7.【2022·苏州】氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图如下。下列说法不正确的是( )A.盐酸中存在的微粒有水分子和氯化氢分子B.该反应的微观实质是H+和OH-结合生成水分子C.Na+和Cl-在该反应过程中没有被消耗D.恰好完全反应时,溶液呈中性
【点拨】盐酸中存在的微粒有水分子、氢离子、氯离子,故A说法错误;由氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图知,该反应的微观实质是H+和OH-结合生成水分子,故B说法正确;Na+和Cl-在该反应过程中没有被消耗,故C说法正确;恰好完全反应时,溶质是氯化钠,溶液呈中性,故D说法正确。
【答案】A
8.【2022·包头】下列生产生活中的应用,利用了中和反应原理的是( )A.生石灰用作食品干燥剂B.用熟石灰和硫酸铜制波尔多液C.用小苏打做面点发酵剂D.服用含Al(OH)3的药物治疗胃酸过多
【点拨】生石灰用作食品干燥剂,是利用生石灰和水反应生成氢氧化钙,反应物是金属氧化物和水,不是酸与碱的反应,不是利用中和反应原理,故A选项错误;用熟石灰和硫酸铜制波尔多液,反应物是碱和盐,不是酸与碱的反应,不是利用中和反应原理,故B选项错误;用小苏打做面点发酵剂,小苏打和酸反应,反应物是盐和酸,不是酸与碱的反应,不是利用中和反应原理,
故C选项错误;服用含Al(OH)3的药物治疗胃酸过多,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故D选项正确。
【答案】D
9.【2021•绥化】中和反应在日常生活和工农业生产中有广泛的应用。(1)向盛有一定量稀盐酸的密闭隔热容器中,加入氢氧化钠固体,利用数字传感器测出反应时间与溶液温度变化的图像如图所示。
①甲同学得出结论:稀盐酸和氢氧化钠反应过程中放热。乙同学不同意他的观点,乙同学的理由是________________________________________________________________;②丙同学取少量反应后的溶液于试管中,加入无色酚酞溶液,无明显现象,于是三位同学对反应后溶液中溶质的成分作出猜想:猜想一:NaCl 猜想二:NaCl和NaOH猜想三:____________
氢氧化钠溶于水放热,也能使温度升高
NaCl和HCl
③同学们经过讨论后认为猜想________一定不正确;④为了验证其余猜想,丙同学进行如下探究。
二
产生气泡
(2)丁同学在试管中加入约1 mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢慢滴入稀硫酸,边不断振荡试管,至溶液颜色____________________________为止,说明氢氧化钠和稀硫酸恰好完全反应,该反应的化学方程式为________________________________________。(3)结合上述实验可知,中和反应的实质是________________________________________。
由红色恰好变成无色
2NaOH+H2SO4===Na2SO4+2H2O
氢离子和氢氧根离子结合生成水分子
10.下列关于中和反应的说法正确的是( )A.可用氢氧化钠治疗胃酸过多症B.有盐和水生成的反应一定是中和反应C.工厂废水中含有的硫酸可以用氨水中和D.中和反应的发生必须借助酸碱指示剂进行判断
【点拨】治疗胃酸过多症常用含Al(OH)3或Mg(OH)2的药片,不能用NaOH、Ca(OH)2等腐蚀性较强的碱去中和过多胃酸;中和反应的生成物一定是盐和水,但有盐和水生成的反应不一定是中和反应,必须紧扣反应物是酸和碱;工厂废水中含有的硫酸可以用碱性物质中和,氨水是碱溶液,可以中和废硫酸;中和反应有的有明显现象,有的没有明显现象,对于没有明显现象的中和
反应常借助酸碱指示剂,根据指示剂颜色的变化判断反应是否发生。
【答案】C
第十单元 酸和碱
课题2 酸和碱的中和反应第2课时 溶液酸碱度的表示方法——pH
提示:点击 进入习题
答案显示
D
见习题
A
B
见习题
C
见习题
D
见习题
D
A
A
B
见习题
A
1.溶液的酸碱度常用________表示,其范围在________之间。常温下,当________时,溶液呈酸性,且pH越小,酸性越________;当________时,溶液呈碱性,且pH越大,碱性越________;当________时,溶液呈中性。
pH
0~14
pH<7
强
pH>7
强
pH=7
2.【2022•乐山】以下是一些身边常见物质的近似pH,其中显碱性的是( )A.苹果汁:3~4 B.厕所清洁剂:1~2C.酱油:4~5 D.炉具清洁剂:12~13
D
3.【2022•连云港】常温下人体内一些液体的正常pH范围如下,其中呈酸性的是( )A.胃液(0.9~1.5) B.胆汁(7.1~7.3)C.血液(7.35~7.45) D.胰液(7.5~8.0)
A
4.【2022•昆明】在pH=2的白醋中滴加石蕊溶液,溶液变( )A.紫色 B.红色 C.无色 D.蓝色
B
5.测定溶液pH的最简单方法是使用_______________。(1)操作方法:在白瓷板或玻璃片上放一小片________,用________蘸取待测液滴在________上,把试纸显示的颜色与______________对照,即可测出溶液的pH。
pH试纸
pH试纸
玻璃棒
pH试纸
标准比色卡
(2)注意事项:①不能直接将pH试纸浸入待测液中,以免污染试剂;②不能将pH试纸润湿,否则待测液被________,测量可能不准确;③用pH试纸测出的pH为整数值,要想测出的pH更精确,可使用______________。
稀释
pH计
6.下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照D.用pH试纸测得该氢氧化钠溶液的pH=12.6
C
7.(1)农业生产中,农作物一般适宜在pH_____________的土壤中生长。若pH过高或过低,一般不适宜种植。(2)由于雨水能与空气中的二氧化碳反应,反应的化学方程式为__________________,故正常雨水呈弱酸性,pH约为________,而酸雨的pH________,通过测定雨水的pH可以了解空气是否受到SO2、NO2等酸性气体的污染。
等于7或接近7
CO2+H2O===H2CO3
5.6
<5.6
8.【2022•黄石】如表为四种植物适宜生长的pH范围,不适宜种植在酸性土壤中的是( )
D
9.下表中列出一些液体的pH。
(1)在厨房清洁剂中滴入酚酞溶液显____________色。(2)人大量饮水后,胃液的pH会________(填“变大”“变小”或“不变”)。
红
变大
(3)洗发时先用洗发水洗发再使用护发素,这样做的化学原理是________________________________________________________________________________________。
利用碱性物质除油污,再利用酸性物质与碱性物质反应,既能除污垢又能使头发健康生长
10.【教材P66T2改编】一些食物的近似pH如表所示,下列说法正确的是( ) A.牛奶放置一段时间后变酸,pH变大B.西瓜汁比苹果汁酸性强C.鸡蛋清和牛奶都显碱性D.胃酸过多的人应该少饮苹果汁
【点拨】牛奶放置一段时间后变酸,即酸性增强,pH变小,A错误;西瓜汁的pH大于苹果汁的pH,所以西瓜汁比苹果汁酸性弱,B错误;牛奶的pH<7,显酸性,C错误;苹果汁的pH<7,显酸性,所以胃酸过多的人应该少饮苹果汁,D正确。
【答案】D
11.下列推理正确的是( )A.酸溶液的pH






