




所属成套资源:2022年高考化学一轮复习高频考点集训(2份打包,解析版+原卷版,可预览)
- 2022年高考化学一轮复习高频考点集训专题09 有机化合物(2份打包,解析版+原卷版,可预览) 试卷 0 次下载
- 2022年高考化学一轮复习高频考点集训专题10 化学与自然资源的开发利用(2份打包,解析版+原卷版,可预览) 试卷 0 次下载
- 2022年高考化学一轮复习高频考点集训专题13 晶体结构与性质(2份打包,解析版+原卷版,可预览) 试卷 0 次下载
- 2022年高考化学一轮复习高频考点集训专题14 化学反应与能量(选修)(2份打包,解析版+原卷版,可预览) 试卷 0 次下载
- 2022年高考化学一轮复习高频考点集训专题11 原子结构与性质(2份打包,解析版+原卷版,可预览) 试卷 0 次下载
2022年高考化学一轮复习高频考点集训专题12 分子结构与性质(2份打包,解析版+原卷版,可预览)
展开
这是一份2022年高考化学一轮复习高频考点集训专题12 分子结构与性质(2份打包,解析版+原卷版,可预览),文件包含2022年高考化学一轮复习高频考点集训专题12分子结构与性质解析版doc、2022年高考化学一轮复习高频考点集训专题12分子结构与性质原卷版doc等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
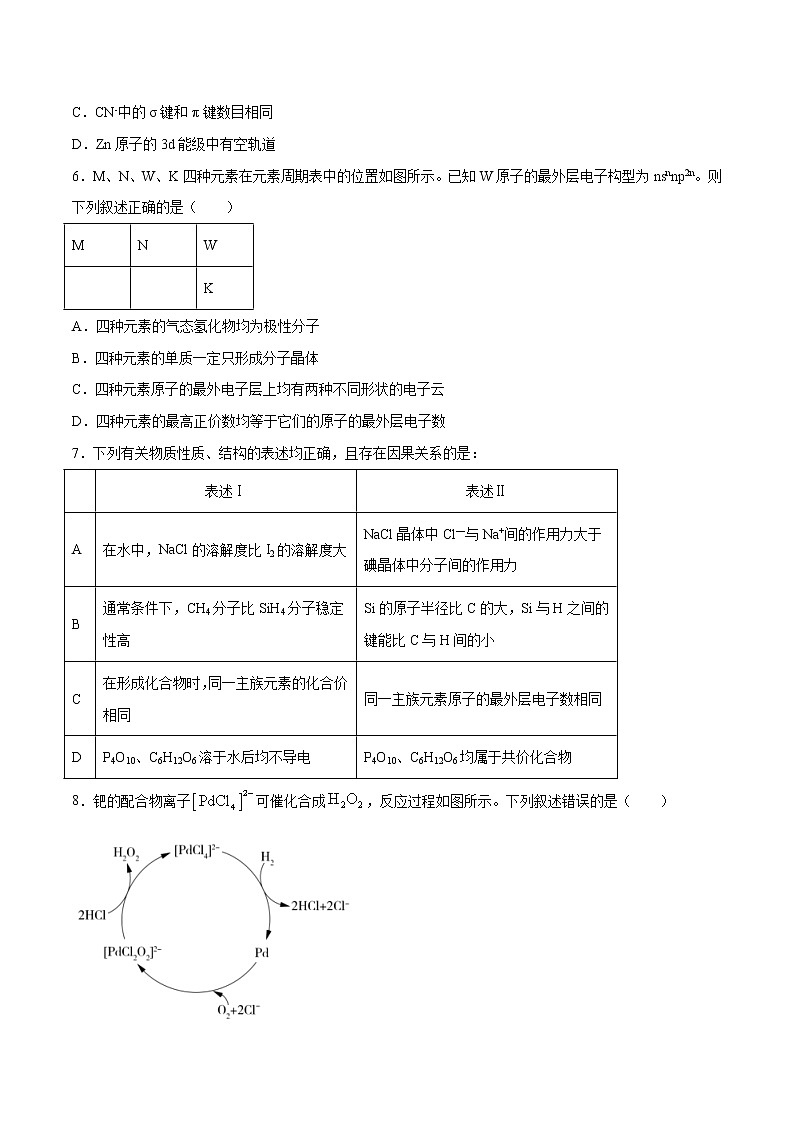
专题12 分子结构与性质一、单选题1.下列有关说法正确的是A.水分子间的氢键是一个水分子中氢原子与另一个水分子中的氧原子间形成的化学健B.与水反应时,增加水的用量可以明显加快化学反应速率C.纯碱溶液清洗油污时,加热可以增强其去污力D.向海水中加入净水剂明矾可以使海水淡化2.缺电子化合物是指电子数不符合路易斯结构(一个原子通过共用电子使其价层电子数达到8,H原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法错误的是( )A.NH3、BF3、CCl4中只有BF3是缺电子化合物B.BF3、CCl4中心原子的杂化方式分别为sp2、sp3C.BF3与NH3反应时有配位键生成D.CCl4的键角小于NH33.砷化氢(AsH3)是一种无色、可溶于水的气体,其分子构型是三角锥形。下列关于AsH3的叙述中正确的是A.AsH3分子中有未成键的电子对 B.AsH3是非极性分子C.AsH3是强氧化剂 D.AsH3分子中的As-H键是非极性键4.X、Y、Z、W、G五种短周期主族元素,其原子序数依次增大。已知Y、W同主族,Y的最外层电子数是Z的6倍,X和Z的质子数之和等于G的质子数。下列说法正确的是A.化合物WY2能使溴水褪色表现为漂白性B.G的简单阴离子比W的简单阴离子还原性强C.X、Y、W三种元素气态氢化物的沸点依次升高D.Z与W形成的化合物中可能含有共价键 5.HCHO与[Zn(CN)4]2-在水溶液中发生反应:,下列有关说法正确的是A.[Zn(CN)4]2-中存在共价健和离子键B.HCHO中碳原子以sp2的形式杂化C.CN-中的σ键和π键数目相同D.Zn 原子的3d能级中有空轨道6.M、N、W、K四种元素在元素周期表中的位置如图所示。已知W原子的最外层电子构型为nsnnp2n。则下列叙述正确的是( )MNW KA.四种元素的气态氢化物均为极性分子B.四种元素的单质一定只形成分子晶体C.四种元素原子的最外电子层上均有两种不同形状的电子云D.四种元素的最高正价数均等于它们的原子的最外层电子数7.下列有关物质性质、结构的表述均正确,且存在因果关系的是: 表述Ⅰ表述ⅡA在水中,NaCl的溶解度比I2的溶解度大NaCl晶体中Cl—与Na+间的作用力大于碘晶体中分子间的作用力B通常条件下,CH4分子比SiH4分子稳定性高Si的原子半径比C的大,Si与H之间的键能比C与H间的小C在形成化合物时,同一主族元素的化合价相同同一主族元素原子的最外层电子数相同DP4O10、C6H12O6溶于水后均不导电P4O10、C6H12O6均属于共价化合物8.钯的配合物离子可催化合成,反应过程如图所示。下列叙述错误的是( )A.是反应中间体B.催化合成总反应为C.反应过程中的成键数目保持不变D.存在反应 9.在乙烯分子中有5个σ键、一个π键,它们分别是( )。A.未杂化的sp2轨道形成σ键、杂化的2p轨道形成π键B.杂化的sp2轨道形成π键、未杂化的2p轨道形成σ键C.C-H之间是sp2形成的σ键,C-C之间有未参加杂化的2p轨道形成的π键D.C-C之间是sp2形成的σ键,C-H之间有未参加杂化的2p轨道形成的π键10.硫代硫酸钠(Na2S2O3)可作为照相业的定影剂,反应的化学方程式为:AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr。下列说法正确的是A.基态Br原子中电子的空间运动状态有35种 B.[Ag(S2O3)2]3-中含有离子键、共价键、配位键C.中心原子S的杂化方式为sp3 D.非金属元素S、O、Br中电负性最大的是Br11.中学化学中很多“规律”都有其适用范围, 下列根据有关“规律”推出的结论合理的是A.SO2 和湿润的 Cl2 都有漂白性, 推出二者混合后漂白性更强B.根据溶液的 pH 与溶液酸碱性的关系, 推出 pH=7.0 的溶液一定显中性C.由 F、 Cl、 Br、 I 非金属性依次减弱, 推出 HF、 HCl、 HBr、 HI 的还原性依次增强D.结构和组成相似的物质, 沸点随 相对分子质量增大而升高, 因此 NH3 沸点低于 PH312.二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法不正确的是( )A.二茂铁属于分子晶体B.在二茂铁结构中,C5H与Fe2+之间形成的化学键类型是离子键C.已知:环戊二烯的结构式为:,则其中仅有1个碳原子采取sp3杂化D.C5H中一定含π键13.下列关于CH3-C≡C-CH2-CH3的说法中正确的是( )A.分子中只有非极性键,没有极性键B.分子中所有的碳原子都在同一条直线上C.能发生加成反应D.不能发生取代反应14.阿伏加德罗常数的值约6.02×1023mol-1,下列叙述中错误的是( )① 12.4 g白磷晶体中含有的P-P键数是0.6×6.02×1023② 电解精炼铜时转移了6.02×1023个电子,阳极溶解 32 g铜③ 7.8 g Na2S和Na2O2的混合物中含有阴离子数大于0.1×6.02×1023④ 2 mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023⑤ 6.8 g熔融的KHSO4中含有0.1NA个阳离子⑥ 1.00 mol NaCl中,所有Na+的最外层电子总数为10×6.02×1023A.①②③④ B.③④⑤⑥ C.②③⑤⑥ D.③④⑥二、综合题15.某小组探究Cu与反应,发现有趣的现象。室温下,的稀硝酸(溶液A)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(见图)遇铜片立即产生气泡。回答下列问题:(1)探究溶液B遇铜片立即发生反应的原因。①假设1:_____________对该反应有催化作用。实验验证:向溶液A中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化。结论:假设1不成立。②假设2:对该反应有催化作用。方案Ⅰ:向盛有铜片的溶液A中通入少量,铜片表面立即产生气泡,反应持续进行。有同学认为应补充对比实验:向盛有铜片的溶液A中加入几滴的硝酸,没有明显变化。补充该实验的目的是_____________。方案Ⅱ:向溶液B中通入氮气数分钟得溶液C。相同条件下,铜片与A、B、C三份溶液的反应速率:,该实验能够证明假设2成立的理由是_________________。③查阅资料:溶于水可以生成和___________________。向盛有铜片的溶液A中加入,铜片上立即产生气泡,实验证明对该反应也有催化作用。结论:和均对Cu与的反应有催化作用。(2)试从结构角度解释在金属表面得电子的能力强于的原因________________。(3)Cu与稀硝酸反应中参与的可能催化过程如下。将ii补充完整。i.ii.______________________iii.(4)探究的性质。将一定质量的放在坩埚中加热,在不同温度阶段进行质量分析,当温度升至时,剩余固体质量变为原来的,则剩余固体的化学式可能为______________。16.本题包括A、B 两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。A.氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知:KCN+H2O2=KOCN+H2O,回答下列问题:(1)OCN-中所含三种元素的第一电离能从大到小的顺序为__________(用元素符号表示,下同),电负性从大到小的顺序为_______,基态氮原子外围电子排布式为______。(2)H2O2中的共价键类型为__(填“σ键”或“π键”),其中氧原子的杂化轨道类型为______;分子中4个原子_______(填“在”或“不在”)同一条直线下;H2O2易溶于水除它们都是极性分子外,还因为_______。(3)与OCN-键合方式相同且互为等电子体的分子为______(任举一例);在与OCN-互为等电子体的微粒中,由一种元素组成的阴离子是_______。B.四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂。实验室制备四碘化锡的主要步骤如下:步骤1:在干燥的圆底烧瓶中加入少量碎锡箔和稍过量的I2,再加入30mL冰醋酸和30mL醋酸酐[(CH3CO)2O]。实验装置如图所示,组装好后用煤气灯加热至沸腾约1-1.5h,至反应完成;步骤2:冷却结晶,过滤得到四碘化锡粗品;步骤3:粗品中加入30mL氯仿,水浴加热回流溶解后,趁热过滤;步骤4:将滤液倒入蒸发皿中,置于通风橱内,待氯仿全部挥发后得到四碘化锡晶体。回答下列问题:(1)图中仪器a的名称为____________;冷却水从接口___________(填“b”或“c”)进入。(2)仪器a上连接装有无水CaCl2的干燥管的目的是___________;锡箔需剪碎的目的是_______________;加入醋酸酐的目的是_______。(3)烧瓶中发生反应的化学方程式为________;单质碘需过量的主要目的是________。(4)反应已到终点的现象是________。(5)步骤3和步骤4的目的是________。17.三种常见元素结构信息如下表,试根据信息回答有关问题:元素ABC结构信息基态原子核外有两个电子层,最外层有3个未成对的电子基态原子的M层有1对成对的p电子基态原子核外电子排布为[Ar]3s104sx,有+1、+2两种常见化合价(1)写出B原子的基态电子排布式____________________;(2)用氢键表示式写出A的氢化物溶液中存在的氢键____________________(任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角____________________(填写“变大”、“变小”、“不变”);(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为____________________,简要描述该配合物中化学键的成键情况____________________;(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。在以上分子中,中心原子采用杂化形成化学键是____________________(填写序号);在②的分子中有____________________个键和____________________个键。18.大连理工大学彭孝军院士课题组报道了基于硼氟荧类荧光染料(BODIPY)的铜荧光探针的设计与应用,利用Cu2+诱导胺的氧化脱氢反应形成的Cu+配合物,进行Hela细胞中的Cu2+荧光成像和检测。其反应如下:回答下列问题:(1)在水溶液里,Cu2+比Cu+稳定,是由于水分子配体的作用。在气态时,Cu2+比Cu+________(填“稳定”或“不稳定”),原因是________________。(2)BODIPY荧光探针分子中,B原子的杂化方式为_______________,1molBODIPY分子中含有_______mol配位键,其分子中第二周期元素原子的第一电离能由大到小的顺序为________________。(3)磷锡青铜是有名的弹性材料,广泛用于仪器仪表中的耐磨零件和抗磁元件等。磷锡青铜晶胞结构如图所示。NA代表阿伏加德罗常数的值,铜、磷原子最近距离为0.5apm。①磷锡青铜的化学式为_______,铜与铜原子最近距离为_______pm。②磷青铜晶体密度为_______g∙cm-3(用代数式表示)。19.用湿法制磷酸副产品氟硅酸(H2SiF6 )生产无水氟化氢的工艺如下图所示:已知:氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于醇。在热水中水解成氟化钾、氟化氢及硅酸。(1)写出反应器中的化学方程式:(2)在实验室过滤操作中所用的玻璃仪器有: ;在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是: ;(3)该流程中哪些物质可以循环使用: (用化学式表达)(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6 ,试写出该反应方程式: ;(5)为了测定无水氟化氢的纯度,取标况下的气体产物2.24L,测得质量为3.1g,并将气体通入含足量的Ca(OH)2 溶液中,得到5.85gCaF2沉淀,则无水氢氟酸质量分数为: 。(保留2位有效数字)通过计算结果,试解释,为什么标况下2.24L产物的质量远远大于2.0g, 。
相关试卷
这是一份2022年高考化学一轮复习高频考点集训专题19 烃和卤代烃(2份打包,解析版+原卷版,可预览),文件包含2022年高考化学一轮复习高频考点集训专题19烃和卤代烃解析版doc、2022年高考化学一轮复习高频考点集训专题19烃和卤代烃原卷版doc等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。
这是一份2022年高考化学一轮复习高频考点集训专题17 电化学基础(2份打包,解析版+原卷版,可预览),文件包含2022年高考化学一轮复习高频考点集训专题17电化学基础解析版doc、2022年高考化学一轮复习高频考点集训专题17电化学基础原卷版doc等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
这是一份2022年高考化学一轮复习高频考点集训专题11 原子结构与性质(2份打包,解析版+原卷版,可预览),文件包含2022年高考化学一轮复习高频考点集训专题11原子结构与性质解析版doc、2022年高考化学一轮复习高频考点集训专题11原子结构与性质原卷版doc等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。








