

湖南省衡阳市第八中学2022-2023学年高一化学上学期期末考试试题(Word版附答案)
展开衡阳市八中2022级高一第一学期期末考试
化 学
请注意:时量75分钟 满分100分
可能用到的相对原子质量:H~1 C~12 O~16 Na~23 S~32 Fe~56 Cu~64
第Ⅰ卷 选择题
一、单选题(本题共10小题,每小题3分,共30分。每小题只有一个选项符合题意)
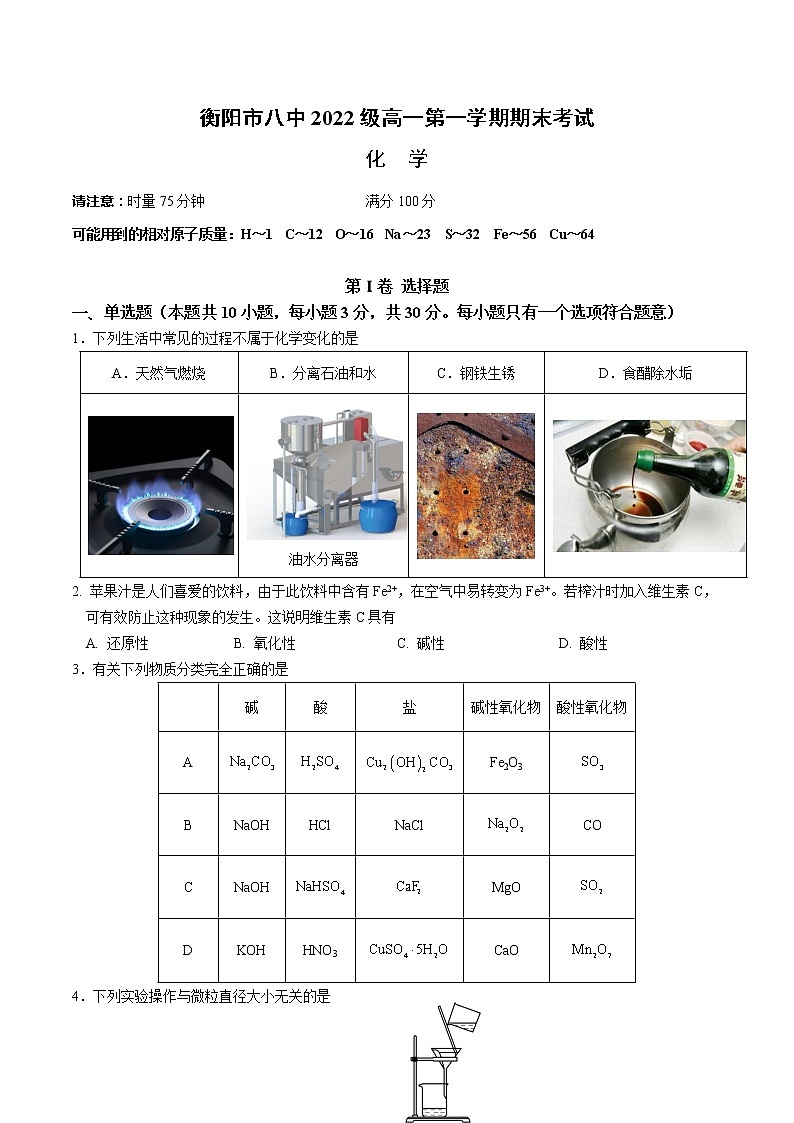
1.下列生活中常见的过程不属于化学变化的是
A.天然气燃烧 | B.分离石油和水 | C.钢铁生锈 | D.食醋除水垢 |
油水分离器 |
2. 苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,在空气中易转变为Fe3+。若榨汁时加入维生素C,可有效防止这种现象的发生。这说明维生素C具有
A. 还原性 B. 氧化性 C. 碱性 D. 酸性
3.有关下列物质分类完全正确的是
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Fe2O3 | ||||
B | NaOH | HCl | NaCl | CO | |
C | NaOH | MgO | |||
D | KOH | HNO3 | CaO |
4.下列实验操作与微粒直径大小无关的是
A.渗析 B.升华 C.过滤 D.验证丁达尔效应
5.下列化学用语描述正确的是
A.质量数为31的磷原子:
B. 硫离子结构示意图:
C.硫酸铁的化学式:FeSO4
D.KHSO4熔融状态下的电离方程式:KHSO4 = K+ + H+ + SO
6.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.碱性溶液中:Ca2+、Na+、HCO3-、NO3-
B.c(H+) = 1 mol/L的溶液中:Na+、Fe3+、NO3-、Cl-
C.无色溶液中:K+、H+、Cl-、Cu2+
D.加入适量酸性KMnO4的溶液中:Fe2+、NO3-、Cl-、SO42-
7.下列反应的离子方程式书写正确的是
A.向次氯酸钠溶液中通入少量二氧化碳气体:2ClO-+CO2+H2O = 2HClO+CO2- 3
B.铁锈溶于稀硫酸:Fe2O3 + 6H+ = 2Fe3+ + 3H2O
C.用FeCl3溶液制备Fe(OH)3胶体:Fe3+ + H2O = Fe(OH)3↓ + 3H+
D.将铜片插入硝酸银溶液中:Cu + Ag+ = Cu2+ + Ag
8.每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的一种写法为6:02 10/23,
外观与阿伏加德罗常数近似值6. 02 ×1023相似。用NA代表阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,18 g水所占的体积约为22.4 L
B.1 mol OH- 中含有电子的数目为10 NA
C.0.1 mol FeCl3·6H2O加入沸水中完全反应生成胶体的粒子数为0.1 NA
D.将22.4 L HCl配成1 L溶液,c(H+)为1 mol/L
9.已知(CN)2的性质与卤素单质相似,下列关于(CN)2的性质推测不合理的是
A.(CN)2属于化合物 B.AgCN难溶于水
C.(CN)2具有强还原性 D.(CN)2+ H2O ⇋HCN + HOCN
10.为了防止枪支生锈,常采用化学处理使钢铁零件表面生成Fe3O4的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:。下列有关叙述不正确的是
A.的氧化性大于的氧化性
B.反应中转移电子2 mol,则生成还原产物0.5 mol
C.枪支“发蓝”实质上是使铁表面钝化导致难以生锈
D.上述反应中,单质铁被氧化,而NaNO2作为氧化剂
二、不定项选择题(本题共4小题,每小题4分,共16分。每小题有一个或两个选项符合题意,全部选对的得4分,选对但不全的得2分,有选错的得0分)
11.铯是制造光电管的主要材料,铯元素的部分信息如右图所示。
下列关于铯的说法中,不正确的是
A.原子序数为55 B.CsOH是一种弱碱
C.相对原子质量是132.9 g·mol-1 D.铯是ⅠA族元素
12.为增强口罩的密封性,均放了鼻梁条,有的鼻梁条是铝合金的,关于铝合金的说法正确的是
A.铝合金属于纯净物
B.鼻梁条使用铝合金,利用其密度大、抗腐蚀性好的优点
C.铝合金属于金属材料
D.铝合金的熔点比金属铝低
13.某实验小组通过下图所示实验,探究Na2O2与水的反应:
下列说法错误的是
A.②中,大量气泡的主要成分是H2
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有漂白性物质造成的
D.⑤中MnO2的主要作用是作催化剂
14.部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:
下列说法不正确的是
A.样品中Fe元素的质量为2.24 g B.V<896
C.参与反应的n(H2SO4) = 0.04 mol D.滤液A中的阳离子为Fe2+、Cu2+、H+
第Ⅱ卷 非选择题
三、填空题(每空2分,本题共14分)
15. 请根据题意回答下列问题:
(1) 对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
①现有下列9种微粒:、、、、、、、、。
其中,核素有___________种,涉及到的元素有___________ 种。
②现有以下物质:
①稀盐酸 ②Cl2 ③BaSO4固体 ④NaOH溶液 ⑤熔融的NaHSO4 ⑥CO2 ⑦铝条 ⑧蔗糖
以上物质中属于电解质的是___________(填标号,下同),属于非电解质的是___________。
(2)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相。对月壤中化学元素的分析有助于认识月球表面环境。元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如下:
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| b |
|
|
|
|
|
|
|
|
|
|
|
| c | d |
|
|
e | f |
|
|
|
|
|
|
|
|
|
|
| g | h | i |
|
|
j |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
①月壤中含有大量的g元素,g在周期表中的位置为____________________;
②g、h、i三种元素的气态氢化物最稳定的是_________(用化学式表示);
③根据元素周期律,请你试着写出j元素所对应的单质与a和d元素所形成的简单化合物反应的离子方程式:__________________________。
四、工业流程题(每空2分,本题12分)
16. 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。
(1)根据上述流程图,写出过程 Ⅰ 的化学方程式______________________________。
(2)生产过程中,可循环利用的物质是__________、__________(填化学式)。
(3)在工业生产中,需在饱和食盐水中通入NH3和CO2,建议先通入气体是___________(填名称)。
(4)制得的纯碱样品表面可能附着有NaCl、NH4Cl等杂质。检验该样品中是否含有氯离子杂质的操作方法是______________________________________________________________。
(5)取8.2g制得的纯碱样品,充分溶解后再加入足量稀硫酸,得到3.3g CO2(CO2全部逸出)。则样品中纯碱的质量分数为_______%(计算结果保留两位小数)。
五、推断题(每空2分,本题共14分)
17. 某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出,所用试剂均足量),其中X是氨水,I为红褐色沉淀。
请回答下列问题:
(1)F的化学式为_________,J的化学式为_________;
(2)D→E的离子方程式为________________________________;
(3)H→I的化学方程式为_________________________________,现象为_______________________;
(4)B和水蒸气反应的化学方程式为__________________________________;
(5)证明某溶液中不含,而可能含有,进行如下实验操作的最佳顺序为 。
①加入适量氯水 ②加入足量溶液 ③加入少量溶液
A.①③ B.②③ C.③① D.③①②
六、实验题(每空2分,本题14分)
18. 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
(1)写出实验室制取氯气的化学方程式:____________________________________________________;
(2)装置D的作用是_________________;
(3)E中红色布条是否褪色(填“是”或“否”)_______,F中的反应产物化学式为_______;
(4)若H处溶液为KI与KOH的混合液,充分反应后会生成KCl和KIO3,试写出H处所发生反应的离子反应方程式并用双线桥标出电子转移情况:_______________________________________________________________________;
(5)某兴趣小组在实验中发现浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。对用稀盐酸实验没有氯气生成的原因,兴趣小组经讨论后有如下猜想:
猜想一:小明认为是c(H+)低导致。
猜想二:小红认为是_______低导致。
小组设计了以下实验方案进行验证:
a.稀盐酸滴入MnO2中,然后通入HCl气体加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸加热
d. MnO2与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、MnO2固体共热
实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。
由此可知猜想_______成立。
衡阳市八中2022级高一第一学期期末考试
化学参考答案
一、单选题(本题共10小题,每小题3分,共30分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | B | A | D | B | A | B | B | B | C | B |
二、不定项选择题(本题共4小题,每小题4分,共16分。每小题有一个或两个选项符合题意,全部选对的得4分,选对但不全的得2分,有选错的得0分)
题号 | 11 | 12 | 13 | 14 |
答案 | BC | CD | AB | D |
三、填空题(每空2分,本题14分)
15.(1)5,5 ; ③⑤ ,⑥⑧。
(2)①第三周期第ⅣA族; ②H2S; ③2K+2H2O == 2K++2OH-+H2↑
四、工业流程题(每空2分,本题12分)
16.(1) NH3 + CO2 + NaCl + H2O == NaHCO3↓+ NH4Cl
(2)CO2 、 NaCl ; (3)氨气(写化学式不给分)
(4)取少量样品于试管中,加入足量稀硝酸酸化,再加入2~3滴溶液,若有白色沉淀产生,说明存在杂质,反之,则不存在。
(5)96.95(未精确到小数点后两位不给分) ;
五、推断题(每空2分,本题14分)
17.(1)Al2O3 , Fe2O3 ; (2)Al3+ + 3NH3·H2O == Al(OH)3↓ + 3NH ;
(3)4Fe(OH)2+O2+2H2O == 4Fe(OH)3 ;
现象:白色沉淀迅速变成灰绿色,最后变成红褐色。
(4)3Fe + 4H2O(g)Fe3O4 + 4H2 。 (5)C
六、实验题(每空2分,本题14分)
18.(1) MnO2 + 4HCl(浓) MnCl2 + Cl2↑ + 2H2O 。 (2)干燥氯气/吸收氯气中水蒸气。
(3) 否 ;CuCl2
(4) (5)c(Cl-) ; 一
湖南省衡阳市第八中学2022-2023学年高一化学上学期第一次月考试题(Word版附解析): 这是一份湖南省衡阳市第八中学2022-2023学年高一化学上学期第一次月考试题(Word版附解析),共16页。试卷主要包含了可能用到的相对原子质量, 下列物质所含分子数最多的是,2 ml H2B等内容,欢迎下载使用。
湖南省长沙市长郡中学2022-2023学年高一化学下学期期末考试试题(Word版附答案): 这是一份湖南省长沙市长郡中学2022-2023学年高一化学下学期期末考试试题(Word版附答案),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
湖南省衡阳市2022-2023学年高一化学下学期期末联考试题(Word版附答案): 这是一份湖南省衡阳市2022-2023学年高一化学下学期期末联考试题(Word版附答案),共10页。试卷主要包含了氮及其化合物的转化具有重要应用,下列说法不正确的是等内容,欢迎下载使用。












