




人教版 (2019)必修 第二册第一节 硫及其化合物教案配套课件ppt
展开
这是一份人教版 (2019)必修 第二册第一节 硫及其化合物教案配套课件ppt,共26页。PPT课件主要包含了酸硫浓,知识回顾,---稀硫酸,H2SO4,SO42-+2H+,酸的通性,4与某些盐反应,硫酸的物理性质,浓硫酸的特性,吸水性等内容,欢迎下载使用。
硫酸(H2SO4)-------现代工业之母 硫酸在化学、冶金、医药、染料等有极为广泛的应用。 生产10t青霉素要消耗2.5t硫酸,生产1t有机玻璃要消耗3t硫酸,生产1kg金属锆,要消耗20t硫酸。 有人称硫酸是化学工业生产的“发动机”。世界上常把硫酸的产量作为衡量一个国家工业发达程度的标志。
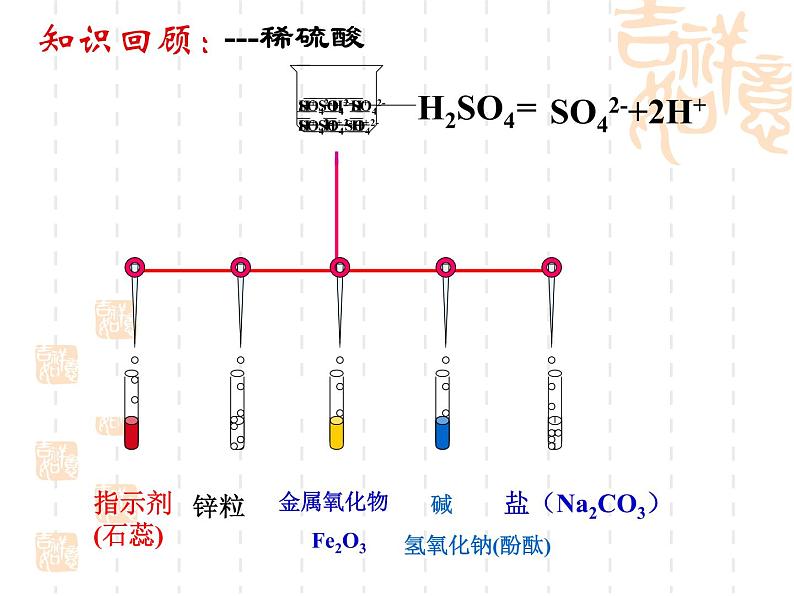
(1)与活泼金属反应生成盐和氢气
(2)与金属氧化物反应生成盐和水
(3)与碱反应生成盐和水
(5)使酸碱指示剂变色
Zn + 2H+ = Zn2++H2↑
Fe2O3 + 6H+ = 2Fe3+ + 3H2O
H+ + OH- = H2O
CO32- + 2H+ = CO2 ↑ + H2O
1、纯硫酸是无色粘稠的油状液体(常用的浓硫酸质量分数为98.3%)。
2、纯硫酸难挥发,沸点338℃(高沸点酸).
3、密度:质量分数为98.3%的硫酸的密度为1.84g/cm3 (高密度酸).
4、能以任意比与水混溶
(浓硫酸溶解时放出大量的热)
思考:如何稀释浓硫酸?
将浓硫酸沿着容器内壁(或沿着玻璃棒)缓慢地注入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散。
扩展: 将浓硫酸与其它低密度的液体混合时,方法与硫酸在水中的溶解方法相同.
“酸入水,沿器壁,慢慢倒,不断搅
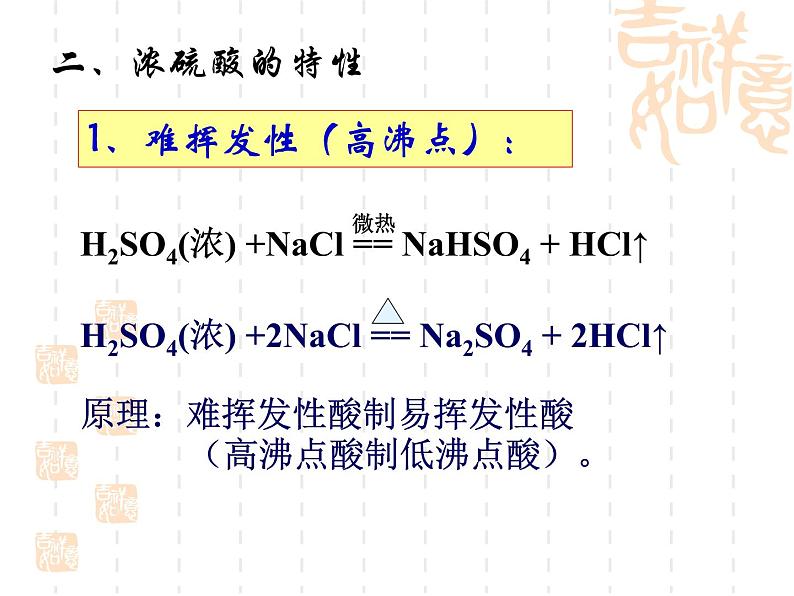
1、难挥发性(高沸点):
原理:难挥发性酸制易挥发性酸 (高沸点酸制低沸点酸)。
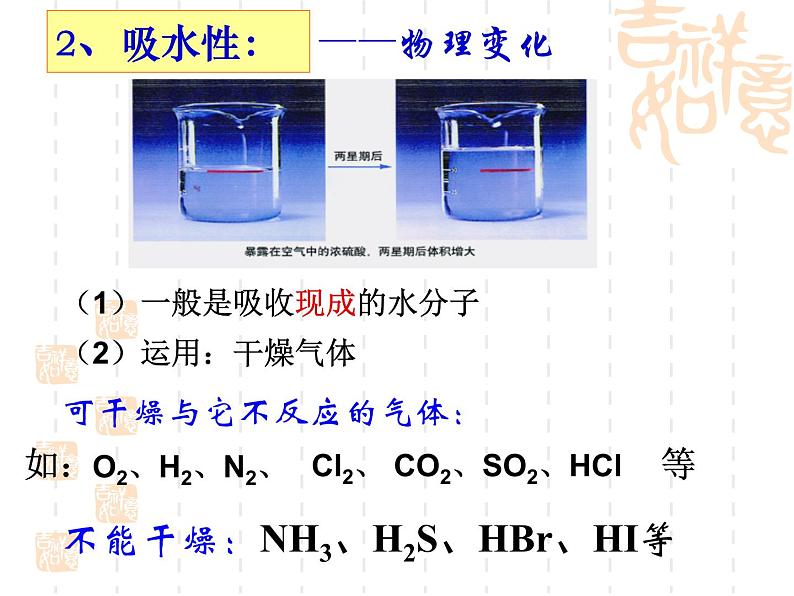
(1)一般是吸收现成的水分子
不能干燥:NH3、H2S、HBr、HI等
可干燥与它不反应的气体:
1、下列不能用浓硫酸干燥的气体是 ( ) ①Cl2 ② O2 ③ SO2 ④ H2 ⑤ HCl ⑥NH3 ⑦ CO2
2、实验室常用浓盐酸跟浓硫酸混合来快速简易制取HCl气体,请简述原因。
脱水性:浓硫酸能把有机物中的氢氧原子按2:1的个数比(H2O)脱去或脱去结晶水合物中的结晶水。
实验:将浓硫酸慢慢加入蔗糖中,并用玻璃棒搅拌
现象:蔗糖变黑,体积膨胀,变成疏松多孔的海绵状,并放出有刺激性气味的气体
——称此过程为“炭化”
1、烧杯壁为什么是热的?
3、为什么体积会膨胀?
5、这一过程表现了浓硫酸的什么性质?
4、刺激性气味气体可能含什么?
2、为什么蔗糖会变黑?
吸水性、脱水性、强氧化性
1、把少量浓硫酸滴在纸片或火柴梗上,有什么现象?
2、把少量浓硫酸滴在pH试纸上,有什么现象?
A、常温下, Fe、Al 在浓硫酸中会发生钝化
B、加热时,浓硫酸能与大多数金属反应(Au、Pt除外) ,一般没有氢气生成,通常生成SO2气体。
——体现了硫酸的酸性和氧化性
现象:加热,产生气体使品红溶液褪色,紫色石蕊溶液变红,溶液稀释后呈蓝色。
思考:在含1mlH2SO4的浓硫酸中加入足量的铜粉,完全反应后可生成标准状况下SO2 L
Zn + H2SO4(稀)= ZnSO4+ H2 Cu + 2H2SO4(浓)== CuSO4 + 2H2O+SO2
0 +1 +2 0
0 +6 +2 +4
H+表现的氧化性(酸的通性),通常称“酸的氧化性”,浓硫酸中+6价的硫表现的氧化性,通常称“氧化性酸”
(2)与某些非金属的反应,如C、S、P等:
——体现了硫酸的氧化性
★蔗糖与浓硫酸的实验过程中:体现了浓硫酸的吸水性、脱水性和强氧化性。
(3)与某些还原剂反应
如何用实验方法证明木炭与浓硫酸反应的产物?
⑴用何试剂检验H2O、SO2、CO2?
⑵三种产物检验有先后吗?
1、高沸点——制取挥发性酸。2、吸水性——做干燥剂。3、脱水性——做催化剂。4、酸性——去金属表面的氧 化物、制取硫酸盐、制造化肥。5、强氧化性——制炸药。
你如何区别稀硫酸和浓硫酸?
一、浓硫酸的物理性质
(1)浓硫酸可作气体干燥剂____(2)浓硫酸不能干燥氨气____(3)浓硫酸不能干燥H2S____(4)实验室用浓硫酸和氯化钠固体制HCl____(5)浓硫酸不能制取HI____(6)实际生产中,浓硫酸可用钢瓶储运____(7)浓硫酸与金属铜的反应____(8)浓硫酸使蔗糖变黑,并有刺激性气味气体产生(9)敞口放置于空气中的浓硫酸会增重____
1、浓硫酸有以下性质:A.酸性、B.强氧化性、C.难挥发性、D.吸水性、E.脱水性
2、在试管中加入一块Cu片,注入一定量的浓硫酸,对试管加热充分反应后,(1)若Cu片还有剩余,H2SO4是否消耗完 ________(填是或否),其理由是______________________________________________________________________________(2)若用足量锌代替铜,硫酸是否消耗完________(填是或否),其理由是____________________________________________
随着反应的进行,硫酸浓度变小,一旦变为稀硫酸,反应就停止
锌与浓硫酸,稀硫酸都反应
相关课件
这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物图片ppt课件,共25页。PPT课件主要包含了与水反应,分类酸性氧化物,2SO2化学性质,与碱反应,与碱性氧化物反应,体现较强还原性,3应用,4小结,⑶杀灭霉菌和细菌,⑴制造硫酸等内容,欢迎下载使用。
这是一份5.1硫及其化合物——2022-2023学年高中化学学业水平复习课件(人教版2019必修二),共41页。PPT课件主要包含了硫化物,硫酸盐,有机物,硫的存在,硫的物理性质,硫的化学性质,硫的用途,二氧化硫,二氧化硫的用途,硫酸的工业制法等内容,欢迎下载使用。
这是一份高中人教版 (2019)第一节 硫及其化合物教学ppt课件,共41页。PPT课件主要包含了知识回顾,排除碳酸根离子的干扰,硫酸根离子的检验,生成白色,不溶解,淀不溶解,沉淀溶,解且有气泡,白色沉淀,实验5-4等内容,欢迎下载使用。










