

所属成套资源:安徽省桐城市某中学2022-2023学年高二各学科上学期月考(1)试卷(Word版附解析)
安徽省桐城市某中学2022-2023学年高二化学上学期月考(1)试卷(Word版附解析)
展开
这是一份安徽省桐城市某中学2022-2023学年高二化学上学期月考(1)试卷(Word版附解析),共24页。
高二化学试卷
1. 化学与生产生活息息相关,下列说法不正确的是( )
A. 泡沫灭火器喷出的主要物质是和
B. 长期使用作化肥会使土壤酸化
C. 电解饱和食盐水可以得到金属钠和氯气
D. 合成氨工业中,将及时液化分离有利于提高反应物的利用率
2. 下列有关电解质电离过程的叙述不正确的是( )
A. NaCl溶于水破坏了离子键
B. HCl溶于水破坏了共价键
C. 溶于水促进了水的电离
D. 在水中的电离方程式为
3. 下列说法正确的是( )
A. 图1为放热反应,放热反应不需要加热就能反应
B. 图2为吸热反应,分解反应均为吸热反应
C. 反应热描述的是化学反应前后的热量变化,任何化学反应都有反应热
D. 同温同压下,反应在光照和点燃条件下的不同
4. 实验测得:101kPa时,完全燃烧生成液态水,放出的热量;完全燃烧生成液态水和,放出的热量。下列热化学方程式书写正确的是( )
A.
B.
C.
D.
5. 化学反应的方向问题对于理论研究与生产实践都有及其重要的意义,下列有关化学反应方向的判断不正确的是( )
A. ,的反应在温度低时不能自发进行
B. 某吸热反应能自发进行,因此该反应是熵增反应
C. Na与的反应是熵增的放热反应,该反应能自发进行
D. 在常温下能自发进行,则该反应的
6. 一定条件下,在密闭恒容的容器中,发生反应:⇌,能表示该反应达到平衡状态的是( )
A.
B.
C. 混合气体密度保持不变
D. :::3:6
7. 铁的配合物离子用表示催化某反应的一种反应机理如图所示,下列说法不正确的是( )
A. 该过程的总反应为
B. 增大浓度有利于反应速率加快
C. 增大浓度有利于反应速率加快
D. 该催化循环中Fe元素的化合价发生了变化
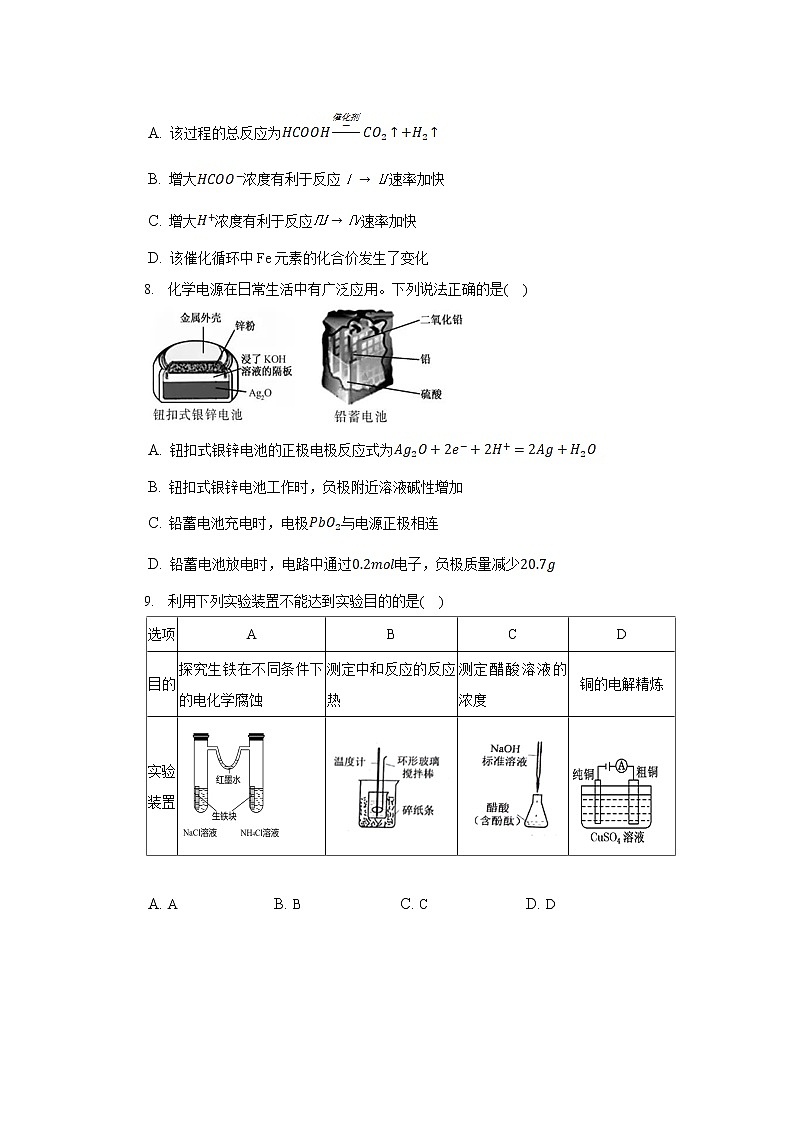
8. 化学电源在日常生活中有广泛应用。下列说法正确的是( )
A. 钮扣式银锌电池的正极电极反应式为
B. 钮扣式银锌电池工作时,负极附近溶液碱性增加
C. 铅蓄电池充电时,电极与电源正极相连
D. 铅蓄电池放电时,电路中通过电子,负极质量减少
9. 利用下列实验装置不能达到实验目的的是( )
选项
A
B
C
D
目的
探究生铁在不同条件下的电化学腐蚀
测定中和反应的反应热
测定醋酸溶液的浓度
铜的电解精炼
实验装置
A. A B. B C. C D. D
10. 已知:⇌,向一恒温恒容的密闭容器中充1molA和3molB发生反应,时达到平衡状态I,在时改变某一条件,时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( )
A. 时改变的条件:向容器中加入C B. 容器内压强不变,表明反应达到平衡
C. 平衡时A的体积分数: D. 平衡常数K:
11. 2022年北京冬奥会火炬的主要燃料是氢气。利用太阳能光伏电池电解水制高纯氢的工作示意图如下,通过控制开关连接或,可交替得到和。下列有关说法错误的是( )
A. 制时,连接开关
B. 产生的电极反应式是
C. 制时,电极3的电极反应式为
D. 连接或时,电极3分别作为阴极材料和阳极材料,并且NiOOH和相互转化提供电子转移
12. 一定条件下,关于工业合成氨的反应,图甲表示该反应过程中的能量变化,图乙表示1L密闭容器中随时间的变化曲线,图丙表示在其他条件不变的情况下,改变起始时对该平衡的影响。下列说法正确的是( )
A. 甲:升高温度,该反应的平衡常数增大
B. 乙:从起其他条件不变,压缩容器的体积,则的变化曲线为d
C. 乙:内该反应的平均速率
D. 丙:温度,a、b、c三点所处的平衡状态中,b点的转化率最高
13. 常温下,下列有关电解质溶液的说法不正确的是( )
A. 向溶液中通入,减小
B. 将的溶液从升温至,增大
C. 向的HF溶液中滴加NaOH溶液至中性,
D. 向的溶液中加入少量水,增大
14. 某小组探究溶液能否鉴别和溶液时,进行如图所示实验。下列说法中正确的是( )
A. 加入溶液前两溶液的pH:
B. 加入溶液前两溶液中离子种类及浓度完全相同
C. 加入溶液后生成的沉淀的量:
D. 加入溶液后溶液中生成沉淀的方程式为
15. 为了探究外界条件对氯化铵水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
实验
温度
pH
1
5
25
x
2
5
30
y
3
5
25
z
下列说法不正确的是( )
A. 由可知:升高温度能促进氯化铵的水解
B. 由可知:增大盐的浓度,水解平衡正向移动,水解程度增大
C. 由可知:稀释氯化铵溶液,水解平衡正向移动
D. 与的关系为: 为水的离子积常数
16. 用盐酸滴定溶液,溶液中、、的分布分数随pH变化曲线及滴定曲线如图。下列说法不正确的是【如分布分数:】( )
A. 的为 B. c点:
C. 第一次突变,可选酚酞作指示剂 D.
17. 根据已学物质结构与性质的有关知识,回答下列问题:
请写出第三周期元素中p轨道上有3个未成对电子的元素符号:______,某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是,该元素的名称是______.
根据价层电子对互斥理论推测下列离子或分子的空间立体构型:______,______.
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关反应的离子方程式______、______.
金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为______;若两种晶体中最邻近的铁原子间距离相同,则体心立方晶胞和面心立方晶胞的密度之比为______.
18. 在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
下列状态的镁中,电离最外层一个电子所需能量最大的是 ______填标号。
乙二胺是一种有机化合物,分子中氮的杂化类型分别是 ______。乙二胺能与等金属离子形成稳定环状离子,其原因是 ______。
一些氧化物的熔点如下表所示:
氧化物
MgO
熔点
1570
2800
解释表中氧化物之间熔点差异的原因 ______。
原子晶体GaAs的晶胞参数,它的晶胞结构如图所示。该晶胞内部存在的共价键数为 ______;A原子距离B原子所在六面体的侧面的最短距离为______用x表示;该晶胞的密度为 ______。阿伏加德罗常数用表示。
19. 是一种食品添加剂,还是重要的漂白剂和抗氧化剂,也是导致酸雨的重要物质。工业常用足量氨水吸收处理尾气。根据相关信息回答下列问题。
下列操作能使氨水溶液中的电离程度增大的是______填字母序号,下同,能使电离常数增大的是______。
A.通少量氨气
B.降低温度
C.加水稀释
D.升高温度
E.加少量的固体
已知:常温下,常温下,的水溶液中由水电离出的______填“>”、“”、“;=;
①用NaOH标准溶液滴定溶液,指示剂是无色酚酞,达到滴定终点的标志是当滴入最后一滴标准液时,锥形瓶内溶液由无色变为浅红色且30s内不褪色,
故答案为:>;=;
②读数时,若滴定前平视液面,滴定后俯视液面,NaOH标准溶液体积偏小,则对滴定结果的影响是偏低,
故答案为:偏低;
③由表知,,根据可知的质量为:,该葡萄酒中的二氧化硫含量为:,
故答案为:。
20.【答案】 抑制水解,增大的浓度,使充分转化为沉淀析出
【解析】解:已知中N为价、H为价、O为价,结合正负化合价代数和为0可知Mo的化合价为,
故答案为:;
“浸出”转化为的离子方程式:,
故答案为:;
和FeS的分别为和,则,,越小的越先沉淀,则先生成沉淀;要使浓度小于,则浓度大于,要使浓度小于,则浓度大于,综述:,时,,,综上所述,为了使溶液中的杂质离子浓度小于,应控制溶液的pH不小于,
故答案为:;;
溶液中加入适量将其氧化为,则氧化剂为,还原产物为价的O,还原剂为,氧化产物为,反应的离子方程式为,
故答案为:;
由流程可知“沉淀”时,产生的沉淀为,因此加入的目的是提供,使充分转化为沉淀析出,加入的目的是抑制水解,增大的浓度,使充分转化为沉淀析出,
故答案为:抑制水解,增大的浓度,使充分转化为沉淀析出。
21.【答案】降低温度或增大压强 40
【解析】解:①在水中溶解度随着温度的升高而减小,随着压强的增大而增大,则增大在水中溶解度的措施有降低温度、增大压强等,
故答案为:降低温度或增大压强;
②与反应生成,电离方程式为⇌,⇌,则溶液中存在的电荷守恒关系为,
故答案为:>;
①由图可知,随着横坐标增大,升高温度,反应a、b的和值均增大,反应c的和值随着温度的升高而减小,说明升高温度,反应a、b平衡正向移动,反应c的平衡逆向移动,则反应a、b的正反应为吸热反应,反应c的正反应为放热反应,
故答案为:c;
②反应c为⇌,其相对压力平衡常数表达式为,
故答案为:;
③设原料中,初始总压为100kPa,初始压强为50kPa,即该条件下amol气体产生的压强为50kPa,体系达到平衡时的平衡转化率为,则平衡时,由于恒温恒容条件下气体的压强之比等于其物质的量之比,所以产生的压强,图中A点对应温度下反应b的,即,,即的分压,
故答案为:40。
相关试卷
这是一份安徽省滁州市2022-2023学年滁州中学高二上学期期中化学试卷(Word版附解析),共19页。试卷主要包含了6是因为, 反应过程中的能量变化如图所示, 过渡态理论认为, 已知25℃物质的溶度积常数为, 下列说法正确的是等内容,欢迎下载使用。
这是一份2021-2022学年安徽省桐城市桐城中学高二下学期月考(二十一)化学试题(Word版),共12页。试卷主要包含了单选题等内容,欢迎下载使用。
这是一份2021-2022学年安徽省桐城市桐城中学高二下学期月考(二十四)化学试题(Word版),共10页。试卷主要包含了单选题等内容,欢迎下载使用。









