
湖南省临澧县2022-2023学年高二上学期期末考试化学试卷(Word版含答案)
展开临澧县2022-2023学年高二上学期期末考试
化学
时量:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cu-64 Fe-56
一、单项选择题(本大题共10题,每题只有一个正确答案,每小题3分,共30分)
1. 下列有关热化学方程式的叙述正确的是
A. 已知,则金刚石比石墨稳定
B. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
C. 甲烷的燃烧热为,则甲烷燃烧的热化学方程式可表示为
D. 已知,则含稀溶液与稀醋酸完全中和,放出小于的热量
2. 下列说法正确的是
A. 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
B. 用加热的方法就可以除去KCl溶液中的Fe3+
C. 洗涤油污常用热的Na2CO3溶液,这是利用了盐类水解的原理
D. 将AlCl3溶液和Na2SO3溶液分别加热蒸干、灼烧后,所得固体为Al2O3和Na2SO3
3. 对下列现象或事实的解释错误的是
选项 | 现象或事实 | 解释 |
A | 明矾可用于生活用水净化 | 胶体具有杀菌消毒的作用 |
B | 用铁罐贮存浓硝酸 | 常温下铁在浓硝酸中钝化 |
C | 用氯化铁溶液蚀刻覆铜线路板 | 的氧化性比的强 |
D | 漂白粉在空气中久置变质 | 与、反应,生成的分解 |
A. A B. B C. C D. D
4. 下列说法不正确是(已知:)
A. 的溶液一定是中性
B. 大的酸溶液中一定比小的酸溶液中大
C. 将的盐酸和的硫酸等体积混合(混合后体积变化不计),所得溶液
D. 常温下,某溶液中由水电离出时,此溶液的或者3
5. 实验室用标准KMnO4溶液滴定未知浓度的FeSO4溶液,下列说法或操作正确的是
A. 盛FeSO4溶液的锥形瓶滴定前用FeSO4溶液润洗2~3次
B. 选碱式滴定管盛放标准KMnO4溶液,并用碘化钾淀粉溶液作指示剂
C. 锥形瓶内溶液颜色变化由黄色变浅紫色,立即记下滴定管液面所在刻度
D. 滴定后俯视读数会导致滴定结果偏低
6. 在一定的温度和压强下,将按一定比例混合的和通过装有催化剂的反应器可得到甲烷。已知:
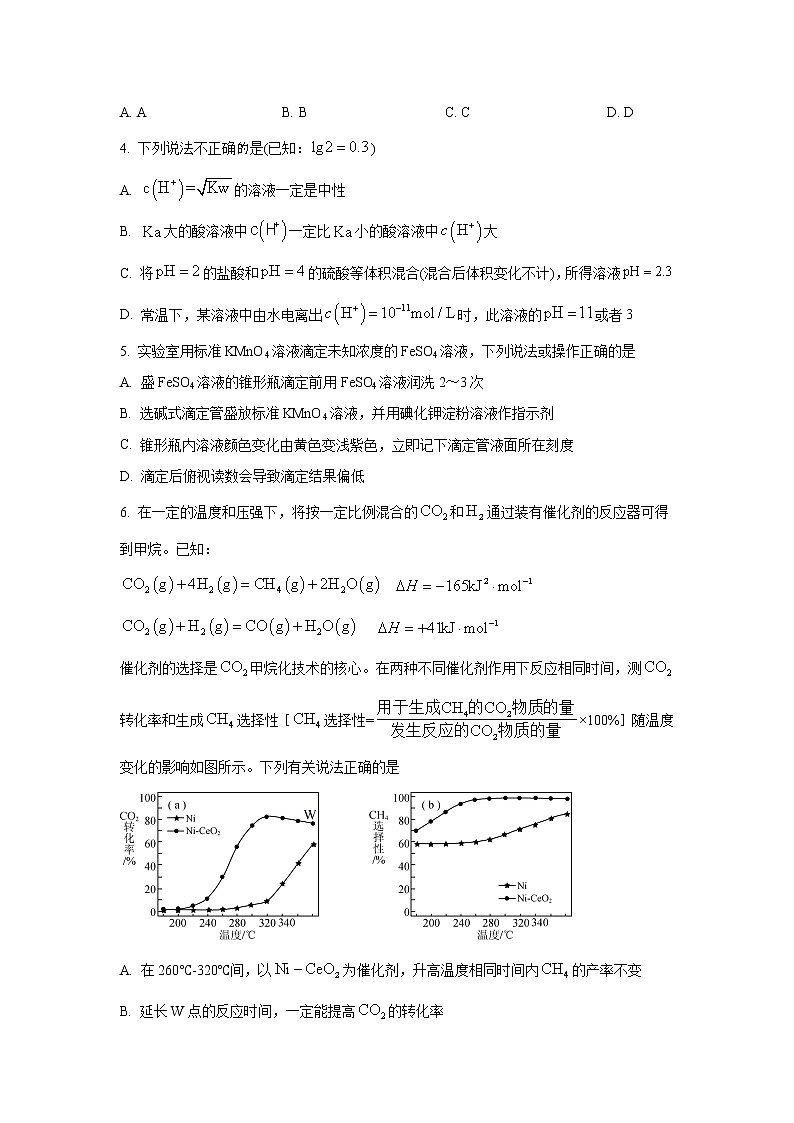
催化剂的选择是甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测转化率和生成选择性[选择性=×100%]随温度变化的影响如图所示。下列有关说法正确的是
A. 在260℃-320℃间,以为催化剂,升高温度相同时间内的产率不变
B. 延长W点的反应时间,一定能提高的转化率
C.
D. 高于320℃后,以Ni为催化剂,随温度的升高转化率上升的原因是催化剂活性增大,反应速率加快
7. 下列各项关系中正确的是
A. 已知NaHSO3溶液显酸性,则溶液中c()<c(H2SO3)
B. 0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合后溶液中存在:c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH)
C. 常温下pH=2的稀硫酸与pH=12的氨水等体积混合后溶液呈碱性
D. 等浓度的溶液①NH4Cl,②(NH4)2SO4,③NH4HSO4中c(NH4+)大小关系为②>①>③
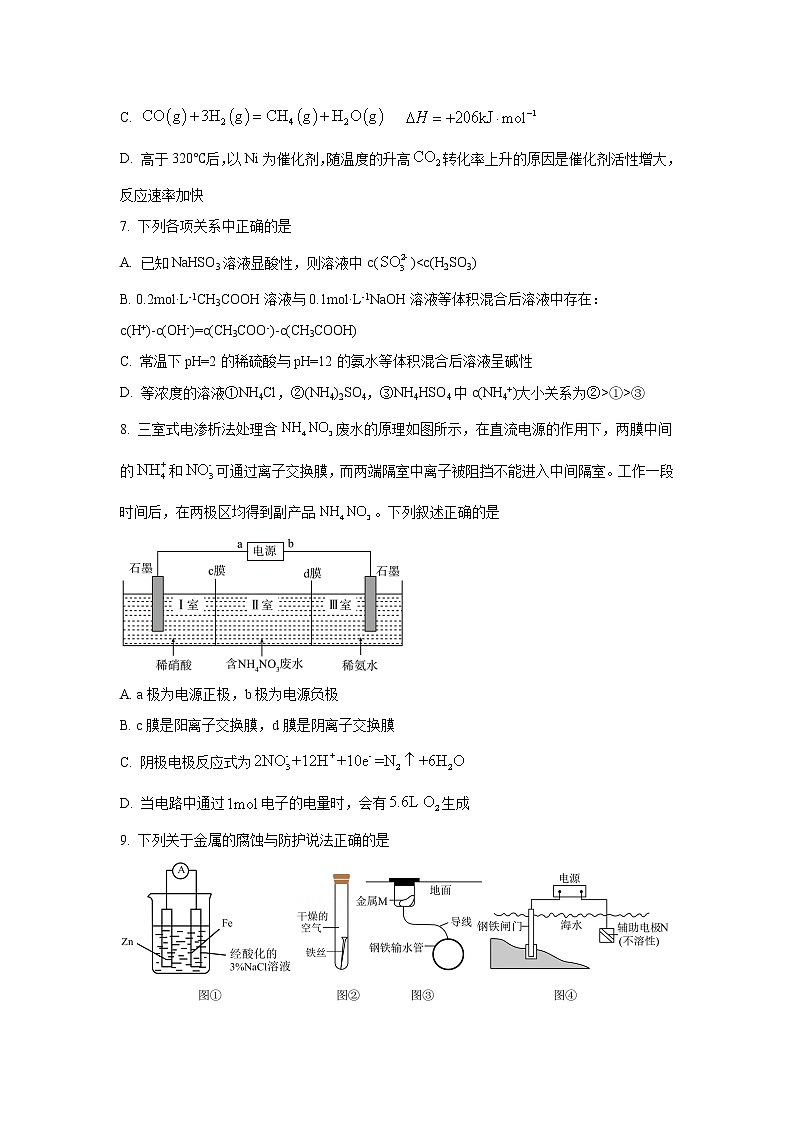
8. 三室式电渗析法处理含废水的原理如图所示,在直流电源的作用下,两膜中间的和可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。工作一段时间后,在两极区均得到副产品。下列叙述正确的是
A. a极为电源正极,b极为电源负极
B. c膜是阳离子交换膜,d膜是阴离子交换膜
C. 阴极电极反应式为
D. 当电路中通过电子的电量时,会有生成
9. 下列关于金属的腐蚀与防护说法正确的是
A. 图①中往Fe电极区滴入2滴K3[Fe(CN)6],产生蓝色沉淀
B. 图②中铁丝容易生成Fe2O3·xH2O
C. 图③中M可用石墨代替
D. 图④中若电源断开,闸门易发生吸氧腐蚀
10. 四种短周期主族元素X、Y、Z、W的原子序数依次增大,其中X是元素周期表中原子半径最小的元素;Y元素基态原子的最外层有1个未成对电子,次外层有2个电子;Z元素原子最高能级的不同轨道都有电子,且自旋方向相同;W元素原子的价层电子排布式是nsnnp2n。下列说法正确的是
A. 氢化物的稳定性:一定有Z<W
B. 同周期中第一电离能小于Z的有5种
C. Y、Z的最高价氧化物对应的水化物为强酸
D. X、Z可形成Z2X4,该分子中所有原子均满足8e﹣稳定结构
二、不定项选择题(本大题共4题,每题有一个或两个正确答案,每小题4分,共16分)
11. 下列实验操作与实验目的或结论一致的是
选项 | 实验操作 | 实验目的或结论 |
A | 将0.1 mol/LNa2CO3溶液滴入BaCl2溶液至不再有沉淀产生,再滴加0.1 mol/LNa2SO4溶液,无明显现象 | 证明Ksp(BaSO4)>Ksp(BaCO3)
|
B | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液,前者溶液变蓝色,后者有黄色沉淀 | 证明KI3溶液中存在I3-I2+I-平衡 |
C | 向NaAlO2溶液中持续通入气体Y,先出现白色沉淀,最终沉淀又溶解 | Y可能是CO2气体 |
D | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 证明氧化性:H2O2比Fe3+强 |
A. A B. B C. C D. D
12. 用CO还原可减轻汽车尾气对空气的污染,该反应的热化学方程式为:。在体积为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1mol和0.4molCO,测得容器中转化率随时间变化关系如图。下列说法正确的是
A. A容器中的转化率随时间的变化关系是图中的曲线a
B. 可通过缩小容器体积来缩短b曲线对应容器达到平衡的时间,同时不改变的平衡转化率
C. 500℃该反应的化学平衡常数
D. 在平衡后向A容器中加入0.075mol与0.025mol,则平衡正向移动
13. 设计如图装置处理含甲醇的废水并进行粗铜的精炼。下列说法正确的是
A. 甲电极增加的质量等于乙电极减少的质量
B. 装置工作一段时间后,原电池装置中溶液的pH不变
C. 理论上每产生标准状况下,甲电极增重9.6g
D. 原电池正极反应式为
14. 25℃,有c(CH3COOH)+c(CH3COO﹣)=0.1mol⋅L﹣1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO﹣)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是
A. pH=5溶液中:c(CH3COO﹣)>c(CH3COOH)>c(H+)>c(OH﹣)
B. W点表示溶液中:c(Na+)+2c(OH﹣)=c(CH3COO﹣)+2c(H+)
C. pH=3.5溶液中:c(Na+)+c(H+)﹣c(OH﹣)+c(CH3COOH)=0.1mol⋅L﹣1
D. 取W点溶液1L,通入0.05mol HCl气体(溶液体积变化可忽略): c(H+)=c(CH3COOH)+c(OH﹣)
三、填空题(本大题共4题,每空2分,共54分)
15. 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有_______个伸展方向。
(2)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①Cr原子的价电子排布图为_______。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有_______(填元素符号)。
(4)目前合成氨通常采用的压强为10MPa﹣30MPa、温度为400﹣500℃,十分耗能。我国科研人员研制出了“Fe﹣LiH”等催化剂,温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。第三电离能I3(Fe) _______I3(Mn)(填“>”或“<”),原因是_______。
16. I.回答下列问题:
(1)若在空气中加热MgCl2•6H2O,生成的是Mg(OH)Cl或MgO,写出生成Mg(OH)Cl关反应的化学方程式 _______。
(2)用电解法制取金属镁时,需要无水氯化镁。需要在干燥的HCl气流中加热MgCl2•6H2O,才能得到无水MgCl2,其原因是 _______。
II.现有常温下的0.1mol•L-1纯碱溶液。
(3)已知25℃时,Kh1=2×10-4,则当溶液中c(HCO):c(CO)=2:1时,溶液的pH=_______。
(4)0.1mol•L-1Na2CO3溶液中c(OH﹣)﹣c(H+)= _______[用含c(HCO)、c(H2CO3)的关系式表示]。
(5)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式_______。
(6)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl﹣时,采用K2CrO4为指示剂,利用Ag+与CrO反应生成砖红色沉淀指示滴定终点。当溶液中的Cl﹣恰好沉淀完全(浓度等于1.0×10-5mol•L﹣1)时,溶液中c(Ag+)=_______mol•L﹣1,c(CrO)=_______ mol•L﹣1。(已知25°C时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)
17. 2022年7月13日,化学所碳中和中心召开碳中和会议,白春礼做了“在碳中和愿景下的能源化学”的特邀报告,战略性阐述了二氧化碳转化利用如何支撑实现碳中和目标。现为实现碳中和目标,利用CO、CO2加氢制甲醇的有关反应如下:
I.2H2(g)+CO(g) CH3OH(g)ΔH1<0
II.H2(g)+CO2(g) CO(g)+H2O(g)ΔH2>0
III3H2(g)+CO2(g) CH3OH(g)+H2O(g)ΔH3
(1)反应I的△H1=_______(用含ΔH2、ΔH3的式子表示)。
(2)要使反应I的反应速率加快,可采取的措施有 _______(填序号)。
A.缩小反应容器的容积 B.往密闭容器中不断通入氮气 C.升高温度D.保持恒压状态不断通入氮气 E.使用合适的催化剂
(3)一定温度下,往5L反应釜中充入1molCO2、3molH2,发生反应III,反应了5min后,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=_______。
(4)在不同温度、压强和相同催化剂条件下,发生反应III,初始时CO2、H2分别为1.0mol、3.0mol,测得H2的平衡转化率[a(H2)]随温度和压强的变化如图1所示。
①如图可知压强p1、p2、p3的大小关系为 _______。
②250℃、p3条件下,反应的化学平衡常数Kp=_______(用含p3的式子表示,Kp= ,p为各物质的分压,分压=总压×物质的量分数)。
(5)在密闭容器中充入CO2、H2,发生上述反应II和反应III,在不同催化剂Cat1、Cat2作用下,测得温度与甲醇选择性的关系如图2所示。在其他条件相同时,若想主要发生反应III,催化效率较高的是 _______(填“Cat1”或“Cat2”。)。在Cat2作用下,温度高于500℃时,甲醇的产率降低的可能原因是 _______。
18. 高铁酸钾是常见的水处理剂,工业上制备高铁酸钾有多种方法。某兴趣小组以铁屑为原料模拟制备高铁酸钾的流程如图:
【查阅资料】高铁酸钾呈紫红色,酸性或中性溶液中快速产生O2。
回答下列问题:
(1)“氧化”阶段通入空气作氧化剂,它比用氯气具有的优点是_______。
(2)为了检验“氧化”过程中所得FeCl3溶液中是否还含有Fe2+,最佳的检验试剂是_______(填标号)。
a.K3[Fe(CN)6]溶液 b.NaOH溶液 c.淀粉KI试纸
(3)请写出“制备”反应的离子方程式_______。
(4)“转化”过程使用过量饱和KOH溶液的原因是_______。
(5)“分离”过程获得K2FeO4晶体的系列操作是蒸发,结晶、过滤、洗涤、干燥,其中洗涤使用的最佳洗涤剂是_______(填标号)。
a.冷水 b.冷的稀NaOH溶液 c.冷的浓KOH溶液
(6)电解法制备K2FeO4,操作简单,易于实验室制备原理如图所示,其中阳极的电极反应式是_______。
(7)探究K2FeO4的性质。取电解后的紫红色溶液,加入稀盐酸,观察到溶液由紫红色逐渐变为黄色,并收集到黄绿色气体。甲同学认为:气体中一定含有Cl2;乙同学认为:气体中还可能含有别的气体,请设计实验证明乙同学的猜测_______。
答案
1-10 DCABD DCBDB 11.B 12.BC 13.CD 14.AC
15. (1)3 (2)N>O>B
(3) ①. ②. Al、O
(4) ①. < ②. 铁元素失去的第三个电子是3d6上的电子,而3d6容易失去一个电子形成比较稳定的3d5半满状态,而Mn的价电子排布式为3d53s2,失去的第三个电子是3d5上的电子,这是比较稳定的半充满状态,所以难失去
16. (1)MgCl2•6H2OMg(OH)Cl+HCl↑+5H2O↑
(2)在干燥的HCl气流中,抑制了MgCl2水解,且带走MgCl2•6H2O受热产生的水气,故能得到无水MgCl2
(3)10 (4)c(HCO)+2c(H2CO3)
(5)3+2Al3++3H2O=2Al(OH)3↓+3CO2↑
(6) ①. 1.8×10-5 ②. 6.2×10-3
17. (1)△H3-△H2
(2)ACE (3)0.048mol/(L∙min)
(4) ①. p1<p2<p3 ②.
(5) ①. Cat1 ②. 催化剂选择性降低,副产物增多(或催化剂失活)
18. (1)选用通入空气经济、而且氯气有毒,污染环境
(2)a (3)2Fe3++3ClO- +10OH- =2+3Cl-+5H2O
(4)降低K2FeO4的溶解度
(5)c (6)Fe-6e-+8OH- ═+4H2O
(7)将所得气体中通入过量NaOH溶液的洗气瓶,收集气体,用带火星的木条检验,若木条复燃,则乙猜测正确
湖南省临澧县第一中学2022-2023学年高二化学上学期第三次阶段性考试试卷(Word版附答案): 这是一份湖南省临澧县第一中学2022-2023学年高二化学上学期第三次阶段性考试试卷(Word版附答案),共10页。试卷主要包含了单项选择题,不定项选择题,填空题等内容,欢迎下载使用。
2020-2021学年湖南省临澧县第一中学高二上学期期中考试化学试题(非高考) Word版: 这是一份2020-2021学年湖南省临澧县第一中学高二上学期期中考试化学试题(非高考) Word版,共6页。试卷主要包含了5 Fe-56,5 ml/L B.1,1g等内容,欢迎下载使用。
湖南省临澧县第一中学2022-2023学年高二上学期第三次阶段性考试化学试卷 (含答案): 这是一份湖南省临澧县第一中学2022-2023学年高二上学期第三次阶段性考试化学试卷 (含答案),共11页。试卷主要包含了单项选择题,不定项选择题,填空题等内容,欢迎下载使用。












