
鲁教版九年级下册第九单元 金属第三节 钢铁的锈蚀与防护课后测评
展开(基础篇)2022-2023学年下学期初中化学鲁教版九年级同步分层作业9.3钢铁的锈蚀与防护
一.选择题(共9小题)
1.分类是学习化学的重要方法。下列分类错误的是( )
A.黑色固体:铁粉、二氧化锰
B.疏松多孔:铁锈、活性炭
C.金属材料:水银、四氧化三铁
D.易燃物质:面粉、焦炉气
2.下列关于金属的说法正确的是( )
A.钨的合金的熔点高,可用于制造保险丝
B.铝制品抗腐蚀能力比铁制品强
C.用 FeSO4 溶液、Cu 和 Ag 三种物质可以验证 Fe、Cu、Ag 三种金属的活动性强弱D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是 Fe3O4
3.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐 B.过度开采金属矿物
C.防止金属的腐蚀 D.寻找金属代用品
4.对化学知识的归纳不正确的是( )
A.金属的回收利用有利于保护金属资源
B.生活中常用煮沸的方法软化硬水
C.含硫杂质的燃料燃烧会产生空气污染物
D.室内放一盆石灰水,可防止煤气中毒
5.下列有关媒体的报道与化学知识不相违背的是( )
A.回收处理废旧电池,既可节约资源又可减少环境污染
B.某品牌饮品为绿色食品,不含任何化学物质
C.科研人员发明了一种特殊催化剂,可以将水变为汽油
D.有关部门提倡多开私家车,促进国内经济发展
6.下列关于资源、能源的叙述正确的是( )
A.世界上已有50%以上的金和90%以上的铁得到了回收利用
B.金属的回收和利用可以节约金属资源,减少对环境的污染
C.地壳中含量最高的金属元素是铁
D.空气是宝贵的自然资源,其中稀有气体约占总体积的0.97%
7.下列有关金属及合金的说法错误的是( )
A.钢的含碳量比生铁的含碳量高
B.铝合金的硬度比铝的硬度大
C.铁制品在潮湿的空气中易生锈
D.钢铁是人类目前使用最多的金属材料
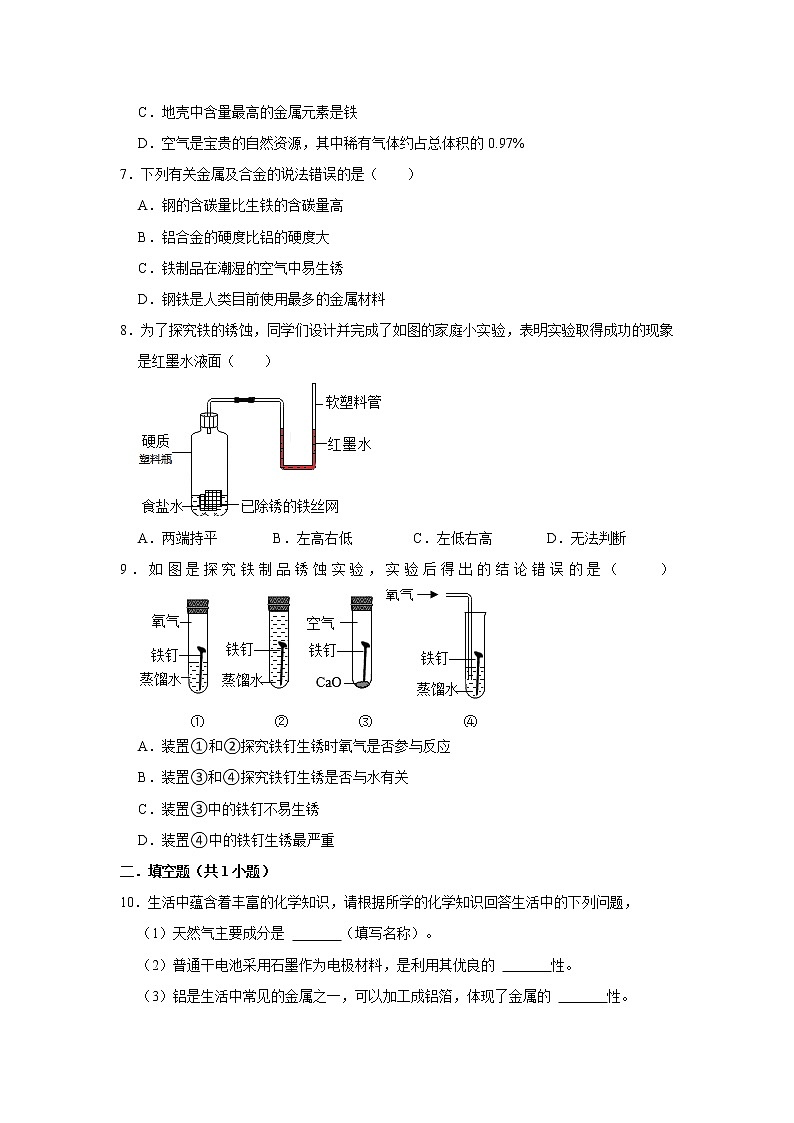
8.为了探究铁的锈蚀,同学们设计并完成了如图的家庭小实验,表明实验取得成功的现象是红墨水液面( )
A.两端持平 B.左高右低 C.左低右高 D.无法判断
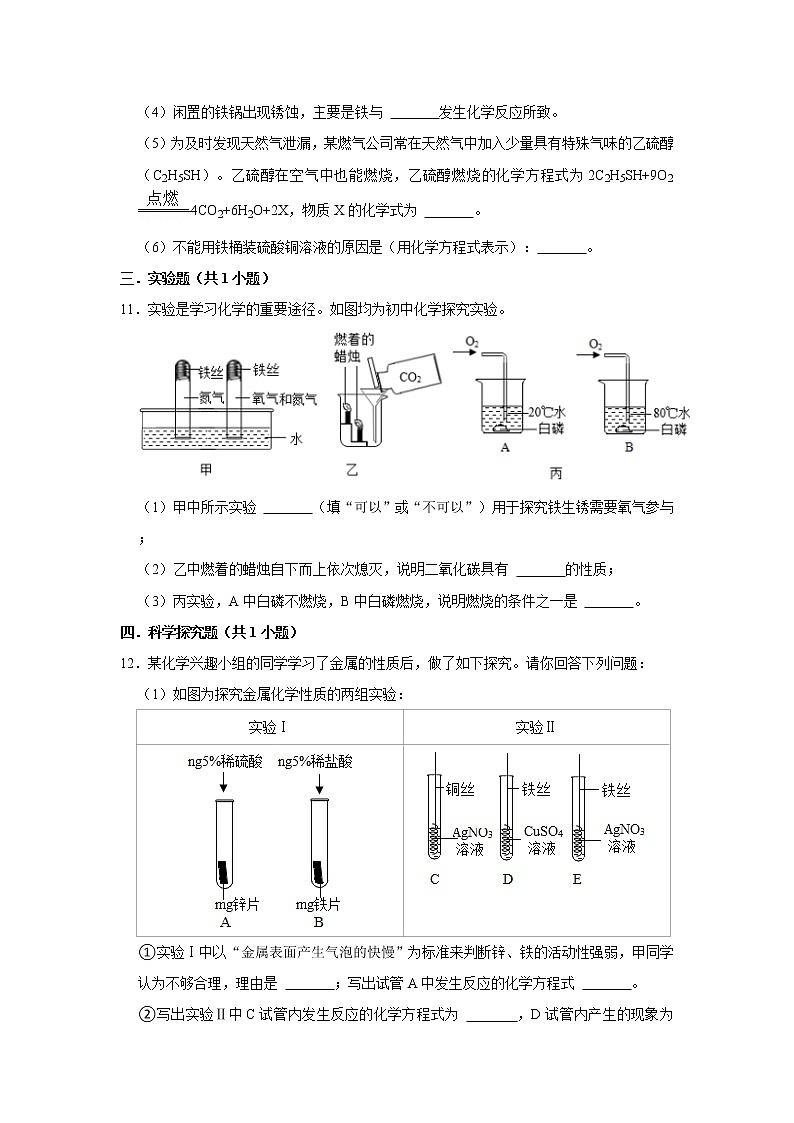
9.如图是探究铁制品锈蚀实验,实验后得出的结论错误的是( )
A.装置①和②探究铁钉生锈时氧气是否参与反应
B.装置③和④探究铁钉生锈是否与水有关
C.装置③中的铁钉不易生锈
D.装置④中的铁钉生锈最严重
二.填空题(共1小题)
10.生活中蕴含着丰富的化学知识,请根据所学的化学知识回答生活中的下列问题,
(1)天然气主要成分是 (填写名称)。
(2)普通干电池采用石墨作为电极材料,是利用其优良的 性。
(3)铝是生活中常见的金属之一,可以加工成铝箔,体现了金属的 性。
(4)闲置的铁锅出现锈蚀,主要是铁与 发生化学反应所致。
(5)为及时发现天然气泄漏,某燃气公司常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。乙硫醇在空气中也能燃烧,乙硫醇燃烧的化学方程式为2C2H5SH+9O24CO2+6H2O+2X,物质X的化学式为 。
(6)不能用铁桶装硫酸铜溶液的原因是(用化学方程式表示): 。
三.实验题(共1小题)
11.实验是学习化学的重要途径。如图均为初中化学探究实验。
(1)甲中所示实验 (填“可以”或“不可以”)用于探究铁生锈需要氧气参与;
(2)乙中燃着的蜡烛自下而上依次熄灭,说明二氧化碳具有 的性质;
(3)丙实验,A中白磷不燃烧,B中白磷燃烧,说明燃烧的条件之一是 。
四.科学探究题(共1小题)
12.某化学兴趣小组的同学学习了金属的性质后,做了如下探究。请你回答下列问题:
(1)如图为探究金属化学性质的两组实验:
实验Ⅰ | 实验Ⅱ |
①实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,甲同学认为不够合理,理由是 ;写出试管A中发生反应的化学方程式 。
②写出实验Ⅱ中C试管内发生反应的化学方程式为 ,D试管内产生的现象为 。
③实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,不必要做的实验是 (填字母序号);请你设计不同的实验方案验证三种金属的活动性顺序,所需药品为 。
(2)如图为探究铁生锈条件的对比实验(每支试管中均放有完全相同的洁净铁片):
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,他认为必须全面观察 (选填试管编号)发生的现象,并通过科学严谨的推论,才能得到上述结论。B中植物油的作用是 。
②试管D和E实验的目的是进一步探究铁在 环境中更容易发生锈蚀。
(基础篇)2022-2023学年下学期初中化学鲁教版九年级同步分层作业9.3钢铁的锈蚀与防护
参考答案与试题解析
一.选择题(共9小题)
1.分类是学习化学的重要方法。下列分类错误的是( )
A.黑色固体:铁粉、二氧化锰
B.疏松多孔:铁锈、活性炭
C.金属材料:水银、四氧化三铁
D.易燃物质:面粉、焦炉气
【解答】解:A、铁粉、二氧化锰都是黑色固体,说法正确;
B、铁锈、活性炭都具有疏松多孔的结构,说法正确;
C、四氧化三铁是一种金属氧化物,不是金属材料,说法错误;
D、面粉、焦炉气均具有可燃性,均为易燃物质,说法正确。
故选:C。
2.下列关于金属的说法正确的是( )
A.钨的合金的熔点高,可用于制造保险丝
B.铝制品抗腐蚀能力比铁制品强
C.用 FeSO4 溶液、Cu 和 Ag 三种物质可以验证 Fe、Cu、Ag 三种金属的活动性强弱
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是 Fe3O4
【解答】解:A.钨的合金的熔点低,可用于制造保险丝,故错误;
B.铝和空气中的氧气反应会生成致密的氧化铝薄膜,所以铝制品抗腐蚀能力比铁制品强,故正确;
C.铁比铜活泼,铜比银活泼,把铜和银分别伸入硫酸亚铁溶液中时,都无明显现象,说明铁比铜和银活泼,但是无法确定银和铜的活泼性,故错误;
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe2O3,故错误;
故选:B。
3.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐 B.过度开采金属矿物
C.防止金属的腐蚀 D.寻找金属代用品
【解答】解:A、回收易拉罐,经过处理后再利用可以节约金属资源,故选项错误。
B、过度开采金属矿物,不利于金属资源的保护,故选项正确。
C、防止金属的腐蚀,减少金属的损耗,可以节约金属资源,故选项错误。
D、寻找金属代用品,可以节约金属资源,故选项错误。
故选:B。
4.对化学知识的归纳不正确的是( )
A.金属的回收利用有利于保护金属资源
B.生活中常用煮沸的方法软化硬水
C.含硫杂质的燃料燃烧会产生空气污染物
D.室内放一盆石灰水,可防止煤气中毒
【解答】解:A.金属的回收利用有利于保护金属资源,故A正确;
B.生活中常用煮沸的方法软化硬水,故B正确;
C.含硫杂质的燃料燃烧会生成有毒的气体二氧化硫,进入空气会污染环境,故C正确;
D.一氧化碳不和氢氧化钙反应,所以室内放一盆石灰水,不能防止煤气中毒,故D错误。
故选:D。
5.下列有关媒体的报道与化学知识不相违背的是( )
A.回收处理废旧电池,既可节约资源又可减少环境污染
B.某品牌饮品为绿色食品,不含任何化学物质
C.科研人员发明了一种特殊催化剂,可以将水变为汽油
D.有关部门提倡多开私家车,促进国内经济发展
【解答】解:A、废旧电池对环境有危害,回收处理废旧电池,既可节约资源,又可减少环境污染,故A说法正确;
B、任何物质都属于化学物质,所以饮料中肯定含有化学物质,故B说法错误;
C、水中只含有氢、氧元素,汽油中含有碳元素,催化剂只能改变反应速度,根据质量守恒定律可知,不可以将水变为汽油,故C错误;
D、有关部门提倡多开私家车,促进国内经济发展,增加了化石燃料的使用,会增加环境污染,故D错误;
故选:A。
6.下列关于资源、能源的叙述正确的是( )
A.世界上已有50%以上的金和90%以上的铁得到了回收利用
B.金属的回收和利用可以节约金属资源,减少对环境的污染
C.地壳中含量最高的金属元素是铁
D.空气是宝贵的自然资源,其中稀有气体约占总体积的0.97%
【解答】解:A、收利用金属,能节约金属资源、减少污染等,目前世界上已有50%以上的铁和90%以上的金得到了回收利用,故选项说法错误。
B、金属的回收和利用可以节约金属资源,减少对环境的污染,故选项说法正确。
C、地壳中含量最高的金属元素是铝,故选项说法错误。
D、空气是宝贵的自然资源,其中稀有气体约占总体积的0.94%,故选项说法错误。
故选:B。
7.下列有关金属及合金的说法错误的是( )
A.钢的含碳量比生铁的含碳量高
B.铝合金的硬度比铝的硬度大
C.铁制品在潮湿的空气中易生锈
D.钢铁是人类目前使用最多的金属材料
【解答】解:A、生铁和钢是铁的两种重要的合金,它们的主要区别是含碳量不同,生铁的含碳量要比钢的高,故选项说法错误。
B、合金的硬度比组成它的纯金属的硬度大,铝合金的硬度比铝的硬度大,故选项说法正确。
C、铁在空气中锈蚀,实际上是铁跟空气中的氧气和水蒸气共同作用的结果,铁制品在潮湿的空气中易生锈,故选项说法正确。
D、钢铁是使用最多的金属材料,故选项说法正确。
故选:A。
8.为了探究铁的锈蚀,同学们设计并完成了如图的家庭小实验,表明实验取得成功的现象是红墨水液面( )
A.两端持平 B.左高右低 C.左低右高 D.无法判断
【解答】解:铁与氧气和水同时接触时会生锈,图中实验,食盐水会加快铁锈蚀的速率,一段时间后铁丝会生锈;由于氧气被消耗,塑料瓶中气体减少,压强减少,则表明实验取得成功的现象是红墨水液面左高右低。
故选:B。
9.如图是探究铁制品锈蚀实验,实验后得出的结论错误的是( )
A.装置①和②探究铁钉生锈时氧气是否参与反应
B.装置③和④探究铁钉生锈是否与水有关
C.装置③中的铁钉不易生锈
D.装置④中的铁钉生锈最严重
【解答】解:A、装置①中铁钉(有铁、有水、有氧气)生锈,装置②中铁钉(有铁、有水、无氧气)不生锈,可得出装置①和②探究铁钉生锈时氧气是否参与反应,故选项说法正确。
B、装置③中铁钉[有铁、无水、有氧气(空气)]不生锈,装置④(有铁、有水、有氧气[空气+通入氧气]),装置④和装置③中含氧量不同,变量不唯一,不能得出装置③和④探究铁钉生锈是否与水有关,故选项说法错误。
C、装置③中氧化钙与水反应可以将空气干燥,铁钉在干燥的空气中不容易生锈,故选项说法正确。
D、装置④中的铁钉(有铁、有水、有空气),而且向水中不断通入氧气,与装置①相比,铁钉与水和氧气可以更直接的接触,铁钉生锈最严重,故选项说法正确。
故选:B。
二.填空题(共1小题)
10.生活中蕴含着丰富的化学知识,请根据所学的化学知识回答生活中的下列问题,
(1)天然气主要成分是 甲烷 (填写名称)。
(2)普通干电池采用石墨作为电极材料,是利用其优良的 导电 性。
(3)铝是生活中常见的金属之一,可以加工成铝箔,体现了金属的 延展 性。
(4)闲置的铁锅出现锈蚀,主要是铁与 氧气和水 发生化学反应所致。
(5)为及时发现天然气泄漏,某燃气公司常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。乙硫醇在空气中也能燃烧,乙硫醇燃烧的化学方程式为2C2H5SH+9O24CO2+6H2O+2X,物质X的化学式为 SO2 。
(6)不能用铁桶装硫酸铜溶液的原因是(用化学方程式表示): Fe+CuSO4═FeSO4+Cu 。
【解答】解:(1)天然气主要成分是甲烷,故答案为:甲烷;
(2)石墨具有导电性,所以可用石墨作为电极材料,故答案为:导电性;
(3)铝具有延展性,可制作铝箔,故答案为:延展;
(4)铁的锈蚀是铁与空气中的氧气和水发生化学反应所致,故答案为:氧气和水;
(5)由化学方程式可知,反应前出现了4个碳原子、12个氢原子、2个硫原子和18个氧原子,反应后出现了4个碳原子、12个氢原子和14个氧原子,根据质量守恒定律可知,反应后尚缺的2个硫原子和4个氧原子存在于2X中,则X的化学式为SO2,故答案为:SO2;
(6)不能用铁桶装硫酸铜溶液的原因是铁与硫酸铜反应生成硫酸亚铁和铜会影响药效,故反应的化学方程式写为:Fe+CuSO4=FeSO4+Cu。故答案为:Fe+CuSO4═FeSO4+Cu。
三.实验题(共1小题)
11.实验是学习化学的重要途径。如图均为初中化学探究实验。
(1)甲中所示实验 可以 (填“可以”或“不可以”)用于探究铁生锈需要氧气参与;
(2)乙中燃着的蜡烛自下而上依次熄灭,说明二氧化碳具有 密度比空气大,不可燃、不助燃 的性质;
(3)丙实验,A中白磷不燃烧,B中白磷燃烧,说明燃烧的条件之一是 温度达到着火点 。
【解答】解:(1)实验甲中左侧试管中的铁丝与水蒸气、氮气接触,右侧试管中的铁丝与水蒸气、氮气、氧气接触,一段时间后观察到右侧试管中铁丝生锈,左侧试管中铁丝基本不发生变化,对比可知:该实验可以证明铁丝生锈需要氧气参与;
(2)将二氧化碳倒入装有阶梯蜡烛的烧杯中,观察到蜡烛自下而上依次熄灭,说明CO2密度比空气大,且不能燃烧,也不支持燃烧;
(3)A中的白磷与氧气接触在20℃的水中,B中的白磷与氧气接触在80℃的水,观察到A中的白磷不燃烧,B中的白磷燃烧,说明燃烧的条件之一是温度需要达到物质着火点。
故答案为:(1)可以;
(2)密度比空气大,不可燃、不助燃;
(3)温度达到着火点。
四.科学探究题(共1小题)
12.某化学兴趣小组的同学学习了金属的性质后,做了如下探究。请你回答下列问题:
(1)如图为探究金属化学性质的两组实验:
实验Ⅰ | 实验Ⅱ |
①实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,甲同学认为不够合理,理由是 加入的酸的种类不同 ;写出试管A中发生反应的化学方程式 Zn+H2SO4=ZnSO4+H2↑ 。
②写出实验Ⅱ中C试管内发生反应的化学方程式为 Cu+2AgNO3=Cu(NO3)2+2Ag ,D试管内产生的现象为 铁丝表面有红色固体析出,溶液逐渐由蓝色变成浅绿色 。
③实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,不必要做的实验是 E (填字母序号);请你设计不同的实验方案验证三种金属的活动性顺序,所需药品为 Fe(NO3)2溶液、铜丝、AgNO3溶液(合理即可) 。
(2)如图为探究铁生锈条件的对比实验(每支试管中均放有完全相同的洁净铁片):
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,他认为必须全面观察 ABC (选填试管编号)发生的现象,并通过科学严谨的推论,才能得到上述结论。B中植物油的作用是 隔绝氧气 。
②试管D和E实验的目的是进一步探究铁在 盐和酸存在的 环境中更容易发生锈蚀。
【解答】解:(1)①判断锌、铁的活动性强弱,加入的酸的种类、浓度应相同,实验 I 中,A试管中的放有稀硫酸,B试管中放入稀盐酸,两支试管中的酸的种类不同,不能来判断锌、铁的活动性强弱,由图可知,试管 A 中发生的反应是锌与稀硫酸反应生成硫酸锌和氢气,故反应的化学方程式写为:Zn+H2SO4=ZnSO4+H2↑。故答案为:加入的酸的种类不同;Zn+H2SO4=ZnSO4+H2↑;
②由图可知,实验 II 中 C 试管内发生的反应是铜和硝酸银反应生成硝酸铜和银,故反应的化学方程式写为:Cu+2AgNO3=Cu(NO3)2+2Ag;D试管内发生的反应是铁与硫酸铜反应生成硫酸亚铁和铜,观察到的现象是铁丝表面有红色固体析出,溶液逐渐由蓝色变成浅绿色,故填铁丝表面有红色固体析出,溶液逐渐由蓝色变成浅绿色。故答案为:Cu+2AgNO3=Cu(NO3)2+2Ag;铁丝表面有红色固体析出,溶液逐渐由蓝色变成浅绿色;
③实验 II 中,C 试管内发生的反应是铜和硝酸银反应生成硝酸铜和银,能够证明铜的活动性比银强,D试管内发生的反应是铁与硫酸铜反应生成硫酸亚铁和铜,证明铁的活动性比铜强,两个实验已经证明三种金属的活动性的关系为Fe>Cu>Ag,所以要验证 Cu、Fe、Ag 的金属活动性顺序,不必要做的实验是E;
验证三种金属的活动性顺序,还可以选择活动性居中金属的单质和另外两支金属的盐溶液,所以验证 Cu、Fe、Ag 的金属活动性顺序,可以选择Fe(NO3)2溶液、铜丝、AgNO3溶液,故填Fe(NO3)2溶液、铜丝、AgNO3溶液(合理即可);故答案为:E;Fe(NO3)2溶液、铜丝、AgNO3溶液(合理即可);
(2)①A试管中的铁钉既能够接触水分也能够接触空气中的氧气,一段时间后生锈,B试管中的铁钉只能够接触水分,一段时间后不生锈,说明铁的锈蚀与氧气有关,A试管中的铁钉既能够接触水分也能够接触空气中的氧气,一段时间后生锈,C试管中的铁钉只能够接触空气,不能接触水分,一段时间后不生锈,说明铁的锈蚀与水有关,所以探究铁锈蚀的条件必须全面观察ABC三支试管中的现象,故选:ABC;B 中植物油的作用是隔绝氧气,探究氧气对铁锈蚀的影响,故答案为:ABC;隔绝氧气;
②试管 D中加入食盐水,食盐属于盐,试管 E中加入的铁钉用食醋浸湿,食醋属于酸,所以试管 D 和 E实验的目的是进一步探究铁在盐和酸存在的环境中更容易发生锈蚀,故答案为:盐和酸存在的。
鲁教版九年级下册第三节 钢铁的锈蚀与防护课后作业题: 这是一份鲁教版九年级下册第三节 钢铁的锈蚀与防护课后作业题,共15页。试卷主要包含了下列不是保护金属资源的途径的是,“垃圾是放错地方的资源”,化学与生活密切相关等内容,欢迎下载使用。
鲁教版九年级下册第三节 钢铁的锈蚀与防护一课一练: 这是一份鲁教版九年级下册第三节 钢铁的锈蚀与防护一课一练,共20页。试卷主要包含了分类是学习化学常用的方法,化学与人类生活、生产密不可分等内容,欢迎下载使用。
初中化学鲁教版九年级下册第二节 化学与材料研制习题: 这是一份初中化学鲁教版九年级下册第二节 化学与材料研制习题,共9页。试卷主要包含了下列说法等内容,欢迎下载使用。













