
高考化学二轮复习专项分层特训练18 化学反应历程与反应机理图像分析 含答案
展开
这是一份高考化学二轮复习专项分层特训练18 化学反应历程与反应机理图像分析 含答案,共10页。试卷主要包含了[2022·山东德州月考]等内容,欢迎下载使用。
下列有关四种不同反应进程的说法正确的是( )
A.进程Ⅰ是放热反应
B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ
D.进程 Ⅳ 中,Z没有催化作用
2.[2021·重庆卷]“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物N2O和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283 kJ·ml-1,则2N2O(g)===2N2(g)+O2(g)的反应热ΔH(kJ·ml-1)为( )
A.-152 B.-76
C.+76 D.+152
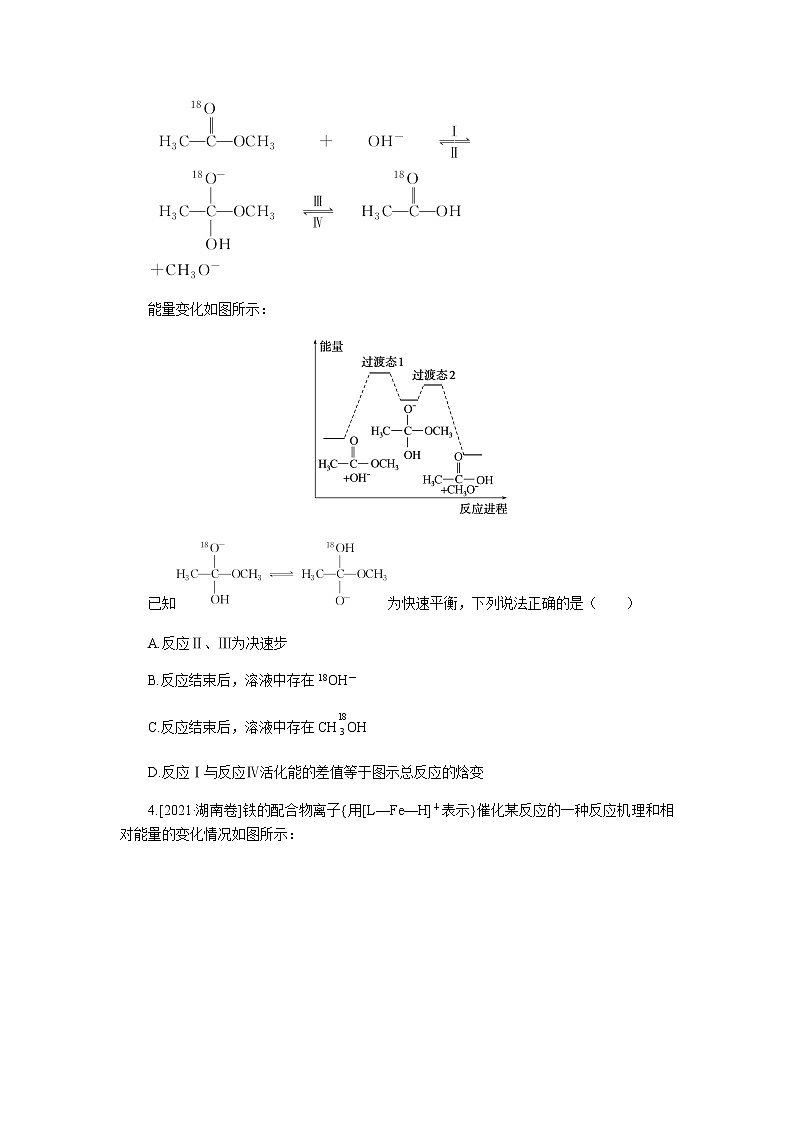
3.[2021·山东卷]18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为
能量变化如图所示:
已知为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH eq \\al(\s\up1(18),\s\d1(3)) OH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
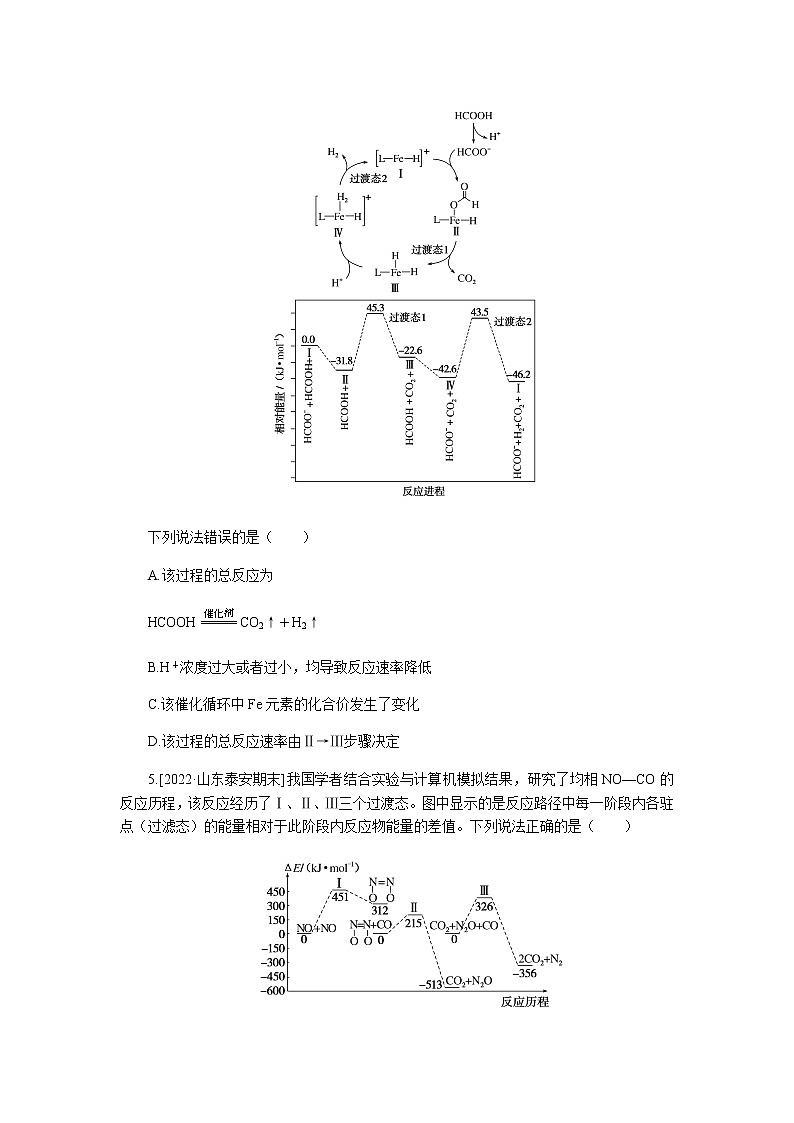
4.[2021·湖南卷]铁的配合物离子{用[L—Fe—H]+表示}催化某反应的一种反应机理和相对能量的变化情况如图所示:
下列说法错误的是( )
A.该过程的总反应为
HCOOH eq \(=====,\s\up7(催化剂)) CO2↑+H2↑
B.H+浓度过大或者过小,均导致反应速率降低
C.该催化循环中Fe元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
5.[2022·山东泰安期末]我国学者结合实验与计算机模拟结果,研究了均相NO—CO的反应历程,该反应经历了Ⅰ、Ⅱ、Ⅲ三个过渡态。图中显示的是反应路径中每一阶段内各驻点(过滤态)的能量相对于此阶段内反应物能量的差值。下列说法正确的是( )
A.N2O比更容易与CO发生反应
B.整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大
C.2NO(g)+2CO(g)⇌N2(g)+2CO2(g)ΔH>0
D.其他条件不变,增大压强或使用催化剂均可以增大反应速率,提高反应物平衡转化率
6.[2022·山东德州月考](双选)研究发现Pd2团簇可催化CO的氧化,在催化过程中不同路径生成不同的过渡态和中间产物(过渡态已标出),如图为路径1和路径2催化的能量变化。下列说法不正确的是( )
A.反应主要通过反应路径2进行
B.决定路径1速率快慢的活化能E=1.77 eV
C.该过程中只有极性键的断裂和生成
D.整个反应的热化学方程式为2CO(g)+O2(g) eq \(=====,\s\up7(Pd2)) 2CO2(g) ΔH=-6.28 kJ·ml-1
7.[2022·山东烟台二中考试]LnFe(Ⅲ)—Cl配合物能够受光激发产生高活性的氯自由基(Cl·),Cl·可将烷烃中难以活化的C(sp3)—H键转化为C—N,反应机理变化情况如图所示:
下列说法错误的是( )
A.HCl是反应过程的中间产物
B.催化循环过程中铁元素的化合价不发生变化
8.[2022·山东枣庄二模](双选)一定条件下HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示。
下列说法错误的是( )
A.HCOOH催化脱氢反应在该温度下能自发进行
B.在状态Ⅰ~Ⅴ中,由Ⅳ到Ⅴ的反应为决速步
C.由反应历程可得出HCOOH中第2个H原子更易脱去
D.在该反应历程中,HCOOH所有的化学键均发生断裂
9.[2022·河北石家庄质检](双选)科研工作者通过计算机模拟和数学计算,设计出三条在含[Pt—O]结构的化合物中插入CO的反应路径,其相对能量变化如图所示:
下列说法错误的是( )
A.该反应为放热反应
B.通过对图像的分析得出,该反应按照路径Ⅲ进行
C.反应过程中Pt的成键数目不变
D.图中M与N互为同分异构体
10.[2022·山西柳林期中]甲烷在光照条件下发生的氯代反应历程如图所示。下列说法错误的是( )
(1)Cl—Cl―→2Cl·
(2)Cl·+CH3—H―→CH3·+H—Cl
(3)CH3·+Cl—Cl―→CH3—Cl+Cl·
A.反应Cl·+CH3—H―→CH3·+H—Cl
ΔH=+7.5 kJ·ml-1
B.反应Cl·+CH3—H―→CH3·+H—Cl的活化能Ea=+16.7 kJ·ml-1
C.反应(2)比反应(3)更容易进行
D.CH4(g)+Cl2(g)===CH3Cl(g)+HCl(g)
ΔH=-105.4 kJ·ml-1
练18 化学反应历程与反应机理图像分析
1.答案:AD
解析:
2.答案:A
解析:根据题中信息可依次书写出热化学方程式:
①CO(g)+ eq \f(1,2) O2(g)===CO2(g) ΔH1=-283 kJ·ml-1;
②N2O(g)+CO(g)===N2(g)+CO2(g) ΔH2=-(330+229-123-77) kJ·ml-1=-359 kJ·ml-1;根据盖斯定律,2×(②-①)得反应2N2O(g)===2N2(g)+O2(g),ΔH=2(ΔH2-ΔH1)=-152 kJ·ml-1,故选A。
3.答案:B
解析:根据18O标记的乙酸甲酯在足量NaOH溶液中发生水解的部分反应历程的能量变化图可知,正反应中过程Ⅰ所需活化能最大,则该步反应速率最慢,是决速步,A项错误;结合题给已知信息和反应历程Ⅱ可知,反应结束后,溶液中存在18OH-,B项正确;由题给信息可知:有机物中的18O-仅和—OH发生互换,不与—OCH3互换,则不可能存在CH eq \\al(\s\up1(18),\s\d1(3)) OH,C项错误;反应Ⅰ与反应Ⅲ活化能之和与反应Ⅱ与反应Ⅳ活化能之和的差值等于图示总反应的焓变,D项错误。
4.答案:D
解析:分析题给反应机理图,可知该过程的反应物为HCOOH,生成物为CO2和H2,则该过程的总反应为HCOOH eq \(=====,\s\up7(催化剂)) CO2↑+H2↑,A说法正确;H+浓度过大,抑制HCOOH的电离,HCOO-浓度减小,会降低Ⅰ→Ⅱ步骤的反应速率,H+浓度过小,会降低Ⅲ→Ⅳ步骤反应速率,故H+浓度过大或者过小,均会导致反应速率降低,B说法正确;由Ⅱ→Ⅲ过程中,脱去CO2,碳元素化合价升高,则Fe元素化合价降低,C说法正确;由相对能量的变化情况图可以得出,该反应过程中的Ⅳ→Ⅰ步骤的活化能Ea=86.1 kJ·ml-1,为该反应进程中的最大活化能,故该过程的决速步骤为Ⅳ→Ⅰ步骤,D说法错误。
5.答案:B
解析:由题图可知,与CO反应的活化能比N2O与CO反应的活化能低,则比N2O更容易与CO发生反应,故A错误;由图可知,整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大,为451 kJ·ml-1,故B正确;由题图可知,反应②、③放出的热量大于反应①吸收的热量,则总反应为放热反应,ΔH
相关试卷
这是一份热点06 化学反应机理(反应历程)图像分析-2024年高考化学【热点·重点·难点】专练(新高考专用),文件包含热点06化学反应机理反应历程图像分析-2024年高考化学热点·重点·难点专练新高考专用原卷版docx、热点06化学反应机理反应历程图像分析-2024年高考化学热点·重点·难点专练新高考专用解析版docx等2份试卷配套教学资源,其中试卷共68页, 欢迎下载使用。
这是一份鲁科版高考化学一轮复习课时分层作业39化学反应速率与反应历程(机理)含答案,文件包含鲁科版高考化学一轮复习课时分层作业39化学反应速率与反应历程机理含答案docx、鲁科版高考化学一轮复习课时分层作业39参考答案docx等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
这是一份高考化学二轮复习小题提速练7反应历程(机理)的分析及应用含答案,共7页。








