
所属成套资源:鲁科版化学必修第一册同步学案
- 新教材2021-2022学年鲁科版化学必修第一册学案:第3章 物质的性质与转化 章末总结探究课 学案 0 次下载
- 新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第1节 基础课时13 亚铁盐和铁盐 铁的单质 学案 0 次下载
- 新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第2节 基础课时15 自然界中的硫 二氧化硫的性质 学案 1 次下载
- 新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第3节 基础课时17 自然界中的氮循环 氮气与氮氧化物 学案 1 次下载
- 新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第3节 基础课时19 硝酸 人类活动对氮循环和环境的影响 学案 1 次下载
新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第1节 基础课时14 铁的氧化物和铁的氢氧化物铁及其化合物之间的转化关系
展开
这是一份新教材2021-2022学年鲁科版化学必修第一册学案:第3章 第1节 基础课时14 铁的氧化物和铁的氢氧化物铁及其化合物之间的转化关系,共10页。
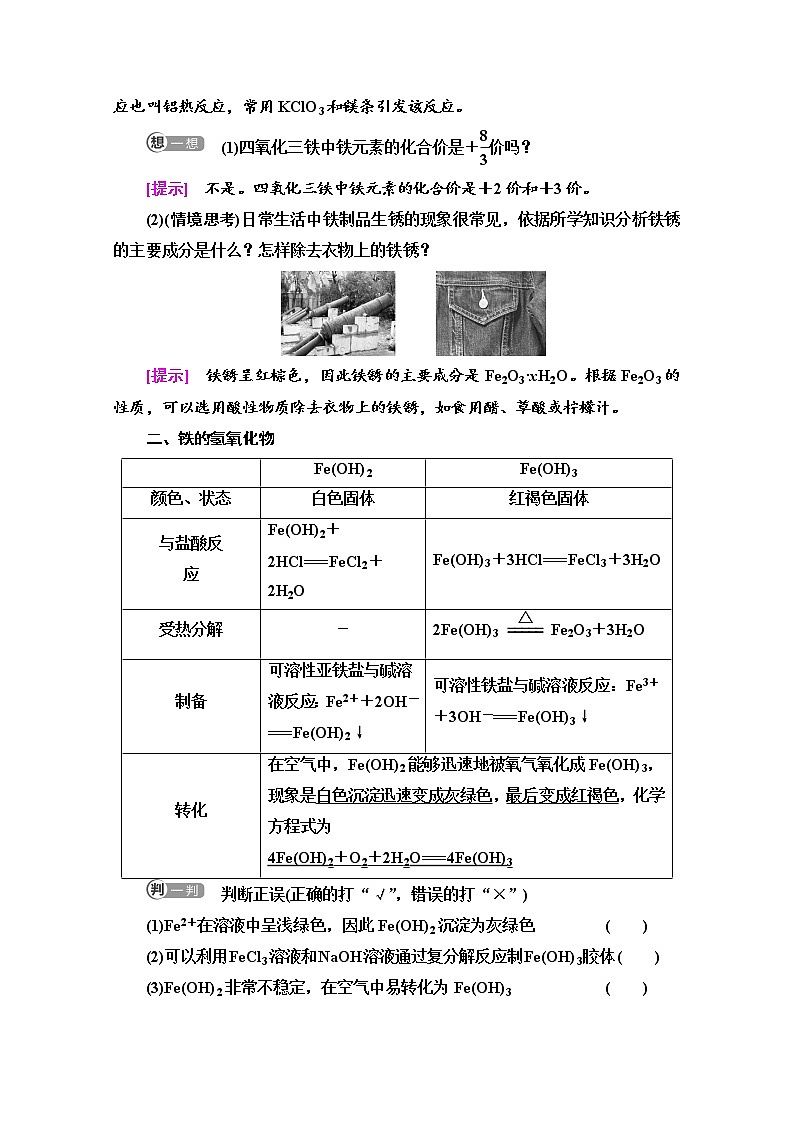
www.ks5u.com基础课时14 铁的氧化物和铁的氢氧化物铁及其化合物之间的转化关系学 习 任 务1.从物质类别、元素价态的角度,依据复分解反应规律和氧化还原反应原理,预测含有铁元素的物质的性质及物质之间的转化,设计实验进行初步验证,并能分析解释有关实验现象,培养科学探究与创新意识的化学核心素养。2.利用含有铁元素的物质的性质和转化关系,设计制备、分离、检验等简单任务的方案;能从物质类别和元素价态变化的角度说明物质的转化路径,培养证据推理与模型认知的意识。3.分别根据含有铁元素的物质的性质,分析生产、生活中的实际问题,如补铁剂中铁元素价态的检验、线路板废液的回收利用等,培养科学态度与社会责任的化学核心素养。一、铁的氧化物名称(化学式)氧化亚铁(FeO)四氧化三铁(Fe3O4)三氧化二铁(Fe2O3)俗名—磁性氧化铁铁红色态黑色粉末黑色晶体红棕色粉末铁的价态+2+2、+3+3与盐酸反应FeO+2H+===Fe2++H2OFe3O4+8H+===Fe2++2Fe3++4H2OFe2O3+6H+===2Fe3++3H2O与铝粉反应3FeO+2Al3Fe+Al2O3—2Al+Fe2O32Fe+Al2O3说明:(1)FeO、Fe2O3均为碱性氧化物,Fe3O4为复杂的氧化物。(2)FeO、Fe2O3、Fe3O4、MnO2、WO3、V2O5等难熔金属氧化物与铝粉的反应也叫铝热反应,常用KClO3和镁条引发该反应。 (1)四氧化三铁中铁元素的化合价是+价吗?[提示] 不是。四氧化三铁中铁元素的化合价是+2价和+3价。(2)(情境思考)日常生活中铁制品生锈的现象很常见,依据所学知识分析铁锈的主要成分是什么?怎样除去衣物上的铁锈?[提示] 铁锈呈红棕色,因此铁锈的主要成分是Fe2O3·xH2O。根据Fe2O3的性质,可以选用酸性物质除去衣物上的铁锈,如食用醋、草酸或柠檬汁。二、铁的氢氧化物 Fe(OH)2Fe(OH)3颜色、状态白色固体红褐色固体与盐酸反应Fe(OH)2+2HCl===FeCl2+2H2OFe(OH)3+3HCl===FeCl3+3H2O受热分解-2Fe(OH)3Fe2O3+3H2O制备可溶性亚铁盐与碱溶液反应:Fe2++2OH-===Fe(OH)2↓可溶性铁盐与碱溶液反应:Fe3++3OH-===Fe(OH)3↓转化在空气中,Fe(OH)2能够迅速地被氧气氧化成Fe(OH)3,现象是白色沉淀迅速变成灰绿色,最后变成红褐色,化学方程式为4Fe(OH)2+O2+2H2O===4Fe(OH)3 判断正误(正确的打“√”,错误的打“×”)(1)Fe2+在溶液中呈浅绿色,因此Fe(OH)2沉淀为灰绿色 ( )(2)可以利用FeCl3溶液和NaOH溶液通过复分解反应制Fe(OH)3胶体 ( )(3)Fe(OH)2非常不稳定,在空气中易转化为Fe(OH)3 ( )(4)为防止Fe(OH)2被氧化,在制备时,常采用新制的FeSO4溶液和煮沸的NaOH溶液制取 ( )[答案] (1)× (2)× (3)√ (4)√三、铁及其化合物之间的转化关系1.绘制铁及其化合物的“价—类”二维图[答案] 2.补铁剂中铁元素价态的检验实验步骤实验现象实验结论(1)取少量补铁口服液于试管中,滴入KSCN溶液a.溶液不变红无Fe3+b.溶液变红有Fe3+(2)若出现现象a,向反应后的溶液中滴加氯水溶液变红有Fe2+(3)若出现现象b,另取补铁剂滴加酸性KMnO4溶液溶液紫红色褪去有Fe2+溶液紫红色不褪去无Fe2+ 判断正误(正确的打“√”,错误的打“×”)(1)FeCl2不能通过化合反应制得 ( )(2)同价态含铁物质间的转化一般可通过复分解反应实现 ( )(3)不同价态的含铁物质间的转化必须通过氧化还原反应实现 ( )(4)食用富含维生素C的食物利于人体对铁元素吸收,是利用维生素C的氧化性 ( )(5)向补铁口服液中滴加KSCN溶液,溶液变为红色,则补血口服液中铁的价态只有+3价 ( )[答案] (1)× (2)√ (3)√ (4)× (5)×Fe(OH)2的制备用下图所示的密封反应装置来制备氢氧化亚铁。B A具体操作:注射器A吸入NaOH溶液后用硅胶塞封口,再用注射器B将FeSO4溶液缓慢推入注射器A中,使两溶液混合反应。为保证实验的顺利进行,对反应液进行了如下处理:[问题1] 用硅胶塞封口的原因是什么?[提示] 防止空气中的O2进入。[问题2] 配制硫酸亚铁溶液加入维生素C(100 mL溶液中加入半片维生素C),其目的是什么?[提示] 维生素C具有还原性,可以防止Fe2+被氧化。[问题3] 为了较长时间看到白色沉淀,用于制备Fe(OH)2的氢氧化钠溶液应该事先进行怎样的操作?为什么?[提示] 煮沸。Fe(OH)2容易被氧气氧化,故用于制备Fe(OH)2的氢氧化钠溶液应加热煮沸赶走溶液中的溶解氧。 氢氧化亚铁的制备1.制备Fe(OH)2的注意事项(1)Fe2+必须是新制的,并放入铁粉,以防Fe2+被氧化成Fe3+;(2)除去溶液中溶解的O2,其方法是加热煮沸NaOH溶液;(3)滴管末端插入液面以下;(4)必要时可在液面上加植物油或苯进行液封。2.Fe(OH)2的制备方法(1)有机覆盖层法将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或植物油(不能用CCl4,它的密度大于水),以防止空气与Fe(OH)2接触发生反应,如图1所示。图1 图2(2)还原性气体保护法用H2将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可长时间观察到白色沉淀,如图2所示。1.实验室用FeCl2和烧碱制备Fe(OH)2,为了使生成的产物不容易被氧化,下列说法不正确的是( )A.配制FeCl2和烧碱溶液所用的蒸馏水通常要煮沸B.可在FeCl2溶液的上面加一层植物油,以隔绝空气C.向FeCl2溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入试管内D.产生Fe(OH)2沉淀后,不能振荡试管C [ FeCl2和烧碱溶液要现用现配,且配制溶液的蒸馏水要煮沸以除去氧气,确保Fe(OH)2的生成在无氧的环境里,故A项正确;在FeCl2溶液的上面加一层苯或一层植物油,以隔绝空气防止氧气溶入,故B项正确;向FeCl2溶液中滴加烧碱溶液时,要将胶头滴管的尖嘴伸入FeCl2溶液中,防止氢氧化钠溶液在滴入时接触空气中的氧气,故C项错误;产生Fe(OH)2沉淀后,若振荡试管,会增大沉淀与空气接触的机会,使沉淀更易被氧化,故D项正确。] 2.如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。A B填写下列空白:(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是____________,A中反应的离子方程式为__________________。(2)实验开始时应先将止水夹a________(填“打开”或“关闭”)。(3)简述生成Fe(OH)2的操作过程_____________________________。(4)实验完毕,打开b处止水夹,放入一部分空气,此时B中发生反应的化学方程式为___________________________________________。(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。[解析] A为氢气的发生装置,B为产生Fe(OH)2沉淀的装置,当a打开时,H2通过a进入B中排出B内氧气,a关闭时,A内气体压强增大,使A中FeSO4、H2SO4混合液进入B中与NaOH溶液反应产生Fe(OH)2沉淀。[答案] (1)铁屑 Fe+2H+===Fe2++H2↑ (2)打开 (3)首先打开止水夹a,让分液漏斗中酸液流下,使A中产生的H2通入B中,一段时间后关闭止水夹a,A中液体沿导管流入B中,产生少量白色沉淀 (4)4Fe(OH)2+O2+2H2O===4Fe(OH)3 (5)能Fe2+、Fe3+的检验方法[问题1] 怎样用化学方法检验FeSO4试剂是否变质?[提示] FeSO4变质就是Fe2+被空气中的氧气氧化为Fe3+,可用KSCN溶液检验是否含有Fe3+。[问题2] 先向溶液中滴加少量氯水,再加KSCN溶液,溶液变为红色,能否证明原溶液中含有Fe2+?[提示] 不能证明原溶液中含有Fe2+,因为若原溶液中含有Fe3+,溶液也变红色,干扰Fe2+的检验。[问题3] 如何检验溶液中既含Fe2+又含Fe3+?[提示] 取一份待检液,滴入几滴KSCN溶液,溶液呈红色,说明含Fe3+;另取一份待检液,滴入几滴酸性KMnO4溶液,溶液紫红色褪去,说明含Fe2+。Fe3+、Fe2+的检验1.观察溶液颜色法2.KSCN溶液和氯水法3.NaOH溶液法4.酸性KMnO4溶液法1.为了检验某FeCl2溶液是否变质,可向溶液中加入( )A.NaOH溶液 B.铁片C.KSCN溶液 D.石蕊溶液C [FeCl2变质会被氧化为FeCl3,Fe3+遇KSCN溶液变红色,故可用KSCN溶液检测溶液是否变红色,来判断FeCl2溶液是否变质。]2.将铁的化合物溶于盐酸,滴加KSCN溶液不发生颜色变化,再加入适量氯水,溶液立即呈红色,该铁的化合物是( )A.Fe2O3 B.FeCl3C.Fe2(SO4)3 D.FeOD [由题意可知溶于盐酸后溶液中只有Fe2+没有Fe3+,只有FeO溶解在盐酸中能得到Fe2+:FeO+2H+===Fe2++H2O。]3.下列离子的检验方法合理的是( )A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+B.向某溶液中通入Cl2,然后加入KSCN溶液,溶液变为红色,说明原溶液中含有Fe2+C.向某溶液中加入NaOH溶液,生成红褐色沉淀,说明溶液中含有Fe3+D.向某溶液中加入NaOH溶液生成白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+C [向某溶液中滴加KSCN溶液,溶液呈红色,证明存在Fe3+,不能证明没有Fe2+,故A项错误;若原溶液中不含Fe2+,含有Fe3+,通入Cl2,加入KSCN溶液,溶液也变为红色,故B项错误;加入NaOH溶液,生成红褐色沉淀,说明溶液中含有Fe3+,故C项正确;若存在Mg2+,生成的氢氧化镁为白色沉淀,氢氧化铁沉淀的红褐色可掩盖氢氧化镁沉淀的白色,故D项错误。]1.下列各组物质反应后,再滴入KSCN溶液,显红色的是( )A.向CuCl2溶液中加入铁粉B.向FeO粉末中加入稀硫酸C.Fe与过量稀盐酸反应后的溶液中再加入少量氯水D.Fe(OH)3与过量稀盐酸反应后的溶液中再加入过量铁粉C [A项,铁粉与CuCl2溶液反应生成FeCl2,溶液中不存在Fe3+,滴入KSCN溶液,溶液不会显红色,错误;B项,向FeO粉末中加入稀硫酸,反应生成FeSO4和水,不含有Fe3+,滴入KSCN溶液,溶液不会显红色,错误;C项,Fe与过量稀盐酸反应生成FeCl2和氢气,FeCl2与氯气反应生成FeCl3,溶液中存在Fe3+,滴入KSCN溶液,溶液显红色,正确;D项,Fe(OH)3与过量稀盐酸反应生成FeCl3和水,FeCl3与过量铁粉反应生成FeCl2,溶液中不存在Fe3+,滴入KSCN溶液,溶液不会显红色,错误。]2.鉴别Fe2+和Fe3+可用下列试剂中的( )①NaOH溶液 ②稀H2SO4 ③KSCN溶液 ④铜片 ⑤KI淀粉溶液A.①②③ B.①③④⑤C.③④⑤ D.②③④B [①向Fe2+溶液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色;Fe3+与OH-反应,生成红褐色Fe(OH)3沉淀;②稀硫酸和Fe2+及Fe3+都不反应,不能区别Fe2+和Fe3+;③加入KSCN溶液,Fe3++3SCN-Fe(SCN)3,溶液立即呈红色,证明含有Fe3+;④2Fe3++Cu===Cu2++2Fe2+,铜片溶解,溶液由黄色变成蓝绿色,Fe2+与铜片不反应;⑤2Fe3++2I-===2Fe2++I2,碘遇淀粉溶液变蓝色。]3.下列说法正确的是( )A.Fe在一定条件下与水反应生成H2和Fe(OH)3B.Fe3O4溶于盐酸后加入几滴KSCN溶液,溶液不会显红色C.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁D.Fe3+具有氧化性,据此可用KSCN溶液鉴别Fe3+C [高温下铁能与水蒸气反应生成Fe3O4和H2,故A项错误;Fe3O4溶于盐酸生成Fe3+和Fe2+,Fe3+与KSCN反应得到红色溶液,故B项错误;一般炼铁的过程就是用CO还原Fe2O3生成Fe,故C项正确;用KSCN溶液鉴别Fe3+主要是利用了Fe3+与KSCN溶液反应显示红色,而非Fe3+的氧化性,故D项错误。]4.下列叙述不正确的是( )选项被提纯物质杂质除杂试剂或方法AFeCl3溶液FeCl2通入适量Cl2BFeCl2溶液FeCl3加入过量铁粉并过滤C银粉铁粉加入过量盐酸并过滤DFe(OH)3Fe(OH)2在空气中灼烧D [A项发生反应:2FeCl2+Cl2===2FeCl3,正确;B项发生反应:Fe+2FeCl3===3FeCl2,正确;C项银与盐酸不反应,而Fe与盐酸反应,正确;D项混合物在空气中灼烧时,Fe(OH)3最终转变为Fe2O3,错误。]5.已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。(1)写出A、C、F、G的化学式A.________ C.________ F.________ G.________。(2)检验D中阳离子的方法为_____________________________________。(3)写出下列转化的离子方程式或化学方程式。①E→F:__________________________________________________。②C→D:___________________________________________________。[解析] 根据F是红褐色沉淀知F是Fe(OH)3,从而推知A为Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,G为Fe2O3,X为H2。[答案] (1)Fe FeCl2 Fe(OH)3 Fe2O3(2)取D溶液少许于洁净试管中,加入几滴KSCN溶液,溶液变红色,证明含Fe3+(合理即可)(3)①4Fe(OH)2+O2+2H2O===4Fe(OH)3②2Fe2++Cl2===2Fe3++2Cl-





