
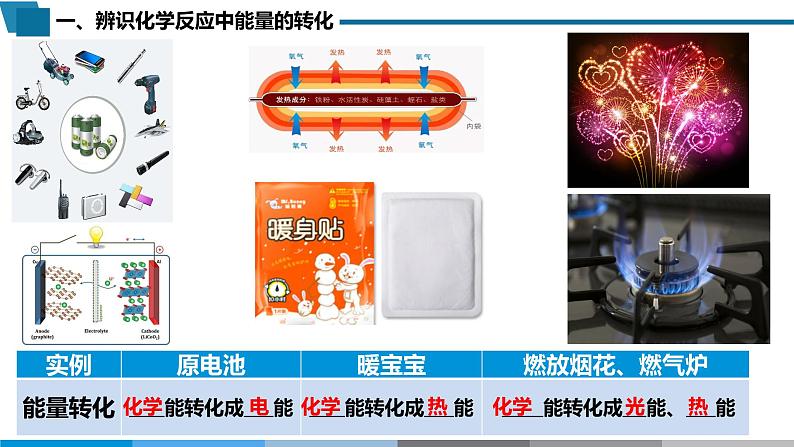



高中人教版 (2019)第一节 反应热优秀教学课件ppt
展开为什么化学反应会有能量的变化?
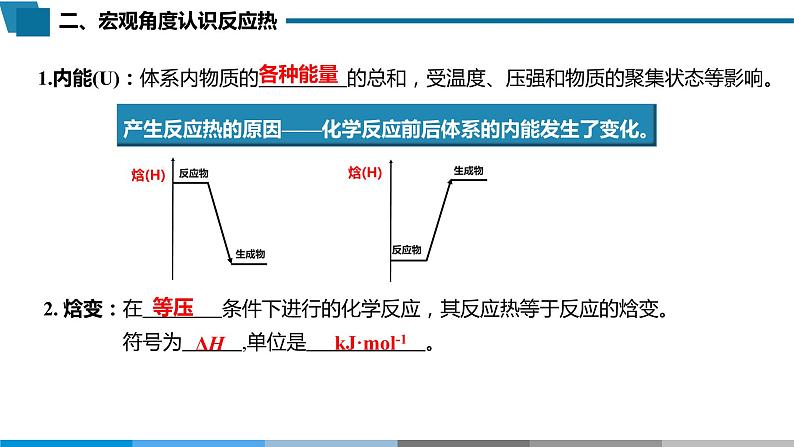
1.内能(U):体系内物质的 的总和,受温度、压强和物质的聚集状态等影响。
2. 焓变:在 条件下进行的化学反应,其反应热等于反应的焓变。 符号为 ,单位是 。
产生反应热的原因——化学反应前后体系的内能发生了变化。
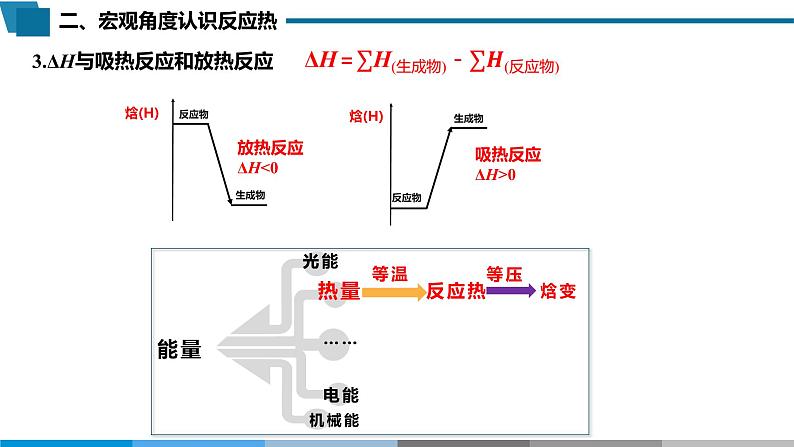
3.ΔH与吸热反应和放热反应
在25℃,101kPa下,1 ml H2与1 ml Cl2反应生成2 ml HCl,放出184.6 kJ的热量,该反应的反应热为
ΔH= -184.6 kJ·ml-1
在25℃,101kPa下,1 ml C 与1 ml H2O(g) 反应生成1 ml CO和1 ml H2,需要吸收131.5 kJ的热量,该反应的反应热为
ΔH= + 131.5 kJ·ml-1
注意:“+” 、 “-”不能省略!
化学反应能量是如何转化的?
键能:在25 ℃,101 kPa下,1ml 气态分子解离成气态原子所吸收的能量。 用符号 E 表示,单位为 kJ.ml-1。
243 kJ.ml-1
243 kJ.ml-1
以H2(g)+Cl2(g)===2HCl(g)反应的能量变化为例
-183 kJ·ml-1
结论:化学键的断裂和形成时的能量变化是化学反应中能量变化的主要原因。
实测值(ΔH= -184.6 kJ·ml-1)
【利用键能估算反应热】
反应热 ΔH= 。
E1:反应物断裂化学键吸收的总能量,E2:生成物形成化学键放出的总能量,
吸收能量 >放出能量 ΔH > 0 吸收能量 <放出能量 ΔH < 0
【 利用键能估算反应热】
【例1】化学反应N2(g)+3H2(g)⇌2NH3(g)的能量变化如图所示: 已知N≡N、N—H的键能分别为946 kJ·ml-1、391 kJ·ml-1
(1)该反应为______反应(填“吸热”或“放热”)。(2)拆开1 ml H2中化学键所需能量为______ kJ。(3)该反应的反应热ΔH=______________。
- 92 kJ·ml-1
【例2】下列判断氢气燃烧生成气态水时的热量变化的说法中一定正确的是( )
A. 生成1 ml H2O(g)时吸收热量245 kJB. H2O(g)分解为H2与O2时放出热量C. 氢气和氧气的总能量小于气态水的能量D. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
ΔH=436+249-930= -245 (kJ·ml-1)
反应放热,且用量未注明
研究反应热的意义是什么?
反应热估算键能估算能耗……
给吸热反应加热;给放热反应及时转移热量;热能循环利用。
负 极:2Fe - 4e- = 2Fe2+正 极: O2 + 4e- + 2H2O = 4OH-总反应:2Fe + 2O2 + 2H2O = 2Fe(OH)2 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
铁粉的缓慢氧化放热,形成原电池加速氧化,利用蛭石材料保温。
ΔH>0 反应吸热;ΔH<0反应放热
工艺条件优化;理论研究
1.下列说法正确的是( ) A.化学变化中的能量变化都是化学能与热能间的相互转化 B.伴有能量变化的一定是化学反应 C.加热条件下发生的反应均为吸热反应 D.一个化学反应中,当反应物总焓大于生成物的总焓时,反应放热ΔH为负值
2.白磷和红磷分别与氧气反应生成1 ml P4O10(s)过程中焓变化如图,下列说法正确的是( )A.红磷比白磷稳定B.白磷燃烧是吸热反应C.红磷转变为白磷是放热反应D.红磷燃烧反应的:4P(s)+5O2(g)===P4O10(s) ΔH=-(E3-E2) kJ/ml
3. 在日常生活和学习中,我们经常接触到下列反应: ①化石燃料燃烧 ②强酸、强碱的中和反应 ③用C和H2O在高温下制水煤气 ④锌和盐酸反应制氢气 ⑤氢氧化钡晶体和氯化铵晶体研磨放出氨气 ⑥煅烧石灰石 其中焓变为负值的有________,焓变为正值的有________。
4.化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示。下列有关叙述正确的是( ) A. 该反应每生成2 ml AB(g)吸收b kJ热量 B. 反应热ΔH=+(a-b) kJ·ml-1 C. 该反应中反应物的总能量高于生成物的总能量 D. 断裂1 ml A—A 和1 ml B—B放出 a kJ 能量
5. 根据下图所示的过程中的能量变化情况,判断下列说法正确的是( )
A.H2(g)转化为氢原子是一个放热过程 B.1 ml H2和1 ml Cl2的总能量比2 ml HCl的总能量高 C.1个HCl(g)分子中的化学键断裂时需要吸收431 kJ能量 D.2HCl(g)===H2(g)+Cl2(g)的反应热ΔH=-183 kJ·ml-1
①②④ ③⑤⑥
高中化学人教版 (2019)选择性必修1第一节 反应热教课课件ppt: 这是一份高中化学人教版 (2019)选择性必修1第一节 反应热教课课件ppt,共60页。
化学选择性必修1第一节 反应热获奖课件ppt: 这是一份化学选择性必修1第一节 反应热获奖课件ppt,共24页。PPT课件主要包含了学习目标,一反应热及其测定,实验用品,实验步骤,注意事项等内容,欢迎下载使用。
人教版 (2019)选择性必修1第一节 反应热评优课ppt课件: 这是一份人教版 (2019)选择性必修1第一节 反应热评优课ppt课件,共21页。PPT课件主要包含了反应热与焓变,反应热的应用,复习与思考,化学反应,放热反应,吸热反应,常见的放热反应,常见的吸热反应,偏二甲肼燃烧,★主要原因等内容,欢迎下载使用。













