





- 第3章 本章知识体系构建与核心素养提升课件PPT 课件 0 次下载
- 第3章 第一节 卤代烃课件PPT 课件 0 次下载
- 第3章 第二节 第1课时 醇课件PPT 课件 0 次下载
- 第3章 第二节 第2课时 酚课件PPT 课件 0 次下载
- 第3章 第五节 第1课时 有机合成的主要任务课件PPT 课件 1 次下载
高中人教版 (2019)第三节 醛酮精品课件ppt
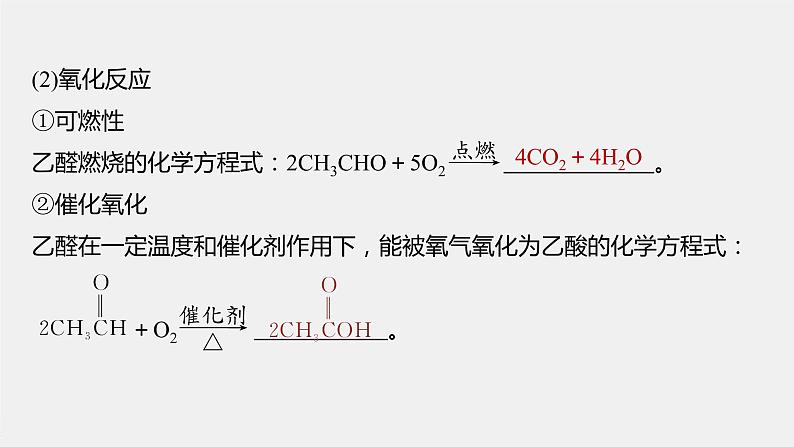
展开第三节 醛 酮1.通过醛基中原子成键情况的分析,了解醛类的结构特点,理解乙醛 的化学性质与醛基的关系,学会醛基的检验方法。2.了解甲醛对环境和健康的影响,关注有机化合物安全使用的问题。一、乙醛的性质随堂演练 知识落实课时对点练二、醛的结构与常见的醛内容索引 三、酮的结构与性质1.醛的概念及结构特点醛是由烃基(或氢原子)与 相连而构成的化合物。醛类官能团的结构简式是 ,饱和一元醛的通式为 或 。2.乙醛的结构与物理性质一、乙醛的性质醛基—CHOCnH2nO(n≥1)CnH2n+1CHOC2H4O无刺激性挥发燃烧水乙醇3.乙醛的化学性质(1)加成反应①催化加氢(还原反应)乙醛中的碳氧双键和烯烃中的碳碳双键性质类似,也能与氢气发生加成反应,化学方程式为CH3CHO+H2 。CH3CH2OH②与HCN加成在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分 ,碳原子带部分 ,从而使醛基具有较强的 。乙醛能和一些极性试剂例如氰化氢(HCN)发生加成反应: +H—CN―→ 。负电荷正电荷极性(2-羟基丙腈)(2)氧化反应①可燃性乙醛燃烧的化学方程式:2CH3CHO+5O2 。②催化氧化乙醛在一定温度和催化剂作用下,能被氧气氧化为乙酸的化学方程式: +O2 。4CO2+4H2O③与银氨溶液反应先产生白色沉淀后变澄清光亮的银镜AgNO3+NH3·H2O===AgOH↓(白色)+NH4NO3,AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2OCH3CHO+2[Ag(NH3)2]OH 2Ag↓+CH3COONH4+3NH3+H2O④与新制氢氧化铜反应蓝色絮状沉淀砖红色沉淀2NaOH+CuSO4===Cu(OH)2↓+Na2SO4CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O⑤乙醛能被酸性高锰酸钾溶液、溴水等强氧化剂氧化。(1)乙醛能使酸性高锰酸钾溶液褪色( )(2)乙醛和乙酸的混合液可以用分液漏斗分离( )(3)用新制银氨溶液可区分甲酸甲酯和乙醛( )(4)银氨溶液的配制,将硝酸银溶液滴加到氨水中至生成的白色沉淀恰好完全溶解为止( )(5)乙醛加氢得到乙醇的反应是加成反应,也称为还原反应( )√×××√完成银镜反应实验:在AgNO3溶液中逐滴加入氨水,开始时在AgNO3溶液中出现_________,反应的离子方程式为_________________________________,继续滴入氨水则______________,反应的化学方程式为_______________________________________,边滴边振荡直滴到____________为止。再加入乙醛溶液后,水浴加热,现象是___________,化学方程式为_____________________________________________________________。白色沉淀Ag++NH3·H2O===AgOH↓白色沉淀溶解AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2O沉淀恰好溶解有银镜产生1.醛与弱氧化剂发生化学反应的注意事项(1)银镜反应①试管内壁必须洁净;②银氨溶液随用随配,不可久置;③水浴加热,不可用酒精灯直接加热;④醛用量不宜太多;⑤不可搅拌、振荡。(2)与新制的Cu(OH)2反应①Cu(OH)2必须用新配制的;②配制Cu(OH)2时,所用NaOH必须过量;③反应液必须直接加热煮沸。2.使溴水、酸性KMnO4溶液褪色的有机物注:“√”代表能褪色,“×”代表不能褪色。返回1.常见的醛(1)甲醛:又名蚁醛,是结构最简单的醛,结构简式为 。通常状况下是一种 色有强烈 气味的气体,易溶于水。它的水溶液又称 ,具有杀菌、防腐性能,可用于消毒和制作生物标本。①结构特点甲醛的分子式为CH2O,其分子可以看成含两个醛基,如图:二、醛的结构与常见的醛HCHO无刺激性福尔马林②甲醛氧化反应的特殊性甲醛发生氧化反应时,可理解为 。所以,甲醛分子中相当于有2个—CHO,当与足量的银氨溶液或新制的Cu(OH)2作用时,可存在如下量的关系:1 mol HCHO~ mol Ag;1 mol HCHO~ mol Cu(OH)2~2 mol Cu2O。44(2)苯甲醛苯甲醛是最简单的芳香醛,俗称 ,是一种有苦杏仁气味的无色液体。苯甲醛是制造染料、香料及药物的重要原料。苦杏仁油2.醛的化学通性(1)醛可被氧化为羧酸,也可被氢气还原为醇,因此醛既有 性,又有 性,其氧化、还原的关系为R—CH2OH 。(2)有机物的氧化、还原反应①氧化反应:有机物分子中失去 或加入 的反应,即加氧去氢。②还原反应:有机物分子中加入 或失去 的反应,即加氢去氧。氧化还原氧原子氢原子氧原子氢原子③醛基的检验:在洁净的试管中加入新制银氨溶液和少量试样后,水浴加热,有银镜生成,或在洁净的试管中加入少量试样和新制的Cu(OH)2,加热煮沸,有砖红色沉淀生成。(1)1 mol HCHO发生银镜反应最多生成2 mol Ag( )(2)甲醛的水溶液俗称福尔马林,浸制生物标本,具有防腐性( )(3)碳原子数相同的醛和醚互为同分异构体( )×√×1.乙醇、乙醛和乙酸三者转化关系如图所示,请结合具体反应和三者的分子结构、官能团的变化情况,谈谈有机化学反应中的氧化反应和还原反应的特点。答案 乙醇被氧化为乙醛时醇羟基被氧化为—CHO,从组成上看减少了2个氢原子,乙醛被氧化成乙酸时,—CHO变成—COOH,从组成上看增加了氧原子,乙醛被还原为乙醇时—CHO变成—CH2OH,从组成上看增加了氢原子。因此,有机化学反应若从氢氧原子数目变化角度来看,失去氢原子、增加氧原子的反应过程称为氧化反应。增加氢原子、失去氧原子的过程称为还原反应。2.下列物质各1 mol与足量的银氨溶液反应,析出银的质量相等的是①HCHO ②CH3CHO ③(CH3)2CHCHO ④OHC(CH2)3CHOA.①②③ B.①④ C.①②③④ D.③④解析 由甲醛结构式可知甲醛相当于二元醛,1 mol甲醛与足量银氨溶液反应能生成4 mol Ag;OHC(CH2)3CHO为二元醛,1 mol该醛与足量银氨溶液反应生成4 mol Ag;②③中的醛均为一元醛,1 mol醛与足量银氨溶液反应均生成2 mol Ag。故答案为①④或②③。√3.茉莉醛具有浓郁的茉莉花香,其结构简式为 ,下列说法错误的是______(填字母)。A.在加热和催化剂作用下,能被氢气还原B.能被酸性高锰酸钾溶液氧化C.在一定条件下能与液溴发生取代反应D.不能与HBr发生加成反应E.1 mol茉莉醛发生银镜反应,可生成1 mol银F.1 mol茉莉醛最多与4 mol H2加成DEF解析 茉莉醛能与H2发生加成反应,即能发生还原反应,A正确;该物质中存在碳碳双键,可以使酸性高锰酸钾溶液褪色,B正确;苯环上的氢在铁粉作用下能与溴单质发生取代反应,C正确;碳碳双键不仅可与H2加成,还可与H2O、HX等加成,D错误;1 mol茉莉醛含有1 mol醛基,可生成2 mol银,E错误;能与氢气反应的基团:苯环3 mol、碳碳双键1 mol、醛基1 mol,共消耗 5 mol H2。(1)醛的官能团为—CHO,不能写作—COH。(2) 分子中相当于有两个醛基,与银氨溶液反应,1 mol该分子生成4 mol Ag。(3)能发生银镜反应的物质不一定为醛,如 、 等均能发生银镜反应。返回1.酮的概念和结构特点三、酮的结构与性质2.丙酮(1)丙酮是最简单的酮类化合物,结构简式为: 。(2)丙酮的物理性质常温下丙酮是无色透明液体,沸点56.2 ℃,易 ,能与 等互溶。挥发水、乙醇(3)丙酮的化学性质不能被 等弱氧化剂氧化,但能催化加氢生成 。反应的化学方程式:银氨溶液、新制的氢氧化铜醇 。(1)酮类物质能与氢气发生加成反应,不能被银氨溶液氧化,所以只能发生还原反应,不能发生氧化反应( )(2)丙酮是结构最简单的酮,也可以发生银镜反应和加氢还原( )(3)丙酮难溶于水,但丙酮是常用的有机溶剂( )×××1.β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料。(1)β-紫罗兰酮分子式是________。解析 由结构简式可知该有机物分子式为C13H20O。C13H20O(2)1 mol β-紫罗兰酮最多能与____mol H2发生加成反应。3解析 碳碳双键和羰基都可与氢气发生加成反应,则1 mol β-紫罗兰酮最多能与3 mol H2发生加成反应。(3)β-紫罗兰酮与等物质的量溴加成时,能生成 ____种产物。解析 分子中有2个位置不同的碳碳双键,可发生1,2-加成或1,4-加成,与1 mol溴发生加成反应可得到3种不同产物。32.如何鉴别丙酮与丙醛?答案 用新制银氨溶液分别与两种物质混合,水浴加热,生成银镜的是丙醛,没有银镜生成的是丙酮。醛和酮的区别与联系返回解析 乙醛和甲醛都为醛类物质,都含有醛基,故A正确;乙醛由甲基和醛基组成,甲醛由氢原子和醛基组成,故B错误;乙醇经催化氧化生成乙醛,故C错误;醛基应表示为—CHO,故D错误。1.下列说法正确的是A.乙醛和甲醛分子中都有醛基B.乙醛由乙基和醛基组成,甲醛由甲基和醛基组成C.乙醇经催化还原可生成乙醛D.乙醛的官能团是醛基,醛基可表示为—COH随堂演练 知识落实123456√2.(2019·天津南开中学高二课时练习)下列物质不属于醛类的是① ② ③CH2==CH—CHO ④Cl—CH2—CHOA.①③ B.②④C.②③ D.①④12345√6解析 醛是由烃基(或氢原子)与醛基相连而构成的化合物。为苯甲醛,分子中含有官能团醛基,属于醛类,故不选①; 为甲酸甲酯,官能团为酯基,不属于醛类,故选②;CH2==CH—CHO为丙烯醛,分子中含有官能团醛基,属于醛类,故不选③;Cl—CH2—CHO中含有官能团醛基和碳氯键,属于氯代醛,不符合醛的概念,不属于醛类,故选④。1234563.下列有关银镜反应的说法中,正确的是A.配制银氨溶液时氨水必须过量B.1 mol甲醛发生银镜反应最多生成2 mol AgC.银镜反应通常采用水浴加热D.银镜反应后的试管一般采用稀盐酸洗涤12345√612345解析 配制银氨溶液时氨水不能过量,过量会生成易爆物质,故A错误;一个甲醛分子中含2个—CHO,故1 mol甲醛能反应生成4 mol Ag,故B错误;水浴加热能保证试管受热均匀,且易于控制反应温度,直接加热受热不均匀,故C正确;银和盐酸不反应,银镜反应所得的银镜,应用稀硝酸洗涤,故D错误。64.用2 mL 1 mol·L-1 CuSO4溶液与3 mL 0.5 mol·L-1 NaOH溶液混合后,加入40%的甲醛溶液0.5 mL,加热至沸腾,无砖红色沉淀生成,实验失败的主要原因是A.甲醛的量太少 B.CuSO4的量太少C.NaOH的量太少 D.加热的时间太短12345√6解析 该反应的本质是:甲醛中的醛基具有还原性,新制的Cu(OH)2具有弱氧化性,醛基与Cu(OH)2中的+2价的铜发生氧化还原反应。只要有醛基即可与新制的Cu(OH)2发生反应;根据题意可知:n(CuSO4)=2× 10-3 L×1 mol·L-1=0.002 mol,根据反应:Cu2++2OH-===Cu(OH)2↓,可知n(OH-)=2n(Cu2+)=0.004 mol,则需要0.5 mol·L-1 NaOH溶液的体积为 =8×10-3 L=8 mL,反应过程中要保持碱过量,则所需NaOH溶液的体积V>8 mL,而题中该NaOH溶液的体积为 3 mL,NaOH的量不够,导致实验中未见砖红色沉淀。故由以上结论可知,实验失败的主要原因是NaOH的量不够,C项正确。1234565.(2019·天津南开中学高二课时练习)下列说法中正确的是A.凡能发生银镜反应的物质一定是醛B.乙醛能发生银镜反应,表明了醛具有氧化性C.在加热和有催化剂的条件下,醇都能被空气中的O2所氧化,生成对应 的醛D.福尔马林是35%~40%的甲醛的水溶液,可用于浸制生物标本12345√612345解析 能发生银镜反应的物质含有醛基,但不一定为醛,如甲酸,A项错误;乙醛能发生银镜反应,表明了醛具有还原性,B项错误;在加热和有催化剂(如铜)的条件下,与羟基所连碳上有氢原子的醇可能被空气中的O2所氧化,生成对应的醛或酮,C项错误;福尔马林是35%~40%的甲醛水溶液,可以使蛋白质发生变性,可用于浸制生物标本,D项正确。66.(2020·湖北省高二月考)乙醛能与银氨溶液反应析出银,如果条件控制适当,析出的银会均匀分布在试管上,形成光亮的银镜,这个反应叫银镜反应。某实验小组对银镜反应产生兴趣,进行了以下实验。(1)配制银氨溶液时,随着向硝酸银溶液中滴加氨水,观察到先产生灰白色沉淀,而后沉淀消失,形成无色透明的溶液。该过程可能发生的反应有________(填字母)。A.AgNO3+NH3·H2O===AgOH↓+NH4NO3 B.AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2OC.2AgOH===Ag2O+H2OD.Ag2O+4NH3·H2O===2[Ag(NH3)2]OH+3H2OABCD123456解析 向硝酸银溶液中滴加氨水,首先发生复分解反应:AgNO3+NH3·H2O===AgOH↓+NH4NO3,AgOH能够被氨水溶解,会发生反应:AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2O;反应产生的AgOH不稳定,会发生分解反应:2AgOH===Ag2O+H2O,分解产生的Ag2O也会被氨水溶解得到氢氧化二氨合银,反应的化学方程式为Ag2O+4NH3·H2O=== 2[Ag(NH3)2]OH+3H2O,故合理选项是ABCD。123456(2)该小组探究乙醛发生银镜反应的最佳条件,部分实验数据如表:123456请回答下列问题:①推测当银氨溶液的量为1 mL,乙醛的量为3滴,水浴温度为60 ℃,反应混合液pH为11时,出现银镜的时间范围是___________。1234565~6 min解析 当银氨溶液的量为1 mL,乙醛的量为3滴,水浴温度为60 ℃,反应混合液pH为11时,由实验1和实验4可知出现银镜的时间范围是在5~ 6 min之间。②进一步实验还可探索_____________________________对出现银镜快慢的影响(写一条即可)。123456银氨溶液的用量不同或pH不同解析 根据实验1、2可知,反应温度不同,出现银镜时间不同;根据实验1、3 可知:乙醛的用量不同,出现银镜时间不同;在其他条件相同时,溶液的pH不同,出现银镜时间也会不同,故还可以探索银氨溶液的用量或溶液pH对出现银镜快慢的影响。(3)该小组查阅资料发现强碱条件下,加热银氨溶液也可以析出银镜,并做了以下两组实验进行分析证明。已知:[Ag(NH3)2]++2H2O Ag++2NH3·H2O。123456①两组实验产生的气体相同,该气体化学式为______,检验该气体可用________________试纸。123456NH3湿润的红色石蕊②实验Ⅰ的黑色固体中有Ag2O,产生Ag2O的原因是______________________________________________________________________________________________________________________________________________________________________________________________。123456在NaOH存在下,加热促进NH3·H2O的分解,逸出NH3,促使[Ag(NH3)2]++2H2O Ag++2NH3·H2O平衡正向移动,c(Ag+)增大,Ag+、OH-反应产生的AgOH立即转化为Ag2O:2Ag++2OH-===Ag2O↓+H2O(4)该小组同学在清洗试管上的银镜时,发现用FeCl3溶液清洗的效果优于Fe2(SO4)3溶液,推测可能的原因是____________________________;实验室中,我们常选用稀HNO3清洗试管上的银镜,写出Ag与稀HNO3反应的化学方程式:_________________________________________。123456产物AgCl的溶解度小于Ag2SO43Ag+4HNO3(稀)===3AgNO3+NO↑+2H2O解析 FeCl3和Fe2(SO4)3的阳离子都是Fe3+,阴离子不同,而在清洗试管上的银镜时,发现用FeCl3溶液清洗的效果优于Fe2(SO4)3溶液,这是由于Cl-与Ag+结合形成的AgCl是难溶性的物质,而 与Ag+结合形成的Ag2SO4微溶于水,物质的溶解度:Ag2SO4>AgCl,物质的溶解度越小,越容易形成该物质,使银单质更容易溶解而洗去,因此使用FeCl3溶液比Fe2(SO4)3溶液清洗效果更好。返回课时对点练题组一 醛类的组成与结构1.下列关于醛的说法中正确的是A.醛的官能团是B.所有醛中都含醛基和烃基C.一元醛的分子式符合CnH2nO的通式D.所有醛都能使溴水和酸性KMnO4溶液褪色,并能发生银镜反应123456789101112131415√解析 醛的官能团是醛基(—CHO);醛分子中都含有醛基(—CHO),醛基有较强的还原性,可还原溴水和酸性KMnO4溶液;甲醛中无烃基;只有饱和一元醛的通式为CnH2nO。1234567891011121314152.分子式为C5H10O,且结构中含有 的有机物共有A.4种 B.5种 C.6种 D.7种1234567891011121314√15123456789101112131415解析 分子式为C5H10O满足饱和一元醛、酮的通式CnH2nO,且结构中含有 ,故可以从醛类、酮类两方面考虑。醛类:可写为C4H9—CHO,因为C4H9—有4种结构,故醛有4种形式。酮类:可写为CH3COC3H7,因—C3H7有2种结构,故此种形式有2种,分别为CH3COCH2CH2CH3、CH3COCH(CH3)2;也可写成C2H5COC2H5,此种形式只有1种,所以酮类共有3种形式。综上所述,满足条件的有机物共有4+3=7种。12345678910111213143.(2020·合肥一六八中学高二)甲醛、乙醛、丙醛的混合物中,氢元素的质量分数为9%,则氧元素的质量分数为A.16% B.37%C.48% D.无法计算√15解析 由甲醛(HCHO)、乙醛(CH3CHO)和丙醛(CH3CH2CHO)组成的混合物中,C、H两种元素的原子个数始终是1∶2,C、H两种元素的质量比为(1×12)∶(2×1)=6∶1,由氢元素的质量分数为9%,则碳元素的质量分数为54%,因混合物中共有三种元素,则氧元素的质量分数为1-54%-9%=37%,故选B。题组二 醛、酮的结构与性质4.(2020·云南省墨江第二中学高二期末)下列醇中能由醛加氢还原制得的是A.CH3CH2CH2OH B.(CH3)2CHCH(CH3)OHC.(CH3)3COH D.(CH3)2CHOH123456789101112131415解析 CH3CH2CH2OH能够由CH3CH2CHO加成反应生成,故A正确;(CH3)2CHCH(CH3)OH中与羟基相连的碳原子上有1个氢原子,故B错误;(CH3)3COH中与羟基相连的碳原子上没有氢原子,不能够由醛或酮加氢还原制得,故C错误;(CH3)2CHOH中与羟基相连的碳原子上有1个氢原子,故D错误。√5.(2020·枣庄市第三中学高二月考)已知醛或酮可与格氏试剂(R′MgX)发生加成反应,所得产物经水解可得醇,若用此种方法制取HOC(CH3)2CH2CH3,可选用的醛或酮与格氏试剂是A. 与 B.CH3CH2CHO与CH3CH2MgXC.CH3CHO与 D. 与CH3CH2MgX√123456789101112131415解析 二者反应后水解生成HOCH2CH(CH3)CH2CH3,A不符合题意;二者反应后水解生成CH3CH2CH(OH)CH2CH3,B不符合题意;二者反应后水解生成CH3CH(OH)CH(CH3)2,C不符合题意;二者反应后水解生成HOC(CH3)2CH2CH3,D符合题意。1234567891011121314156.(2020·应城市第一高级中学高二期中)有机物A是一种重要的化工原料,其结构简式为 ,下列关于A的说法不正确的是A.能被银氨溶液氧化B.能使酸性KMnO4溶液褪色C.1 mol A只能与1 mol H2发生加成反应D.检验A中官能团的一种方法:先加入足量的新制Cu(OH)2,微热,酸化 后再加溴水123456789101112131415√解析 有机物A中所含的官能团有—CHO,能被银氨溶液氧化,故A正确;有机物A含有碳碳双键和—CHO,都能使酸性KMnO4溶液褪色,故B正确;1 mol A中含碳碳双键和—CHO各1 mol,能与2 mol H2发生加成反应,故C错误;碳碳双键和—CHO均能使溴水褪色,先加新制Cu(OH)2,微热产生砖红色沉淀,能检验出—CHO,反应后溶液仍显碱性,溴水能与碱反应,需加酸酸化,再加溴水,溴水褪色检验出碳碳双键,故D正确。1234567891011121314157.(2020·河北省张家口一中高二期中)C、H、O三种元素组成的T、X在一定条件下可以发生如下转化:X不稳定,易分解。为使转化能够成功进行,方框内不可能加入的试剂是A.新制的Cu(OH)2 B.NaOH溶液C.KMnO4溶液 D.[Ag(NH3)2]OH溶液123456789101112131415√解析 HCHO中含有两个—CHO,能被新制的Cu(OH)2氧化为—COOH,从而生成H2CO3,A不符合题意;NaOH溶液没有氧化性,与HCHO不发生反应,不能将其氧化为H2CO3,B符合题意;KMnO4溶液为强氧化剂,能将HCHO氧化为H2CO3,C不符合题意;[Ag(NH3)2]OH溶液具有与新制的Cu(OH)2类似的性质,D不符合题意。1234567891011121314158.格林尼亚试剂简称“格氏试剂”,它是卤代烃与金属镁在无水乙醚中作用得到的,如:CH3CH2Br+Mg CH3CH2MgBr,它可与羰基发生加成反应,其中的“—MgBr”部分加到羰基的氧上,所得产物经水解可得醇。今欲通过上述反应合成2-丙醇,选用的有机原料正确的一组是A.溴乙烷和甲醛 B.溴乙烷和丙醛C.甲烷和丙酮 D.甲烷和乙醛1234567891011121314√15解析 考查有机物的合成。根据题意,要得到2-丙醇,则必须有CH3CH(OMgBr)CH3,因此必须有CH3CHO和CH3MgBr;答案选D。题组三 醛类的简单计算9.1 mol有机物 与足量的氢气和新制备的氢氧化铜反应,消耗的氢气与氢氧化铜的物质的量分别是A.1 mol 2 mol B.3 mol 4 molC.3 mol 2 mol D.1 mol 4 mol√123456789101112131415解析 由有机物的结构简式知,1 mol有机物中含2 mol —CHO和1 mol ,故需加3 mol H2,—CHO~2Cu(OH)2,故2 mol —CHO消耗4 mol Cu(OH)2,故选B项。10.(2020·馆陶县第一中学高二月考)某饱和一元醛发生银镜反应,可得21.6 g银,等物质的量的该醛完全燃烧时生成7.2 g水,则该醛可能是A.乙醛 B.丙醛C.甲醛 D.丁醛√解析 21.6 g银的物质的量是n(Ag)= 21.6 g ÷108 g·mol-1= 0.2 mol,根据醛发生银镜反应后产生的银之间的物质的量关系R—CHO~2Ag,反应产生0.2 mol Ag,则饱和一元醛物质的量为0.1 mol。醛完全燃烧时,生成水的质量为7.2 g,n(H2O)= 7.2 g ÷18 g·mol-1=0.4 mol,则其中含H为0.8 mol,根据饱和一元醛分子式通式CnH2nO,2n=8,所n=4,则该醛为丁醛,故合理选项是D。123456789101112131415题组四 新情境下醛的性质考查11.(2020·大同高二期中)有机物A是合成二氢荆芥内酯的重要原料,其结构简式为 ,下列检验A中官能团的试剂和顺序正确的是A.先加酸性高锰酸钾溶液,后加银氨溶液,微热B.先加溴水,后加酸性高锰酸钾溶液C.先加新制的氢氧化铜,微热,再加入溴水D.先加入银氨溶液,微热,酸化后再加溴水√123456789101112131415解析 先加酸性高锰酸钾溶液,碳碳双键、—CHO均被氧化,不能检验,故A项错误;先加溴水,碳碳双键发生加成反应,—CHO被氧化,不能检验,B项错误;先加新制的氢氧化铜,加热,可检验—CHO,但没有酸化,加溴水可能与碱反应,C项错误;先加入银氨溶液,微热,可检验—CHO,酸化后再加溴水,可检验碳碳双键,故D项正确。123456789101112131415123456789101112131412.(2020·张家界期中)人们能够在昏暗的光线下看见物体,是因为视网膜中的“视黄醛”吸收光线后,其分子结构由顺式转变为反式(如图所示),并从所在蛋白质上脱离,这个过程产生的信号传递给大脑。下列有关“视黄醛”的说法正确的是A.“视黄醛”属于烯烃B.“视黄醛”的分子式为C20H15OC.“视黄醛”能与银氨溶液发生银镜反应D.在金属镍催化并加热条件下,1 mol“视黄醛”最多能与5 mol H2发生 加成反应√15解析 因烯烃只含C、H元素,而“视黄醛”中含有O元素,则不属于烯烃,故A错误;由结构可知,每个折点都有1个C原子,则1个“视黄醛”分子中含有19个C原子,故B错误;分子中含有—CHO,能发生银镜反应,则“视黄醛”能与银氨溶液发生银镜反应,故C正确;1 mol“视黄醛”分子中含有5个碳碳双键和1个醛基,所以在金属镍催化并加热条件下,1 mol“视黄醛”最多能与6 mol H2发生加成反应,故D错误。12345678910111213141513.(2020·安徽省长丰县第一中学高二月考)向溴水中加入足量乙醛溶液,可以看到溴水褪色。据此对溴水与乙醛发生的有机反应类型进行如下探究,请你完成下列填空:Ⅰ.猜测:(1)溴水与乙醛发生取代反应;(2)溴水与乙醛发生加成反应;(3)溴水与乙醛发生______反应。氧化解析 乙醛中官能团为—CHO,—CHO具有还原性,可被氧化,所以可能发生氧化反应。123456789101112131415123456789101112131415Ⅱ.设计方案并论证:为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:方案1:检验褪色后溶液的酸碱性。方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-的物质的量。(1)方案1是否可行?_______。理由是_________________________________________________________________________。解析 方案1中,无论取代(生成HBr)或氧化乙醛(生成CH3COOH),均使反应后溶液显酸性,故不可行。不可行溴水与乙醛发生取代反应有HBr生成,乙醛被氧化生成乙酸和HBr,溶液均呈酸性123456789101112131415(2)假设测得反应前用于溴水制备的Br2的物质的量为a mol,若测得反应后n(Br-)=_____ mol,则说明溴水与乙醛发生加成反应;若测得反应后n(Br-)=_____ mol,则说明溴水与乙醛发生取代反应;若测得反应后n(Br-)=_____ mol,则说明猜测(3)正确。解析 由于乙醛是足量的,乙醛中官能团为—CHO,溴水中的溴全部参与反应:取代反应后生成n(Br-)=a mol,加成反应后n(Br-)=0 mol,氧化反应后n(Br-)=2a mol。0a2a123456789101112131415Ⅲ.实验验证:某同学在含0.005 mol Br2的10 mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀1.88 g(已知反应生成的有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为____________________________________________。解析 得到固体1.88 g为AgBr的质量,n(AgBr)= =0.01 mol,n(Br-)=2n(Br2),则反应为氧化反应,其离子方程式为CH3CHO+Br2+H2O===CH3COOH+2H++2Br-。CH3CHO+Br2+H2O===CH3COOH+2H++2Br-123456789101112131415Ⅳ.拓展:请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。在两支洁净的试管中分别加入2 mL新制银氨溶液,各滴入几滴乙醛和乙醇,振荡,水浴加热滴加乙醛的试管中有银镜生成,而滴加乙醇的试管无现象乙醛的还原性比乙醇强123456789101112131415解析 乙醛能与银氨溶液发生氧化反应,乙醇不能,依此设计实验。123456789101112131414.(2020·绥棱县第一中学高二月考)已知:醛在一定条件下可以两分子间反应RCH2CHO+RCH2CHO ,兔耳草醛是重要的合成香料,它具有独特的新鲜水果的清香。由枯茗醛( )合成兔耳草醛的路线如下:151234567891011121314(1)枯茗醛的核磁共振氢谱有____种峰;A→B的反应类型是__________。15解析 枯茗醛除醛基外,分子中上下对称,其对称位上的氢是等效的,故其核磁共振氢谱有5种峰,A→B的过程中A脱去了一个H2O生成B中多了一个碳碳双键,所以反应类型是消去反应。5消去反应(2)B中含有的官能团是_____________________(写结构式);检验B中含氧官能团的实验试剂是___________。解析 根据B的结构可知B中含有的官能团是碳碳双键和醛基,结构式为 、 ,其中含氧官能团为醛基,检验醛基可用银氨溶液,其方法是将B加入到银氨溶液中再水浴加热,如果出现银镜,说明其中有醛基。银氨溶液、123456789101112131415(3)写出C→兔耳草醛的化学方程式:_______________________________________________________________。解析 由上述分析,C发生催化氧化生成兔耳草醛,反应的化学方程式为 +O2 +2H2O。123456789101112131415(4)枯茗醛发生银镜反应的化学方程式:____________________________________________________________________________________________。12345678910111213141512345678910111213141515.甲醛是众多醛类物质中的一种,是一种具有较高毒性的物质。结合相关知识回答下列问题:(1)下列说法不正确的是____(填字母)。A.选购家具时,用鼻子嗅一嗅家具抽屉等部位可初步判断家具是否含有 较多甲醛B.甲醛就是福尔马林,可用于浸制动物标本C.甲醛可使酸性KMnO4溶液褪色B123456789101112131415解析 根据分析可知:甲醛具有刺激性气味,室内空气中的甲醛主要来源于装修材料及家具使用的人造木板,故选购家具时,可以靠近家具的抽屉及衣橱等部位,用鼻子嗅一嗅,看是否有刺激性气味,是否强烈,A项正确;福尔马林是35%~45%的甲醛水溶液,故甲醛就是福尔马林的说法错误,B项错误;甲醛具有还原性,可被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,C项正确;答案选B。1234567891011121314151234567891011121314(2)甲醛也是一种重要的工业原料,以HCHO和CH≡CH为有机原料,经过下列反应可得化合物C(C4H8O4):15①反应Ⅰ的反应类型为__________。加成反应解析 由分析可知,在反应Ⅰ中,甲醛的醛基中的C==O断裂,与乙炔发生了加成反应生成HOCH2C≡CCH2OH,反应类型为加成反应。1234567891011121314②HOCH2C≡CCH2OH分子中,在同一平面上的原子最多有_____个。158解析 根据与三键直接相连的原子共直线可知,4个C原子在一条直线上,又—CH2—为四面体结构,最多有3个原子共面,单键O—H可旋转,则在同一个平面上的原子最多有8个。1234567891011121314③写出反应Ⅳ的化学方程式:________________________________________________________。15HOOCCH2CH2COOH解析 反应Ⅳ为丁二醛(OHCCH2CH2CHO)被O2氧化成丁二酸(HOOCCH2CH2COOH)的过程,反应方程式为:OHCCH2CH2CHO+O2 HOOCCH2CH2COOH。④写出B与新制的Cu(OH)2反应的化学方程式:________________________________________________________________________________。OHCCH2CH2CHO+解析 由分析知B为丁二醛(OHCCH2CH2CHO),能与新制的Cu(OH)2反应生成丁二酸(HOOCCH2CH2COOH)、Cu2O和H2O,反应方程式为OHCCH2CH2CHO+4Cu(OH)2+2NaOH NaOOCCH2CH2COONa+2Cu2O↓+6H2O。123456789101112131415返回
高中化学第三节 醛酮一等奖课件ppt: 这是一份高中化学第三节 醛酮一等奖课件ppt,共38页。
人教版 (2019)选择性必修3第三节 醛酮优质课课件ppt: 这是一份人教版 (2019)选择性必修3第三节 醛酮优质课课件ppt,共39页。
人教版 (2019)选择性必修3第三节 醛酮课前预习ppt课件: 这是一份人教版 (2019)选择性必修3第三节 醛酮课前预习ppt课件













