
所属成套资源:各地区2020-2022三年高一化学下学期期末试题按题型汇编
山东省菏泽市2020-2022三年高一化学下学期期末试题汇编1-选择题①
展开
这是一份山东省菏泽市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共15页。试卷主要包含了化学与生产生活密切相关,下列有关化学用语表示正确的是,实验是化学研究的基础等内容,欢迎下载使用。
山东省菏泽市2020-2022三年高一化学下学期期末试题汇编1-选择题①
1.(2020春·山东菏泽·高一统考期末)在下列自然资源的开发利用中,不涉及化学变化的是
A.石油分馏 B.从海带灰中提取碘单质
C.用石油裂解生产乙烯 D.用煤干馏生产焦炭
2.(2020春·山东菏泽·高一统考期末)中国核工业集团核工业北京地质研究院院长李子颖带领的科研团队首次在自然界中发现零价金属铀,这一重大发现将使我国的可控核聚变乃至无限能源研究富有更广阔的前景。铀元素有3种核素,其中一种是U,其核内的中子数和质子数之差是
A.146 B.54 C.238 D.92
3.(2020春·山东菏泽·高一统考期末)化学与生产生活密切相关。下列说法错误的是
A.淀粉、蛋白质、油脂都能发生水解反应
B.75%酒精可用于消毒杀死新冠病毒, 不能与含氯消毒剂混用
C.84 消毒液的主要成分是次氯酸钠, 次氯酸钠具有氧化性, 可作衣物等的漂白剂
D.羊毛、棉花等天然纤维的主要成分都是纤维素
4.(2020春·山东菏泽·高一统考期末)下列有关化学用语表示正确的是
A.氮气的结构式:N N
B.苯的结构式为:
C.乙烯的结构简式:CH2CH2
D.聚丙烯的结构简式为:
5.(2020春·山东菏泽·高一统考期末)甲、乙分别是周期表中同周期IIA和IIIA的两种元素, 若甲的原子序数为 x,则乙的原子序数可能为
①x+l ②x+4 ③x+ ll ④x+25 ⑤ x+32
A.①③⑤ B.② C.③ D.①③④
6.(2020春·山东菏泽·高一统考期末)下列有关短周期元素的性质及其递变规律错误的是
A.I A 族与VIIA族元素形成的一定是离子化合物
B.第 3 周期主族元素从左到右, 最高正价从+1 递增到+7
C.同主族元素的简单阴离子还原性越强,元素非金属性越弱
D.同周期金属元素的化合价越高,其阳离子得电子能力越强
7.(2020春·山东菏泽·高一统考期末)X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的某种核素无中子,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族周期元素可形成常见气体。下列说法正确的是
A.原子半径:W>M>Z>Y>X
B.X、Y、Z三种元素形成的化合物中可能存在离子键
C.由W与Z两元素形成的化合物结构与二氧化碳相似
D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点:XM> X2Z
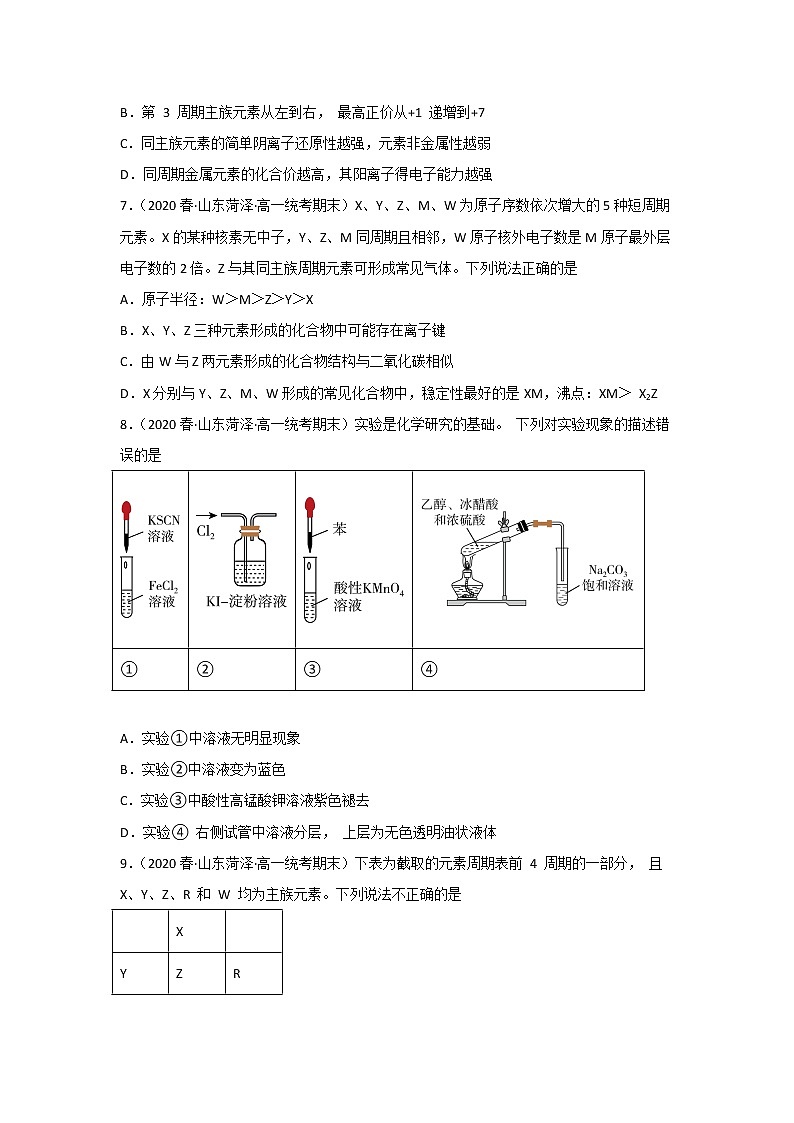
8.(2020春·山东菏泽·高一统考期末)实验是化学研究的基础。 下列对实验现象的描述错误的是
①
②
③
④
A.实验①中溶液无明显现象
B.实验②中溶液变为蓝色
C.实验③中酸性高锰酸钾溶液紫色褪去
D.实验④ 右侧试管中溶液分层, 上层为无色透明油状液体
9.(2020春·山东菏泽·高一统考期末)下表为截取的元素周期表前 4 周期的一部分, 且 X、Y、Z、R 和 W 均为主族元素。下列说法不正确的是
X
Y
Z
R
W
A.五种元素为原子最外层电子数一定大于2
B.X、Z 原子序数-定相差 8
C.Y 高价氧化物的水化物不可能是强酸
D.Z 的氧化物与 X 单质不可能发生置换反应
10.(2020春·山东菏泽·高一统考期末)以下列物质中, 只含离子键的化合物是
A.MgCl2 B.NaOH C.Na2O2 D.H2S
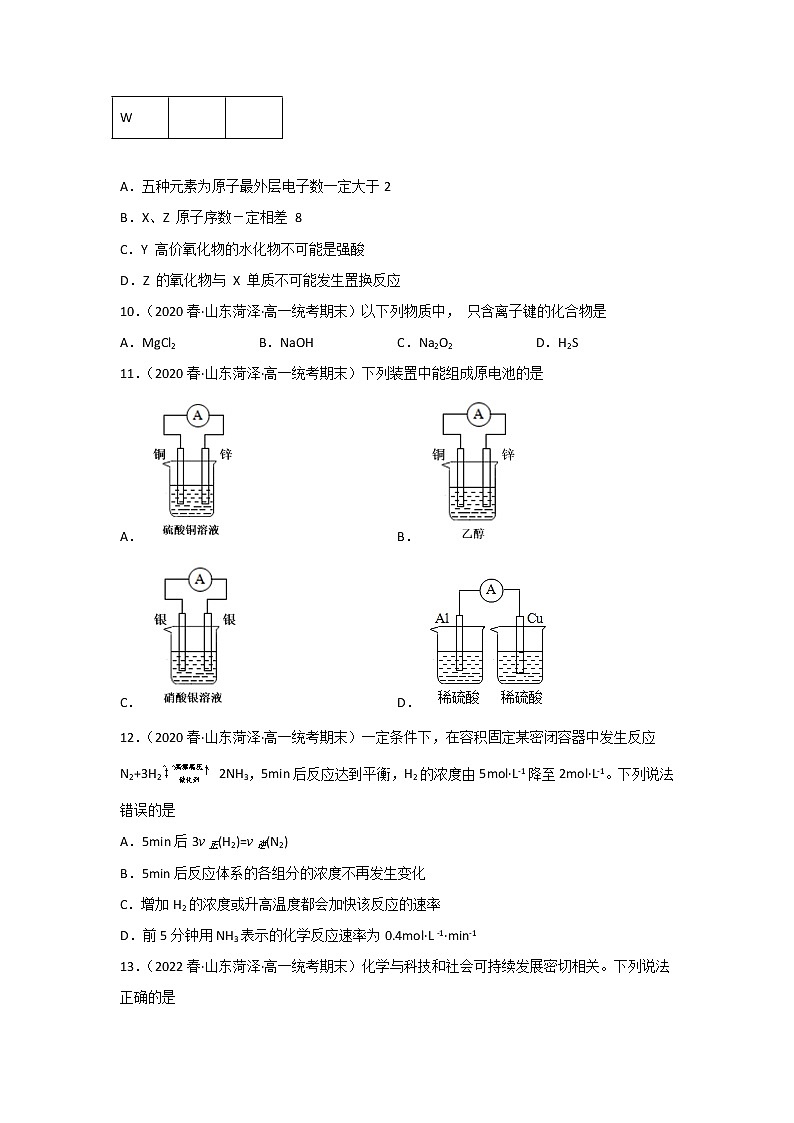
11.(2020春·山东菏泽·高一统考期末)下列装置中能组成原电池的是
A. B.
C. D.
12.(2020春·山东菏泽·高一统考期末)一定条件下,在容积固定某密闭容器中发生反应N2+3H22NH3,5min后反应达到平衡,H2的浓度由5mol∙L-1降至2mol∙L-1。下列说法错误的是
A.5min后3v正(H2)=v逆(N2)
B.5min后反应体系的各组分的浓度不再发生变化
C.增加H2的浓度或升高温度都会加快该反应的速率
D.前5分钟用NH3表示的化学反应速率为0.4mol∙L -1∙min-1
13.(2022春·山东菏泽·高一统考期末)化学与科技和社会可持续发展密切相关。下列说法正确的是
A.石油的分馏、裂化和裂解均属于化学变化
B.北京冬奥服装面料的成分聚氨酯纤维属于天然有机高分子材料
C.中国科学院研发“东方超环”(人造太阳)用到的氕、氘、氚互为同位素
D.“北斗系统”组网成功具有战略意义,北斗芯片中的基体材料为二氧化硅
14.(2022春·山东菏泽·高一统考期末)下列有机物性质与用途的对应关系错误的是
A.淀粉可以发生水解反应,糖米中的淀粉水解后就酿成了酒
B.乙醇具有还原性,利用乙醇与酸性反应检验“酒驾”
C.能使蛋白质变性,可用于游泳池的消毒
D.葡萄糖可以使新制的氢氧化铜转化成砖红色沉淀,可以用来检测病人尿液中的葡萄糖
15.(2022春·山东菏泽·高一统考期末)下列有关化学用语表示错误的是
A.中子数为7的氮原子:
B.的结构式:O=C=O
C.用电子式表示HCl的形成过程:
D.乙烯的填充模型:
16.(2022春·山东菏泽·高一统考期末)设为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,11.2L己烷中含有的分子数为
B.0.5mol苯中含有碳碳双键的数目为
C.1mol与1mol在光照下反应生成的分子数为
D.常温常压下,14g由乙烯和丙烯组成的混合气体所含原子总数为
17.(2022春·山东菏泽·高一统考期末)下列实验装置正确且能达到相应实验目的是
A.装置甲:证明氧化性:
B.装置乙:制取乙酸乙酯
C.装置丙:探究、对分解速率的影响
D.装置丁:检验石蜡中是否含有不饱和烃
18.(2022春·山东菏泽·高一统考期末)下列关于元素周期表知识的说法正确的是
A.元素周期表的第一列都是碱金属元素
B.共有18个族,IIIB族含元素种类最多
C.在金属元素与非金属元素的交界处寻找半导体材料
D.某元素原子最外电子层上只有两个电子,该元素一定是IIA族元素
19.(2022春·山东菏泽·高一统考期末)部分短周期元素原子半径、最高正化合价或最低负化合价随原子序数的变化关系如图所示,下列说法正确的是
A.离子半径的大小:f>e>d
B.简单离子的还原性:h>g
C.简单氢化物的稳定性:y>z>d
D.e、f、g的最高价氧化物对应的水化物之间可以相互反应
20.(2022春·山东菏泽·高一统考期末)下列关于化学键说法正确的是
A.只含共价键的化合物是共价化合物 B.破坏化学键的过程,一定发生了化学变化
C.既有离子键又有共价键 D.干冰升华过程中破坏了共价键
21.(2022春·山东菏泽·高一统考期末)用括号内试剂和分离方法除去下列物质中的少量杂质,错误的是
A.乙醇中混有水(生石灰,蒸馏) B.甲烷中混有乙烯(酸性溶液,洗气)
C.苯中混有溴(NaOH溶液,分液) D.乙酸乙酯中混有乙酸(饱和碳酸钠溶液,分液)
22.(2022春·山东菏泽·高一统考期末)我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应: ,反应过程示意图如下:
下列说法错误的是
A.过程I、过程II均为吸热过程
B.使用催化剂提高了该反应的反应速率
C.该反应中,CO(g)和的总能量高于和的总能量
D.示意图中:起始时的2个在反应过程中并未都参与了反应
23.(2022春·山东菏泽·高一统考期末)海带是一种含碘量很高的海藻,从中提取的磷广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图,下列有关说法正确的是
A.实验室将干海带置于蒸发皿中灼烧
B.操作a与操作c方法相同
C.操作b中用于提取碘的试剂还可以是乙醇
D.③的离子方程式:
24.(2022春·山东菏泽·高一统考期末)臭氧是理想的烟气脱硝试剂,可逆反应在体积固定的密闭容器中进行,反应过程中测得的浓度随时间1的变化曲线如图所示
下列叙述错误的是
A.a-c段反应速率加快的原因可能是反应放热
B.若向容器内充入一定体积的,化学反应速率加快
C.向反应体系中通入氢气,反应速率降低
D.2~8min的化学反应速率
参考答案:
1.A
【详解】A.石油分馏的过程中没有新物质生成,属于物理变化,不涉及化学变化,故A符合题意;
B.从海带灰中提取碘单质的过程中有新物质生成,属于化学变化,故B不符合题意;
C.用石油裂解生产乙烯的过程中有新物质生成,属于化学变化,故C不符合题意;
D.用煤干馏生产焦炭的过程中有新物质生成,属于化学变化,故D不符合题意;
故选A。
2.B
【详解】
铀元素有3种核素,其中一种是U,元素符号左下角的数字为质子数,左上角的数字为质量数,质量数等于质子数加上中子数,其核内的中子数=238-92=146,质子数是92,核内的中子数和质子数之差=146-92=54。
答案选B。
3.D
【详解】A.淀粉为多糖,油脂是高级脂肪酸甘油酯,蛋白质含有肽键,在一定条件下都能水解,选项A正确;
B.酒精有强还原性,含氯消毒剂有较强的氧化性,两者能发生氧化还原反应,不能混用,选项B正确;
C.84消毒液属于含氯消毒剂,是以次氯酸钠(NaClO)为主要有效成分的消毒液,适用于一般物体表面、白色衣物、医院污染物品的消毒,选项C正确;
D.羊毛的主要成分是蛋白质,棉花的主要成分是纤维素,选项D错误。
答案选D。
4.A
【详解】A.氮原子的最外层电子数5,氮分子之间形成三对共用电子对,氮气的结构式:NN,故A正确;
B.苯的结构简式为: ,苯的结构式为: ,故B错误;
C.乙烯的结构简式:CH2=CH2,故C错误;
D.聚丙烯为丙烯通过加聚反应生成的,聚丙烯的结构简式为: ,故D错误;
答案选A。
【点睛】结构简式要体现出有机物的官能团,为易错点。
5.D
【详解】由元素周期表结构可知:若甲、乙两种元素处于第二、三周期,两个主族元素处于相邻位置,若甲的原子序数为 x,则乙的原子序数是x+1;
若甲、乙两种元素处于第四、五周期,由于IIA与第IIIA之间之间了7个副族和1个第VIII族,共10个纵行,所以若甲的原子序数为 x,则乙的原子序数是x+11;
若甲、乙两种元素处于第六、七周期,由于在第IIIB存在镧系元素和锕系元素共15种元素占据元素周期表的一个格,所以若甲的原子序数为 x,则乙的原子序数是x+25,故乙的原子序数可能为x+l、x+ ll、x+25,合理序号是①③④,故正确选项是D。
6.A
【详解】A.氢元素位于I A 族,氢元素与VIIA族元素形成的氢化物是共价化合物,故A错误,符合题意;
B.主族元素的最外层电子数与最高正化合价相等,则第3周期主族元素从左到右,最高正价从+1 递增到+7,故B正确,不选;
C.元素的非金属性越强,单质的氧化性越强,对应还原产物简单阴离子还原性越弱,则同主族元素的简单阴离子还原性越强,元素非金属性越弱,故C正确,不选;
D.同周期金属元素从左到右,元素的化合价依次升高,金属性依次减弱,元素的金属性越弱,单质的还原性越弱,对应氧化产物阳离子得电子能力越强,故D正确,不选;
故选A。
7.B
【分析】X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的某种核素无中子,则X为氢(H);Z与其同主族的短周期元素可形成常见气体,则Z为氧(O);Y、Z、M同周期且相邻,则Y为氮(N),M为氟(F);W原子核外电子数是M原子最外层电子数的2倍,则W为硅(Si),X、Y、Z、M、W分别为H、N、O、F、Si,据此分析。
【详解】A.X、Y、Z、M、W分别为H、N、O、F、Si,氢原子位于第一周期,原子半径最小,N、O、F位于第二周期,半径逐渐减小,硅位于第三周期,五种元素中原子半径最大,原子半径:W>Y>M>Z>X,故A错误;
B.X、Y、Z三种元素分别为H、N、O,形成的化合物如果为NH4NO3,存在离子键,故B正确;
C.由W与Z两元素形成的化合物是二氧化硅,硅原子和氧原子之间存在共价键,二氧化碳中含有二氧化碳分子,二氧化碳分子里存在共价键,结构与二氧化碳不相似,故C错误;
D.H分别与N、O、F、Si形成的常见化合物中,F的非金属性最强,所以稳定性最好的是HF,虽然H2O、HF分子间都能形成氢键,但常温下H2O呈液态,而HF呈气态,所以沸点H2O>HF,故D错误;
答案选B。
8.C
【详解】A.FeCl2与KSCN不反应,实验①中溶液无明显现象,选项A正确;
B.氯气与KI反应生成碘单质,淀粉遇碘单质变蓝,则观察到溶液变为蓝色,选项B正确;
C. 苯不能使酸性高锰酸钾溶液褪色,实验③中酸性高锰酸钾溶液不褪色,选项C错误;
D. 乙醇与冰醋酸在浓硫酸催化下发生酸化反应生成乙酸乙酯,乙酸乙酯通入饱和碳酸钠溶液中,溶液分层, 上层为无色透明油状液体乙酸乙酯,选项D正确。
答案选C。
9.D
【分析】图为元素周期表钱四周期的一部分,有元素在周期表中的位置可知,应是周期表的2、3、4周期,由于周期表中IIA、IIIA之间相隔10列,且X、Y、Z、R 和 W 均为主族元素,故Y可能为IIIA族、IVA族或者VA族,若Y为IIIA族元素,则Y为Al、Z为Si、X为C、R为P、W为Ga;若Y为IVA族元素,则Y为Si、Z为P、X为N、R为S、W为Ge;若Y为VA族元素,则Y为P、Z为S、X为O、R为CL、W为As。据此结合元素周期律内容分析。
【详解】A. Y为IIIA族或者IVA族元素,其他元素的原子的最外层电数都大于或者等于Y的最外层电子数,故5种元素的最外层电子数都大于2,A正确;
B.依据分析可知,Y、W分别位于第二周期、第三周且同主族,起源自序数相差8,B正确;
C.当Y为VA族P元素时,其最高价氧化物对应水化物为H3PO4,不是强酸,C正确;
D.当Y为Al、Z为Si、X为C时,Z的氧化物SiO2与C在高温时能发生置换反应,D错。
答案选D
10.A
【详解】A.MgCl2中只有镁离子与氯离子形成的离子键,属于离子化合物,选项A正确;
B.NaOH中钠离子与氢氧根离子以离子键结合,O、H之间以极性共价键结合,则NaOH为含有极性共价键和离子键的离子化合物,选项B错误;
C.Na2O2中钠离子与过氧根据离子以离子键结合,过氧根离子中O、O之间以非极性共价键结合,为存在离子键和共价键的离子化合物,选项C错误;
D.H2S中只存在共价键,且为共价化合物,选项D错误。
答案选A。
11.A
【详解】A.符合原电池的构成条件,锌作负极发生氧化反应,溶液中铜离子在铜电极得到电子发生还原反应生成铜单质,能组成原电池,故A正确;
B.乙醇不是电解质,没有构成闭合回路,不满足原电池的形成条件,不能构成原电池,故B错误;
C.两个电极材料相同,且银和硝酸银不能发生自发进行的氧化还原反应,不能构成原电池,故C错误;
D.没有形成闭合回路,不能构成原电池,故D错误;
答案选A。
【点睛】原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应。
12.A
【详解】
A.5min后反应达到平衡,根据化学反应速率之比等于化学计量数之比,v正(H2)=3v正(N2),处于平衡状态,v正(N2)= v逆(N2),v正(H2)=3v逆(N2),故A错误;
B.5min后反应达到平衡,反应体系的各组分的浓度不再发生变化,故B正确;
C.增大浓度或升高温度都会加快化学反应速率,故增加H2的浓度或升高温度都会加快该反应的速率,故C正确;
D.前5分钟用H2表示的化学反应速率为v(H2)===0.6mol∙L-1∙min-1,根据化学反应速率之比等于化学计量数之比,v(NH3): v(H2)=2:3,v(NH3)=0.4mol∙L-1∙min-1,故D正确;
答案选A。
【点睛】
化学反应速率之比等于化学计量数之比是计算的关键。
13.C
【详解】A.石油的分馏属于物理变化,石油的裂化、裂解属于化学变化,A错误;
B.聚氨酯纤维是人工合成材料,不是天然有机高分子材料,B错误;
C.质子数相同,中子数不同的核素为同位素,氕、氘、氚质子数相同,中子数不同,互为同位素,C正确;
D.晶体硅为良好的半导体材料,可用作制造计算机芯片,D错误;
故答案选C。
14.A
【详解】A.淀粉可以发生水解反应,糖米中的淀粉水解得到的是葡萄糖而不是乙醇,故A错误;
B.乙醇具有还原性, K2Cr2O7具有强氧化性,可以利用乙醇与酸性 K2Cr2O7 反应来检验“酒驾”,故B正确;
C.CuSO4 能使蛋白质变性,可以用于游泳池的消毒,故C正确;
D.葡萄糖中含有醛基,可以使新制的氢氧化铜转化成砖红色沉淀,所以能用来检测病人尿液中的葡萄糖,故D正确;
故答案选A。
15.C
【详解】A.中子数为7的氮原子为:,故A正确;
B.的结构式为:O=C=O,故B正确;
C.HCl为共价化合物,用电子式表示HCl的形成过程为:,故C错误;
D.乙烯的填充模型为:,故D正确;
故答案选C。
16.D
【详解】A.己烷在标准状况下是液体,不是气体,不能直接运用22.4L/mol进行计算,故A错误;
B.苯中不含碳碳双键,故B错误;
C.甲烷和氯气发生反应生成CH3Cl、CH2Cl2、CHCl3、CCl4,因此1mol甲烷与1mol氯气反应生成一氯甲烷的物质的量小于1mol,分子数小于,故C错误;
D.乙烯和丙烯通式为CnH2n,14g由乙烯和丙烯组成的该混合物所含碳原子物质的量为=1mol,则混合气体所含原子总数为,故D正确;
答案选D。
17.B
【详解】A.装置甲:氯气可以和碘化钾反应置换出碘,会干扰实验,故不能证明氧化性:,A错误;
B.乙酸乙酯中混有乙醇和乙酸可用饱和碳酸钠溶液除去,装置乙中的导管未插入饱和碳酸钠溶液中可以防止倒吸, 故装置乙可制取乙酸乙酯,B正确;
C. 装置丙中双氧水的浓度不同:故该实验有2个变量,不能探究、对分解速率的影响,C错误;
D.装置丁中溴的四氯化碳溶液褪色只能说明从试管中出来的气体中含有不饱和烃,石蜡是的成分是饱和烃,故可用装置丁检验石蜡的分解产物含有不饱和烃, D错误;
答案选B。
18.C
【详解】A.元素周期表中第一列的氢元素不是碱金属元素,A错误;
B.元素周期表有7个主族,7个副族,1个0族和一个Ⅷ族,共16个族,B错误;
C.金属元素和非金属元素交界处的元素具有金属性、非金属性,可用作半导体材料,C正确;
D.He元素最外层电子数为2,但是其为零族元素,D错误;
故答案选C。
19.D
【分析】由图可知,x为H元素、y为C元素、z为N元素、d为O元素、e为Na元素、f为Al元素、g为S元素、h为Cl元素。
【详解】A.电子层结构相同的离子,核电荷数越大,离子半径越小,则氧离子、钠离子、铝离子的离子半径依次减小,故A错误;
B.元素的非金属性越强,对应简单离子的还原性越弱,氯元素的非金属性强于硫元素,则氯离子的还原性弱于硫离子,故B错误;
C.同周期元素,从左到右元素的非金属性依次增强,简单氢化物的稳定性依次增强,则甲烷、氨气、水的稳定性依次增强,故C错误;
D.氢氧化铝是两性氢氧化物,能与强碱氢氧化钠溶液和强酸硫酸溶液反应生成盐和水,故D正确;
故选D。
20.A
【详解】A.只含共价键的化合物是共价化合物,故A正确;
B.破坏化学键的过程,不一定发生了化学变化,如氯化氢溶于水时H-Cl键断裂,故B错误;
C.电子式为,只含离子键,故C错误;
D.干冰升华过程中二氧化碳分子不变,只破坏分子间作用力,故D错误;
选A。
21.B
【详解】A.乙醇中混有水,可加入生石灰,再蒸馏,A正确;
B.乙烯和酸性高锰酸钾反应生成二氧化碳,引入了新的杂质,B错误;
C.溴单质和氢氧化钠溶液反应生成溴化钠和次溴酸钠,两者溶于水,苯不溶于水,分液进行分离,C正确;
D.饱和碳酸钠能中和乙酸,降低乙酸乙酯的溶解度,再进行分液可将二者分离,D正确;
故答案选B。
22.D
【详解】A.根据图示可知,过程Ⅰ和过程Ⅱ中水分子中的O-H键断裂,化学键断裂吸热,A正确;
B.使用催化剂可以降低反应物的活化能,从而提高反应速率,B正确;
C.ΔH=生成物总能量-反应物总能量,ΔH
相关试卷
这是一份山东省枣庄市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共14页。试卷主要包含了对下列各项事实的判断错误的是,下列装置可以构成原电池的是,下列变化中,气体被还原的是等内容,欢迎下载使用。
这是一份山东省威海市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共16页。试卷主要包含了化学与我们的生产、生活密切相关,下列化学用语表述正确的是,在一定条件下发生如下反应,下列说法正确的是等内容,欢迎下载使用。
这是一份山东省泰安市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共16页。试卷主要包含了下列说法正确的是,下列说法中正确的是等内容,欢迎下载使用。









