
所属成套资源:各地区2020-2022三年高一化学下学期期末试题按题型汇编
四川乐山市2020-2022三年高一化学下学期期末试题汇编1-选择题①
展开
这是一份四川乐山市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共17页。试卷主要包含了一种镁盐水电池的结构如图所示等内容,欢迎下载使用。
四川乐山市2020-2022三年高一化学下学期期末试题汇编1-选择题①
1.(2019春·四川乐山·高一统考期末)下列电池中不属于充电电池的是( )
A.A B.B C.C D.D
2.(2019春·四川乐山·高一统考期末)化学与生产、生活密切相关,下列叙述错误的是( )
A.料酒可以除去食物中的腥味 B.纤维素在人体内水解之后生成葡萄糖
C.玉米、高粱发酵可以制得乙醇 D.乙烯是一种植物生长调节剂
3.(2019春·四川乐山·高一统考期末)未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②太阳能 ③风能 ④石油 ⑤煤 ⑥生物质能 ⑦氢能
A.①②③④ B.②③⑥⑦ C.①②⑤⑥⑦ D.③④⑤⑥⑦
4.(2019春·四川乐山·高一统考期末)下列反应原理不符合工业冶炼金属实际情况的是( )
A.2HgO2Hg+O2↑ B.4A1+3MnO22Al2O3+3Mn
C.2MgO2Mg+O2↑ D.3CO+Fe2O32Fe+3CO2
5.(2019春·四川乐山·高一统考期末)我国著名的化学家张清莲准确测得铟(49In)的相对原子质量为114.818被国际原子量委员会采用为新的标准值。下列关于In的说法不正确的是( )
A.In为长周期元素 B.In为过渡元素
C.In易导电导热 D.In原子核外有49个电子
6.(2019春·四川乐山·高一统考期末)根据元素周期律的知识,下列两者性质比较中,不正确的是( )
A.热稳定性:PH3<NH3 B.金属性强弱:Na>Mg>Al
C.酸性强弱:HF>HCl>HBr>HI D.原子半径:K>Si>Cl>F
7.(2019春·四川乐山·高一统考期末)下列说法正确的是( )
A.乙烯和苯使溴水褪色的原理相同
B.甲烷和乙烯都可以与氯气反应
C.乙醇与Na反应比水与Na反应剧烈
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
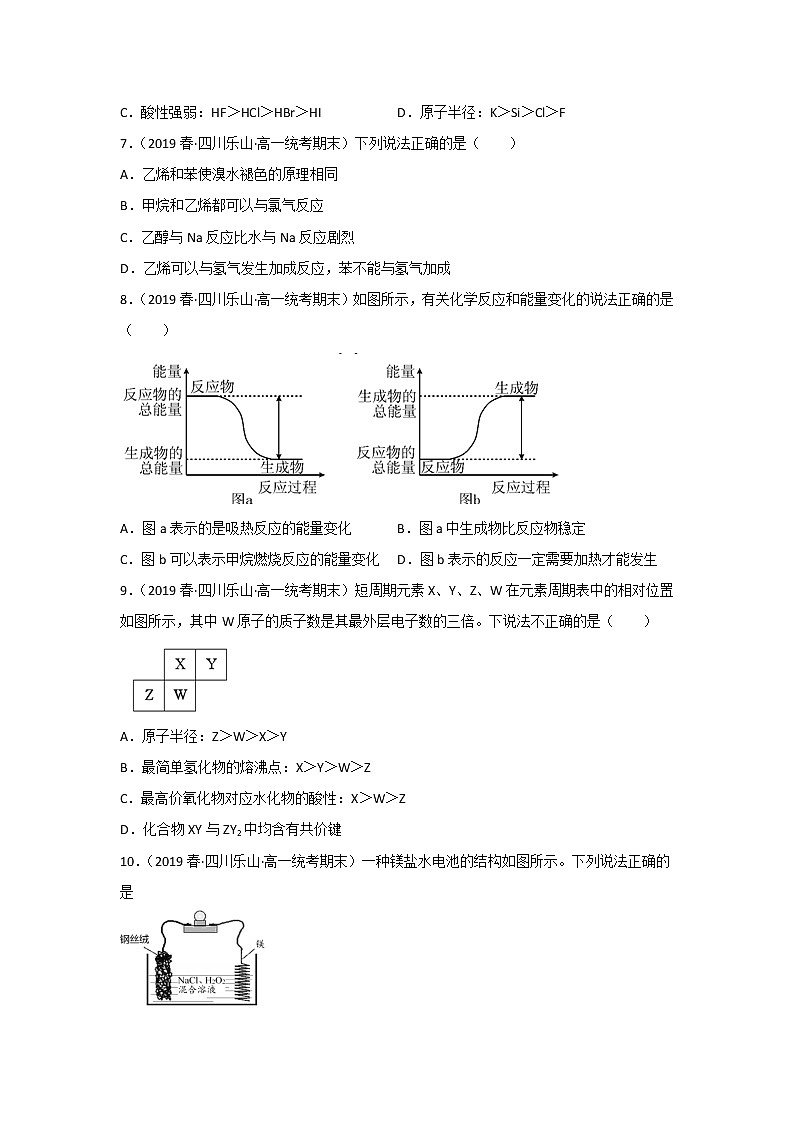
8.(2019春·四川乐山·高一统考期末)如图所示,有关化学反应和能量变化的说法正确的是( )
A.图a表示的是吸热反应的能量变化 B.图a中生成物比反应物稳定
C.图b可以表示甲烷燃烧反应的能量变化 D.图b表示的反应一定需要加热才能发生
9.(2019春·四川乐山·高一统考期末)短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍。下说法不正确的是( )
A.原子半径:Z>W>X>Y
B.最简单氢化物的熔沸点:X>Y>W>Z
C.最高价氧化物对应水化物的酸性:X>W>Z
D.化合物XY与ZY2中均含有共价键
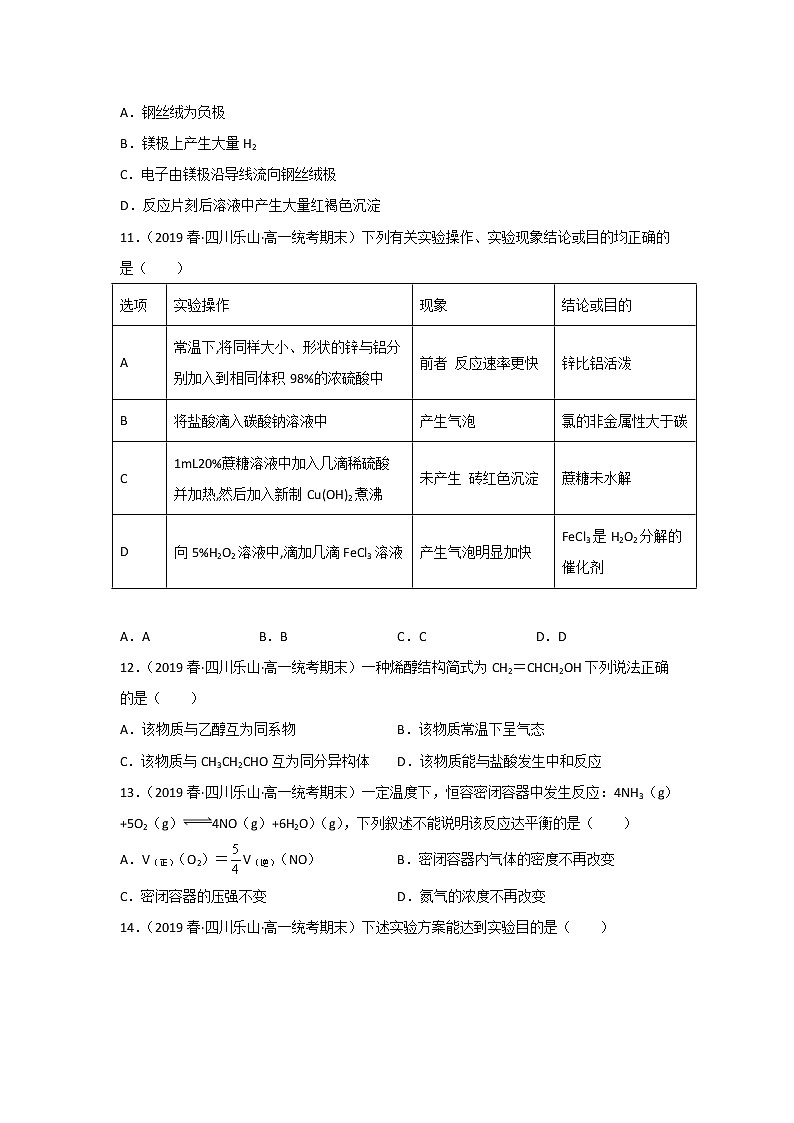
10.(2019春·四川乐山·高一统考期末)一种镁盐水电池的结构如图所示。下列说法正确的是
A.钢丝绒为负极
B.镁极上产生大量H2
C.电子由镁极沿导线流向钢丝绒极
D.反应片刻后溶液中产生大量红褐色沉淀
11.(2019春·四川乐山·高一统考期末)下列有关实验操作、实验现象结论或目的均正确的是( )
选项
实验操作
现象
结论或目的
A
常温下,将同样大小、形状的锌与铝分别加入到相同体积98%的浓硫酸中
前者 反应速率更快
锌比铝活泼
B
将盐酸滴入碳酸钠溶液中
产生气泡
氯的非金属性大于碳
C
1mL20%蔗糖溶液中加入几滴稀硫酸并加热,然后加入新制Cu(OH)2煮沸
未产生 砖红色沉淀
蔗糖未水解
D
向5%H2O2溶液中,滴加几滴FeCl3溶液
产生气泡明显加快
FeCl3是H2O2分解的催化剂
A.A B.B C.C D.D
12.(2019春·四川乐山·高一统考期末)一种烯醇结构简式为CH2=CHCH2OH下列说法正确的是( )
A.该物质与乙醇互为同系物 B.该物质常温下呈气态
C.该物质与CH3CH2CHO互为同分异构体 D.该物质能与盐酸发生中和反应
13.(2019春·四川乐山·高一统考期末)一定温度下,恒容密闭容器中发生反应:4NH3(g)+5O2(g)4NO(g)+6H2O)(g),下列叙述不能说明该反应达平衡的是( )
A.V(正)(O2)=V(逆)(NO) B.密闭容器内气体的密度不再改变
C.密闭容器的压强不变 D.氮气的浓度不再改变
14.(2019春·四川乐山·高一统考期末)下述实验方案能达到实验目的是( )
A.A B.B C.C D.D
15.(2019春·四川乐山·高一统考期末)浩瀚的海洋是一个巨大的物质宝库,工业上常用浓缩海水提取溴.
下列说法不正确的是( )
A.海水的淡化方法主要有蒸馏法、电渗析法、离子交换法等
B.步骤②中体现了溴易挥发的性质
C.步骤③反应的离子方程式为Br2+SO2+2H2O═2HBr+2H++SO42﹣
D.①﹣④目的是为了富集溴元素
16.(2019春·四川乐山·高一统考期末)如图是某空间站能量转化系统的局部示意图:其中燃料池采用KOH溶液为解液,下列有关说法中不正确的是( )
A.燃料电池系统产的能量实际上来自于太阳能
B.该能量转化系统中的水可以循环利用
C.背日面时,燃料电池负极反应为:H2+2OH﹣﹣2e﹣═2H2O
D.向日面时,水电解产生的H2和O2的体积比为1:2(相同条件)
17.(2021春·四川乐山·高一统考期末)下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是
A.
B.
C.
D.
电解水
水力发电
太阳能热水器
干电池工作
A.A B.B C.C D.D
18.(2021春·四川乐山·高一统考期末)化学与生产生活密切相关。下列叙述中不正确的是
A.动物毛皮和蚕丝的主要成分为蛋白质
B.天然气是一种高效、低耗、污染小的清洁能源
C.普通食醋中含有的乙酸,乙酸是一种烃
D.红葡萄酒长时间密封储存,会生成有香味的酯
19.(2021春·四川乐山·高一统考期末)下列化学用语描述正确的是
A.苯分子的比例模型: B.甲烷分子的球棍模型:
C.乙烯的结构简式: D.HCl的电子式:
20.(2021春·四川乐山·高一统考期末)下列事实或做法与化学反应速率无关的是
A.将食物存放在温度低的地方 B.用铁作催化剂合成氨
C.将煤块粉碎后燃烧 D.用浓硝酸和铜反应制备NO2气体
21.(2021春·四川乐山·高一统考期末)科学家利用回旋加速器,用钙原子轰击钚原子得到了鈇元素,半衰期达30秒。下列有关说法正确的是
A.鈇是一种非金属元素
B.鈇原子核外电子数为114
C.鈇元素位于周期表第六周期IVA族
D.鈇元素的主要化合价有+4、+2、-4价
22.(2021春·四川乐山·高一统考期末)火法炼铜的原理为:,下列说法正确的是
A.火法炼铜或湿法炼铜反应中,铜元素均被还原
B.产物是硫酸的酸酐
C.该反应每生成2molCu,转移4mol电子
D.工业上常用加热分解CuO的方法制Cu
23.(2021春·四川乐山·高一统考期末)分子式为,且能与Na反应放出的同分异构体种数为
A.2 B.3 C.4 D.7
24.(2021春·四川乐山·高一统考期末)下图是的能量变化图,根据信息分析下列说法正确的是
A.该反应为放热反应
B.的能量比的能量高
C.某容器内充入反应后,吸收热量
D.该化学反应历程中既有能量的吸收又有能量的释放
25.(2021春·四川乐山·高一统考期末)某些资源在自然界中的含量很低,因此获取这些资源的一个重要步骤就是富集,下列选项中虚线框内的流程不是富集的是
A.
B.
C.
D.
26.(2021春·四川乐山·高一统考期末)下列装置或操作能达到实验目的的是
A.
B.
C.
D.
将海带灼烧成灰
制取乙酸乙酯
除去中的
石油分馏
A.A B.B C.C D.D
27.(2021春·四川乐山·高一统考期末)下图为元素周期表短周期的一部分,下列关于X、Y、Z、W四种元素的叙述中正确的是
X
Y
Z
W
A.原子半径:
B.简单离子还原性:
C.最高价氧化物对应水化物的酸性:
D.的简单氢化物中所有原子满足8电子稳定结构
28.(2021春·四川乐山·高一统考期末)第16届海南国际车展上展出了中国研制的新型燃料电池汽车,该汽车由质子交换膜燃料电池提供能量。某种质子交换膜燃料电池结构如图所示。下列说法不正确的是
A.a为电池负极,发生氧化反应
B.正极反应为:
C.质子(H+)通过质子交换膜移动到b电极
D.该燃料电池对环境友好无污染
参考答案:
1.A
【分析】铅蓄电池、镍镉电池、锂离子电池等属于可充电电池,是二次电池,碱性锌锰电池不能充电,是一次电池,为不可充电电池。
【详解】充电电池之所以能够充电,原因是电池中的化学反应是可逆反应,能够通过外加电源,将电能转化为化学能,使放过电的电池恢复到原来的状态。如果其中的化学反应不可逆,电池就不能充电,普通干电池就是这样。
铅蓄电池、镍镉电池、锂离子电池等可以反复充电放电属于可充电电池,是二次电池,为可充电电池;碱性锌锰电池不能充电,完全放电后不能再使用,是一次电池;
答案选A。
2.B
【详解】A.有腥味的物质易溶于乙醇,故料酒可以除去食物中的腥味,选项A正确;
B.人体内无纤维素酶,不能消化纤维素,纤维素在人体内不能水解生成葡萄糖,选项B错误;
C、高粱、玉米等植物的种子为原料,经发酵、蒸馏得到乙醇,选项C正确;
D、乙烯是一种植物生长调节剂,可用作果实催熟剂,选项D正确。
答案选B。
3.B
【分析】新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且可以再生。
【详解】天然气、石油、煤是不可再生能源,能引起严重的空气污染,不是新能源;太阳能、风能、生物质能、氢能对环境污染小,属于对环境友好型的新能源,故选B。
【点睛】本题考查了新能源,注意新能源的特征及开发利用是解答关键。
4.C
【详解】A.Hg活动性较弱,用热分解的方法治炼,选项A正确;
B.Mn是比较活泼的金属,用热还原的方法治炼,选项B正确;
C.Mg是活泼的金属,用电解的方法治炼,由于氧化镁的熔点太高,应电解熔融氯化镁,选项C错误;
D.Fe是比较活泼的金属,用热还原的方法治炼,选项D正确。
答案选C。
【点睛】金属的冶炼方法与金属的活动性关系密切。金属活动性越强,其离子获得电子被还原的能力就越小,越难冶炼。钾、钙、钠、镁、铝特别活泼的金属用电解熔融的离子化合物的方法治炼;从铝之后到铜(包括铜)等比较活泼的金属用热还原(包括铝热反应)冶炼,不活泼的金属,如Hg、Ag用热分解它们的化合物的方法治炼。掌握金属活动性顺序表与金属活动性的关系是本题解答的关键。
5.B
【分析】由In原子结构示意图可知,In位于周期表第五周期ⅢA族,原子序数为49,属于长周期元素,金属性较强,具有良好的导电性、导热性。
【详解】A.元素周期表前三周期为短周期,由In原子结构示意图可知,In位于周期表第五周期ⅢA族,属于长周期元素,选项A正确;
B.In位于周期表第四周期ⅢA族,属于主族元素,不属于过渡元素,选项B错误;
C.In与Al同主族,且金属性较Al强,具有良好的导电导热性,选项C正确;
D.In原子序数为49,原子核外有49个电子,选项D正确。
答案选B。
6.C
【详解】A.非金属性N>P,热稳定性:NH3>PH3,故A正确;
B.同周期主族元素核电荷数越大,金属性越弱,则金属性强弱:Na>Mg>Al,故B正确;
C.非金属性F>Cl>Br>I,同主族元素的非金属性越强,对应氢化物的酸性越弱,则酸性强弱:HI>HBr>HCl>HF,故C错误;
D.同周期主族元素核电荷数越大,原子半径越小,同主族核电荷数大,原子半径大,则原子半径:K>Si>Cl>F,故D正确;
答案选C。
7.B
【详解】A.乙烯使溴水褪色是因为乙烯能够与溴发生加成反应,苯能够使溴水褪色是因为发生萃取,选项A错误;
B、甲烷与氯气反应属于取代反应,乙烯与氯气反应属于加成反应,选项B正确;
C、因为钠与乙醇及水反应能放出氢气,都是因为水和乙醇中含有羟基,因为水中羟基氢更活泼,所以钠与水反应更剧烈,选项C错误;
D、乙烯可以与氢气发生加成反应生成乙烷,苯能与氢气发生加成反应生成环己烷,选项D错误;
答案选B。
8.B
【详解】A、图a中反应物总能量高于生成物总能量,故为放热反应,选项A错误;
B、图b中反应物总能量低,反应物稳定,选项B正确;
C、图b中反应物总能量低于生成物总能量,可以表示吸热反应,而甲烷燃烧反应为放热反应,选项C错误;
D、图b表示的是吸热反应,吸热反应发生不一定需要加热也能发生,如氢氧化钡晶体和氯化铵固体在常温下就可发生,故D错误。
答案选B。
9.B
【详解】从元素周期表的局部图可知X、Y、Z、W为二、三周期元素,W位于第三周期,W原子的质子数是其最外层电子数的三倍,故W是P元素,据此推出X、Y、Z分别是氮、氧、硅。
A、根据四种元素在周期表中的位置关系可知,原子半径:Z>W>X>Y,选项A正确;
B、氢化物的热稳定性:H2O>NH3>PH3>SiH4,即Y>X>W>Z,选项B不正确;
C、非金属性:O>N>P>Si,最高价氧化物对应水化物的酸性:HNO3>H3PO4>H2SiO3,即X>W>Z,选项C正确;
D、化合物XY与ZY2分别为NO、SiO2,均含有共价键,选项D正确。
答案选B。
10.C
【详解】A、镁的金属性强于铁,故镁为负极,钢丝绒为正极,选项A错误;
B、镁极上镁失去电子产生镁离子与氢氧根离子结合产生氢氧化镁,选项B错误;
C、镁为负极,钢丝绒为正极,电子由负极镁极沿导线流向正极钢丝绒极,选项C正确;
D、反应片刻后溶液中产生大量白色沉淀氢氧化镁,选项D错误。
答案选C。
11.D
【详解】A.常温下浓硫酸有强氧化性,铝遇浓硫酸钝化,无法比较Al与Zn的活泼性,选项A错误;
B.比较元素的非金属性要比较最高价氧化物的水化物的酸性强弱,即根据HClO4酸性比H2CO3强,可判断出氯的非金属性大于碳,选项B错误;
C、蔗糖水解生成葡萄糖,葡萄糖与新制氢氧化铜悬浊液反应应在碱性条件下进行,该实验没有用碱液中和硫酸,所以达不到实验目的,选项C错误;
D、过氧化氢分解,FeCl3在此反应中作催化剂,起催化作用,能加快过氧化氢分解产生氧气的速率,选项D正确。
答案选D。
12.C
【详解】A、CH2=CHCH2OH含有碳碳双键,与乙醇结构不相似,所以与乙醇不互为同系物,选项A错误;
B. CH2=CHCH2OH常温下为无色液体,选项B错误;
C、CH2=CHCH2OH与CH3CH2CHO,分子式相同结构不同的化合物互为同分异构体,选项C正确;
D、CH2=CHCH2OH含有碳碳双键和醇羟基,不含OH-,不能与盐酸发生中和反应,选项D错误。
答案选C。
13.B
【详解】A. 化学反应速率V(正)(O2)=V(逆)(NO)=V(逆)(O2),正逆反应速率相等,反应达到平衡状态,选项A不选;
B、根据ρ=,气体的质量没有变,容器的体积也不变,密度ρ在整个过程中一直不变,平衡不一定达平衡,选项B选;
C、恒温恒容密闭容器中,只要未达到平衡状态,压强一直在变,P不变就说明反应达平衡,选项C不选;
D、各反应物的浓度保持不变则反应达平衡状态,氮气的浓度不再改变则达平衡,选项D不选;
答案选B。
【点睛】本题考查化学平衡状态的判断,根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡。其中注意B项为易错点,反应物和生成物都是气体,质量守恒,容器的体积不变,则密度不变。
14.D
【详解】A、乙烯的密度和空气接近,不能用排空气法收集,选项A错误;
B、苯和四氯化碳互溶,不能用分液的方法分离,选项B错误;
C.甲烷与氯气在光照的条件下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢的混合物,不能制取纯净的一氯甲烷,选项C错误;
D、实验室制备乙酸乙酯时,为防止倒吸右端导管口应位于饱和碳酸钠溶液的液面上,选项D正确;
答案选D。
15.C
【详解】由分离流程可知,浓缩海水中溴离子的浓度较大,①中与氯气发生2Br-+C12=Br2+2C1-,用空气和水蒸气将溴吹出,并用SO2氧化吸收,从而达到富集溴,③中发生Br2+2H2O+SO2=2HBr+ H2SO4,④中发生Cl2+2HBr=Br2+2HCl。
A、海水淡化的主要方法有:蒸馏法、电渗析法、离子交换法等,选项A正确;
B.溴单质易挥发,用热的空气可以吹出,选项B正确;
C.步骤③反应是二氧化硫具有还原性还原溴单质,反应的离子方程式为Br2+2H2O+SO2=4H++2Br-+SO42﹣,选项C错误;
D.步骤①-④,先生成溴单质,热空气吹出溴单质后,用二氧化硫还原后再用氯气氧化的目的是富集溴元素,选项D正确。
答案选C。
16.D
【详解】A、水电解系统中的能量来自于光电转换器,能量实际上来自于太阳能,选项A正确;
B、由转化图可知,水电解产生氢气和氧气,燃料电池系统中发生化合反应生成了水,故该能量转化系统中的水可以循环使用,选项B正确;
C、背日面时,碱性条件下燃料电池负极反应为:H2+2OH﹣﹣2e﹣═2H2O,选项C正确;
D、向日面时,根据电解的反应式2H2O2H2↑+O2↑,水电解产生的H2和O2的体积比为2:1(相同条件),选项D不正确;
答案选D。
【点睛】本题考查电化学基础,出题的切入点新颖,以信息的形式考查了化学反应与能量的关系,解答时要根据所学知识细心分析,根据空间站能量转化系统局部示意图,利用水的分解反应和燃料电池中的反应来分析反应中的能量变化。
17.D
【详解】A.电解是电能变成化学能,A错误;
B.没有化学反应,B错误;
C.是太阳能变热能,C错误;
D.干电池是化学能变电能,D正确;
故选D。
18.C
【详解】A.动物毛皮、蚕丝的主要成分均为蛋白质,故A正确;
B.天然气的主要成分是甲烷,燃烧产物为二氧化碳和水,是一种高效、低耗、污染小的清洁能源,故B正确;
C.乙酸含有C、H、O三种元素,是烃的含氧衍生物,故C错误;
D.葡萄酒中含有酒精,乙醇被氧化可生成乙酸,乙酸和乙醇发生酯化反应生成具有香味的乙酸乙酯,因此红葡萄酒长时间密封储存,会产生香味,故D正确;
故选C。
19.A
【详解】A.苯为平面分子,碳原子的相对体积大于氢原子,则苯分子的比例模型为,故A正确;
B.甲烷为正四面体结构,碳原子为中心,四个H在四个顶点上,碳原子的原子半径较大,球棍模型为,故B错误;
C.乙烯的结构简式中含有C=C双键,结构简式为CH2═CH2,故C错误;
D.氯化氢为共价化合物,电子式为,故D错误;
故选A。
20.D
【详解】A.将易腐败的食物储存在冰箱里,温度降低,化学反应速率减小,故A不选;
B.用铁作催化剂合成氨,化学反应速率增大,故B不选;
C.将煤块粉碎后燃烧,固体的表面积增大,化学反应速率增大,故C不选;
D.用浓硝酸和铜反应制备NO2气体与反应物的性质有关,与反应速率无关,故D选;
答案选D。
21.B
【详解】A.鈇是一种金属元素,故A错误;
B.根据提供数据知原子序数是114号,即质子数是114,故B正确;
C.目前共有118种元素,114号元素应当在第七周期倒数第五种元素,根据周期表中族的排列,应当是ⅣA族,所以该元素位于第七周期ⅣA族,故C错误;
D.根据最高正化合价=最外层电子数=主族序数,知该元素的最高正价是+4价,则最低负价是+4-8=-4价,+4、+2价都在此范围内,故D错误;
故选B。
22.A
【详解】A.火法炼铜的原理为,湿法炼铜的原理为CuSO4+Fe═FeSO4+Cu,反应中,铜元素的化合价均降低,被还原,故A正确;
B.是亚硫酸的酸酐,硫酸的酸酐为SO3,故B错误;
C.反应中Cu由+1价变成0价,每生成2molCu,转移2mol电子,故C错误;
D.CuO加热不分解,不能用加热分解CuO的方法制Cu,故D错误;
故选A。
23.C
【详解】分子式为C4H10O并能与金属钠反应放出氢气的有机物应为丁醇,由于-C4H9有4种结构,则丁醇有4种,故选C。
24.D
【详解】A.由图可知,该反应为吸热反应,A错误;
B.由图可知,该反应为吸热反应,但是的能量和的能量,无法比较,B错误;
C.该反应为可逆反应,某容器内充入反应后,但是SO3反应不玩,所以无法判断吸收热量的多少,C错误;
D.该化学反应历程反应物到过渡态是吸收能量,过渡态到产物是能量的释放,D正确;
故选D。
25.B
【详解】A.金的密度比沙大,大量水冲洗可分离金与沙,提高金的含量,虚线框内的流程是富集,故A不选;
B.虚线框内Si的量不变,虚线框内的流程不是富集,故B选;
C.海水中溴离子浓度较低,在浓缩海水中通入氯气置换出溴,再用空气吹出溴,用二氧化硫吸收,虚线框内的流程是富集,故C不选;
D.海水中镁离子浓度较低,在浓缩海水中加入石灰乳,生成氢氧化镁沉淀,过滤后用盐酸溶解,虚线框内的流程是富集,故D不选;
故选B。
26.C
【详解】A.灼烧应在坩埚中进行,不能在烧杯中灼烧固体,故A错误;
B.乙酸乙酯能够与NaOH溶液反应,小试管中应为饱和碳酸钠溶液,故B错误;
C.乙烯与溴能够发生加成反应,而甲烷不反应,图中除杂装置合理,故C正确;
D.分馏是将不同沸点的物质分离,温度计的水银球应位于蒸馏烧瓶支管口附近,故D错误;
故选C。
27.B
【分析】根据元素在周期表中的位置可知,X为N元素,Y为O元素,Z为S元素,W为Cl元素,结合元素周期律分析判断。
【详解】A.同一周期,从左到右,原子半径逐渐减小,则原子半径:X>Y,故A错误;
B.非金属性越强,简单离子还原性越弱,非金属性:Z<W,简单离子还原性:,故B正确;
C.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性:Z<W,最高价氧化物对应水化物的酸性:Z<W,故C错误;
D.的简单氢化物中H原子为2电子结构,不满足8电子稳定结构,故D错误;
故选B。
28.B
【详解】A.该电池的a极是氢气失电子,产生氢离子,发生氧化反应,为负极,A正确;
B.该电解质溶液为酸性,正极反应为O2+4e-+4H+=2H2O,B错误;
C.在原电池的电解质溶液中,阳离子向正极移动,质子(H+)通过质子交换膜移动到b电极,C正确;
D.该燃料电池中最终生成产物式水,D正确。
故选B。
相关试卷
这是一份四川乐山市2020-2022三年高二化学下学期期末试题汇编1-选择题①,共17页。试卷主要包含了下列叙述中与盐类水解有关的是,下列除去杂质的方法中正确的是等内容,欢迎下载使用。
这是一份四川雅安市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共14页。试卷主要包含了下列不是化石能源的是,下列有机物易溶于水的是,下列变化属于物理变化的是,下列物质属于离子化合物的是,下列物质通常用电解法冶炼的是等内容,欢迎下载使用。
这是一份四川省绵阳市2020-2022三年高一化学下学期期末试题汇编1-选择题①,共13页。试卷主要包含了化学与生产、生活密切相关,下列化学用语表示正确的是,下列工业冶炼金属的方法错误的是等内容,欢迎下载使用。









