









化学九年级下册第三节 溶液的酸碱性集体备课课件ppt
展开第七单元 第3节 溶液的酸碱性 教案
【教学目标】
1.知识与技能
(1)认识溶液的酸碱性,学会用酸碱指示剂判断溶液的酸碱性。
(2)学会利用pH试纸来定量的测定溶液的酸碱度。
(3)知道酸碱性对生命活动及其农作物生长的重要性及影响。
2.过程与方法
(1)学会使用酸碱指示剂来检验溶液的酸碱性。
(2)能通过实验现象对某些问题初步作出正确的科学判断。
3.情感态度和价值观
(1)通过酸碱指示剂的使用,了解化学测量在化学研究和生产、生活中的重要作用。
【教学重点】
(1)酸碱指示剂在酸碱溶液中显示不同的颜色。
(2)用pH试纸来表示溶液的酸碱度。
(3)从H+和OH-的角度认识溶液呈酸碱性的原因,进一步建立宏观与微观相联系的思维方式。
【教学难点】
(1)溶液酸碱性与pH的关系。
(2)从微观粒子H+和OH-的角度去认识溶液呈酸性或碱性的原因。
【课前准备】
多媒体、实验所需物品与器具
【课时安排】
1课时
【教学过程】
一、导入新课
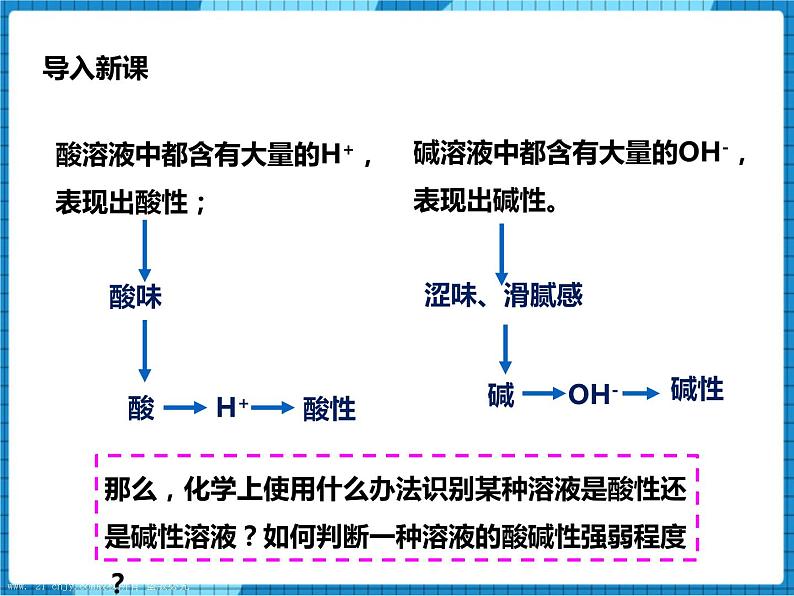
我们已经知道,酸溶液中都含有大量的H+,表现出酸性;碱溶液中都含有大量的OH-,表现出碱性。
也就是酸性表现为酸味,有酸味为酸,因有H+,所以酸性。碱性表现为涩味、油腻感,为碱,因有OH-,所以碱性。
那么,化学上使用什么办法识别某种溶液是酸性还是碱性溶液?如何判断一种溶液的酸碱性强弱程度?
二、新课学习
一、如何检验溶液的酸碱性
酸或碱的各种通性都可以作为我们判断溶液是呈酸性还是呈碱性的依据。
其中最为简捷的方法是:将石蕊试液或酚酞试液滴加到待检验的溶液中,根据试液的颜色变化情况来判断溶液的酸碱性。
有许多物质像石蕊试液一样,遇到酸或碱时能发生特定的颜色变化,化学上把这类物质叫做酸碱指示剂。
常用的酸碱指示剂有紫色石蕊试液和无色酚酞试液等。
实验探究:酸碱指示剂在不同溶液中的颜色变化
参考视频:指示剂与白醋、石灰水
在6支试管(或点滴板)中分别加入少量白醋、柠檬汁、石灰水、肥皂水、食盐水和蔗糖水;然后向其中分别加入几滴紫色石蕊试液。观察溶液颜色的变化。在另外6支试管(或点滴板)中分别加入少量上述6种物质;然后向其中分别加入几滴无色酚酞试液。观察溶液颜色的变化。
间接观察:借助酸碱指示剂,通过观察试液颜色的变化,能帮助人们确定溶液的酸碱性,这种方法属于间接观察法。
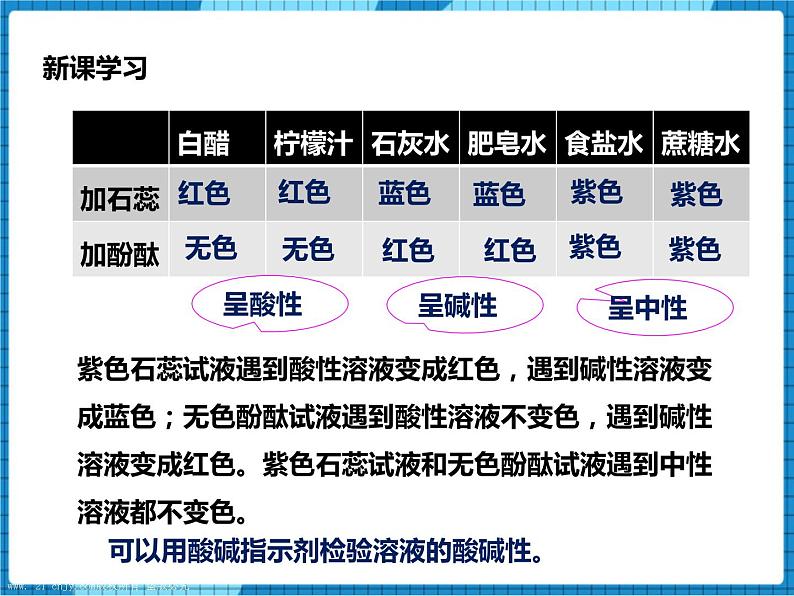
| 白醋 | 柠檬汁 | 石灰水 | 肥皂水 | 食盐水 | 蔗糖水 |
加石蕊 | 红色 | 红色 | 蓝色 | 蓝色 | 紫色 | 紫色 |
加酚酞 | 无色 | 无色 | 红色 | 红色 | 紫色 | 紫色 |
可见,紫色石蕊试液遇到酸性溶液变成红色,遇到碱性溶液变成蓝色;无色酚酞试液遇到酸性溶液不变色,遇到碱性溶液变成红色。紫色石蕊试液和无色酚酞试液遇到中性溶液都不变色。
可以用酸碱指示剂检验溶液的酸碱性。
即:
| 酸性溶液 | 中性溶液 | 碱性溶液 |
紫色石蕊 | 红色 | 紫色 | 蓝色 |
无色酚酞 | 无色 | 无色 | 红色 |
想一想:
1.某一溶液加入无色酚酞后没变色,则该溶液的酸碱性是怎样的?
[中性或酸性]
2.若要测一未知溶液的酸碱性,你认为石蕊溶液和酚酞溶液哪个更好?
[石蕊溶液]
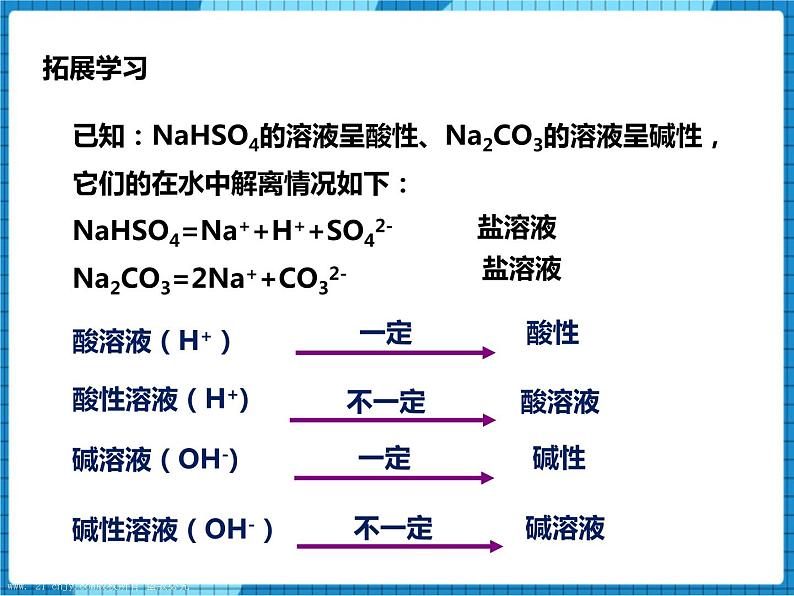
已知:NaHSO4的溶液呈酸性、Na2CO3的溶液呈碱性,它们的在水中解离情况如下:
NaHSO4=Na++H++SO42-
Na2CO3=2Na++CO32-
[二者由金属离子和酸根离子构成,不是酸,不是碱,是盐]
可见:
酸溶液一定酸性
酸性溶液不一定是酸溶液
碱溶液一定碱性
碱性溶液不一定是碱溶液。
多识一点:酸碱指示剂的发现
观察与实验是科学发现与发明的基础。英国化学家波义耳一生中有众多科学发现,酸碱指示剂的发现就是他敏锐观察的结果。
在一次实验中,波义耳不慎将浓盐酸溅到了紫罗兰花瓣上。爱花的波义耳急忙将紫罗兰用水冲洗了一下。过了一会儿,波义耳惊奇地发现深紫色的紫罗兰花瓣变成了红色!
波义耳没有放过这一奇怪的现象,提出了许多猜想和假设,并做了大量的实验来验证他的猜想。他发现大部分花草与酸性或碱性物质作用都能改变颜色,其中从一种叫做石蕊的地衣植物中提取的紫色浸液的变色效果最明显:遇酸性溶液变成红色,遇碱性溶液变成蓝色。利用这一特点,波义耳用石蕊浸液将纸浸透,然后烘干,制成了实验室中常用的酸碱试纸——石蕊试纸。
蓝色石蕊试纸遇酸性溶液变成红色
红色石蕊试纸遇碱性溶液变成蓝色
石蕊试纸携带和使用比石蕊试液更方便
二、怎样判断溶液酸碱性的强弱
你一定有这样的生活经验:同样是酸酸甜甜的桔子,有的略带酸味,而有的却很酸。酸味的强弱程度跟什么因素有关呢?怎样判断溶液酸碱性的强弱?
在一定量的水溶液中,H+越多酸性越强,OH-越多碱性越强。
化学上可以用pH表示溶液酸碱性的强弱程度,pH的数值通常在0和14之间。
pH<7的溶液呈酸性, pH越小,溶液的酸性越强;
pH=7的溶液呈中性;
pH>7的溶液呈碱性,pH越大,溶液的碱性越强。
可以用pH试纸来粗略测定溶液的pH。
溶液pH的测定方法
在洁净干燥的玻璃片或白瓷板上放一片pH试纸,用玻璃棒蘸取待测溶液,滴到试纸上,将试纸显示的颜色与pH标准比色卡对照,读出对应的pH。
用pH试纸测得的pH为整数
要想测得的酸碱度更加精确,要用精密pH试纸,也常使用一种叫做pH计的电子仪器来测定溶液的pH。
用试纸测溶液的酸碱度时要注意:
1.用pH试纸的测出值为整数;
2.不能将pH试纸伸入溶液中,否则会污染试液;
3.不能用蒸馏水将pH试纸润湿,否则测量值不准确;
4. pH试纸测量的是溶液的pH,不能测量固体或气体的pH;
5.不能测浓硫酸的pH。
视频:测定溶液的pH
请选择你感兴趣的物质(如白醋、柠檬汁、石灰水、肥皂水、食盐水、蔗糖水、雨水、自来水、汽水、啤酒和洗涤剂等),用pH试纸测定它们的pH
如图是生活中常见物质的pH
与同学们交流你的测试结果,如果有较大差异,请找出原因。
想一想:
有一包可溶性固体粉末,如何检验它是酸性物质还是碱性物质?
[将粉末溶于水中,用pH试纸测其酸碱度,如小于7则为酸性,大于7则为碱性。]
甲同学在测定某溶液的pH时,先把pH试纸用水湿润再测,他所得的结果准确吗?
[如果是酸性溶液:测量值变大;
如果是碱性溶液:测量值变小;
如果是中性溶液:测量值不变;]
三、物质的酸碱性对生命活动的意义
物质的酸碱性对人类的生命活动至关重要。
人的体液的pH必须维持在一定的范围内,如果pH超出正常范围,就会导致生理机能失调或产生疾病。
如表格中是人体内的一些液体和排泄物的正常pH范围
胃液中的胃酸(主要成分是盐酸)能帮助消化食物,但如果胃酸分泌过多,使胃液的pH降到正常水平以下,就会导致胃痛。剧烈运动时,肌肉里产生乳酸过多,会导致肌肉酸痛。不过,只要休息一段时间,待乳酸氧化分解后,酸痛感就会消失。
参考视频:洗发剂和护发酸碱性
多识一点:pH和洁肤用品
我们在选择洗发液、沐浴露和洁面乳时,需要考虑其酸碱性。成人皮肤的pH通常为4.5〜6.5(初生婴儿接近于7),呈弱酸性,其原因是汗液中含乳酸和氨基酸,皮脂中含脂肪酸。微弱的酸性能抑制皮肤表面病菌的繁殖,并能阻止天然润湿因子的流失。若所选用的洁肤品pH过高,会破坏由皮脂和汗液共同形成的皮脂膜。若洗发液、沐浴露的pH与头发或皮肤的pH相近,则能保持头发、皮肤光洁亮泽。
土壤的酸碱性强弱对植物生长具有非常重要的意义。大多数植物适宜在接近中性的土壤中生长,土壤的酸性太强(pH<4)或碱性太强(pH>8),作物就不能正常生长。
如表格中是几种作物生长最适宜的pH范围
那么,如何测定土壤溶液的pH呢?我们可参考如下视频:
视频:测定土壤溶液的pH
课堂练习:
1.用石蕊试液和酚酞试液分别滴入同一物质的溶液中,下列现象不可能发生的是( D )
A.滴入石蕊试液变红色,滴入酚酞试液不变色
B.滴入石蕊试液不变色,滴入酚酞试液不变色
C.滴入石蕊试液变蓝色,滴入酚酞试液变红色
D.滴入石蕊试液变红色,滴入酚酞试液变红色
2.下列用pH值表示溶液酸性最强的( A )
A.pH=0 B.pH=1
C.pH=7 D.无法判断
3.医生提醒胃酸过多的病人应少吃苹果,那么苹果的pH值( B )
A.大于7 B.小于7
C.等于7 D.无法判断
4.以下物质溶于水形成 的溶液中,pH值大于7的是( C )
A.二氧化碳 B.二氧化硫
C.氧化钙 D.氯化钠
5.将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( B )
A.6 B.8 C.11 D.14
课堂小结:
本节我们学习的主要内容是什么?
[1. 利用石蕊试液、酚酞试液等酸碱指示剂能够检验溶液的酸碱性。紫色石蕊试液遇到酸性溶液变成红色,遇到碱性溶液变成蓝色;无色酚酞试液遇到酸
性溶液不变色,遇到碱性溶液变成红色。
2. 用pH试纸可以测定溶液酸碱性强弱。pH<7的溶液呈酸性,pH越小,酸性越强;pH>7的溶液呈碱性,pH越大,碱性越强;pH=7的溶液呈中性。
3. 物质的酸碱性对生命活动具有重要意义。]
【板书设计】
一、如何检验溶液的酸碱性
将石蕊试液或酚酞试液滴加到待检验的溶液中,根据试液的颜色变化情况来判断溶液的酸碱性。
二、怎样判断溶液酸碱性的强弱测定溶液的pH
pH值>7,溶液呈碱性;
pH值=7,溶液呈中性;
pH值<7,溶液呈酸性
三、物质的酸碱性对生命活动的意义
【作业布置】
1. 尝试自制酸碱指示剂
2. P15在线测试
3. P17挑战自我
【教学反思】
这节课我充分创设与生活有关的问题情境,激发学生的学习兴趣,引导学生从生活入手,理性地分析生活,研究生活,得到经验,获得真知,达到增强学生对化学实验和生活中化学现象的好奇心和探究欲,让学生获得成功的愉悦感,以轻松的心情去认识多姿多彩的化学知识的效果。然后将得到的东西再灵活地运用到生活中去,展现了科学研究与发现的真实过程,实现了“从生活走进化学,从化学走向社会”。并且在整节课中,始终把学生放在主体地位,对于实验的现象、结论全部由学生合作总结得出。老师只是适时点拨,对一些重要的地方进行点拨和引导。通过这节课我深深体会到,我们不仅要教会学生知识,更重要的是教会学生如何生活,教给学生的应是终生受用的思想和能力。我们老师每上一节课,都应该站在有益于学生终身发展的高度上,而不是仅仅让学生学会几个知识点。
初中化学鲁教版九年级下册第四节 酸碱中和反应课文ppt课件: 这是一份初中化学鲁教版九年级下册第四节 酸碱中和反应课文ppt课件,文件包含鲁教版九年化学下第七单元第4节酸碱中和反应课件pptx、鲁教版九年化学下第七单元第4节酸碱中和反应教案docx、鲁教版九年化学下第七单元第4节酸碱中和反应一课一练docx、鲁教版九年化学下第七单元第4节酸碱中和反应素材中和反应的微观过程swf、鲁教版九年化学下第七单元第4节酸碱中和反应素材在氢氧化钠中滴加稀盐酸wmv、鲁教版九年化学下第七单元第4节酸碱中和反应素材氢氧化铜与硫酸反应wmv等6份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
鲁教版九年级下册第二节 碱及其性质多媒体教学ppt课件: 这是一份鲁教版九年级下册第二节 碱及其性质多媒体教学ppt课件,文件包含鲁教版九年化学下第七单元第2节碱及其性质第1课时课件pptx、鲁教版九年化学下第七单元第2节碱及其性质第1课时一课一练doc、鲁教版九年化学下第七单元第2节碱及其性质第1课时教案doc、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材氢氧化钙溶于水wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材氢氧化钠溶于水放热wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材氢氧化钠的一些性质wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材氢氧化钠的腐蚀性wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材生石灰与水反应wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材碱与指示剂wmv、鲁教版九年化学下第七单元第2节碱及其性质第1课时素材锻烧大理石wmv等10份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
初中化学鲁教版九年级下册第一节 酸及其性质教课课件ppt: 这是一份初中化学鲁教版九年级下册第一节 酸及其性质教课课件ppt,文件包含鲁教版九年化学下第七单元第1节酸及其性质第2课时课件pptx、鲁教版九年化学下第七单元第1节酸及其性质第2课时教案doc、鲁教版九年化学下第七单元第1节酸及其性质第2课时一课一练doc、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材氯化钡与硫酸wmv、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材硝酸银与盐酸wmv、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材碳酸钠粉末与稀盐酸wmv、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材酸与指示剂作用wmv、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材酸与铁锈反应wmv、鲁教版九年化学下第七单元第1节酸及其性质第2课时素材镁条与盐酸的反应wmv等9份课件配套教学资源,其中PPT共27页, 欢迎下载使用。













