
所属成套资源:各地区2020-2022三年高二化学下学期期末试题汇编
四川省成都市2020-2022三年高二化学下学期期末试题汇编2-选择题②
展开
这是一份四川省成都市2020-2022三年高二化学下学期期末试题汇编2-选择题②,共21页。试卷主要包含了1—4等内容,欢迎下载使用。
四川省成都市2020-2022三年高二化学下学期期末试题汇编2-选择题②
1. (2021春·四川成都·高二统考期末)实验室用Na2CO3溶液、BaCl2溶液、NaOH溶液等试剂除去粗盐中含有的Ca2+、Mg2+、,下列有关粗盐提纯正确的是
A.除去粗盐中的泥沙,所需玻璃仪器有烧杯、玻璃棒、漏斗
B.除杂质离子时,应先加Na2CO3溶液,再加BaCl2溶液
C.加入NaOH溶液的目的是除去溶液中的Ca2+、Mg2+
D.每加入一种除杂试剂,必须过滤除去产生的沉淀后,再在滤液中加入除杂试剂
2. (2021春·四川成都·高二统考期末)下列实验现象或结论均正确的是
A.将装有甲烷和氯气(体积比1∶3)的试管倒立于饱和食盐水中,光照后管壁出现的油状液滴是CHCl3
B.石蜡油加强热分解,产生的气体为烯烃,能使酸性KMnO4溶液褪色
C.乙醇能与酸性K2Cr2O7溶液反应,酸性K2Cr2O7溶液能鉴别乙醇和乙酸
D.取1mL20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5分钟后取少量溶液,加入少量新制Cu(OH)2加热3~5min,无红色沉淀生成,证明蔗糖未水解
3. (2021春·四川成都·高二统考期末)如图为实验室制备乙酸乙酯的装置,下列有关实验操作或叙述错误的是
A.先在试管中加入2mL浓硫酸,然后边振荡试管边慢慢加入3mL乙醇和2mL乙酸
B.实验中加入几片碎瓷片的作用是防暴沸
C.加热和加入浓硫酸,均可提高酯化反应的速率
D.饱和Na2CO3溶液可除去乙酸乙酯中的乙醇和乙酸,同时降低乙酸乙酯的溶解度
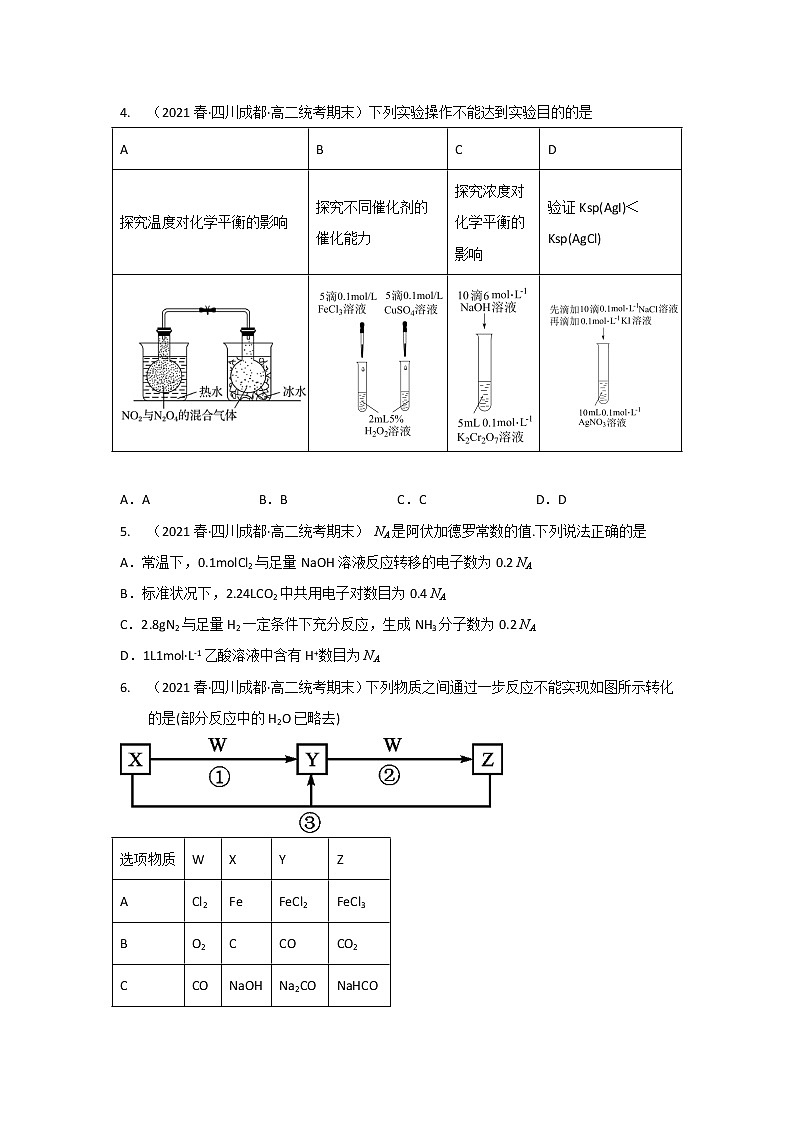
4. (2021春·四川成都·高二统考期末)下列实验操作不能达到实验目的的是
A
B
C
D
探究温度对化学平衡的影响
探究不同催化剂的催化能力
探究浓度对化学平衡的影响
验证Ksp(AgI)<Ksp(AgCl)
A.A B.B C.C D.D
5. (2021春·四川成都·高二统考期末) NA是阿伏加德罗常数的值.下列说法正确的是
A.常温下,0.1molCl2与足量NaOH溶液反应转移的电子数为0.2 NA
B.标准状况下,2.24LCO2中共用电子对数目为0.4 NA
C.2.8gN2与足量H2一定条件下充分反应,生成NH3分子数为0.2 NA
D.1L1mol·L-1乙酸溶液中含有H+数目为NA
6. (2021春·四川成都·高二统考期末)下列物质之间通过一步反应不能实现如图所示转化的是(部分反应中的H2O已略去)
选项物质
W
X
Y
Z
A
Cl2
Fe
FeCl2
FeCl3
B
O2
C
CO
CO2
C
CO2
NaOH
Na2CO3
NaHCO3
D
O2
H2S
S
SO2
A.A B.B C.C D.D
7. (2021春·四川成都·高二统考期末)CO2催化加氢反应可生成乙烯等低碳烯烃。向恒容密闭容器加入等物质的量的CO2和H2,一定条件下发生反应制取乙烯,主要的三个竞争反应为:
ⅰ.
ⅱ.
ⅲ.
下列说法正确的是
A.
B.反应ⅰ中H2的转化率与CO2的转化率相等
C.反应ⅲ反应物总能量小于生成物总能量
D.反应达平衡后,缩小容器体积,反应ⅱ平衡不移动
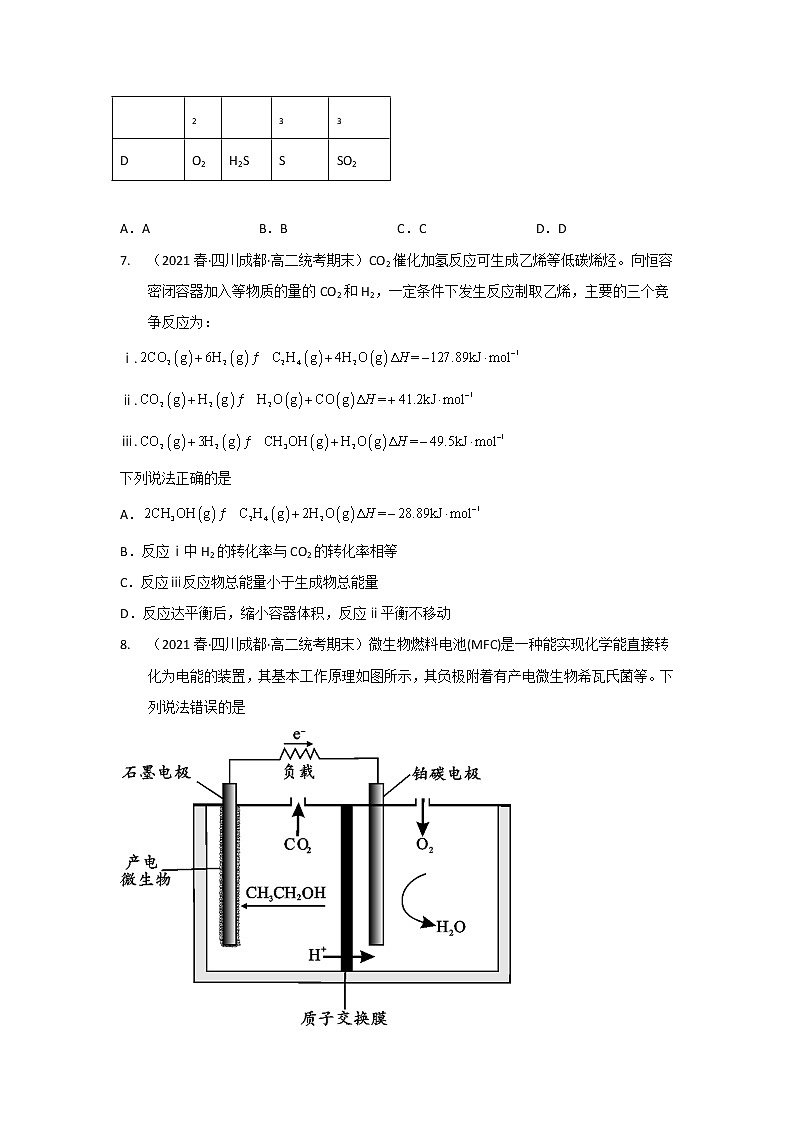
8. (2021春·四川成都·高二统考期末)微生物燃料电池(MFC)是一种能实现化学能直接转化为电能的装置,其基本工作原理如图所示,其负极附着有产电微生物希瓦氏菌等。下列说法错误的是
A.电池放电时,电流由铂碳电极经导线流向石墨电极
B.放电时正极区酸性溶液的pH增大
C.正极区消耗氧气0.224L(标况),则电路中转移0.04mol电子
D.负极区产电微生物作催化剂,不参与CH3CH2OH氧化成CO2的反应
9. (2021春·四川成都·高二统考期末)下列叙述正确的是
A.NaHCO3的电离方程式为
B.pH=11的氨水溶液稀释10倍后pH=10
C.NaOH溶液中通入CO2气体至过量,水的电离程度先增大后减小
D.升高温度,NaOH溶液的pH不变
10. (2021春·四川成都·高二统考期末)室温下向20mL0.1mol·L-1NaOH溶液中加入0.1mol·L-1的CH3COOH溶液,溶液中,pH、分布系数δ随滴加CH3COOH溶液体积V(CH3COOH)的变化关系如图所示。[比如CH3COOH的分布系数:]。下列说法正确的是
A.曲线①代表δ(CH3COOH),曲线②代表δ(CH3COO-)
B.pH=7时,
C.a点所示溶液中
D.该温度下CH3COOH溶液的电离平衡常数
11. (2022春·四川成都·高二统考期末)2022年北京冬奥会中使用了大量高科技材料,下列说法中错误的是
A.钛合金速滑冰刀属于无机非金属材料
B.颁奖礼服保暖用到的石墨烯与金刚石互为同素异形体
C.火炬中的聚硅氮烷树脂属于高分子化合物
D.跨临界直冷制冰技术用到的节能、安全无毒
12. (2022春·四川成都·高二统考期末)下列化学用语或图示表达正确的是
A.S2-结构示意图为 B.HClO的结构式:H-O-Cl
C.CO2的电子式: D.丙烯的球棍模型为
13. (2022春·四川成都·高二统考期末)代表阿伏加德罗常数的值。下列说法正确的是
A.中含有的中子数为
B.80gNaOH溶解在1L水中,所得溶液物质的量浓度为2mol/L
C.1L0.1mol/L碳酸钠溶液中碳酸根离子数小于
D.标况下22.4L中含有的分子数等于
14. (2022春·四川成都·高二统考期末)下列有关物质分类正确的是
A.SiO2——两性氧化物 B.水玻璃——弱电解质
C.小苏打——正盐 D.石油——混合物
15. (2022春·四川成都·高二统考期末)下表中是部分短周期元素的原子半径及主要化合价的信息。下列叙述正确的是
元素代号
A
B
C
D
原子半径/nm
0.186
0.143
0.102
0.074
要化合价
+1
+3
+6、-2
-2
A.与的核外电子数不可能相等
B.离子半径大小:
C.最高价氧化物对应水化物的碱性:A>B
D.简单氢化物的稳定性;D<C
16. (2022春·四川成都·高二统考期末)下列物质与水反应,转化成对应物质时有气体逸出的是
A. B.
C. D.
17. (2022春·四川成都·高二统考期末)下列方程式能正确解释其事实的是
A.沸水中滴加饱和氯化铁溶液制胶体:
B.自然界的天然固氮:
C.氯化铝溶液与浓氨水混合:
D.过量铁粉与新制氯水反应:
18. (2022春·四川成都·高二统考期末)下列应用与对应物质的性质关系正确的是
A.非金属性C>Si,故可用碳单质高温下与二氧化硅反应制粗硅
B.氢氟酸显弱酸性,故可用于雕刻玻璃
C.密度比空气大,故可作钠着火时的灭火剂
D.明矾溶于水可产生胶体,故可作净水剂
19. (2022春·四川成都·高二统考期末)下列实验设计能达到目的的是
A
B
C
D
储存少量氯化氢气体
收集NO
比较酸性:硼酸
蒸发结晶
A.A B.B C.C D.D
20. (2022春·四川成都·高二统考期末)观察是化学学习的重要方法。金属钠放置于空气中观察到下列现象,下列推证正确的是
A.若将钠放置于坩埚中加热,观察到的现象与①、②相同
B.取①得到的产物,滴加适量水和溶液,可观察到蓝色沉淀生成
C.取③后液滴的稀溶液滴加酚酞溶液,可观察到酚酞先变红后褪色
D.加热④的白色晶体,通入水中有气泡则可证明白色晶体是
21. 2022春·四川成都·高二统考期末)天然气在催化剂作用下热解可制得可再生的绿色能源氢气,其反应为: 。下列有关判断正确的是
A.催化剂可以提高活化分子百分数
B.时:反应达到了平衡状态
C.恒温恒容下加入C(s);平衡逆向移动
D.恒温恒压下通入氦气;平衡正向移动,正反应速率增大,逆反应速率减小
22. (2022春·四川成都·高二统考期末)某烃的结构简式为,有关它的分析正确的是
A.分子式为 B.一氯代物有8种
C.能发生取代、氧化、加聚反应 D.最多有7个碳原子在一条直线上
23. (2022春·四川成都·高二统考期末)下列过程不涉及氧化还原反应的是
A.蔗糖水解为葡萄糖和果糖 B.直接加热氧化银冶炼银
C.含氯消毒剂用于消毒环境 D.大气中二氧化氮参与酸雨形成
24. (2022春·四川成都·高二统考期末)下图是某同学用500mL容量瓶配制NaOH溶液的过程:
下列关于该实验的叙述正确的是
A.如图所示,用托盘直接称量2.0g烧碱
B.配制的正确顺序为①④③⑤②⑥
C.②中定容时仰视刻线会导致溶液浓度偏高
D.能用容量瓶贮存配制好的溶液
25. (2022春·四川成都·高二统考期末)下列实验操作、现象及解释或所得结论均正确的是
选项
实验操作
现象
解释或结论
A
加热固体,在试管口放一小片湿润的蓝色石蕊试纸
石蕊试纸变红
可用此方法实验室制备氨
B
在某盐溶液中滴入几滴溶液
有白色沉淀生成
原盐溶液中不一定含有
C
向品红溶液中通入气体A,振荡
品红褪色
气体A为
D
将铜丝放入盛有浓硫酸的试管中加热,反应完后静置,直接加入少量水
试管中出现蓝色澄清溶液
浓硫酸具有强氧化性
A.A B.B C.C D.D
26. (2022春·四川成都·高二统考期末)我国科学家实现了二氧化碳到淀粉的人工合成,在“碳中和”领城做出了卓越贡献,其转化过程示意图如下:
下列叙述正确的是
A.反应①:,
B.反应②:有极性键、非极性键的断裂与形成
C.该过程实现了能量的储存,将太阳能最终转变成了化学能
D.向所得淀粉溶液中加适量稀硫酸,加热,冷却后加过量NaOH溶液,再滴加少量碘水,溶液未变蓝,证明淀粉已完全水解
27. (2022春·四川成都·高二统考期末)生产生活中,盐类水解有着广泛的应用。下列做法错误的是
A.洗餐具油污时,用热的纯碱溶液较冷的好
B.用泡沫灭火剂灭火时,将溶液和溶液混和
C.将溶于大量水并加热制备
D.为增加肥效将草木灰与铵态氮肥混合施用
28. (2022春·四川成都·高二统考期末)25℃时,向的一元弱酸HA中逐滴加入NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。下列说法错误的是
A.a>1
B.可用甲基橙指示滴定终点c
C.水的电离程度:b点和d点近似相同
D.d点时,
29. (2022春·四川成都·高二统考期末)在pH=4.5时,利用原电池原理,用铁粉将废水中无害化处理的实验如下表:
方案一
方案二
初始条件
pH=4.5
pH=4.5,Fe2+
去除率
<50%
接近100%
24小时pH
接近中性
接近中性
铁的最终物质形态
下列说法正确的是A.该电池中Fe作负极,可被完全氧化
B.正极的电极反应为:
C.方案二的去除率高,原因可能是Fe2+破坏了FeO(OH)层
D.改变铁粉粒径大小,的去除速率不变
30. (2022春·四川成都·高二统考期末)难溶电解质存在沉淀溶解平衡,已知:,,下列叙述中正确的是
A.在含有固体的悬浊液中加入少量固体,不变
B.悬浊液液中逐渐加入溶液,一定不发生
C.将几滴溶液滴入溶液,得到白色沉淀,再滴加溶液,出现红褐色沉淀,证明
D.另取少量C中白色沉淀,滴入浓溶液使其溶解,可能是导致沉淀溶解
参考答案:
1. A
【详解】A.除去粗盐中的泥沙,主要方法是过滤,因此所需玻璃仪器有烧杯、玻璃棒、漏斗,故A正确;
B.除杂质离子时,由于加入的试剂都是过量的,碳酸钠不仅除掉钙离子,还要除掉加入过量的钡离子,因此Na2CO3溶液应加在BaCl2溶液后面,故B错误;
C.加入NaOH溶液的目的是除去溶液中的Mg2+,Na2CO3溶液除去溶液中的Ca2+和过量的Ba2+,故C错误;
D.每加入一种除杂试剂必须过量,将所有除杂的物质全部加入后过滤(避免重复操作),过滤后再加入盐酸除掉多余的NaOH溶液和Na2CO3溶液,故D错误。
综上所述,答案为A。
2. C
【详解】A.将装有甲烷和氯气(体积比1∶3)的试管倒立于饱和食盐水中,光照后管壁出现的油状液滴是CHCl3、CH2Cl2、CCl4,甲烷与氯气是发生一系列的反应,故A错误;
B.石蜡油加强热分解,产生的气体为烯烃和烷烃,烯烃能使酸性KMnO4溶液褪色,故B错误;
C.乙醇能与酸性K2Cr2O7溶液反应,因此酸性K2Cr2O7溶液能鉴别乙醇和乙酸,故C正确;
D.取1mL 20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5分钟后取少量溶液,先加入NaOH溶液,再加入少量新制Cu(OH)2加热3~5min,通过看是否有红色沉淀生成来证明蔗糖是否水解,故D错误。
综上所述,答案为C。
3. A
【详解】A.先在试管中加入2mL乙醇,然后边振荡试管边慢慢加入3mL浓硫酸,再缓缓加入2mL乙酸,故A错误;
B.实验中加入几片碎瓷片的作用是防液体暴沸,故B正确;
C.加热和加入浓硫酸,均可提高酯化反应的速率,但温度不能太高,易将乙醇和乙酸挥发,故C正确;
D.饱和Na2CO3溶液可除去乙酸乙酯中的乙酸,溶解乙酸乙酯中的乙醇,同时降低乙酸乙酯的溶解度,故D正确。
综上所述,答案为A。
4. D
【详解】A.实验中存在平衡2NO2(红棕色)N2O4(无色)可通过混合气体的颜色来判断平衡的移动情况,故能探究温度对化学平衡的影响,A不合题意;
B.所发生的反应为:2H2O22H2O+O2↑,可通过产生气泡的速率来比较反应快慢,从而探究不同催化剂的催化能力,B不合题意;
C.C中存在平衡:Cr2O+H2O2CrO+2H+,加入NaOH将改变H+的浓度,从而使平衡移动,改变溶液颜色的变化,故能探究浓度对化学平衡的影响,C不合题意;
D.向10mL0.1mol/L的AgNO3溶液中先加入10滴0.1mol/L的NaCl溶液后,AgNO3过量,在加入0.1mol/L的KI溶液,由于没有沉淀的转化,故不能验证Ksp(AgI)<Ksp(AgCl),D符合题意;
故答案为:D。
5. B
【详解】A.Cl2+2NaOH =NaCl+NaClO+H2O,常温下,0.1molCl2与足量NaOH溶液反应转移的电子数为0.1NA,故A错误;
B.标准状况下,2.24L CO2即物质的量为1mol,CO2电子式为,1mol CO2共用电子对数目为0.4 NA,故B正确;
C.氮气与氢气反应是可逆反应,因此2.8gN2即物质的量为0.1mol,0.1mol N2与足量H2一定条件下充分反应,生成NH3分子数小于0.2 NA,故C错误;
D.1L1mol·L-1乙酸溶液中乙酸物质的量为1mol,由于乙酸是弱酸,部分电离,因此溶液中含有H+数目小于NA,故D错误。
综上所述所,答案为B。
6. A
【详解】A.变价金属铁和强氧化剂氯气反应生成高价态金属氯化物:FeCl3,A中X和W不能生成FeCl2,A错误;
B.氧气和过量的碳生成一氧化碳,一氧化碳继续和氧气反应生成二氧化碳,碳和二氧化碳化合生成一氧化碳,B正确;
C.少量二氧化碳和氢氧化钠生成碳酸钠,向碳酸钠中继续通入二氧化碳生成碳酸氢钠,碳酸氢钠和氢氧化钠反应生成碳酸钠,C正确;
D.硫化氢和氧气反应生成单质硫,硫和氧气化合生成二氧化硫,硫化氢和二氧化硫反应生成单质硫,D正确;
答案为:A。
7. A
【详解】A.根据盖斯定律得,故A正确;
B.向恒容密闭容器加入等物质的量的CO2和H2,反应ⅰ中H2与CO2按照1:3反应,转化率不相等,故B错误;
C.反应ⅲ为放热反应,反应物总能量大于生成物总能量,故C错误;
D.反应达平衡后,缩小容器体积,反应ⅰ和ⅲ正向移动,造成CO2、H2浓度减小,H2O的物质的量浓度变大,反应ⅱ平衡逆向移动,故D错误;
故答案为A。
8. D
【详解】A.燃料电池通入O2一侧为正极,所以题目中电池结构铂碳电极为正极,故电流由正极流出,经外电路进入负极——石墨电极,描述正确,不符题意;
B.电池正极,H+被消耗,H+浓度下降,pH值上升,描述正确,不符题意;
C.由B选项分析:,标况下0.224LO2物质的量是0.01mol,按方程式比例换算转移电子0.04mol,描述正确,不符题意;
D.催化剂参与反应,通过改变反应途径使反应速率发生改变,自身重新生成原有结构,所以选项描述错误,符合题意;
综上,本题选D。
9. C
【详解】A.NaHCO3是强电解质,NaHCO3的电离方程式为,故A错误;
B.pH=11的氨水溶液稀释10倍,假设一水合氨不电离,则溶液中氢氧根浓度变为原来十分之一,但由于一水合氨电离,因此溶液中氢氧根浓度比原来十分之一大一点,因此稀释后pH>10,故B错误;
C.NaOH溶液中通入CO2气体至过量,NaOH碱性强,抑制水的电离,通入二氧化碳气体至生成碳酸钠,促进水的电离,该过程是水的电离程度增大,继续通入二氧化碳气体,反应生成碳酸氢钠,促进水的电离,但促进程度比碳酸钠促进水的电离程度小,因此该过程是水的电离程度减小,故C正确;
D.升高温度,水的离子积常数增大,因此NaOH溶液中氢离子浓度增大,溶液的pH减小,故D错误。
综上所述,答案为C。
10. D
【详解】A.开始的时候氢氧化钠过量醋酸主要以分子形式存在,随着醋酸的增加,醋酸分子分布系数减小,醋酸根离子增加,所以曲线①代表δ(CH3COO-),曲线②代表δ(CH3COOH),A错误;
B.这个等式是醋酸钠溶液中物料守恒,可是醋酸钠溶液显碱性,B错误;
C.根据电荷守恒,溶液显中性,可是a溶液显碱性,C错误;
D.该温度下CH3COOH溶液的电离平衡常数,由图可知曲线①,曲线②交叉的时候,则,D正确;
故选D。
11. A
【详解】A. 钛合金属于金属材料,故A错误;
B. 石墨烯与金刚石为碳元素组成的不同的单质,互为同素异形体,故B正确;
C. 聚硅氮烷树脂属于高分子化合物,故C正确;
D. 跨临界直冷制冰技术用到的节能、安全无毒,故D正确;
故选A。
12. B
【详解】A.S2-是S原子获得2个电子形成的,离子核外电子排布为2、8、8,故S2-结构示意图为,A错误;
B.HClO分子中O原子分别与H、Cl原子各形成1对共用电子对,使分子中各个原子都达到稳定结构,故其结构式是H-O-Cl,B正确;
C.CO2分子中C原子与2个O原子形成4对共用电子对,使分子中各个原子都达到最外层8个电子的稳定结构,故CO2的电子式为,C错误;
D.丙烯分子结构简式是CH2=CH-CH3,分子中存在一个碳碳双键,结合C原子价电子数目是4,可知其图示为丙烷的球棍模型,D错误;
故合理选项是B。
13. C
【详解】A.的摩尔质量为54g/mol,1个中的中子数为(18-8)×3=30,故中含有的中子数为,故A错误;
B. 80gNaOH物质的量为2mol,但是1L为溶剂水的体积,不是溶液的体积,故不能计算溶液物质的量浓度,故B错误;
C.碳酸钠的物质的量为1L×0.1mol/L=0.1mol,碳酸根离子发生水解反应,故碳酸根离子数小于,故C正确;
D. 标况下,水为固体,则22.4L的物质的量不是1mol,故D错误;
故选C。
14. D
【详解】A.SiO2只能与碱反应产生盐和水,故SiO2是酸性氧化物,A错误;
B.水玻璃是Na2SiO3的水溶液,是混合物,不是纯净物,因此不属于电解质,B错误;
C.小苏打是NaHCO3的俗称,属于酸式盐,而不是正盐,C错误;
D.石油中含有多种烷烃、环烷烃,因此石油属于混合物,D正确;
故合理选项是D。
15. C
【分析】由表中数据可知A为钠,B为铝,C为硫,D为氧。
【详解】A.B为铝,D为氧,则与的核外电子数相等,故A错误;
B.A为钠,D为氧,O2-、Na+的核外电子排布相同,核电荷数越大,离子半径越小,则离子半径大小:O2->Na+,故B错误;
C. 金属性越强,最高价氧化物对应水化物的碱性越强,金属性:Na>Mg,则最高价氧化物对应水化物的碱性:NaOH>Mg(OH)2,故C正确;
D. 非金属性越强,简单氢化物越稳定,非金属性:O>S,则简单氢化物的稳定性:H2O>H2S,故D错误;
故选C。
16. B
【详解】A.Cl2与水反应:,没有气体逸出,A不符合题意;
B.Mg与水反应:,有气体逸出,B符合题意;
C.NH3与水反应:,没有气体逸出,C不符合题意;
D.SO3与水反应:,没有气体逸出,D不符合题意;
故选B。
17. A
【详解】A. 沸水中滴加饱和氯化铁溶液制胶体,化学方程式正确,故A符合题意;
B. 该反应为工业合成氨,属于人工固氮,故B不符合题意;
C. 氢氧化铝不能与弱碱反应,故氯化铝溶液与浓氨水混合生成氢氧化铝沉淀,正确的离子方程式为:,故C不符合题意;
D. 过量铁粉与新制氯水反应,应生成氯化亚铁,故D不符合题意;
故选A。
18. D
【详解】A.非金属性C>Si,但制粗硅与其非金属性没有关系,A错误;
B.氢氟酸显弱酸性,但与其用于雕刻玻璃没关系,雕刻玻璃是由于SiO2与HF反应的特殊性,B错误;
C.能与Na加热条件下反应,不可作钠着火时的灭火剂,C错误;
D.明矾溶于水可产生胶体,胶体具有吸附性,故可作净水剂,D正确;
故选D。
19. B
【详解】A.氯化氢气体极易溶于水,因此不能采用该装置储存少量氯化氢气体,故A不符合;
B.NO难溶于水也不与水反应,因此NO能够采用排水法收集,故B符合;
C.硼酸不能和Na2CO3反应生成CO2,石灰水中无现象,因此不能得出硼酸酸性强于,故C不符合;
D.蒸发结晶氯化钠溶液应该在蒸发皿中进行,故D不符合;
故选B。
20. B
【分析】金属钠露置于空气中发生的变化中,①是钠被氧化为氧化钠为灰暗色;②是氧化钠和水反应生成氢氧化钠为白色;③氢氧化钠潮解形成氢氧化钠溶液;④是二氧化碳和氢氧化钠反应生成碳酸钠晶体,
【详解】A.钠放置于坩埚中加热,钠首先融化成小球,继而剧烈燃烧产生黄色火焰,燃烧产物为淡黄色的固体过氧化钠,A错误;
B.①是钠被氧化为氧化钠,水与氧化钠反应生成NaOH,加入溶液生成Cu(OH)2沉淀,可观察到蓝色沉淀生成,B正确;
C.③氢氧化钠潮解形成氢氧化钠溶液,滴加酚酞溶液,溶液只变红不褪色,C错误;
D.加热④的白色晶体,即加热Na2CO3·10H2O,对其加热通入水中无明显现象,D错误;
故选:B。
21. A
【详解】A.催化剂通过改变反应途径,降低反应活化能,从而使活化分子变相增加,故新反应路径下活化分子百分含量上升,描述正确,符合题意;
B.反应速率未标注反应正逆方向,不能明确反应速率是同向还是逆向,描述错误,不符题意;
C.固体反应物的添加不会影响反应平衡,不会破坏原有平衡,描述错误,不符题意;
D.恒温恒压条件下通入氦气,容器容积会增大,相当于减小压强,平衡正向移动,反应体系中各气体浓度均下降,所以正逆反应速率均会减小,描述错误,不符题意;
综上,本题选A。
22. C
【详解】A.根据该烃的结构简式可知,其分子式为C11H10,A错误;
B.该烃上的苯环关于两对位取代基团连线对称,不同化学环境的H原子有6种,则一氯代物有6种,B错误;
C.该烃苯环上的氢原子可发生取代反应,有不饱和碳可发生氧化反应,碳碳双键和碳碳叁键可发生加聚反应,C正确;
D.碳碳叁键及其连接的苯环碳原子、苯环上对位碳原子在同一直线,碳碳双键是平面结构,碳原子及取代氢原子位置的甲基碳原子不可能在同一直线,故最多有5个碳原子在一条直线上,D错误;
故选C。
23. A
【详解】A. 蔗糖水解为葡萄糖和果糖,是水解反应,不是氧化还原反应,故A符合题意;
B. 直接加热氧化银冶炼银,生成银单质和氧气,化合价发生变化,是氧化还原反应,故B不符合题意;
C. 含氯消毒剂用于消毒环境,是利用含氯物质的强氧化性,涉及氧化还原反应,故C不符合题意;
D. 大气中二氧化氮与水反应生成硝酸和NO,有化合价的变化,是氧化还原反应,故D不符合题意;
故选A。
24. B
【详解】A. 氢氧化钠易潮解,且有腐蚀性,故应在烧杯中称取氢氧化钠,而不能直接用托盘称量,故A错误;
B. 配制一定物质的量浓度的溶液的步骤为:计算、称量、溶解、冷却、移液洗涤、定容、摇匀、装瓶,故配制的正确顺序为①④③⑤②⑥,故B正确;
C.定容时仰视刻线会导致溶液的体积偏大,所溶液浓度偏低,故C错误;
D.容量瓶只能用于配溶液,不能用于贮存配制好的溶液,故D错误;
故选B。
25. B
【详解】A.用湿润的红色石蕊试纸检验氨气,氨气使湿润的红色石蕊试纸变蓝,该实验操作生成多种气体,也不用来制取氨气,选项A错误;
B.原盐溶液中不一定含有Cl-,可能含有、等,选项B正确;
C.气体A不一定是SO2,可能是Cl2, Cl2和水反应生成的次氯酸具有强氧化性,能漂白,使品红褪色,选项C错误;
D.试管中可能有剩余的浓硫酸,不能直接向试管中加入水,应将试管中的液体冷却后缓慢注入盛水的烧杯中,观察溶液颜色,选项D错误;
答案选B。
26. C
【详解】A.氢气燃烧为放热反应,反应①是其逆反应,则水分解为吸热反应,,A项错误;
B.反应②为二氧化碳和氢气反应,生成甲醇,该反应有极性键的断裂与形成,非极性键的断裂,B项错误;
C.由图可知,该过程实现了能量的储存,将太阳能最终转变成了淀粉中的化学能,C项正确;
D.加过量NaOH溶液,再滴加少量碘水,碘单质与氢氧化钠发生了反应,则溶液未变蓝,不能证明淀粉已完全水解,D项错误;
答案选C。
27. D
【详解】A.Na2CO3溶液中水解,加热能使其水解程度增大,溶液中碱性增强,更容易使油脂分解从而达到清洗目的,描述正确,不符题意;
B.两种盐溶液混合会发生离子反应:,形成大量糊状泡沫,Al(OH)3和CO2都能阻隔可燃物与空气接触,达到灭火目的,描述正确,不符题意;
C.TiCl4接触水并加热会发生比较明显的水解反应,生成含结晶水的TiO2•xH2O细小颗粒,描述正确,不符题意;
D.草木灰中有效成分是K2CO3,与铵态氮肥同时使用,在土壤的水分环境中会发生反应生成NH3和CO2,造成化肥中氮元素损失,所以该操作应避免发生,描述错误,符合题意;
综上,本题选D。
28. B
【详解】A. HA为一元弱酸,HA部分电离,溶液中H+物质的量浓度低于0.10,故溶液的pH大于1即a > 1,故A正确;
B.强碱弱酸盐呈碱性,甲基橙的变色范围为pH 3.1—4.4,不可以作为强碱滴定弱酸的指示剂,故B错误;
C. b点溶质为HA、NaA,pH=3,c(H+)=1×10-3 mol∙L-1,c(OH-) =1×10-11 mol∙L-1,则水电离出的c(OH-) =1×10-11 mol∙L-1,d点溶质为NaA、NaOH,pH = 11,c(OH-) =1×10-3 mol∙L-1,c(H+)=1×10-11 mol∙L-1,则水电离出的c(OH-) =1×10-11 mol∙L-1,故b、d两点水的电离程度相同,故C正确;
D. d点时,由电荷守恒:可知,,则,故D正确;
故选B。
29. C
【详解】A.用铁粉将废水中无害化处理,则Fe为负极,由于反应产生的FeO(OH)不能导电,该物质不能溶于水,其将Fe全部覆盖,阻碍电子转移,因此Fe不能被完全氧化,A错误;
B.在正极上得到电子被还原为,在酸性环境中不可能存在NH3,正极的电极反应式为:+8e-+10H+=+3H2O,B错误;
C.方案二的去除率高,原因可能是Fe2+与FeO(OH)反应产生了Fe3O4,将不能导电的FeO(OH)反应产生易导电的Fe3O4,有利于电子的转移,因此加入Fe2+可以提高去除率,C正确;
D.改变铁粉粒径大小,可以形成许多微小原电池,从而使的去除速率加快,D错误;
故合理选项是C。
30. D
【详解】A. 含有固体的悬浊液中存在溶解平衡,加入少量Na2SO4固体,溶液中增大,减小,故A错误;
B. 当加入的Na2CO3溶液达到一定量时,BaSO4可以向BaCO3转化,故B错误;
C. NaOH溶液的浓度和体积都比MgCl2的大,两者反应后NaOH有剩余,再滴加FeCl3溶液,出现红褐色沉淀,无法证明是与NaOH反应产生的,还是Mg(OH)2转化为Fe(OH)3的,故C错误;
D. Mg(OH)2中滴入NH4Cl溶液使其溶解,反应式可能为Mg(OH)2(s)+ 2(aq) = Mg2+ (aq)+ 2NH3∙H2O (aq),可能是导致沉淀溶解,故D正确;
故选D。
相关试卷
这是一份四川省绵阳市2020-2022三年高二化学下学期期末试题汇编2-选择题②,共12页。试卷主要包含了8×10-10,Ksp=7等内容,欢迎下载使用。
这是一份四川省成都市2020-2022三年高二化学下学期期末试题汇编1-选择题①,共18页。试卷主要包含了化学与生活密切相关,下到分析错误的是,下列离子在溶液中能大量共存的是,,下列说法正确的是,下列反应的应用错误的是,下列实验操作正确的是,下列说法正确的是等内容,欢迎下载使用。
这是一份四川省遂宁市2020-2022三年高二化学下学期期末试题汇编2-选择题②,共15页。试卷主要包含了7,则溶液中,50mL,9×10-8ml/L等内容,欢迎下载使用。









