
初中化学中考复习 2020届九年级中考化学一轮复习知识点训练卷:酸与碱
展开
这是一份初中化学中考复习 2020届九年级中考化学一轮复习知识点训练卷:酸与碱,共14页。试卷主要包含了1%),小凯整理归纳得出的规律合理的是等内容,欢迎下载使用。
酸与碱考点一:酸碱中和反应1.天平的左端和右端分别放着盛有浓盐酸和浓硫酸的敞口烧杯,过段时间后,天平( )A.左端下沉B.右端下沉C.仍平衡D.无法判断2.中和反应在工农业生产和日常生活中有广泛的用途。下列应用一定与中和反应原理无关的是( )A.食物过咸时加食醋调和 B.服用含Al(OH)3的药物治疗胃酸过多C.施用熟石灰改良酸性土壤 D.用NaOH溶液洗涤石油产品中的残余硫酸3.室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )
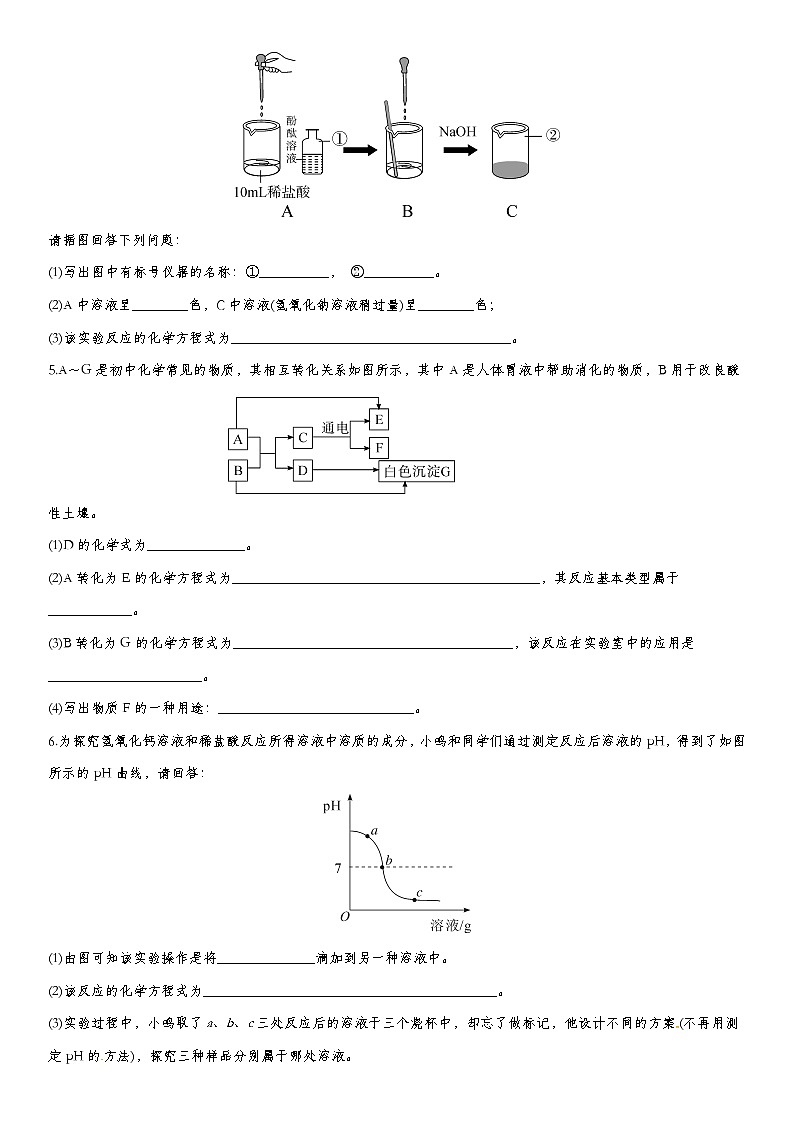
A.a点溶液中有两种溶质B.b点溶液中滴加紫色石蕊溶液,溶液变蓝C.c点烧杯内液体的pH=7D.d点溶液中有较多的Ba2+、OH-、SO、H+4.酸碱中和反应在工农业生产和日常生活中应用十分广泛。如图所示是氢氧化钠与稀盐酸反应的实验示意图。请据图回答下列问题:(1)写出图中有标号仪器的名称:①__________, ②__________。(2)A中溶液呈________色,C中溶液(氢氧化钠溶液稍过量)呈________色;(3)该实验反应的化学方程式为________________________________________。
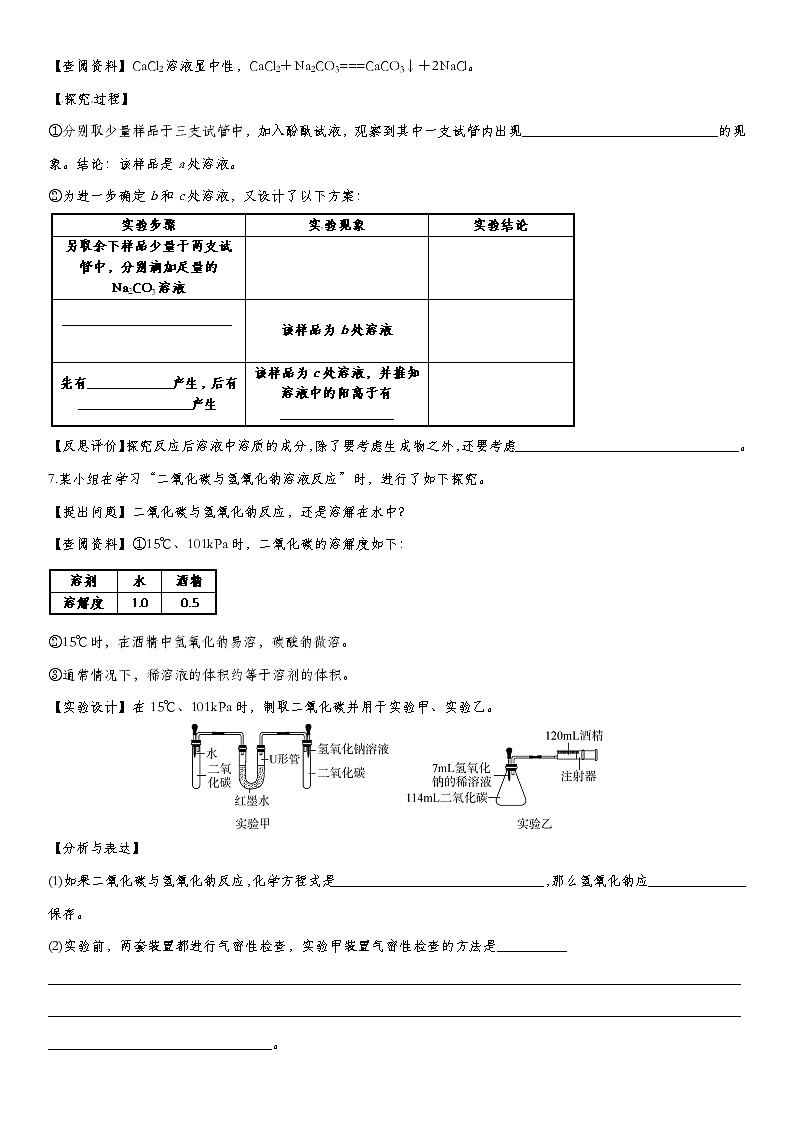
5.A~G是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤。(1)D的化学式为______________。(2)A转化为E的化学方程式为____________________________________________,其反应基本类型属于____________。(3)B转化为G的化学方程式为________________________________________,该反应在实验室中的应用是______________________。(4)写出物质F的一种用途:____________________________。6.为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定反应后溶液的pH,得到了如图所示的pH曲线,请回答:(1)由图可知该实验操作是将______________滴加到另一种溶液中。(2)该反应的化学方程式为__________________________________________。(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了做标记,他设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3===CaCO3↓+2NaCl。【探究过程】①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现____________________________的现象。结论:该样品是a处溶液。②为进一步确定b和c处溶液,又设计了以下方案:【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑________________________________。7.某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究。【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?【查阅资料】①15℃、101kPa时,二氧化碳的溶解度如下:②15℃时,在酒精中氢氧化钠易溶,碳酸钠微溶。③通常情况下,稀溶液的体积约等于溶剂的体积。【实验设计】在15℃、101kPa时,制取二氧化碳并用于实验甲、实验乙。【分析与表达】(1)如果二氧化碳与氢氧化钠反应,化学方程式是______________________________,那么氢氧化钠应______________保存。(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是________________________________________________________________________________。(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是________(填答案字母)。A.先慢后快 B.先快后慢 C.先慢后快,再变慢实验乙中,还可能观察到的现象是________________________________________。(5)实验乙中,120mL酒精____________(选填“能”或“不能”)换成水,原因是________________________________________________。(6)由以上探究可知,二氧化碳能溶于水,也能与氢氧化钠反应,但实验乙的数据还不够准确,造成实验乙误差的原因可能有________________________________________。(写一条)8.某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表和图所示:(已知BaCl2溶液的pH=7)求:(1)完全反应后生成沉淀的质量为________。(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%) 考点二:常见的酸和碱与酸碱度1.下列物质的名称或俗称,指的不是同一种物质的是( )A.熟石灰 B.氢氧化钙 C.石灰石 D.消石灰2.下列溶液中不能导电的是( )A.澄清石灰水 B.稀硫酸 C.酒精溶液 D.食盐水3.下列做法不符合“改善环境质量,推动绿色发展”这一主题的是( )A.尽量选择公共交通工具出行 B.自带布袋购物C.废酸液直接排入下水道 D.减少使用一次性餐具4.推理是化学学习中常用的思维方法,下列推理正确的是( )A.人的血液呈碱性,则人的体液都呈碱性B.NaCl溶液能够导电,则所有液体都能导电C.KNO3溶液无色透明,则无色透明的液体都是溶液D.酸性溶液能使石蕊变红,能使石蕊变红的溶液都是酸性溶液5.只用石蕊试液就能将下列各组溶液区分开来的是( )A.NaCl NaOH NaNO3 B.NaOH H2SO4 KNO3C.HCl NaCl Na2SO4 D.Na2SO4 H2SO4 K2SO46.如图所示,分别向试管内加入下列物质之一,能使U形管右侧液面显著升高的是( )A.浓盐酸B.浓硫酸C.食盐D.石灰石7.下列图示的实验操作,正确的是( )8.生活中一些食物的近似pH如下,其中显碱性的食物是( )A.柠檬汁(2.0~3.0) B.苹果汁(2.9~3.3) C.牛奶 (6.3~6.6) D.鸡蛋清(7.6~8.0)9.小凯整理归纳得出的规律合理的是( )A.溶液中的溶剂一定是水B.水既能跟某些金属氧化物反应生成碱,也能跟某些非金属氧化物反应生成酸C.酸、碱中一定都含有氧元素D.不能使酚酞溶液变红的溶液一定是酸溶液10.二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中,有着重要的应用。(1)二氧化碳用于制汽水,这是利用了二氧化碳____________________________的性质。(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为_____________________________________________________(用化学方程式表示)。(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有______________,利用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强________(选填“酸”或“碱”)性,能达到消毒杀菌的效果。(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为______________________________________________。 参考答案考点一:酸碱中和反应1.天平的左端和右端分别放着盛有浓盐酸和浓硫酸的敞口烧杯,过段时间后,天平( )A.左端下沉B.右端下沉C.仍平衡D.无法判断【答案】B 【解析】浓盐酸具有挥发性,过一段时间后会变轻;浓硫酸具有吸水性,过一段时间后质量会增加,故右端下沉。2.中和反应在工农业生产和日常生活中有广泛的用途。下列应用一定与中和反应原理无关的是( )A.食物过咸时加食醋调和 B.服用含Al(OH)3的药物治疗胃酸过多C.施用熟石灰改良酸性土壤 D.用NaOH溶液洗涤石油产品中的残余硫酸【答案】A3.室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )
A.a点溶液中有两种溶质B.b点溶液中滴加紫色石蕊溶液,溶液变蓝C.c点烧杯内液体的pH=7D.d点溶液中有较多的Ba2+、OH-、SO、H+【答案】C 【解析】a点时,反应没有开始,溶液中有一种溶质H2SO4;b点溶液中硫酸有剩余,滴加紫色石蕊溶液,溶液变红;c点稀H2SO4与Ba(OH)2完全反应,烧杯内液体的pH=7;d点Ba(OH)2溶液过量,溶液中有Ba2+、OH-,无SO、H+。4.酸碱中和反应在工农业生产和日常生活中应用十分广泛。如图所示是氢氧化钠与稀盐酸反应的实验示意图。请据图回答下列问题:(1)写出图中有标号仪器的名称:①__________, ②__________。(2)A中溶液呈________色,C中溶液(氢氧化钠溶液稍过量)呈________色;(3)该实验反应的化学方程式为________________________________________。【答案】(1)细口瓶 烧杯 (2)无 红 (3)NaOH+HCl===NaCl+H2O
5.A~G是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤。(1)D的化学式为______________。(2)A转化为E的化学方程式为____________________________________________,其反应基本类型属于____________。(3)B转化为G的化学方程式为________________________________________,该反应在实验室中的应用是______________________。(4)写出物质F的一种用途:____________________________。【答案】(1)CaCl2 (2)Mg+2HCl===MgCl2+H2↑ 置换反应 (3)Ca(OH)2+CO2===CaCO3↓+H2O 检验二氧化碳 (4)供给呼吸(或支持燃烧等)6.为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定反应后溶液的pH,得到了如图所示的pH曲线,请回答:(1)由图可知该实验操作是将______________滴加到另一种溶液中。(2)该反应的化学方程式为__________________________________________。(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了做标记,他设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3===CaCO3↓+2NaCl。【探究过程】①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现____________________________的现象。结论:该样品是a处溶液。②为进一步确定b和c处溶液,又设计了以下方案:【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑________________________________。【答案】(1)稀盐酸(2)Ca(OH)2+2HCl===CaCl2+2H2O(3)【探究过程】①溶液由无色变成红色 ②只产生白色沉淀 气泡 白色沉淀 Ca2+、H+【反思评价】反应物是否有剩余7.某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究。【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?【查阅资料】①15℃、101kPa时,二氧化碳的溶解度如下:②15℃时,在酒精中氢氧化钠易溶,碳酸钠微溶。③通常情况下,稀溶液的体积约等于溶剂的体积。【实验设计】在15℃、101kPa时,制取二氧化碳并用于实验甲、实验乙。【分析与表达】(1)如果二氧化碳与氢氧化钠反应,化学方程式是______________________________,那么氢氧化钠应______________保存。(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。(4)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是________________________________________________________________________________。(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是________(填答案字母)。A.先慢后快 B.先快后慢 C.先慢后快,再变慢实验乙中,还可能观察到的现象是________________________________________。(5)实验乙中,120mL酒精____________(选填“能”或“不能”)换成水,原因是________________________________________________。(6)由以上探究可知,二氧化碳能溶于水,也能与氢氧化钠反应,但实验乙的数据还不够准确,造成实验乙误差的原因可能有________________________________________。(写一条)【答案】(1)2NaOH+CO2===Na2CO3+H2O 密封(2)用手紧握左边的试管,若U形管内液面出现右高左低的现象,一段时间后回落到原位置,则说明左侧试管气密性良好,同理检查右侧试管(3)右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,但右侧液面仍高于左侧(4)B 在锥形瓶中观察到白色浑浊现象(5)不能 二氧化碳在水中的溶解度大于在酒精中的溶解度(6)水分子和酒精分子的间隔不同,酒精具有挥发性8.某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表和图所示:(已知BaCl2溶液的pH=7)求:(1)完全反应后生成沉淀的质量为________。(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%) 【答案】(1)4.66g(2)解:设与H2SO4反应的Ba(OH)2质量为x。Ba(OH)2+H2SO4===BaSO4↓+2H2O 171 233 x 4.66g= x=3.42g则与H2SO4反应的Ba(OH)2溶液质量为=20g。由题意可知:与HCl完全反应的Ba(OH)2溶液的质量为60g-20g=40g。设20g该品牌洁厕灵溶液中HCl的质量为y。Ba(OH)2+2HCl===BaCl2+2H2O 171 7340g×17.1% y= y=2.92g20g该品牌洁厕灵溶液中HCl的质量分数为×100%=14.6%。答:20g该品牌洁厕灵溶液中HCl的质量分数为14.6%。考点二:常见的酸和碱与酸碱度1.下列物质的名称或俗称,指的不是同一种物质的是( )A.熟石灰 B.氢氧化钙 C.石灰石 D.消石灰【答案】C2.下列溶液中不能导电的是( )A.澄清石灰水 B.稀硫酸 C.酒精溶液 D.食盐水【答案】C3.下列做法不符合“改善环境质量,推动绿色发展”这一主题的是( )A.尽量选择公共交通工具出行 B.自带布袋购物C.废酸液直接排入下水道 D.减少使用一次性餐具【答案】C4.推理是化学学习中常用的思维方法,下列推理正确的是( )A.人的血液呈碱性,则人的体液都呈碱性B.NaCl溶液能够导电,则所有液体都能导电C.KNO3溶液无色透明,则无色透明的液体都是溶液D.酸性溶液能使石蕊变红,能使石蕊变红的溶液都是酸性溶液【答案】D5.只用石蕊试液就能将下列各组溶液区分开来的是( )A.NaCl NaOH NaNO3 B.NaOH H2SO4 KNO3C.HCl NaCl Na2SO4 D.Na2SO4 H2SO4 K2SO4【答案】B6.如图所示,分别向试管内加入下列物质之一,能使U形管右侧液面显著升高的是( )A.浓盐酸B.浓硫酸C.食盐D.石灰石【答案】B7.下列图示的实验操作,正确的是( )【答案】D8.生活中一些食物的近似pH如下,其中显碱性的食物是( )A.柠檬汁(2.0~3.0) B.苹果汁(2.9~3.3) C.牛奶 (6.3~6.6) D.鸡蛋清(7.6~8.0)【答案】D 【解析】鸡蛋清的pH为7.6~8.0,大于7,显碱性。9.小凯整理归纳得出的规律合理的是( )A.溶液中的溶剂一定是水B.水既能跟某些金属氧化物反应生成碱,也能跟某些非金属氧化物反应生成酸C.酸、碱中一定都含有氧元素D.不能使酚酞溶液变红的溶液一定是酸溶液【答案】B10.二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中,有着重要的应用。(1)二氧化碳用于制汽水,这是利用了二氧化碳____________________________的性质。(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为_____________________________________________________(用化学方程式表示)。(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有______________,利用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强________(选填“酸”或“碱”)性,能达到消毒杀菌的效果。(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为______________________________________________。【答案】(1)可与水反应生成碳酸(2)Ca(OH)2+CO2===CaCO3↓+H2O(3)氢氧化钠 酸(4)2NaCl+2H2O2NaOH+H2↑+Cl2↑
相关试卷
这是一份初中化学中考复习 2020届九年级中考化学一轮复习知识点训练卷:自然界的水,共15页。试卷主要包含了河水净化的主要步骤如下图所示,下列有关水的叙述正确的是,过滤时不需要用到的仪器是,去除粗盐中的泥沙,用化学符号表示等内容,欢迎下载使用。
这是一份初中化学中考复习 2020届九年级中考化学一轮复习知识点训练卷:盐、肥料、化学与生活,共12页。试卷主要包含了下列说法正确的是,下列实验能达到相应目的的是,写出符合下列要求的物质的化学式等内容,欢迎下载使用。
这是一份初中化学中考复习 2020届九年级中考化学一轮复习知识点训练卷:溶液,共12页。试卷主要包含了硝酸钾的溶解度随温度升高而增大,认真分析下列各图,回答相关问题等内容,欢迎下载使用。









