








所属成套资源:鲁教版化学九年级下册 全册课件PPT+教案+练习+素材(含答案)
鲁教版九年级下册第一节 酸及其性质教课内容ppt课件
展开
这是一份鲁教版九年级下册第一节 酸及其性质教课内容ppt课件,文件包含第七单元第一节酸及其性质第二课时pptx、第七单元第一节酸及其性质第二课时教案doc、第七单元第一节酸及其性质第二课时当堂检测doc等3份课件配套教学资源,其中PPT共17页, 欢迎下载使用。
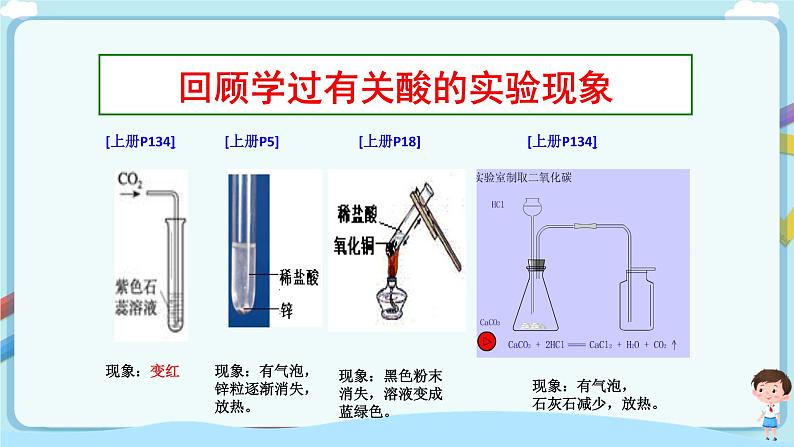
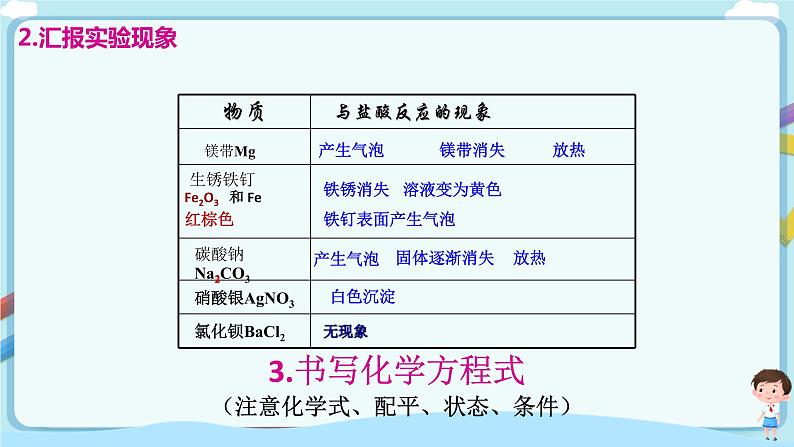
第七单元 第一节 酸及其性质(第二课时)【教学目标】1、通过探究盐酸和硫酸的性质与变化,了解酸的通性,认识酸的通性实质就是氢离子的性质。2、通过实验探究盐酸的化学性质,增进对科学探究的理解,发展科学探究精神。通过观察、实验等方法收集信息。3、通过学习酸与某些化合物的反应,能从形式上认识复分解反应的特点。【教学重点】1、酸的通性;2、化学方程式的书写。【教学难点】化学方程式的书写。【教学过程】一、导入新课在整理实验室的药品时发现有两瓶无色液体的标签模糊不清,但可以肯定的是它们是蒸馏水和稀盐酸,你能通过实验方法帮助老师确定它们的身份吗?带着这个问题,我们走进今天的学习---酸的化学性质。二、明确目标生读,明确重难点三、探究新知【过渡】回顾有关酸的现象1、二氧化碳的水溶液滴加紫色石蕊试液;2、锌粒和稀盐酸反应;3、氧化铜和稀盐酸混合;4、实验室中制取二氧化碳。【合作探究一】1、分组实验完成教材P3实验探究7—1: 明确要求:准确操作,保障安全。(1)组内分工合作:做实验,记录现象,交流汇报。(2)正确取用药品:①顺序:先固后液。②固体药品:粉末状用药匙和纸槽; 颗粒状和块状用镊子。 ③液体药品:量多—倾倒;量少—滴加(胶头滴管:先挤后吸,竖直悬空) ④ 按量取用,不要浪费。(3)观察记录现象:有无颜色变化;固体物质减少;气泡,沉淀;能量变化。(4)实验后把废物放在废液杯,注意环保。2、汇报实验现象(1)盐酸与指示剂作用使紫色石蕊试液_____ 使无色酚酞试液______2、盐酸与金属、金属氧化物、某些盐的反应物质 与盐酸反应的现象镁带Mg 生锈铁钉Fe2O3 和 Fe 碳酸钠Na2CO3 硝酸银AgNO3 氯化钡BaCl2 3.书写化学方程式(注意化学式、配平、状态、条件)【师点拨】一般情况下:含Fe3+的溶液:____色;含Fe2+的溶液:________色;含Cu2+的溶液:________色:【合作探究二】认识复分解反应(阅读教材P4,1分钟)小结:1、定义;2、通式 ;3、特点:交换成分价不变【学以致用】根据复分解反应的特点判断下列反应是否属于复分解反应?说明理由?A.NaOH +HCl==NaCl+H2O B.CO2+ Ca(OH)2===CaCO3↓+H2O C.CaCO3+2HCl==CaCl2+H2O+CO2↑ 【合作探究三】认识什么是盐? (阅读教材P4,1分钟)生总结并举例【学以致用】下列不属于盐的物质是( ) A.CuSO4 B.NaCl C.HNO3 D.CaCO3【活动天地】用稀硫酸代替稀盐酸与镁条、碳酸钠粉末和生锈的铁钉反应,你会观察到哪些现象?生总结并书写化学方程式【我会演绎】通过稀盐酸和稀硫酸化学性质,总结酸的通性及原因?(1)能使紫色石蕊试液变红;无色酚酞试液不变色(2)能与某些金属氧化物反应,生成盐和水;Fe2O3+3H2SO4 =Fe2(SO4)3 + 3H2O CuO+H2SO4= CuSO4+H2O(3)能与某些金属反应,生成盐和氢气;Zn+H2SO4=ZnSO4+H2↑ Mg+H2SO4=MgSO4+H2↑ (4)能与部分盐反应,生成新的酸和新的盐。BaCl2+H2SO4=BaSO4↓+2HClAgNO3+HCl=AgCl↓+HNO3 当然,由于不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。BaCl2+H2SO4=BaSO4↓+2HClBaCl2+HCl 不反应【回扣问题】通过本节课学习,能否解决一开始问题,如何区分蒸馏水和稀盐酸?四、当堂检测1.下列物质放入到稀硫酸中,无气体生成的是( C )A.铝 B.碳酸钠 C.铁锈 D.石灰石2.盐酸和稀硫酸常用作金属表面的清洁剂,是利用了它们化学性质中的( B )A.能与金属反应 B.能与金属氧化物反应C.能使指示剂变色 D.能溶于水3.下列物质可由金属与酸发生置换反应得到的是( C )A.CuCl2 B.Fe2(SO4)3 C.ZnCl2 D.AgCl 4.柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈现酸性,主要用于香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( C )A.Mg B.Fe2O3 C.CO2 D.CuO5.酸类物质具有相似的化学性质,本质的原因是( C )A.酸都含有酸根 B.酸都能与指示剂作用C.酸在水溶液中都能解离出H+D.酸是由多种元素组成的五、课堂小结生总结收获
相关课件
这是一份初中化学鲁教版九年级下册第一节 酸及其性质教学ppt课件,文件包含第七单元第一节酸及其性质第一课时pptx、第七单元第一节酸及其性质第一课时当堂检测doc、第七单元第一节酸及其性质第一课时教学设计doc、浓硫酸的稀释mp4、浓硫酸稀释的错误操作mp4、盐酸硫酸的物理性质mp4等6份课件配套教学资源,其中PPT共11页, 欢迎下载使用。
这是一份初中化学鲁教版九年级下册第一节 酸及其性质课堂教学ppt课件,共40页。PPT课件主要包含了生活中有酸味的物质,认识浓盐酸和浓硫酸,浓盐酸,浓硫酸,浓硫酸具有吸水性,猜一猜,浓硫酸具有脱水性,木棍变黑,什么是酸,酸的化学性质等内容,欢迎下载使用。
这是一份初中化学鲁教版九年级下册第一节 酸及其性质教案配套课件ppt,共32页。PPT课件主要包含了H+和酸根离子,酸的定义,浓硫酸的特性,浓硫酸的稀释等内容,欢迎下载使用。










