



初中化学中考复习 14专题十四 物质的检验与提纯 课件 2021年中考化学(全国)一轮复习
展开A组 2020年全国中考题组
考点一 物质的检验和鉴别
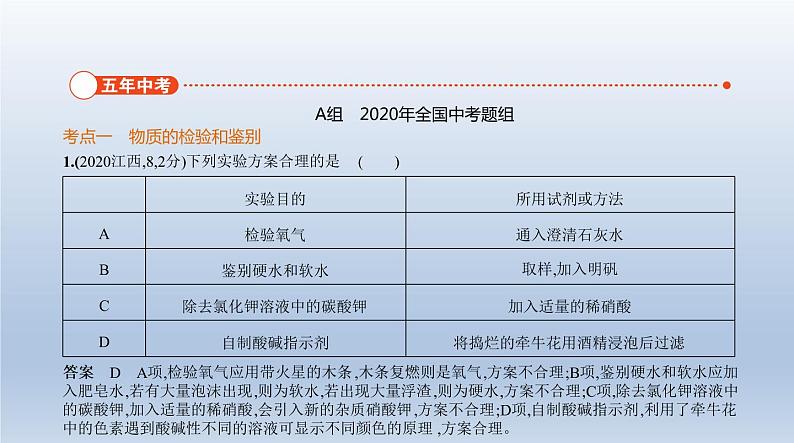
1.(2020江西,8,2分)下列实验方案合理的是 ( )
答案 D A项,检验氧气应用带火星的木条,木条复燃则是氧气,方案不合理;B项,鉴别硬水和软水应加 入肥皂水,若有大量泡沫出现,则为软水,若出现大量浮渣,则为硬水,方案不合理;C项,除去氯化钾溶液中 的碳酸钾,加入适量的稀硝酸,会引入新的杂质硝酸钾,方案不合理;D项,自制酸碱指示剂,利用了牵牛花 中的色素遇到酸碱性不同的溶液可显示不同颜色的原理,方案合理。
2.(2020湖南长沙,13,3分)鉴别是利用物质的性质不同,采用合理的方法进行区分。下列鉴别物质的方法 正确的是 ( )A.用水鉴别NaCl、 NaOH、 NH4NO3三种固体B.用燃着的木条鉴别O2、CO2、N2三种气体C.用Ba(OH)2溶液鉴别KCl、K2SO4、KNO3三种溶液D.用CO2鉴别NaOH、KOH、Ca(OH)2三种溶液
答案 A A项,分别取三种适量固体于三支试管中,加入等量的水溶解,试管外壁发热的是氢氧化钠,试 管外壁变冷的是硝酸铵,温度无明显变化的是氯化钠,正确;B项,二氧化碳和氮气都不能燃烧,也不支持燃 烧,它们都会使木条火焰熄灭,无法鉴别;C项,氢氧化钡与氯化钾、硝酸钾都不反应,无法鉴别;D项,二氧 化碳与氢氧化钠、氢氧化钾反应都无明显现象,无法鉴别。
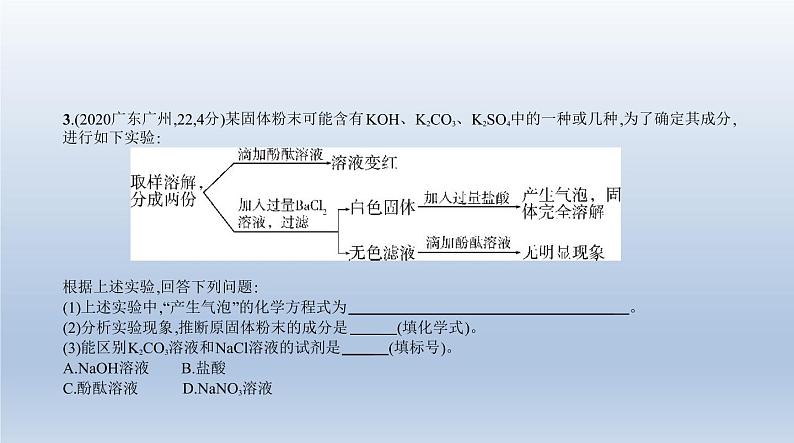
3.(2020广东广州,22,4分)某固体粉末可能含有KOH、K2CO3、K2SO4中的一种或几种,为了确定其成分, 进行如下实验: 根据上述实验,回答下列问题:(1)上述实验中,“产生气泡”的化学方程式为 。(2)分析实验现象,推断原固体粉末的成分是 (填化学式)。(3)能区别K2CO3溶液和NaCl溶液的试剂是 (填标号)。A.NaOH溶液 B.盐酸C.酚酞溶液 D.NaNO3溶液
答案 (1)BaCO3+2HCl BaCl2+H2O+CO2↑(2)K2CO3 (3)BC
解析 (1)往溶液中加入过量BaCl2后,产生的白色固体完全溶解于盐酸,说明白色固体为BaCO3。(2)因白 色固体仅含BaCO3,故原固体粉末中含有K2CO3,不含K2SO4;K2CO3与过量BaCl2反应,生成BaCO3沉淀和 KCl。BaCl2和KCl溶液均呈中性。过滤后,往滤液中滴加酚酞溶液,无明显现象,说明滤液不呈碱性,即原 固体粉末中不含KOH,故原固体粉末仅含K2CO3。(3)NaOH溶液与K2CO3溶液和NaCl溶液均不能反应;盐 酸能与K2CO3反应生成CO2气体,不能与NaCl反应;K2CO3溶液呈碱性,能使酚酞溶液变红,NaCl溶液呈中 性,不能使酚酞溶液变色;NaNO3溶液与K2CO3溶液和NaCl溶液均不能反应。故选BC。
误区警示 KOH、K2CO3溶液均呈碱性,均能使无色酚酞溶液变红。
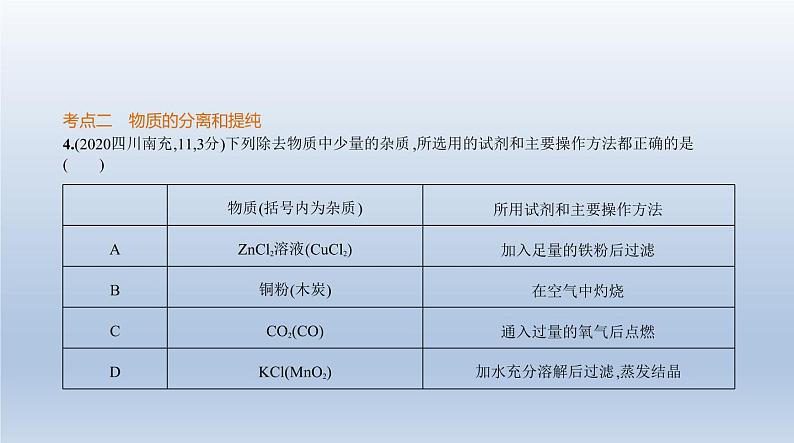
4.(2020四川南充,11,3分)下列除去物质中少量的杂质,所选用的试剂和主要操作方法都正确的是 ( )
考点二 物质的分离和提纯
答案 D A项,加入足量的铁粉后,会生成新的杂质氯化亚铁,错误;B项,除去铜粉中的木炭,在空气中灼 烧,铜粉也能与空气中的氧气反应生成氧化铜,错误;C项,除去CO2中混有的少量CO,通入过量的氧气,CO 无法点燃,故不能除去,错误;D项,MnO2不溶于水,KCl易溶于水,加水充分溶解后过滤,将滤液蒸发结晶可 得纯净的KCl,正确。
规律总结 除杂问题的关键是首先选择合适的除杂试剂或方法,反应条件或除杂过程要尽可能的简 单、易于实现,尤其是要注意除杂过程中不得引入新的杂质。若引入新的杂质,杂质必须能通过简单方 法除去(例如水通过加热蒸发即可除去)。还要注意除杂问题与分离问题的区别,两者的处理方法类似, 但除杂要求得到纯净的原物质即可,而分离要求得到原混合物中的各个组分。
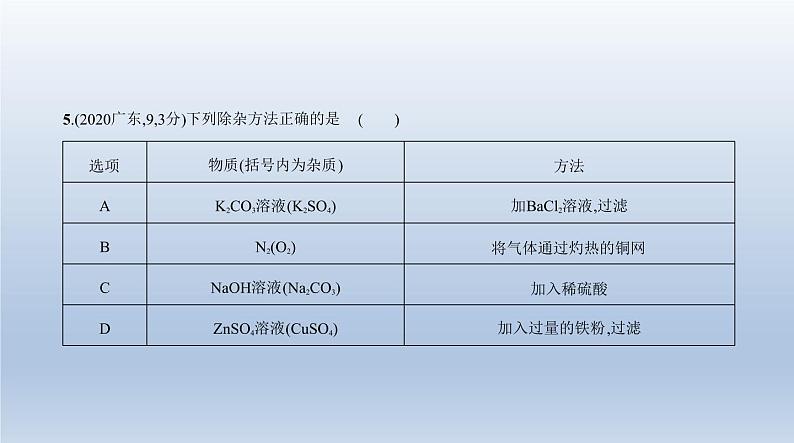
5.(2020广东,9,3分)下列除杂方法正确的是 ( )
答案 B A项,加入BaCl2溶液,能和硫酸钾反应,但会生成新的杂质氯化钾,且BaCl2也能和碳酸钾反应, 错误;B项,氧气会与灼热的铜网反应生成氧化铜,氮气不反应,正确;C项,稀硫酸不仅和杂质碳酸钠反应, 也能与氢氧化钠反应,同时引入新杂质Na2SO4,错误;D项,加入过量的铁粉后,铁与杂质硫酸铜反应,生成 新的杂质硫酸亚铁,错误。
解题关键 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的原则(加入的试 剂一般只与杂质反应,反应后不能引入新的杂质)是正确解题的关键。
6.(2020新疆,10,2分)下列实验操作不能达到实验目的的是(括号内为杂质) ( )
答案 C A项,取样,加入熟石灰粉末、研磨,能够产生刺激性气味的是氯化铵,无明显现象的是尿素,能 够达到实验目的;B项,取样,加水溶解,滴加BaCl2溶液,能够产生白色沉淀的是硫酸钠,因为硫酸钠能和氯 化钡反应生成硫酸钡沉淀和氯化钠,能够达到实验目的;C项,稀盐酸和碳酸钠、碳酸氢钠都反应,不能达 到实验目的;D项,稀硫酸和氢氧化钾反应生成硫酸钾和水,溶液pH=7时恰好完全反应,除去了氢氧化钾, 能够达到实验目的。故选C。
B组 2016—2019年全国中考题组
1.(2019湖南衡阳,15,2分)下列鉴别物质所用的方法或试剂中,错误的是 ( )A.水和白醋——观察颜色B.氯化钾和氯化铵——氢氧化钠C.合成纤维和羊毛纤维——点燃闻气味D.一氧化碳和二氧化碳——灼热的氧化铜
答案 A 水和白醋都是无色的,通过观察颜色不能鉴别,故A错误;氯化钾和氯化铵中加入氢氧化钠,有 刺激性气味气体产生的是氯化铵,无明显现象的是氯化钾,故B正确;合成纤维和羊毛纤维在点燃后,能闻 到烧焦羽毛味的是羊毛纤维,另一种是合成纤维,故C正确;一氧化碳和二氧化碳分别通过灼热的氧化铜, 能看到黑色固体变红的是一氧化碳,无明显现象的是二氧化碳,故D正确。
2.(2018新疆,9,2分)采用下列实验方法鉴别物质不能达到目的的是 ( )A.白酒和矿泉水——闻气味B.黄铜和铜——相互刻画C.纯碱和小苏打——加稀盐酸D.硝酸铵和尿素——加熟石灰研磨闻气味
答案 C 白酒有酒香味,矿泉水无特殊气味,通过闻气味可以鉴别二者,A能达到目的。合金的硬度一 般大于组成它的纯金属的硬度,黄铜和铜相互刻画,留下明显划痕的是铜,B能达到目的。纯碱和小苏打 均能与稀盐酸反应生成二氧化碳气体,二者现象相同,不能鉴别,C不能达到目的。硝酸铵加熟石灰研磨 会产生有刺激性气味的气体,尿素与熟石灰不反应,现象不同,可以鉴别,D能达到目的。
3.(2019福建,8,3分)下列实验操作不能达到实验目的的是 ( )
答案 D 灼烧蚕丝与棉线,能闻到烧焦羽毛气味的是蚕丝,能闻到烧纸气味的是棉线,A正确;滴加酚酞 溶液,变红的是氢氧化钠溶液,不变色的是硫酸溶液,B正确;加肥皂水振荡,浮渣较多、泡沫较少的是硬 水,泡沫较多的是软水,C正确;将20 g浓盐酸加入80 g水中得到的稀盐酸的溶质质量分数小于20%,因为20 g浓盐酸中含有溶质氯化氢的质量达不到20 g,D错误。
易错警示 不能将20 g浓盐酸当成纯净物,应按浓盐酸中溶质氯化氢的质量来计算。
4.(2019吉林,10,1分)下列实验方案设计不能达到实验目的的是 ( )A.用Ba(OH)2溶液除去NaNO3溶液中的CuSO4B.用Na2CO3溶液鉴别NaOH溶液和CaCl2溶液C.用稀H2SO4、Fe2O3和NaOH溶液制备Fe(OH)3D.用酚酞溶液检验CaO中是否含有Ca(OH)2
答案 D A项,氢氧化钡与硫酸铜反应生成两种沉淀,能达到目的;B项,碳酸钠与氯化钙反应生成沉淀, 与氢氧化钠不反应,能达到目的;C项,氧化铁与硫酸反应生成硫酸铁,硫酸铁与氢氧化钠反应即可得到氢 氧化铁沉淀,能达到目的;D项,氧化钙与酚酞溶液中的水反应生成氢氧化钙,故无法用酚酞溶液检验氧化 钙中是否含有氢氧化钙,不能达到目的。
5.(2018四川成都,12,3分)下列各组物质的鉴别方法与结论均正确的是 ( )
答案 B 黄铜是铜锌合金,硬度大于纯铜,相互刻画,铜片上留下痕迹,A错误;高锰酸钾受热分解能生成 氧气,使带火星木条复燃,二氧化锰受热不分解,B正确;氯化钠溶于水温度基本不变,硝酸铵溶于水温度降 低,试管外壁有水雾,C错误;稀盐酸与稀硫酸的浓度未知,无法用pH的大小来鉴别二者,D错误。
6.(2017黑龙江哈尔滨,12,2分)区分下列各组物质的两种方法都正确的是 ( )
答案 B 硬水蒸干有固体存在,软水蒸干也可能有固体存在,所以用蒸干的方法无法区分软水与硬水, A错误。磷矿粉是灰白色固体,碳铵是白色晶体,观察颜色可以区分;磷矿粉没有气味,碳铵有氨味,通过闻 气味可以区分,B正确。呼出气体与空气中伸入带火星的木条都无明显变化,无法区分,C错误。棉线与 尼龙线通过观察颜色无法区分,D错误。
7.(2018陕西A,20,5分)现有一包白色粉末,可能由氯化钾、氢氧化钠、硝酸钠和硫酸铜中的一种或多种 物质组成。为确定其成分,某兴趣小组同学进行了如下探究。(1)甲同学通过观察颜色,认为该粉末中不含硫酸铜,他是根据物质的 性质得出该结论的。乙同 学认为甲同学的方法不能确定该粉末中不含硫酸铜。(2)他们设计并进行了如下实验。(已知Ag2SO4微溶于水) ①写出生成蓝色沉淀的化学方程式 。②通过以上实验,不能确定白色粉末中是否含有 。③加入过量Ba(NO3)2溶液和稀硝酸的目的是 。
答案 (1)物理(2)①2NaOH+CuSO4 Cu(OH)2↓+Na2SO4(未配平或无“↓”符号扣1分,化学式错误扣2分)②NaNO3或硝酸钠③排除S 的干扰或排除S 和OH-的干扰(合理答案即可)
解析 (1)固体的颜色属于物理性质。(2)①白色固体中加入足量的水后,出现蓝色沉淀,因此固体中肯定存在氢氧化钠和硫酸铜,其反应的化学 方程式为2NaOH+CuSO4 Cu(OH)2↓+Na2SO4。②通过题给实验可以判断出白色粉末中一定存在氢氧化钠、硫酸铜、氯化钾,不能确定的是硝酸钠。③加入过量的硝酸钡溶液和稀硝酸的目的是除去溶液中的S 和OH-,防止它们影响Cl-的检验。
8.(2017黑龙江哈尔滨,34,6分)在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种, 进行如下实验: 观察到烧杯中的现象是(1) 。【提出问题】A是哪一种酸?老师要求甲、乙同学从反应后的溶液B分别展开探究。【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸。【实验探究】
【评价交流】甲同学的实验(2) (填“能”或“不能”)得出正确结论,乙同学的实验(3) (填 “能”或“不能”)得出正确结论。实验3发生反应的化学方程式为(4) ,反应后所得溶液中一定含有的离子是(5) 。【归纳总结】通过乙同学的实验可以得出:选择试剂鉴别溶液中的待测离子时,如果待测溶液中含有干 扰离子,则应在鉴别前,先另选试剂将干扰离子变成(6) 除去。经讨论我们能够总结出,除去溶 液中干扰离子的一般方法是:选择试剂将干扰离子变成(7) 除去。
答案 (6分)(1)(溶液中)有气泡冒出(1分)(合理即可)(2)不能(1分)(3)能(1分)(4)Na2SO4+BaCl2 2NaCl+BaSO4 ↓(1分)(5)Na+、Cl-、N (1分)(6)气体(0.5分)(合理即可)(7)沉淀或气体或水(0.5分)(合理即可)
解析 稀盐酸、稀硫酸分别与碳酸钠反应都有二氧化碳生成,故现象为有气泡冒出。【评价交流】由 乙同学的实验2可知溶液B中有剩余的碳酸钠,碳酸钠与硝酸银反应也产生白色沉淀,故甲同学不能得出 正确结论。在溶液B中加入适量的稀硝酸有气泡冒出,说明碳酸钠过量;加入氯化钡溶液产生白色沉淀, 说明溶液中含有硫酸根离子,可以得出A是稀硫酸,故乙同学能得出正确结论。实验3发生反应的化学方 程式为Na2SO4+BaCl2 BaSO4 ↓+2NaCl;反应后所得溶液中一定有硝酸钠、氯化钠,故一定含有的离子是Na+、Cl-、N 。
9.(2019湖南长沙,15,3分)下列除去杂质所选用的试剂正确的是 ( )
答案 A 氮气中含有少量氧气杂质,可用灼热的铜网,利用铜与杂质氧气反应生成氧化铜,除去氧气,故 A正确;氧化钙中含有少量氢氧化钙杂质,若加水,则氧化钙会与水反应生成氢氧化钙,达不到除杂目的,故 B错误;氯化钠溶液中含有少量硫酸钠杂质,若加入硝酸钡溶液,硫酸钠与硝酸钡反应生成硫酸钡白色沉 淀和硝酸钠,硝酸钠会成为新的杂质,故C错误;硫酸亚铁溶液中含有少量硫酸铜杂质,若加入锌粉,硫酸亚 铁和硫酸铜都会与锌粉反应,达不到除杂目的,故D错误。
10.(2019山东潍坊,16,2分)除去下列物质中的少量杂质,所选试剂及操作方法都正确的是 ( )
答案 A 稀盐酸和氧化铜反应,和铜不反应,过滤、洗涤、干燥得到铜,故A正确;少量一氧化碳和二氧 化碳混合在一起时,一氧化碳不能被点燃,故B错误;氢氧化钡虽然能和硫酸钠反应,但是会引入新的杂质 氢氧化钠,故C错误;二氧化锰不溶于水,氯酸钾溶于水,溶解、过滤、洗涤、干燥得到二氧化锰,故D错误。
11.(2019广东广州,19,2分)除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是 ( )A.Zn粉(Fe):用ZnCl2溶液浸泡,过滤B.碳粉(MnO2):滴入H2O2溶液,过滤C.NaCl溶液(Na2SO4):加入适量MgCl2溶液,过滤D.CO2(H2O):通过盛有浓硫酸的洗气瓶
答案 D Fe的金属活动性排在Zn后,不能与ZnCl2溶液反应,故A错误;MnO2能促进H2O2分解,但本身的 质量和化学性质不变,无法除去,故B错误;Na2SO4与MgCl2不反应,故C错误;浓硫酸能吸收CO2气体中混有 的水蒸气,故D正确。
12.(2017山西,9,2分)提纯是化学实验常用的一种方法。除去下表混合物中的杂质,所选除杂试剂错误的 是 ( )
答案 B A项,加入的适量氢氧化钙溶液与杂质Na2CO3反应生成碳酸钙沉淀和氢氧化钠,可以除去杂 质,且不引入新杂质,正确。B项,加入的蒸馏水会与CaO粉末反应,错误。C项,稀硫酸可与杂质Fe反应,且 足量稀硫酸可以将Fe完全消耗,而Cu粉不与稀硫酸反应,可以除去杂质,正确。D项,加入足量的氧化铜粉 末可以将杂质H2SO4完全消耗,且生成物为CuSO4,可以除去杂质且不引入新杂质,正确。
13.(2016天津,13,2分)下列除杂方法(括号内为杂质)中正确的是(双选) ( )A.二氧化碳(一氧化碳):通入氧气,点燃B.硝酸铜溶液(硝酸银):加入足量的铜粉,过滤C.碳酸钙固体(氯化钙):加入足量的水溶解,过滤、洗涤、干燥D.氢氧化钠溶液(碳酸钠):加入适量的稀盐酸至不再产生气泡
答案 BC 除去二氧化碳中的一氧化碳的正确方法是将气体通过灼热的氧化铜,A项错误;足量的铜粉 能与AgNO3溶液反应生成硝酸铜溶液和银,然后过滤,能除去杂质且没有引入新的杂质,B项正确;氯化钙 易溶于水,碳酸钙固体难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,C项正确;氢 氧化钠和碳酸钠均能与稀盐酸反应,不但能把杂质除去,也会把氢氧化钠除去,D项错误。
易错警示 当二氧化碳含量高时,二氧化碳中的一氧化碳不能通过点燃的方法除去。
14.(2019福建,13,7分)用下图所示装置模拟废液(含CuSO4、MgSO4及一些不溶物)净化实验,步骤如下: Ⅰ.往沉降槽中加入适量絮凝剂(混凝剂)甲,加速沉降;Ⅱ.往反应槽中缓慢加入一定浓度的NaOH溶液,至沉淀完全;Ⅲ.通过盛装有活性炭的水槽后,调节溶液的pH=7,储存在指定容器中。(1)测得原废液pH=5,显 (填“酸性”“碱性”或“中性”)。(2)甲是 (写物质名称);操作X可使固体与液体分离,操作X是 ;活性炭的作用是 。(3)反应槽中生成沉淀的化学方程式为 (写一个)。
答案 (7分)(1)酸性(2)明矾(或其他合理答案) 过滤 吸附(3)CuSO4+2NaOH Na2SO4+Cu(OH)2↓[或MgSO4+2NaOH Na2SO4+Mg(OH)2↓]
解析 (1)原废液的pH<7,显酸性。(2)往沉降槽中加入的是絮凝剂,所以甲可以是明矾等物质;能使固体 和液体分离的操作是过滤;活性炭起吸附作用。(3)废液中含硫酸铜、硫酸镁,反应槽中加入氢氧化钠后 会生成氢氧化铜和氢氧化镁沉淀,有关化学方程式为CuSO4+2NaOH Na2SO4+Cu(OH)2↓、MgSO4+2NaOH Na2SO4+Mg(OH)2↓。
1.(2020天津,13,2分)下列实验方案设计正确的是(双选) ( )A.鉴别氮气和二氧化碳,将气体分别通入紫色石蕊溶液中,观察现象B.除去氯化钙溶液中混有的氢氧化钙,加入过量稀盐酸C.检验木炭粉中是否含有氧化铜,取少量样品滴加稀硫酸,观察现象D.从饱和石灰水中得到氢氧化钙固体,采用降低温度的方法
答案 AC A项,将气体分别通入紫色石蕊溶液中,二氧化碳与水反应生成的碳酸可使紫色石蕊溶液变 红,氮气与水不反应,无明显现象,方案可行;B项,加入的稀盐酸过量,除去Ca(OH)2的同时引入新杂质;C项, 滴加稀硫酸,若部分固体溶解,溶液变为蓝色,则含有氧化铜,若固体不溶解,溶液不变为蓝色,则不含有氧 化铜,方案可行;D项,氢氧化钙的溶解度随温度的升高而减小,从饱和石灰水中得到氢氧化钙固体,应采用 升高温度的方法。故选A、C。
方法技巧 除杂的原则是除去杂质且不能引入新杂质,可以采用物理方法,也可以采用化学方法。利用 物质的特性进行检验;利用物质间反应时产生的不同的现象进行鉴别。
2.(2019河北,6,2分)下列实验操作可以达到实验目的的是 ( )
答案 A 木炭与稀硫酸不反应,氧化铜与稀硫酸反应生成硫酸铜溶液,溶液变成蓝色,A符合题意;高锰 酸钾受热分解生成的固体是锰酸钾和二氧化锰的混合物,不能达到除杂目的,B错误;氧气的验满方法是 把带火星的小木条放在集气瓶口,C错误;向氯化钙和碳酸钙的混合物中加入足量水溶解、过滤、再蒸 发滤液才能达到分离目的,D错误。
3.(2019河南,12,1分)下列区分物质的方法或试剂不正确的是 ( )A.用灼烧法区分腈纶线、羊毛线B.用肥皂水区分硬水、软水C.用熟石灰区分氯化铵、硫酸铵D.用水区分硝酸铵、氢氧化钠
答案 C 灼烧后有烧焦羽毛气味的是羊毛线,没有的是腈纶线,可以区分;将肥皂水加入水中,泡沫多、 浮渣少的是软水,反之是硬水,可以区分;氯化铵、硫酸铵中都含有铵根离子,与熟石灰研磨均有氨味产 生,不能区分;硝酸铵溶于水时溶液温度降低,氢氧化钠溶于水时溶液温度升高,用水可以区分。
4.(2018云南,19,3分)下列实验不可行或不能达到实验目的的是 ( )
答案 D 氯化钠溶液是无色的,而氯化铁溶液是黄色的,观察溶液的颜色可以区分氯化钠溶液和氯化 铁溶液,故A正确。去除粗盐中难溶性杂质,加水溶解、过滤之后难溶物留在滤纸上,然后蒸发滤液得到 精盐,故B正确。甲烷燃烧后的产物是水和二氧化碳;一氧化碳燃烧后的产物只有二氧化碳;氢气燃烧后 的产物只有水,检验燃烧产物可以区分三种气体,故C正确。硝酸铵和氯化铵分别与固体氢氧化钙混合, 研磨时都会有氨气放出,所以无法区分硝酸铵与氯化铵,故D错误。
知识拓展 物质鉴别的常用方法(1)观察法:利用物质的颜色等不同鉴别。如硫酸铜溶液显蓝色,氯化铁溶液显黄色。(2)溶解法:利用物质的溶解性不同鉴别。如碳酸钠溶于水,碳酸钙难溶于水。(3)燃烧法:把需要鉴别的物质分别点燃,通过燃烧时的现象或产物的不同进行鉴别。(4)蒸发法:通常在鉴别食盐水(或海水)和水(或盐酸)时可用蒸发法。(5)滴加试剂法:滴加化学试剂是实验室中常用的鉴别物质的方法,在初中化学中,滴加的试剂有酸碱指示 剂,某些酸、碱、盐的溶液等。
5.(2017重庆A,12,2分)实验方法多种多样。下列方法不能达到目的的是 ( )A.用灼热的CuO区别CO和CO2B.用石灰石和稀盐酸制取CO2C.用AgNO3溶液鉴别食盐水和稀盐酸D.用带火星的木条对氧气验满
答案 C A项,一氧化碳能与灼热的氧化铜反应,黑色粉末逐渐变成红色,而二氧化碳不和氧化铜反应, 故可以区别;B项,石灰石和稀盐酸反应可生成二氧化碳,反应速率适中,可以制取二氧化碳;C项,食盐水和 稀盐酸与硝酸银反应均可产生白色沉淀,故不能达到鉴别目的;D项,氧气具有助燃性,可用带火星的木条 检验氧气是否收集满,能达到目的。
6.(2016天津,12,2分)下表中各组物质的鉴别方法正确的是(双选) ( )
答案 AD A项,取样品,滴入紫色石蕊溶液,溶液变红色的是稀盐酸,颜色不变的是氯化钠溶液,变蓝色 的是氢氧化钠溶液,可以鉴别;B项,硫酸钡、碳酸钙都难溶于水,用加水的方法不能鉴别;C项,氮气和二氧 化碳都使燃着的木条熄灭,不能鉴别;D项,铁和稀硫酸反应会生成氢气,溶液由无色变为浅绿色,木炭粉不 与稀硫酸反应,氧化铜和稀硫酸反应可观察到黑色粉末逐渐溶解,溶液由无色变为蓝色,可以鉴别。
7.(2020广西北部湾经济区,19,2分)下列实验方法能达到实验目的的是 ( )
答案 D A项,碳粉和四氧化三铁粉末都是黑色的,无法通过观察颜色鉴别;B项,生石灰和碳酸钙都能 与稀盐酸反应,不能达到除杂的目的;C项,加入适量的NaOH溶液,CuCl2与NaOH反应生成Cu(OH)2沉淀和 NaCl,过滤得到Cu(OH)2和NaCl溶液,不能达到分离的目的;D项,KCl与AgNO3反应生成AgCl沉淀和KNO3, 过滤除去AgCl,能达到实验目的,故选D。
易错警示 易错选C,用适量的氢氧化钠溶液可以除去NaCl中的CuCl2,但不能达到分离NaCl和CuCl2的 目的。
8.(2019江苏苏州,22,2分)除去下列物质中混有的少量杂质,所选用的试剂及操作方法正确的是 ( )
答案 B A项,生石灰能与水反应生成氢氧化钙,氢氧化钙能与二氧化碳反应,不但能把杂质除去,也会 把原物质除去,错误。B项,KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离 除杂,正确。C项,Fe粉能与稀硫酸反应生成硫酸亚铁和氢气,铜不与稀硫酸反应,反而会把原物质除去,错 误。D项,MgCl2与过量的NaOH溶液反应生成氢氧化镁沉淀和氯化钠,能除去杂质,但也引入了新的杂质 氢氧化钠,错误。
9.(2019湖南衡阳,20,2分)除去下列物质中的少量杂质,所选用的试剂及操作方法正确的是 ( )
答案 D 二氧化锰和碳粉都不溶于水,用加水后过滤的方法不能除杂,故A错误;除去二氧化碳中含有 的少量氯化氢杂质,用氢氧化钠溶液洗气时,不仅杂质氯化氢与氢氧化钠反应,二氧化碳也会与氢氧化钠 反应,故B错误;除去氯化钾溶液中含有的少量碳酸钾杂质,滴加稀硫酸后,碳酸钾与稀硫酸反应生成硫酸 钾、水和二氧化碳,其中硫酸钾会成为新杂质,故C错误;除去硫酸铜溶液中含有的少量硫酸,加入过量氧 化铜,氧化铜与硫酸反应生成硫酸铜和水,再过滤除去多余的氧化铜固体,得到的滤液就是硫酸铜溶液,故 D正确。
10.(2019广东,11,2分)除去下列物质中的杂质,所选方法正确的是 ( )
答案 D MnO2不溶于水,KCl易溶于水,混合物加水后,杂质KCl溶解,过滤后,得到MnO2固体,洗涤、烘 干固体即可,无需蒸发,故A错误;稀硫酸与Na2CO3反应生成新的杂质Na2SO4,不符合除杂原则,故B错误;氢 氧化钠能与CO2反应而不能与杂质CO反应,故C错误;CuO能与稀硫酸反应生成硫酸铜和水,而碳(C)不能 与稀硫酸反应,过滤后洗涤、干燥即可得到碳(C),故D正确。
易错警示 容易只看到除杂试剂而忽略除杂方法,而误选A。
解题关键 B项,除杂时不能引入新的杂质,否则无法得到纯净的NaCl。
11.(2018内蒙古包头,4,2分)下列有关叙述正确的是 ( )A.分离Zn和Fe的固体混合物,加适量的FeSO4溶液后过滤B.除去CO2气体中混有的HCl气体,依次通过足量的NaOH溶液和浓硫酸C.配制50 g质量分数为6%的NaOH溶液,将NaOH固体放到纸上称量,再用50 mL量筒量取水D.鉴别NaOH溶液、Ca(OH)2溶液和稀硫酸,可用一种试剂一次鉴别
答案 D 锌和硫酸亚铁溶液反应生成铁和硫酸锌,反应后得不到锌,A错误;氢氧化钠与二氧化碳能反 应,B错误;氢氧化钠易潮解且具有强腐蚀性,不能放在纸上称量,应放在玻璃容器中称量,C错误;碳酸钠与 氢氧化钙反应生成碳酸钙白色沉淀,与稀硫酸反应生成二氧化碳气体,与氢氧化钠不反应,产生三种明显 不同的现象,可以鉴别,D正确。
方法技巧 分离是将物质分开,最终要得到原来的物质。除杂是将杂质除去,只得到原混合物中的主要 物质。选择除杂试剂时,要看除杂试剂是否只与杂质反应,不与主要物质反应,且反应后不能产生新的杂 质。鉴别不同物质时,要看所用试剂与待鉴别物质混合后能否产生明显不同的现象。
12.(2017黑龙江哈尔滨,14,2分)除去下列物质中的少量杂质,所用试剂和操作方法都正确的是 ( )
答案 C 蜡烛在含有少量氧气的氮气中不能燃烧,故A错误;氧化钙与水反应生成氢氧化钙,碳酸钙难 溶于水,加足量水溶解、过滤、洗涤、干燥可除去杂质,故B错误;氯化镁与适量的氢氧化钠溶液反应生 成氯化钠和氢氧化镁沉淀,过滤除去氢氧化镁,故C正确;K2CO3与适量稀硫酸反应生成硫酸钾、二氧化 碳和水,碳酸钾被除去,故D错误。
13.(2016新疆乌鲁木齐,9,2分)除去下列各物质中混有的少量杂质,所用试剂、方法正确的是 ( )
答案 A 向硝酸铜和硝酸银的混合溶液中加入过量的铜粉,铜与硝酸银发生置换反应,生成硝酸铜和 银,过滤后可得到硝酸铜溶液,A正确;B项,稀盐酸会与铁发生反应,不符合题意,B错误;向氯化镁和盐酸的 混合溶液中加入适量氢氧化钠溶液,反应后会增加新的杂质氯化钠,C错误;D项,二氧化碳含量较多时,一 氧化碳不能被点燃,D错误。
14.(2016河南,22,3分)除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作有:①加过量的NaOH溶液;② 加过量的BaCl2溶液;③过滤;④加适量的盐酸;⑤加过量的Na2CO3溶液。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水](1)以上操作合理的先后顺序为 (数字序号不能重复使用)。(2)请写出BaCl2溶液与Na2SO4溶液反应的化学方程式。(3)上述试剂中的Na2CO3不能用K2CO3代替,请说明原因。
答案 (1)①②⑤③④(或②①⑤③④或②⑤①③④)(1分)(2)BaCl2+Na2SO4 BaSO4↓+2NaCl(1分)(3)K2CO3与其他物质反应生成KCl,会引入新的杂质。(1分)
解析 (1)除去氯化钠溶液中的氯化钙、氯化镁和硫酸钠杂质时,选用的试剂分别为碳酸钠、氢氧化钠 和氯化钡溶液,为了将杂质充分除去,所加试剂必须过量,过量的碳酸钠和氢氧化钠最后均可利用适量稀 盐酸除去,而过量的氯化钡需用加入的碳酸钠除去,故碳酸钠溶液一定要在加入氯化钡溶液之后加入,因 此合理的顺序为②⑤①③④或②①⑤③④或①②⑤③④;(2)氯化钡溶液和硫酸钠溶液反应生成硫酸钡 和氯化钠;(3)碳酸钠不能用碳酸钾代替,否则碳酸钾与其他物质反应会产生新的杂质氯化钾。
易错警示 过量的BaCl2需要用碳酸钠除去,故碳酸钠溶液必须在加入氯化钡溶液之后加入,学生易出 错。
1.(2019河北保定竞秀一模,10)有两瓶失去标签的无色液体,一瓶是饱和氯化钠溶液,一瓶是蒸馏水。为 了把它们区分开,同学们提出了以下方法:①蒸发 ②测密度 ③测导电性 ④测pH ⑤加入氯化钠 ⑥加入食醋。你认为可行的是 ( )A.①②③⑤ B.①③④⑤C.②③④⑥ D.②③⑤⑥
答案 A 饱和氯化钠溶液与蒸馏水相比的不同点是:饱和氯化钠溶液不能再溶解氯化钠,有导电性,蒸 发析出白色晶体,密度大于水;但氯化钠溶液与蒸馏水都呈中性,pH相同,都不与醋酸反应,故答案为A。
2.(2019天津红桥一模,5)下列区分物质的方法不正确的是 ( )A.用稀硫酸区分木炭粉和氧化铜粉末B.用水区分硝酸铵固体和氢氧化钠固体C.用灼烧法区分棉花和羊毛D.用燃烧的木条区分二氧化碳和氮气
答案 D A项,氧化铜粉末能与稀硫酸反应生成硫酸铜和水,会观察到黑色粉末逐渐溶解,溶液变蓝色; 木炭粉不与稀硫酸反应,可以鉴别。B项,硝酸铵固体和氢氧化钠固体溶于水分别吸热、放热,使溶液的 温度分别降低、升高,可以鉴别。C项,羊毛的主要成分是蛋白质,灼烧时产生烧焦羽毛的气味,棉花灼烧 时产生烧纸的气味,可以鉴别。D项,二氧化碳和氮气均不能燃烧、不支持燃烧,均能使燃烧的木条熄灭, 不能鉴别,应选D。
3.(2020重庆潼南一模,14)下列实验能达到实验目的的是 ( )
答案 D A项,氢氧化钠固体可作干燥剂,但NaOH能与CO2反应,不但能把杂质除去,也会把原物质除去, 不符合除杂原则,故错误。B项,稀盐酸和稀硫酸均能与碳酸钠粉末反应生成二氧化碳气体,不能鉴别,故 错误。C项,检验一瓶气体是否为CO2,应使用澄清石灰水,故错误。D项,氢氧化钠溶于水放热,使溶液温 度升高;硝酸铵溶于水吸热,使溶液温度降低,可以鉴别,故正确。
知识归纳 除杂时加入的试剂只能与杂质反应,不能与原物质反应,反应后不能引入新的杂质。
4.(2019陕西摸底,12)下列各组物质的鉴别方法中正确的是 ( )A.用水鉴别CuSO4、NaOH、NH4NO3三种固体B.用燃着的木条鉴别O2、CO2、N2三种气体C.用灼烧的方法鉴别木炭粉、CuO、Fe3O4三种黑色粉末D.用酚酞溶液一次性鉴别H2SO4、KOH、NaCl三种溶液
答案 A NaOH、NH4NO3溶于水分别放热、吸热,分别能使溶液的温度升高、降低,硫酸铜溶于水形 成蓝色溶液,可以鉴别。O2能支持燃烧,能使燃着的木条燃烧得更旺,CO2、N2均不能燃烧、不支持燃烧, 均能使燃着的木条熄灭,不能鉴别。木炭粉灼烧时会产生二氧化碳气体,固体逐渐消失,CuO、Fe3O4灼烧 时均无明显变化,不能鉴别。H2SO4、KOH、NaCl三种溶液分别显酸性、碱性、中性,酚酞只能在氢氧 化钾溶液中显红色,不能鉴别硫酸和氯化钠溶液。
5.(2020河南洛阳一模,11)实验室中,区分下列各组物质的方法完全合理的是 ( )
答案 C A项,硬水和软水的不同只是含有可溶性钙镁化合物的量不同,加热蒸干可能都会出现固体, 故错误;B项,空气和二氧化碳都不具有助燃性,带火星的木条都不会复燃,故错误;C项,铁块和铝块的密度 不同,铁能被磁铁吸引,所以体积相同的铁块和铝块,用称量质量的方法可以鉴别,用磁铁吸引的方法也可 以鉴别,故正确;D项,在实验室不能品尝任何药品的味道,故错误。
思路分析 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即 可鉴别。
6.(2020湖南娄底一模,15)某混合气中可能有CO、水蒸气、CO2和N2中的两种或多种。为测定其组成,现 将混合气依次通过浓硫酸、灼热的Fe2O3、澄清石灰水。一段时间后,浓硫酸质量增加,Fe2O3固体由红变 黑,澄清石灰水变浑浊且有剩余气体。下列说法正确的是( )A.该混合气体中一定有CO、水蒸气和N2,可能有CO2B.该混合气体中一定有水蒸气、CO和CO2,可能有N2C.该混合气体中一定有CO2和N2,可能有CO或水蒸气D.该混合气体中一定有水蒸气和CO,可能有CO2或N2
答案 D 将混合气依次通过浓硫酸、灼热的Fe2O3、澄清石灰水,一段时间后,浓硫酸质量增加,说明有 水蒸气;Fe2O3固体由红变黑,说明有CO;石灰水变浑浊,说明石灰水与CO2发生了反应,但二氧化碳可能是 CO与Fe2O3反应生成的,也可能是原混合气体中的二氧化碳;最终剩余的气体可能是通过澄清石灰水时 带出的水蒸气,或者是没有反应完的CO2,或者是原混合气体中含有N2。故该混合气体中一定有水蒸气 和CO,可能有CO2或N2。
解题关键 掌握常见气体的检验方法、浓硫酸具有吸水性、一氧化碳具有还原性等是正确解答本题的 关键。
7.(2018天津南开一模,24)在实验室,有失去标签的五瓶药品,分别是硫酸铜、碳酸钙、碳酸钠、氢氧化 钠、氢氧化钙五种物质(均为纯净物),它们均为白色粉末。现将药品分别标记为A、B、C、D、E,我区 某校化学实验小组的同学们积极思考,利用所学知识设计实验,对这些物质进行了鉴别。【查阅资料】白色的硫酸铜粉末遇水变为蓝色。【实验探究】化学实验小组同学的鉴别实验过程记录如下:步骤1:取五种白色粉末各一药匙,分别放入五支洁净的试管中,各加蒸馏水2 mL,充分振荡后静置。五支 试管底部均有固体存在,只有盛放E的试管中液体呈蓝色,其他均呈无色。步骤2:取B、C、D上层清液滴加稀盐酸,只有B的试管中有气泡产生,其他无明显现象。步骤3:取A、C、D的上层清液放入试管中,分别滴加无色酚酞溶液,A、C显红色。请根据该小组同学的实验过程,回答下列问题:(1)由步骤1可知E为 (写化学式);(2)步骤3中,D的现象是 ;(3)通过上述步骤,除E外,该小组的同学还推断出的是B为 (填化学式,下同)、D为 ;(4)对尚未鉴别出来的物质,同学们设计了实验进行确定,请将下表补充完整:
答案 (1)CuSO4(2)仍为无色(或不变色,或无明显现象等其他合理答案)(3)Na2CO3 CaCO3(4)Na2CO3 Ca(OH)2
解析 (1)盛放E的试管中液体呈蓝色,所以E是硫酸铜。(2)根据步骤2可知B为碳酸钠;步骤3中,分别滴加 酚酞溶液,只有A、C显红色,说明D为碳酸钙,故D的现象为不变红色。(4)未鉴别出来的物质是氢氧化钠 和氢氧化钙,根据这两种物质的不同性质设计实验方案。氢氧化钙溶液能与碳酸钠溶液反应生成白色 沉淀,氢氧化钠溶液与碳酸钠溶液不反应,故分别滴加碳酸钠溶液,试管①中有白色沉淀产生,则①中的物 质为氢氧化钙。
8.(2020辽宁鞍山立山二模,14)除去下列各物质中的少量杂质,所用方法不可行的是 ( )
答案 A A项,Na2CO3能与盐酸反应生成氯化钠、水和二氧化碳,引入了新的杂质氯化钠,故错误。B 项,Fe能与足量的稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,再过滤,能除去杂质且没有引 入新的杂质,故正确。C项,CO 能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的 杂质,故正确。D项,CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,故正 确。
9.(2018广东广大附中一模,18)除去下列物质中少量的杂质,所用方法正确的是 ( )
答案 D A项,在空气中充分灼烧,不但能把杂质除去,也会把原物质转化为CuO,不符合除杂原则,故错 误。B项,CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故错 误。C项,少量的一氧化碳不能被点燃,故错误。D项,铁粉能与CuCl2溶液反应生成氯化亚铁和铜,充分反 应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故正确。
10.(2019辽宁鞍山一模,12)除去下列物质中的少量杂质,所用除杂方法正确的是 ( )
答案 D KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故 A错误。HCl能与过量的氢氧化钡溶液反应生成氯化钡和水,能除去杂质但引入了新的杂质氢氧化钡(过 量的),不符合除杂原则,故B错误。当二氧化碳大量存在时,少量的一氧化碳是不会燃烧的,故C错误。 CuO能与适量的稀盐酸反应生成氯化铜和水,铜不与稀盐酸反应,再过滤、洗涤、干燥,能除去杂质且没 有引入新的杂质,符合除杂原则,故D正确。
思路分析 根据原物质和杂质的性质选择适当的除杂试剂和分离方法,所谓除杂(提纯),是指除去杂质, 同时被提纯物质不得改变。除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物 质反应;②反应后不能引入新的杂质。
11.(2019贵州黔东南模拟,8)下列说法中,不能达到目的的是 ( )
答案 B A项,Na2SO4能与适量的Ba(OH)2溶液反应生成硫酸钡沉淀和氢氧化钠,再进行过滤,能除去杂 质且没有引入新的杂质,符合除杂原则。B项,CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把 原物质除去,不符合除杂原则。C项,CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液 反应,干燥后,能除去杂质且没有引入新的杂质,符合除杂原则。D项,H2SO4能与足量氧化铜粉末反应生 成硫酸铜和水,再进行过滤,能除去杂质且没有引入新的杂质,符合除杂原则。
12.(2020黑龙江绥化模拟,13)下列实验操作中能达到实验目的的是(双选) ( )
答案 BD A项,铁和硫酸铜反应生成硫酸亚铁和铜,铁和稀硫酸反应生成硫酸亚铁和氢气,除去了杂质 也除去了原物质,故错误;B项,二氧化碳和氢氧化钠反应生成碳酸钠和水,再经过浓硫酸,可吸收一氧化碳 中的水蒸气,能够达到实验目的,故正确;C项,稀硫酸和氧化铁反应生成硫酸铁和水,再过滤,只能得到碳 粉,不能得到氧化铁粉末,不能达到分离的目的,故错误;D项,分别加入熟石灰研磨,产生刺激性气味的是 硫酸铵,另一种是硫酸钾,故正确。
一、选择题(每题2分,共10分)
1.(2020江苏苏州,18)下列实验方案不能达到目的的是 ( )A.鉴别:用熟石灰鉴别NH4Cl固体和NH4NO3固体B.除杂:用浓硫酸除去O2中混有的少量水蒸气C.检验:用高锰酸钾溶液检验CO2中是否混有SO2D.制备:实验室用锌粒和稀硫酸制备少量H2
答案 A A项,用熟石灰无法鉴别NH4Cl固体和NH4NO3固体,因为两者都含有铵根离子,都能与熟石灰 发生反应生成有刺激性气味的氨气;B项,浓硫酸具有吸水性且不与氧气反应,用浓硫酸可以除去O2中混 有的少量水蒸气;C项,用高锰酸钾溶液可以检验二氧化碳中是否混有二氧化硫,因为二氧化硫可使高锰 酸钾溶液褪色,而二氧化碳不能;D项,实验室通常用锌粒和稀硫酸制备少量H2。
2.(2020云南,19)下列实验方案设计不合理的是 ( )
答案 B A项,KCl易溶于水,二氧化锰不溶于水,所以除去氯化钾中少量的二氧化锰,可以向混合固体 中加适量水溶解,过滤,蒸发结晶;B项,将生锈的铁丝长时间浸泡在足量的稀盐酸中,不仅表面的铁锈会被 除去,里面的铁也会与稀盐酸反应;C项,硫酸铵能和熟石灰反应,放出有刺激性气味的气体,而硫酸钾不 能,因此可鉴别;D项,硫酸铜溶于水形成蓝色溶液,碳酸钙难溶于水,氯化钠溶于水形成无色溶液,因此,分 别加适量水搅拌,可鉴别三种白色固体;故选B。
3.(2020陕西A,8)下列各组实验方法能达到实验目的的是 ( )
答案 B A项,向硫酸铜溶液和硝酸银溶液中各放入一根镁条,可观察到镁条能置换出铜和银,只能证 明镁的金属活动性最强,无法比较铜和银的金属活动性;B项,高温加热固体,并将生成的气体通入澄清石 灰水中,若固体颜色变为红色,澄清石灰水变浑浊,可说明原黑色固体中含有碳和氧化铜;C项,加入过量 CaCl2溶液,会将碳酸钠除去,不符合除杂要求;D项,题述条件下两根铁钉都没有生锈,无法探究铁生锈的 条件。
4.(2019江苏苏州,20)鉴别下列各组物质,所选用的试剂不正确的是 ( )A.面粉和米粉:碘酒B.NaOH固体和NH4NO3固体:水C.硬水和软水:肥皂水D.NaCl溶液和NaNO3溶液:AgNO3溶液
答案 A A项,面粉和米粉中均富含淀粉,均能使碘酒变蓝色,不能鉴别。B项,NaOH固体溶于水放热, NH4NO3固体溶于水吸热,可以鉴别。C项,硬水和软水的区别在于所含的钙、镁离子的多少,可用肥皂水 来区分,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,可以鉴别。D项,NaCl能与AgNO3反应生 成氯化银白色沉淀和硝酸钠,硝酸钠不能与硝酸银反应,可以鉴别。
5.(2019黑龙江哈尔滨模拟,12)在实验室中区分下列各组物质的两种方法都正确的是 ( )
答案 B A项,用手触摸羊毛和涤纶,手感相同,无法鉴别,故A错误。B项,厨房清洁剂去除油污,主要成 分是氢氧化钠,厕所清洁剂主要成分是盐酸,故厨房清洁剂pH>7,厕所清洁剂pH<7,可以用测pH的方法鉴 别;厨房清洁剂呈碱性,加入紫色石蕊溶液变蓝,厕所清洁剂呈酸性,加入紫色石蕊溶液变红,故加入紫色 石蕊溶液可以鉴别,故B正确。C项,二氧化锰和木炭粉都是黑色粉末,观察颜色无法鉴别,故C错误。D项, 硝酸铵和尿素都属于氮肥,加水都溶解,无法鉴别,故D错误。
6.(2020广东,19)(10分)某兴趣小组在学习碳(C)的化学性质时,了解到高温下C与CuO反应生成CO2,C还 能使CO2转变成CO。于是对过量木炭还原CuO的气体产物中是否含有CO进行了探究。【猜想与假设】C还原CuO时产生的CO2与C进一步反应生成CO,化学方程式是 。【查阅资料】CO不与NaOH、Ca(OH)2及H2SO4反应。【实验方案】取研细和干燥后的木炭(0.3 g)和CuO(2.0 g),混合均匀并装入试管,连接装置,高温反应,检 验气体。【实验过程】(1)由下图所示装置③中粉末的颜色变化可检验CO,除此之外,还可通过几种装置的组合,由另一种明显 的现象来进一步确定CO的存在,则装置连接的最佳顺序为 →尾气处理(填字母)。A.①→②→③→④B.④→①→②→③→①C.①→④→①→③→②D.③→④→①→②
二、非选择题(共10分)
(2)上述进一步确定CO存在的现象是 (装置③中粉末的颜色变化除外)。(3)装置③中发生反应的化学方程式是 。(4)写出CO尾气处理的方法: (一种即可)。【实验结论】高温下,过量木炭还原CuO的气体产物中有CO。【延伸应用】冬天,室内用炭火取暖时,应注意 。
中考化学一轮复习课件14专题十四 物质的检验与提纯 (含答案): 这是一份中考化学一轮复习课件14专题十四 物质的检验与提纯 (含答案),共60页。
初中化学一轮复习课件 专题17 物质的检验与鉴别、分离与提纯(讲通练透): 这是一份初中化学一轮复习课件 专题17 物质的检验与鉴别、分离与提纯(讲通练透),共21页。PPT课件主要包含了中考化学一轮复习策略,聚焦中考复习目标,复习目标,聚焦中考命题解读,命题解读,聚焦中考考点梳理,SO2,紫色石蕊试液,无色酚酞试液,物质的检验方法等内容,欢迎下载使用。
中考化学一轮复习精讲课件专题17 物质的检验与鉴别、分离与提纯 (含详解): 这是一份中考化学一轮复习精讲课件专题17 物质的检验与鉴别、分离与提纯 (含详解),共19页。PPT课件主要包含了聚焦中考复习目标,复习目标,聚焦中考命题解读,命题解读,聚焦中考考点梳理,SO2,紫色石蕊试液,无色酚酞试液,物质的检验方法,带火星的木条等内容,欢迎下载使用。












