





- 5.1.1硫及其化合物课件PPT 课件 1 次下载
- 5.2.1 氮气与氮的固定课件PPT 课件 1 次下载
- 5.2.2 氨和铵盐课件PPT 课件 0 次下载
- 5.2.3 硝酸 酸雨及防治课件PPT 课件 0 次下载
- 5.3.1硅酸盐材料课件PPT 课件 0 次下载
化学第一节 硫及其化合物课前预习课件ppt
展开问题1:根据标签信息求该硫酸的物质的量浓度?已知该硫酸的质量分数为98.08%
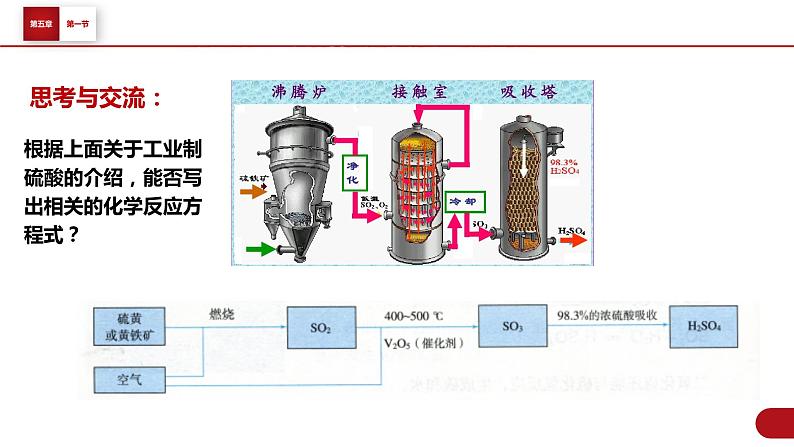
根据上面关于工业制硫酸的介绍,能否写出相关的化学反应方程式?
1、工业制硫酸(接触法制硫酸)
2、物理性质纯净的硫酸是 黏稠状液体,密度比水 ,能与水以任意比混合,沸点 ,难挥发。
稀释浓硫酸时应将浓硫酸沿器壁慢慢注入水中,并不断搅拌。
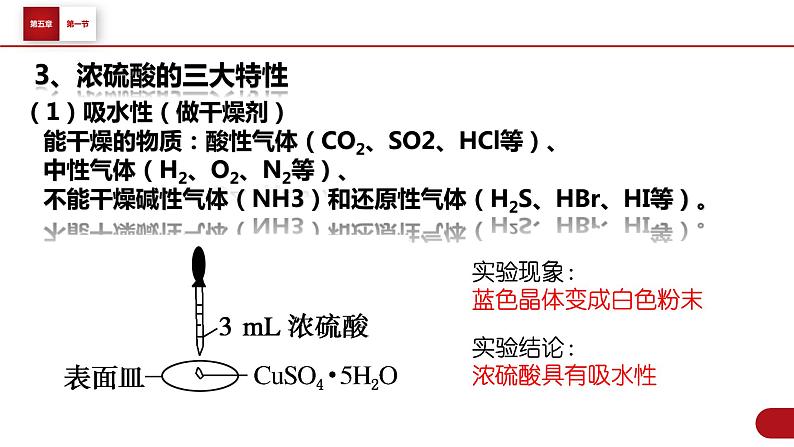
(1)吸水性(做干燥剂) 能干燥的物质:酸性气体(CO2、SO2、HCl等)、 中性气体(H2、O2、N2等)、 不能干燥碱性气体(NH3)和还原性气体(H2S、HBr、HI等)。
实验现象:蓝色晶体变成白色粉末
实验结论:浓硫酸具有吸水性
实验现象:蔗糖逐渐变黑,体积膨胀,形成疏松多孔 的海绵状的炭,并放出有刺激性气味的气体
实验结论:浓硫酸具有脱水性,且能氧化碳单质,生成 CO2,本身被还原为SO2
(2)脱水性指浓硫酸能将某些有机物中的H、O原子的组成比(2:1)脱去, 使其炭化的性质。
①.常温下,当Fe、Al遇到浓硫酸时,会与浓硫酸发生反应,表 面生成一层致密的氧化物薄膜而出现“钝化”现象。
②. 与位于氢之前的活泼金属反应 Zn+2H2SO4(浓)===ZnSO4+SO2↑+2H2O
规律:a. 浓硫酸既表现氧化性,又表现酸性; b. 浓硫酸一旦变稀,就发生: Zn+H2SO4===ZnSO4+H2↑。
实验现象:加热前铜丝在浓硫酸中无现象;加热后,铜丝表面有气泡 产生;品红溶液褪色;紫色石蕊溶液变红
③.与氢之后的不活泼金属(除Au、Pt外)反应
规律:a. 反应需加热,否则不反应;b. 氧化产物是硫酸盐,金属显高价,还原产物为SO2;c. 浓硫酸既表现氧化性,又表现酸性;d. 随反应进行,硫酸浓度变小,一旦变为稀硫酸,反应就会停止。
④.与还原性化合物的反应:常见的还原性物质FeSO4、Na2S、 H2S、HBr、HI等均能被浓H2SO4氧化
4、硫酸的用途——化学工业之母
(1)高沸点——制取挥发性酸(2)吸水性——做干燥剂(3)脱水性——做催化剂(4)酸性——去金属表面的氧化物、制取硫酸盐、制造化肥(5)强氧化性——制炸药
无水硫酸铜用于检测水的存在
CuSO4·5H2O(俗称胆矾)
胆矾可以和石灰乳混合制成一种常用的农药——波尔多液
(1) SO42- 离子的检验
HCl酸化,再加BaCl2,
1.如图所示是实验室制取SO2并检验SO2某些性质的装置图,已知:2H2S+SO2 3S↓+2H2O。
请回答下列问题:(1)⑥中发生反应的化学方程式为 _。 (2)①中的实验现象为 ,证明SO2的水溶液具有 性。 (3)②中的品红溶液 ,证明SO2具有 性。 (4)③中的实验现象为 ,证明SO2具有 性。 (5)④中的实验现象为 ,证明SO2具有 性。 (6)⑤的作用是 ,反应的化学方程式为 。
吸收多余的SO2,防止污染空气
2. 浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )①炽热的木炭 ②H2S气体 ③Cu(加热条件下) ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4·5H2O ⑧铁、铝(常温下)A.③④ B.①②⑤⑧ C.①②③④⑦ D.⑥⑦
3. 向50mL 18ml∙L-1的H2SO4溶液中加入足量的铜片并加热, 充分反应后, 被还原的H2SO4的物质的量。 A. 等于0.45ml B. 等于0.9ml C. 小于0.45ml D. 在0.45ml与0.9ml之间
4.如图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。 思考:图中品红溶液、紫色石蕊溶液、溴水、含酚酞的NaOH溶液如何变化?(科学探究与创新意识)
提示:SO2的水溶液显酸性,能使紫色石蕊溶液变红;SO2有漂白性,能使品红溶液褪色;SO2有强还原性,与溴水发生反应:Br2+SO2+2H2O====H2SO4+2HBr,使溴水褪色;SO2能与NaOH溶液反应生成Na2SO3,使红色变浅或褪色。
高中化学人教版 (2019)必修 第二册第五章 化工生产中的重要非金属元素第一节 硫及其化合物优秀作业课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第五章 化工生产中的重要非金属元素第一节 硫及其化合物优秀作业课件ppt,文件包含512+硫及其化合物课件pptx、512三氧化硫和硫酸分层作业含解析docx、512三氧化硫和硫酸分层作业无答案docx等3份课件配套教学资源,其中PPT共32页, 欢迎下载使用。
高中第一节 硫及其化合物教课ppt课件: 这是一份高中第一节 硫及其化合物教课ppt课件,共23页。PPT课件主要包含了硫酸的用途和制备,稀硫酸的化学性质,浓硫酸的特性,吸水性,Fe和Al,低温或常温,自主检测,Ag+,硫酸根离子的检验,观察有无白色沉淀产生等内容,欢迎下载使用。
高中实验活动2 铁及其化合物的性质备课课件ppt: 这是一份高中实验活动2 铁及其化合物的性质备课课件ppt,共20页。PPT课件主要包含了生产生活中的硫酸,工业制硫酸,思考与交流,浓硫酸的性质,浓硫酸的吸水性,用途可以作干燥剂,浓硫酸的脱水性,浓硫酸的强氧化性,逐渐变黑色,要点点拨等内容,欢迎下载使用。














