

2023年高考第一次模拟考试卷:化学(重庆B卷)(考试版)
展开2023年高考化学第一次模拟考试卷(重庆B卷)
高三化学
本卷满分100分,考试时间75分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 P 31 S 32
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中国诗词中包含了丰富的化学知识,下列说法错误的是
A.梨花淡白柳深青,柳絮飞时花满城:柳絮的主要成分属于糖类
B.忽闻海上有仙山,山在虚无缥缈间:句中海市蜃楼形成美景的本质原因是丁达尔效应
C.火树银花不夜天,兄弟姐妹舞翩跹:“火树银花”中的焰火实质上是金属化合物在灼烧时呈现的各种 艳丽色彩
D.高堂明镜悲白发,朝如青丝暮成雪:青丝与白发的主要成分均属于蛋白质
2.反应可用于制备照相业定影剂硫代硫酸钠。下列说 法正确的是
A.是非极性分子 B.既含离子键又含共价键
C.和具有相同的电子层结构 D.的电子式为
3.下列反应的离子方程式不正确的是
A.碳酸氢镁溶液中加入过量石灰水:
B.次氯酸钙溶液中通入过量的二氧化碳气体:
C.次氯酸钠溶液吸收过量二氧化硫气体:
D.氯化铁溶液与过量硫化钠溶液反应:
4. NA为阿伏伽德罗常数的值,下列说法正确的是
A.标准状况下,2.24L乙烯中σ键的数目为0.4 NA
B.24.5g 和的混合物中含有的O原子数为NA
C.足量Cu与10g 98%的浓硫酸共热反应,转移的电子数为0.2 NA
D.在含0.1mol氯化铁的溶液中,
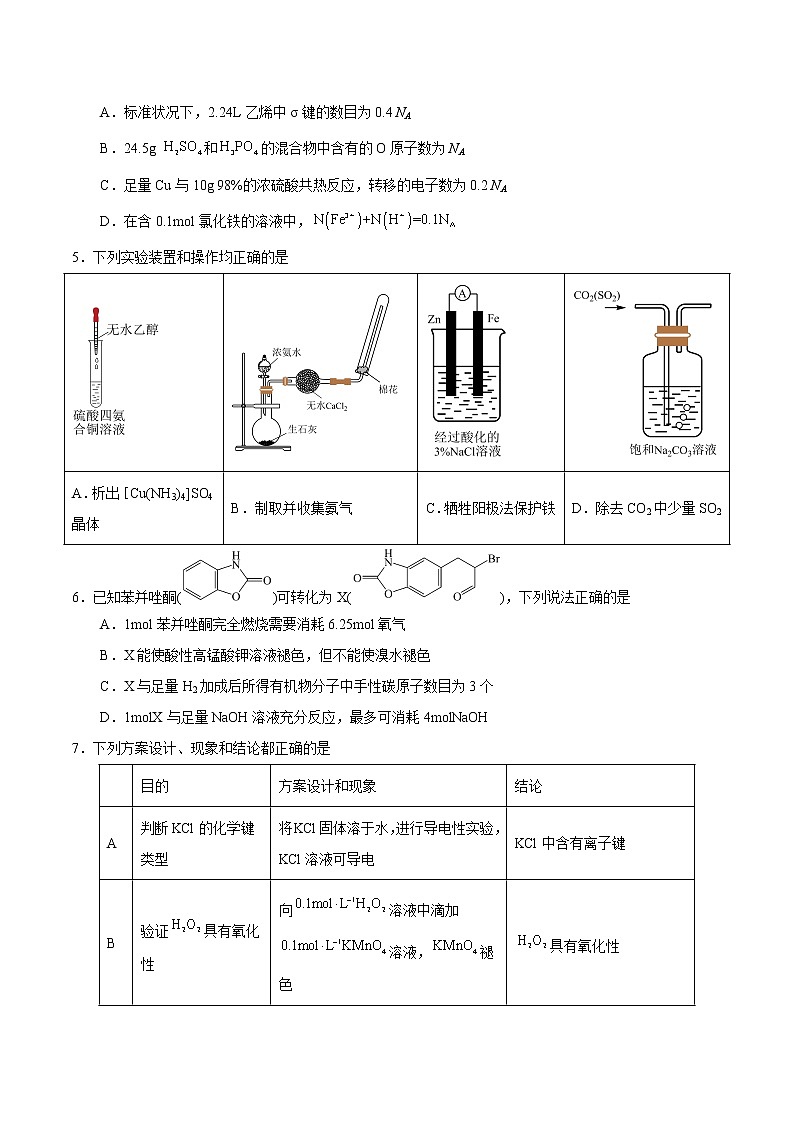
5.下列实验装置和操作均正确的是
A.析出[Cu(NH3)4]SO4晶体 | B.制取并收集氨气 | C.牺牲阳极法保护铁 | D.除去CO2中少量SO2 |
6.已知苯并唑酮()可转化为X(),下列说法正确的是
A.1mol苯并唑酮完全燃烧需要消耗6.25mol氧气
B.X能使酸性高锰酸钾溶液褪色,但不能使溴水褪色
C.X与足量H2加成后所得有机物分子中手性碳原子数目为3个
D.1molX与足量NaOH溶液充分反应,最多可消耗4molNaOH
7.下列方案设计、现象和结论都正确的是
| 目的 | 方案设计和现象 | 结论 |
A | 判断KCl的化学键类型 | 将KCl固体溶于水,进行导电性实验,KCl溶液可导电 | KCl中含有离子键 |
B | 验证具有氧化性 | 向溶液中滴加溶液,褪色 | 具有氧化性 |
C | 比较与的大小 | 向饱和溶液滴加相同浓度的溶液,产生白色沉淀 | |
D | 鉴别与 | 取适量固体于试管,插入温度计,加少量水,温度降低 | 该固体是 |
8.下列对分子性质的解释中,不正确的是
A.在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式 如图1
B.和的中心原子杂化方式不同,前者是后者是
C.、、的VSEPR模型相同
D.由如图2可知酸性,因为分子中有1个非羟基氧原子
9.X、Y、Z、W为原子序数依次增大的短周期主族元素。X与Z同族,Z的原子序数是X的2倍,Y离子在同周期内离子半径最小。下列说法正确的是
A.离子半径:W>Z>Y>X
B.Y2Z3能在水溶液中制得
C.H2X分子间存在氢键,因此稳定性H2X>H2Z
D.元素X和W的某些单质或化合物可作为工业生产上的脱色剂、消毒剂
10.某课题组在研究钒生物化学时有循环过程如图所示下列说法不正确的是
A.在循环过程涉及氢氧键的断裂和形成
B.在该循环中,催化剂为循环图化合物1
C.循环过程中反应①②③④均属于氧化还原反应
D.在循环过程中,无机物发生的反应为:
11.草酸亚铁晶体是生产感光材料的原料,制备流程如下:
下列说法错误的是
A.可用KSCN溶液检验是否变质
B.步骤①酸化的目的是抑制的水解
C.步骤②反应为
D.步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
12.我国科研人员将单独脱除的反应与的制备反应相结合,实现协同转化。
①单独制备:,不能自发进行。
②单独脱除:,能自发进行协同转化装置如下图(在电场作用下, 双极膜中间层的解离为和,并向两极迁移)。
下列分析不正确的是
A.反应②释放的能量可以用于反应①
B.产生的电极反应:
C.反应过程中不需补加稀
D.协同转化总反应:
13.在密闭容器中充入1和1,在一定条件下发生反应: ,测得的平衡转化率与温度及压强的关系如图所示。实验测 得,,(、为速率常数,只与温度有关),下列说法 错误的是
A.达到平衡后,仅升高温度,增大的倍数小于增大的倍数
B.若密闭容器(对应压强下)体积为1L,则b点
C.的物质的量浓度:b点点
D.逆反应速率:a点点
14.已知:常温下,碳酸的电离平衡常数Ka1=4.4 ×10-7, Ka2=4.7×10-11。常温下,向100 mL0.1 mol·L-1K2CO3 溶液中缓慢滴加100 mL 0.2 mol·L-1盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图 所示(H+和OH-未画出)。
下列说法不正确的是
A.滴加至A点时,n(Cl- )=n()> n()
B.滴加至B点时,≈9.4× 103
C.滴加至C点时,c(Cl-)< c()+ 2c()
D.滴加至D点时,溶液的pH<7
二、非选择题:本题共4小题,共58分。
15.(14分)工业上以镍铁硫化矿(主要成分为NiS、FeS、SiO2等)为原料制备兰尼镍(一种带有多孔结构的细 小晶粒组成的镍铝合金,具有优良的储氢性能) ,并获得副产品黄钠铁矾[NaFe3(SO4)2(OH)6]工艺流程 如下:
回答下列问题:
(1)“煆烧过程中NiS、FeS分别转化为Ni2O3、Fe2O3,写出NiS转化为Ni2O3的化学方程式:_______。
(2)已知Ni2O3具有强氧化性,则滤渣1的主要成分为_______(填化学式,下同),气体2是_______。
(3)滤渣2的主要成分为黄钠铁矾,写出生成黄钠铁矾和气体的离子方程式:_______。
(4)在“还原”阶段,析出物中含镍物质的质量分数与NaOH溶液浓度的关系如下图所示:
NaOH溶液浓度不同时,析出产物中Ni的质量分数不同,其原因可能为_______。
(5)“高温熔融”阶段通入Ar的目的是_______。
(6)“高温熔融”后加浓NaOH溶液的目的是使镍铝合金产生多孔结构,其反应原理为_______(用离子方 程式表示)。
(7)Ni(OH)2可用于制备镍钴锰三元电极材料。用NiSO4溶液制备Ni(OH)2时,若要使滤液中的
c(Ni2+)≤1.0 ×10-6 mol·L-1,则滤液的pH不小于_______{已知:Ksp[Ni(OH)2] =2.0 ×10-15,lg2=0.3}。
16. (15分)是一种重要的化学原料,有着重要的用途,可与、、、等多种物 质反应。回答下列问题:
(1)将、、放入一个真空密闭容器中,在150℃下用电火花不断引燃反应,恰好完全反应, 生成物之一为,压强为零,则、、的物质的量之比为_______。
(2)与之间也能进行反应,某科研小组对其反应产物进行了探究分析。
第1步:用如图1所示装置制取,用98.3%浓硫酸吸收(可溶于浓硫酸,加热后又会逸出),得 到无色吸收液。
第2步:用如图2所示装置加热浓硫酸吸收液,使挥发,通入盛有的试管中,至固体颜色 不变后,再通入,气体2min。
第3步:称取图2中反应后的固体0.5g,加水溶解,配制100mL待测溶液。
①与可能发生反应的化学方程式为、_______。
②上述“第3步”中配制100mL待测溶液,需要的玻璃仪器有烧杯、玻璃棒、_______(填1种)。
③图1、图2中的NaOH溶液用于尾气处理,则反应中氧化产物与还原产物的物质的量之比为_______。
(3)某科研兴趣小组运用数字化实验对、的反应过程进行探究(如图3所示)。
步骤如下:
Ⅰ.将计算机、数据采集器、氧气传感器依次相连。
Ⅱ.用无水与浓(70%)反应制取并用仪器A收集气体。
Ⅲ.将氧气传感器塞入仪器A中间接口,进行数据采集,用药匙取少量从仪器A右端加入,迅速 塞紧瓶塞。
①仪器A的名称为_______。
②ab段氧气的含量迅速升高,对应的化学方程式为_______,该反应是_______(填“吸热”或“放热”)反应。
③bc段氧气的含量慢慢降低,可能发生反应的化学方程式为_______。
17.(14分)丙烯腈()是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,副产物有丙 烯醛()、乙腈()等。以丙烯、氨气和氧气为原料,在催化剂存在下合成丙烯腈() 涉及的主要反应如下:
Ⅰ.
Ⅱ.
回答下列问题:
(1) △H=_______kJ/mol。
(2)恒温,体系达到平衡后,若压缩容器体积,则反应Ⅱ的平衡移动方向为_______(填“正反应方向”“逆 反应方向”或“不移动”)。
(3)如图为丙烯产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,有人认为丙烯 腈的产率不是对应温度下的平衡产率,其理由是_______;高于460℃时,丙烯腈产率降低的可能原因 是_______(填标号)。
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应的活化能增大
(4)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图所示。由图可知进料气中氨、空气、丙烯的理论 体积比约为_______(氧气在空气中约占20%)。
(5)已知对于反应:,其标准平衡常数:,T℃, 压强为的恒压密闭容器中,通入1mol丙烯,1mol氨气和3mol氧气发生反应Ⅰ、Ⅱ,达到平衡时, 容器内有a mol(g),b mol(g),则反应Ⅱ的标准平衡常数为_______(用含a、b的代数式表 示)。
(6)以丙烯腈为原料,利用电解原理合成[]可减少氮氧化物的排放,其装置如图所示,电 解时Pb电极发生的电极反应式为_______。
- (15分)异苯并呋喃酮类物质广泛存在。某异苯并呋喃酮类化合物K的合成路线如下。
已知:i.+ROH
ii.
回答下列问题:
(1)试剂a的分子式是_______。
(2)CuCl2催化C→D的过程如下,补充完整步骤②的方程式。
步骤①:C+2CuCl2→D+CO2↑+2CuCl +2HCl
步骤②:_______。
(3)下列说法不正确的是(填序号)_______。
a.A的核磁共振氢谱有2组峰
b.B存在含碳碳双键的酮类同分异构体
c.D存在含酚羟基的环状酯类同分异构体
(4)E→F的化学方程式是_______。
(5)由E和F制备G时发现产率不高。以丙酮和乙醇为原料,其它无机试剂自选,设计高效合成G的合 成路线。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_______。
已知:i.难以被进一步氯代
ii.R-Cl-R-CN
(6)D和G经五步反应合成H,中间产物3无手性异构体,写出中间产物2和3的结构简式_______。 (结 构简式中的“”可用“-R” 表示)
(7)J的结构简式是_______。
2023年高考第二次模拟考试卷-化学(重庆B卷)(考试版): 这是一份2023年高考第二次模拟考试卷-化学(重庆B卷)(考试版),共12页。
2023年高考第一次模拟考试卷:化学(重庆B卷)(全解全析): 这是一份2023年高考第一次模拟考试卷:化学(重庆B卷)(全解全析),共11页。试卷主要包含了B【详解】A,A【详解】A,C【详解】A,D【详解】A等内容,欢迎下载使用。
2023年高考第一次模拟考试卷:化学(重庆B卷)(参考答案): 这是一份2023年高考第一次模拟考试卷:化学(重庆B卷)(参考答案),共3页。试卷主要包含了-162,C2H2O3等内容,欢迎下载使用。












