










初中人教版课题 3 金属资源的利用和保护完整版ppt课件
展开课题3 金属资源的利用和保护
本课题涉及面广,包括地球上及我国的金属资源概况、铁的冶炼、化学反应中有关杂质问题的计算、金属的腐蚀及防护、金属资源的保护等,既有知识、技能方面的内容,又有环境意识和资源意识等情感领域的内容。
第一部分“铁的冶炼”是本课题教学的重点,教案设计时,把铁的冶炼原理和实验室模拟工业冶炼原理的实验设计成了探究内容,然后由矿石之中存在杂质引申到化学反应中有关杂质问题的计算,以便学生主动参与,深刻理解,对金属资源概况这部分内容的学习,也特意的精心设计,一是对学生的视野进行了拓展,二是为他们将来高中的学习作铺垫。
第二部分“金属资源的保护”重点是有关铁的锈蚀以及防护的“活动与探究”内容。此部分内容全由学生通过实验、讨论、应用等环节来完成。关于金属资源的保护,也由学生通过联系实际,发挥想象,进行讨论等方式来认识和学习。
总之,本课题教案的设计,充分体现了学生为主、探究为主,教师引导这一特点。
第1课时 铁的冶炼
环节一
课题 | 铁的冶炼 | 课型 | 新授课 | |
教学目标 | 知识与 技能 | 1.知道常见金属:铁、铝、铜等的矿物,了解从铁矿石中将铁还原出来的方法。 2.会利用化学方程式对含有某些杂质的反应物或生成物进行有关计算。 | ||
过程与 方法 | 1.通过实验,让学生了解炼铁的原理,使学生认识化学原理对实际生产的指导作用。 2.通过对某些含有杂质的物质的计算,使学生把化学原理、计算和生产实际紧密地结合在一起,培养学生灵活运用知识的能力。 | |||
情感、态度与价值观 | 1.通过对我国古代炼铁史的介绍,让学生了解我国的悠久历史,激发学生的爱国热情。 2.增强对生活和自然界中化学现象的好奇心和探究欲。 3.关注与化学有关的社会问题,初步形成主动参与社会决策的意识。 4.树立为社会的进步而学习化学的志向。 | |||
教学重点 | 1.铁的冶炼。 2.有关炼铁的杂质问题计算。 | |||
教学难点 | 有关化学方程式计算中的杂质问题的计算。 | |||
教具准备 | 多媒体课件等。 | |||
特别提醒:
在实验室做一氧化碳还原氧化铁的实验时,应注意:CO是可燃性气体,如果混有空气(或氧气),温度达到着火点或与明火接触可能发生爆炸,在使用前必须检验其纯度,因此在加热之前,必须将管内空气排净。实验中尾气要处理后再排放,防止其污染空气。
课前预习 | 1.地球上的金属资源除金、银等有单质形式存在外,其余都以化合物形式存在。 |
2.CO还原Fe2O3:(1)现象红棕色粉末变黑,澄清的石灰水变浑浊;(2)化学方程式为。 | |
3.工业炼铁:(1)设备:高炉,(2)原料:铁矿石、焦炭、石灰石,(3)原理:在高温的条件下,用CO从铁的氧化物中把铁还原出来。 |
环节二
新课导入 | 地球上的金属资源广泛存在于地壳和浩瀚的海洋中,除少数很不活泼的金属如金、银等以单质形式存在外,其余都以化合物形式存在。以化合物形式存在的金属在自然界中以矿物形式存在,含矿物的岩石称为矿石。工业上就是从矿石中来提炼金属的。 |
进行新课 | 一 常见的金属矿石 【学生活动】 请同学们阅读课本P14~P15,包括图片和资料,交流讨论。回答: 1.常见的金属矿物有哪些?其主要成分是什么? 2.常见的铁矿石中理论上最适宜炼铁的两种矿石是什么?理由? 3.人类目前普遍使用的金属有哪些? 【交流评价】 让学生分析与交换不同意见。 【交流回答】 1.常见的金属矿产有赤铁矿(主要成分是Fe2O3)、磁铁矿(主要成分是Fe3O4)、菱铁矿(主要成分是FeCO3)、铝土矿(主要成分是Al2O3)、黄铜矿(主要成分是CuFeS2)、辉铜矿(主要成分是Cu2S)。 2.最适宜炼铁的两种矿石是磁铁矿和赤铁矿,因为这两种矿石含铁量高(质量分数大),且含硫等“有害元素”少,冶炼时产生的污染小。 3.普遍使用的金属有铁、铝等。 【过渡】 现在,人类每年都要向地壳和海洋索取大量的金属矿物资源,以提炼数以亿吨计的金属。其中提取量最大的是铁。把金属矿物变成金属的过程,叫做金属的冶炼。炼铁的过程称之为铁的冶炼。下面,我们就来学习有关铁的冶炼的知识。 二 铁的冶炼 【学生活动】 1.展示我国古代炼铁图——了解我国炼铁的悠久历史。 2.观看视频——参观炼铁厂和展示P16图8-22。 3.思考工业冶炼铁的原料、原理和设备。 4.炼铁高炉及炉内化学反应过程示意图。 【分析小结】 1.冶炼的原料:铁矿石、焦炭、石灰石和空气 2.冶炼的原理(用化学方程式表示): |
铁矿石的种类很多,最重要的铁矿石有磁铁矿、赤铁矿、褐铁矿和菱铁矿等。铁矿石常按其含铁量的高低分为富矿(含铁量高于50%以上)和贫矿(含铁量在45%~50%以下)。在评定铁矿石的品位和质量时,除看这种铁矿石里的含铁量以外,还要看它的脉石的成分和有害杂质(硫、磷)的含量的多少。
课外拓展:
由于铁矿石里除了铁的氧化物外,还含有难熔化的脉石(主要成分一般为SiO2)。因此,炼铁时还要加入助熔剂(一般用石灰石),利用石灰石(CaCO3)在高温下分解出的生石灰(CaO)与脉石反应生成熔点较低的硅酸钙,这样将脉石从矿石里分离出来。CaCO3高温CaO+CO2↑,CaO+SiO2高温CaSiO3,在冶炼过程中,混在铁矿石里的锰、硅、硫、磷等元素也会被碳或一氧化碳从它们的化合物中还原出来,少量的碳、锰、硅、硫、磷等在高温下熔合在铁里,成为生铁。这就是炼铁时不能得到纯铁的原因。
| 3.冶铁的设备:高炉 4.产品:生铁(铁合金、混合物) 【演示实验】 利用多媒体课件展示——一氧化碳还原氧化铁,分析反应原理,记录现象,分析实验注意事项。 【归纳总结】 1.实验原理: 2.实验步骤:①检查装置气密性;②装入样品并固定;③向玻璃管内通入CO气体;④给氧化铁加热;⑤停止加热;⑥停止通入一氧化碳。 3.实验现象:①红色粉末逐渐变成黑色;②澄清石灰水变浑浊;③点燃尾气时,产生蓝色火焰。 4.注意事项:①先通CO的目的:排出玻璃管内的空气,以免加热时CO与空气混合,发生爆炸;②实验完毕后继续通CO的目的:防止氧化铁还原成铁后,在较高的温度下又被氧化;③尾气处理:多余的CO要燃烧掉,防止CO污染空气;④涉及的其他反应:CO2+Ca(OH)2=CaCO3↓+H2O、 三 有关含杂质化学反应的计算 【课件展示】利用多媒体展示课本P17例题。 【分析】 化学方程式表示的是纯净物之间的质量关系,赤铁矿石中含有纯的氧化铁的质量为:1000t×80%。若设生铁的质量为x,则其纯铁的质量为x×96%,根据化学方程式就可计算出结果。 解:设理论上可以炼出含铁96%的生铁的质量为x。 答:1000t含氧化铁80%的赤铁矿石,理论上可炼出含铁96%的生铁583t。 |
教学板书 | 课题3 金属资源的利用和保护 第1课时 铁的冶炼 一、金属资源的概况 1.存在方式:不活泼金属(金、银等)以单质形式存在,其余金属以化合物形式存在。 2.矿石铁矿石:赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、菱铁矿(FeCO3)、黄铁矿(FeS2) 铜矿石:黄铜矿(CuFeS2)、辉铜矿(Cu2S)铝矿石:铝土矿(Al2O3) |
| 二、铁的冶炼 1.工业炼铁 (1)原料:铁矿石、焦炭、石灰石和空气 (2)原理: (3)设备——高炉 (4)产品——生铁(铁合金、混合物) 2.实验室炼铁 (1)原理:3CO+Fe2O3高温2Fe+3CO2 (2)步骤::①查气密性;②装样品;③通CO;④加热Fe2O3;⑤停止加热;⑥停止通CO。 (3)现象:①红棕色粉末变黑;②澄清石灰水变浑浊;③点燃尾气时产生蓝色火焰。 (4)注意:①先通CO的目的:排出玻璃管内的空气,防止CO与空气混合发生爆炸;②实验完后继续通CO的目的:防止生成的铁在高温下又被氧化;③尾气处理:多余CO燃烧掉,防止CO污染空气。 三、有关杂质问题的计算 根据化学方程式计算时,要把含杂质的物质的质量换算成纯物质的质量。 |
课堂小结 | 本节课我们主要学习了金属资源的概况,铁的冶炼及有关杂质问题的计算等知识。难点是含杂质问题的计算,课后需要练习强化这类计算。 |
教材习题解答 | 练习与应用(P21) 1.(1)Fe2O3 (2)Fe3O4 (3)FeCO3 (4)Al2O3 5.解:设该厂理论上可日产含Fe 98%的生铁的质量为x。 答:该厂理论上可日产含Fe 98%的生铁2714t。 6.解:设需要含Fe3O490%的磁铁矿石的质量为x。 答:需要含Fe3O490%的磁铁矿石2977t。 |
方法点拨:
(1)1000t赤铁矿石是一个干扰因素,它不是纯氧化铁的质量,所以应把混合物变为纯净物; 纯物质质量=混合物质量×纯度。
(2)化学方程式必须配平,计算关系量别忘了计量数与相对分子质量的乘积。
(3)列式计算切莫漏掉单位。
(4)如何将纯净物的量转化成混合物的量?混合物的质量=纯净物的质量÷纯度。
(5)写出简答,切莫略或写“……”。
规律总结:
含杂质问题的计算,一般都假定杂质不参加化学反应,只能把纯净物的质量代入化学式中计算。
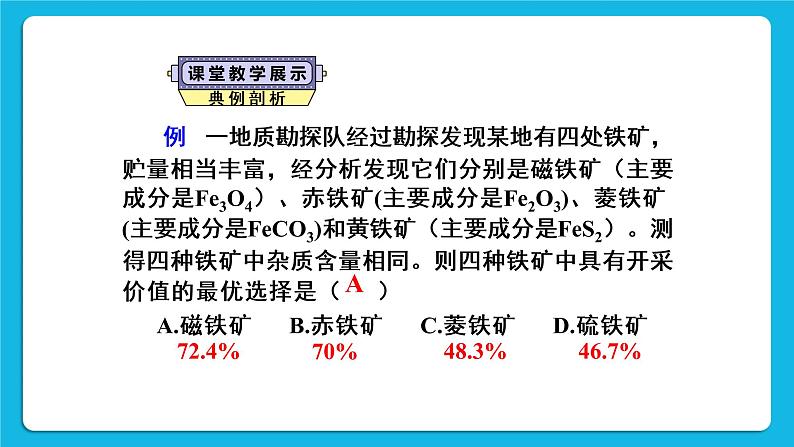
难题解答 | 【例1】一地质勘探队经过勘探发现某地有四处铁矿,贮量相当丰富,经分析发现它们分别是磁铁矿(主要成分是Fe3O4)、赤铁矿(主要成分是Fe2O3)、菱铁矿(主要成分是FeCO3)和黄铁矿(主要成分是FeS2)。测得四种铁矿中杂质含量相同。则四种铁矿中最具有开采价值的是( ) A.磁铁矿 B.赤铁矿 C.菱铁矿 D.硫铁矿 【解析】根据化学式的计算,Fe2O3 、Fe3O4、FeCO3、FeS2中含铁的质量分数分别为70%、72.4%、48.3%、46.7%,黄铁矿及菱铁矿中铁的质量分数都较小,并且黄铁矿中含有硫元素,在炼铁的过程中,很有可能形成二氧化硫气体,排放到空气中引起空气污染,所以上述黄铁矿及菱铁矿不适合用来炼铁。所以最适宜炼铁的两种矿石是磁铁矿和赤铁矿,“最优选择”则应是磁铁矿。 【答案】A 【例2】下列有关高炉炼铁的说法正确的一组是( ) ①高炉中焦炭的作用是产生一氧化碳 ②高炉中焦炭的作用是供热 ③高炉中把铁矿石冶炼成铁的主要反应原理是: ④高炉中把铁矿石冶炼成铁的主要反应原理是: A.①②③ B.②③④ C.①③④ D.①②④ 【解析】焦炭在炼铁过程中的主要作用是转化为一氧化碳,然后再还原铁矿石。故焦炭可提供热量和得到还原剂一氧化碳。 【答案】D 【例3】用2000t含氧化铁80%的赤铁矿矿石理论上可以炼出含铁96%的生铁多少吨? 【解析】纯物质的质量=不纯物质的质量×纯物质的质量分数。含有杂质的物质质量不能直接代入化学方程式中计算,因为杂质没有参加化学反应。本题也可以根据铁元素的质量在化学反应前后不变,利用化学式进行计算。 【答案】解:2000t矿石中含氧化铁的质量为2000t×80%=1600t 设1600t氧化铁理论上可炼出铁的质量为x。 折合为含铁96%的生铁的质量:1120t÷96%≈1166.7t 答:理论上可炼出含铁96%的生铁1166.7t。 |
环节三
布置作业:完成本课时对应练习,并提醒学生预习下一节的内容。
方法点拨:
解答该类题应从以下几个方面入手: ①反应条件; ②成本高低; ③有效成分的质量分数; ④对环境的影响。
归纳总结:
(1)混合物中某物质的质量分数(纯度)= =1-杂质的质量分数
(2)该物质的质量=不纯物质的总质量×该物质的质量分数(纯度)
(3)不纯物质的总质量=
归纳总结:
在一氧化碳还原氧化铁的实验中,规律可用口诀法巧记为:一氧化碳早出晚归,酒精喷灯迟到早退。
教学反思 | 本课教师通过展示我们生活中常见的一些金属材质的物品,让学生切身感受到金属的性质与用途,辅以教科书提供的信息,让学生在阅读讨论中自由发挥、自我表现、获取知识,这种教学方式对于常识性较强的教学内容,是完全适宜的。 |
教学过程中老师的疑问:
| |
教师点评和总结:
|
初中化学第八单元 金属和金属材料课题 3 金属资源的利用和保护试讲课ppt课件: 这是一份初中化学第八单元 金属和金属材料课题 3 金属资源的利用和保护试讲课ppt课件,文件包含第2课时金属资源保护课件pptx、第2课时金属资源保护导学案doc、第2课时金属资源保护教案doc、钢铁的锈蚀与危害mp4等4份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
人教版九年级下册课题 1 金属材料一等奖ppt课件: 这是一份人教版九年级下册课题 1 金属材料一等奖ppt课件,文件包含第2课时合金pptx、第2课时合金导学案doc、第2课时合金教案doc、合金与纯金属颜色光泽硬度的比较mp4等4份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
初中化学人教版九年级下册课题 1 金属材料试讲课ppt课件: 这是一份初中化学人教版九年级下册课题 1 金属材料试讲课ppt课件,文件包含第1课时几种重要的金属课件pptx、第1课时几种重要的金属导学案doc、第1课时几种重要的金属教案doc等3份课件配套教学资源,其中PPT共24页, 欢迎下载使用。














