





所属成套资源:最新九年级化学下册同步教学课件+课时练(人教版)
化学课题1 生活中常见的盐完美版教学ppt课件
展开
这是一份化学课题1 生活中常见的盐完美版教学ppt课件,共40页。PPT课件主要包含了纯净物,非金属,化合物,氧化物,混合物,初中化学物质的分类等内容,欢迎下载使用。
- Learning bjectives -
本课件内嵌3个视频,即点即播,使用方便(此页可删除)。
Vide1:粗盐中难溶性杂质的去除
说明:本课件使用WPS制作,使用WPS体验更佳效果。
Vide2:碳酸钠、碳酸氢钠和稀盐酸的反应
Vide3:碳酸钠与氢氧化钙的反应
生活中的盐是指食盐,主要成分是NaCl。而化学中的盐,不仅仅是指食盐,而是指一类组成里含有 和 的化合物。
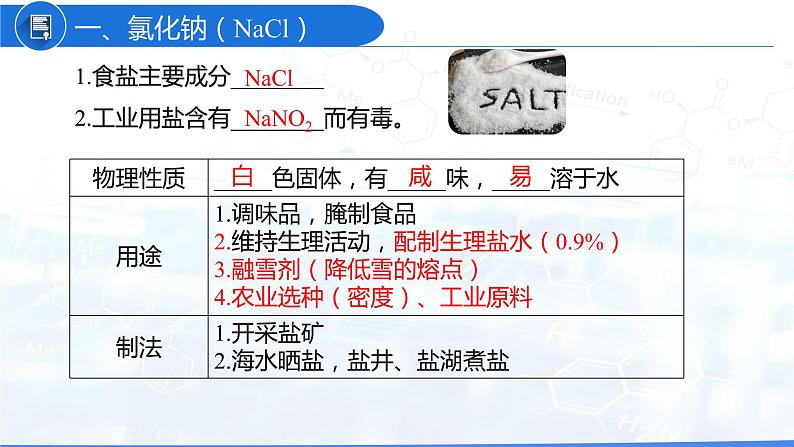
一、氯化钠(NaCl)
1.食盐主要成分________2.工业用盐含有________而有毒。
视频:粗盐中难溶性杂质的去除
1.目的:除去粗盐中的________杂质
2.步骤:3.玻璃棒的作用:
①溶解 →②过滤→ ③蒸发→ ④计算产率
搅拌,防止因局部温度过高,造成液滴飞溅
实验:粗盐中难溶性杂质的去除
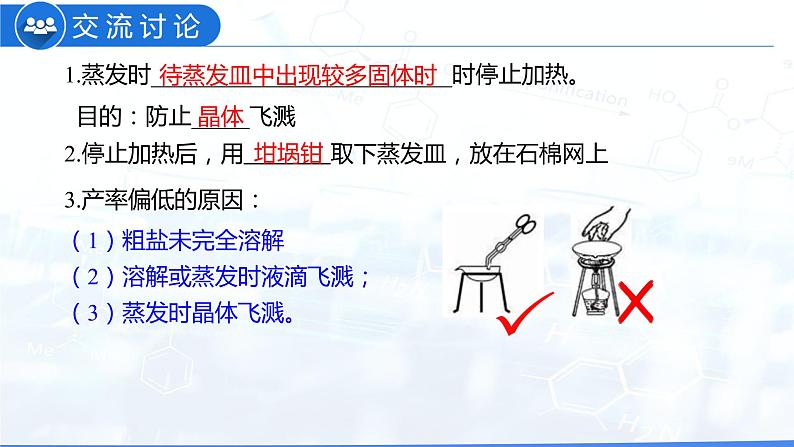
1.蒸发时__________________________时停止加热。 目的:防止_____飞溅
2.停止加热后,用 取下蒸发皿,放在石棉网上
(1)粗盐未完全溶解 (2)溶解或蒸发时液滴飞溅;(3)蒸发时晶体飞溅。
待蒸发皿中出现较多固体时
二、碳酸钠、碳酸氢钠和碳酸钙
玻璃、造纸、纺织、洗涤剂
建筑材料、补钙剂实验室制取CO2
碳酸钠——纯碱是盐不是碱,溶液呈碱性
1.小苏打(碳酸氢钠)受热易分解,可做发酵粉:
NaHCO3+HCl=NaCl+CO2↑+H2O
阅读教材P76“资料卡片”回答问题1.我国化学家侯德榜用“联合制碱法”所制得的纯碱是_______。 A.碳酸钠 B.氢氧化钠
Na2CO3、NaHCO3和CaCO3在组成上相似,都属于碳酸盐。它们是否也有类似的性质呢?
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
CaCO3+ HCl=
回顾:实验室制取CO2的化学方程式:
2 CaCl2+ H2CO3
视频:碳酸钠、碳酸氢钠和稀盐酸的反应
2 =2NaCl+CO2↑+H2O
=NaCl+CO2↑+H2O
2.盐的化学性质(1):碳酸盐 + 酸 = 新盐+H2O+CO2↑
Na2CO3+ HCl
CaCO3+2HCl= CaCl2+ CO2 ↑ +H2O
碳酸盐(CO32- 、HCO3-)的检验方法
该样品是碳酸盐(溶液中存在CO32- 、HCO3-)
逻辑推理:活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属( )
视频:碳酸钠与氢氧化钙的反应
Na2CO3+Ca(OH)2=CaCO3↓ +2NaOH
2.盐的化学性质(2):盐+ 碱= 新盐 + 新碱
Fe + CuSO4 = FeSO4 + Cu
Cu+2AgNO3 = Cu(NO3)2 +2Ag
盐的化学性质(3):盐+ 金属= 新盐 + 新金属
1.由两种化合物互相__________,生成另外两种化合物的反应。2.表达式:AB + CD =___________3.特征:_______________
Na2CO3 + 2HCl= 2NaCl+ H2O + CO2↑
NaHCO3 + HCl = NaCl + H2O + CO2↑
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
三、复分解反应(基本反应类型)
CaCO3 + 2HCl =CaCl2 + H2O + CO2 ↑
四种基本反应类型中一定有化合价变化的反应类型是 ;一定没有化合价变化的反应类型是 。
1.酸+碱→盐+水(中和反应)
2.酸+金属氧化物→盐+水
3.碱+盐→新碱+新盐
4.盐+盐→新盐+新盐
5.酸+盐→新盐+新酸
NaOH + HCl =H2O + NaCl
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
碱+非金属氧化物→盐+水 不属于复分解反应Ca(OH)2+CO2=CaCO3↓+H2O
1.Na2CO3俗称______、______。溶液呈____性。用途:____________________________。2.NaHCO3俗称________。用途:______________________。3.CaCO3是________、__________的主要成分。用途:___________________________________。
Na2CO3+2HCl=2NaCl+ CO2↑+H2O
NaHCO3+HCl=NaCl+ CO2↑+H2O
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Fe+CuSO4 = FeSO4 +Cu
CaCO3+2HCl=CaCl2+ CO2↑ +H2O
建筑材料、补钙剂、实验室制取CO2
1.下列属于复分解反应的是( )A.2NaOH+CO2=Na2CO3+H2O B.Zn+H2SO4=ZnSO4+H2↑ C.Na2CO3+2HCl=2NaCl+CO2↑+H2O D.CaCO3 CaO+CO2↑
本课件内嵌2个视频,即点即播,使用方便(此页可删除)。
Vide1:氢氧化钠、氯化钡与硫酸铜溶液的反应
Vide2:某些酸、碱、盐之间能否发生反应
视频:氢氧化钠、氯化钡与硫酸铜溶液的反应
探究复分解反应发生的条件
CuSO4+BaCl2=BaSO4↓+CuCl2
盐的化学性质(4):盐 + 盐 →新盐1 + 新盐2
视频:某些酸、碱、盐之间能否发生反应
HCl + NaOH =NaCl + H2O
NaHCO3 + HCl = NaCl + H2O + CO2↑
复分解反应发生的条件:生成______、______或____至少一种。
一、复分解反应发生的条件
某些酸、碱、盐之间能否发生反应
不符合复分解反应发生条件
(2)实际参加反应的离子是__________________。
1.(2019.河南)如图是氢氧化钠与盐酸反应示意图。
(1)反应前后没有发生变化的离子是__________。
用离子方程式表示下列反应的实质
H+ + OH-= H2O
Cu2+ + 2OH- =Cu(OH)2↓
Ba2+ + SO42- =BaSO4↓
2H+ + CO32- = CO2↑+H2O
复分解反应发生的条件就是至少有一对离子能反应生成沉淀/气体/水。
2H++ HCO3- = CO2↑+H2O
H+ + OH- → H2O
H+ + CO32- → H2O +CO2↑
OH-+Mg2+→Mg(OH)2↓白OH-+Cu2+ → Cu(OH)2↓蓝OH-+Fe3+ → Fe(OH)3↓红褐OH-+Fe2+ → Fe(OH)2↓白OH-+Al3+ → Al(OH)3↓白
OH-+ NH4+ = NH3↑+H2O
Ba2+ +SO42- =BaSO4↓白Ag+ + Cl- = AgCl↓白
Ba2++CO32- =BaCO3↓白Ca2++CO32- =CaCO3↓白
H++HCO3- → H2O + CO2↑
盐、碱的溶解性规律(P114)K+、Na+、NH4+、NO3-都易溶;氯化物中Ag+不溶;硫酸盐中Ba2+不溶;碳酸盐只溶K+、Na+、NH4+;Mg2+、Al3+、Fe2+/3+、Cu2+碱不溶
二、不共存(能反应)离子对
应用一、判断复分解反应能否发生
(1)Cu(OH)2 + HCl _____________________ (2)Ba(OH)2 + NaCl_____________________ (3)NaNO3 + BaCO3_____________________ (4)NaCl + H2SO4_______________________
2 = CuCl2 + 2H2O
→ BaCl2 + NaOH
→ Na2CO3 + Ba(NO3)2
→ Na2SO4 + HCl
1.下列各组离子中,在碱性溶液里能大量共存,且溶液为无色透明的是( ) A.K+、MnO4-、Cu2+、SO42- B.Na+、CO32-、NO3-、Cl- C.K+、Cu2+、SO42-、HCO3- D.H+、Na+、Cl-、SO42-2.在pH=4的溶液中能大量共存的是( )A.Na2SO4 、Ba(OH)2、HCl B.CuSO4、H2SO4、HNO3 C.FeCl3、NaOH、Ca(OH)2 D.K2SO4 、Na2CO3、NaCl
注意附加隐含条件:⑴溶液无色透明,则一定不含有色离子:Cu2+(蓝)、Fe2+(浅绿)、Fe3+(黄)、MnO4 +(紫)⑵酸性溶液、pH<7:存在H+; 碱性溶液、pH>7:存在OH-
阅读P77资料卡片“石笋和钟乳石的形成”,回答以下问题:1.钟乳石的“生长”属于_____(化学/物理)变化;2.发生反应的化学方程式:(1)_____________________________(2)_____________________________
CaCO3 + H2O + CO2 = Ca(HCO3)2
Ca(HCO3)2 =CaCO3↓ + H2O + CO2↑
H+ + OH- = H2O中和反应
544酸、碱盐的化学性质
相关课件
这是一份人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐公开课教学课件ppt,共18页。PPT课件主要包含了化学中的盐,盐的概念,生活中常见的盐,氯化钠的生理作用,氯化钠,氯化钠的用途,用氯化钠溶液来选种,生理盐水,食盐的制取,粗盐制取等内容,欢迎下载使用。
这是一份化学九年级下册第十一单元 盐 化肥课题1 生活中常见的盐图文课件ppt,共60页。PPT课件主要包含了课前导入,旧知复习,PART1,常见的几种碳酸盐,生活中常见的盐,白色固体易溶于水,小苏打,治疗胃酸过多,白色固体难溶于水,补钙剂等内容,欢迎下载使用。
这是一份化学课题1 生活中常见的盐教课课件ppt,共40页。PPT课件主要包含了课前导入,新闻事件,亚硝酸钠NaNO2,PART1,盐的定义,生活中常见的盐,物质该如何分类,物质分类,盐的分类,盐的命名等内容,欢迎下载使用。










