



2023届高三化学一轮复习 化工流程 课件
展开
这是一份2023届高三化学一轮复习 化工流程 课件,共60页。PPT课件主要包含了核心思想方法,相关知识点,一沉淀的生成,酸碱溶解法,二沉淀的溶解,沉淀的转化,原料的预处理,1调节pH值,抑制水解,③温度控制在某范围等内容,欢迎下载使用。
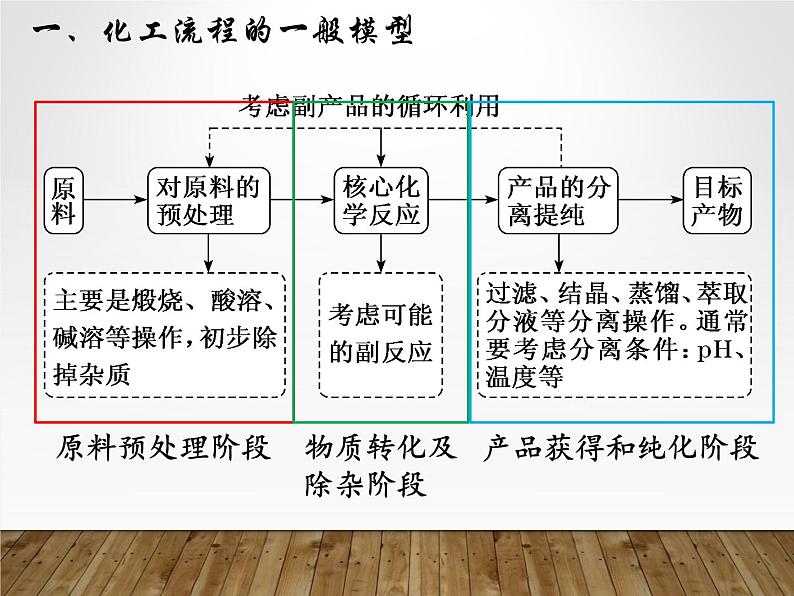
一、化工流程的一般模型
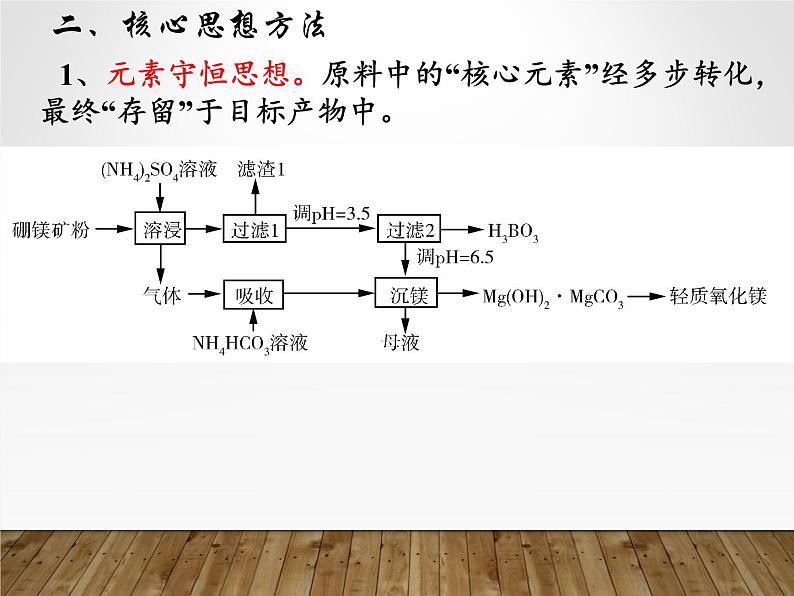
1、元素守恒思想。原料中的“核心元素”经多步转化,最终“存留”于目标产物中。
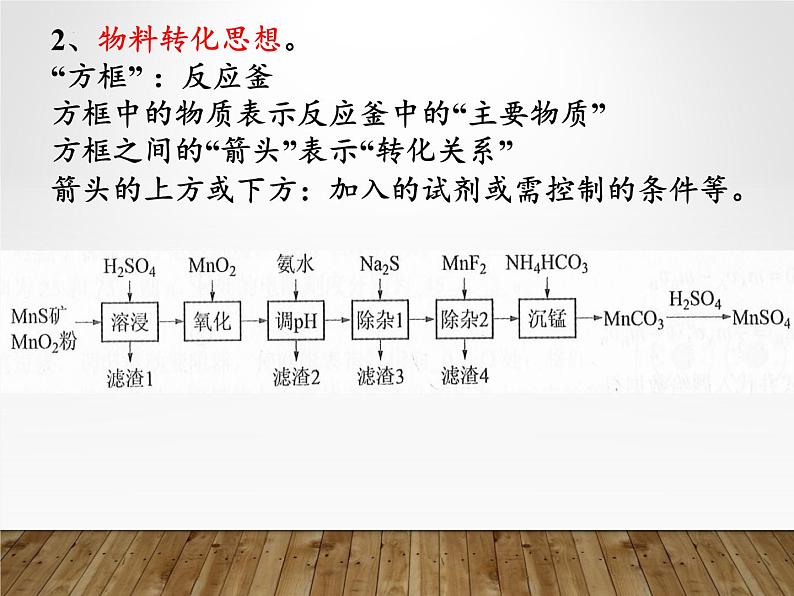
2、物料转化思想。“方框” :反应釜方框中的物质表示反应釜中的“主要物质”方框之间的“箭头”表示“转化关系”箭头的上方或下方:加入的试剂或需控制的条件等。
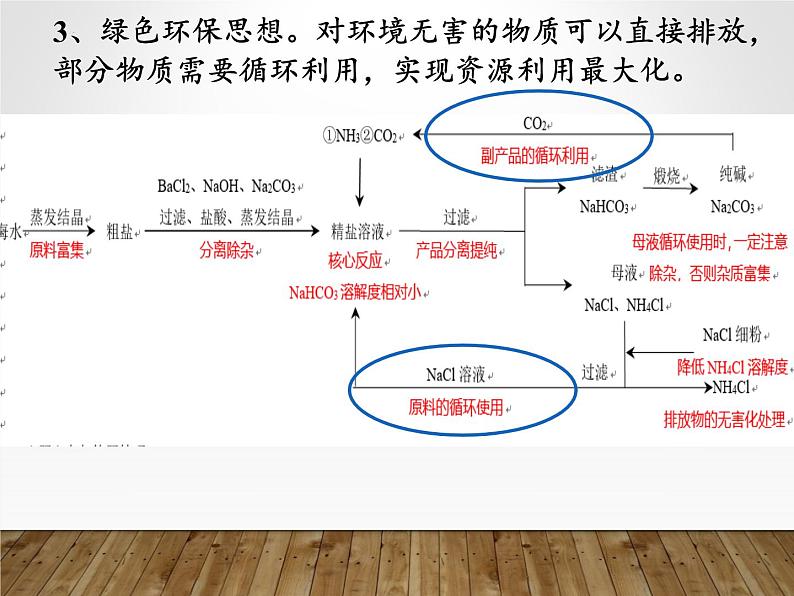
3、绿色环保思想。对环境无害的物质可以直接排放,部分物质需要循环利用,实现资源利用最大化。
【必修1】元素化合物:化合价、氧化性/还原性、离子反应、产率和纯度的计算、实验操作【必修1】氧化还原反应:陌生方程式的书写、产物判断、得失电子守恒、电荷守恒、原子守恒【必修2】元素周期律 / 元素周期表、化学键【选修4】电化学:电极判断、产物判断、方程式书写【选修4】弱电解质电离、盐类水解、沉淀溶解平衡、平衡常数相关计算
1、调节pH法除杂:NH4Cl(FeCl3)
除杂:CuCl2(FeCl3)
已知Ksp[Fe(OH)3]=10-38,求使0.1ml/L的FeCl3(aq)中Fe3+开始沉淀的pH和完全沉淀的pH。
加入CuO、Cu(OH)2 、CuCO3、Cu2(OH)2CO3等调节pH在3~4之间,保证Fe3+沉淀完全,Cu2+还未开始沉淀
MgCl2(FeCl2)
①先加入盐酸酸化的H2O2溶液或通入Cl2
②再加入MgO、Mg(OH)2、MgCO3调节pH
2、沉淀剂法如:用Na2S和H2S作沉淀剂,除去污水中的重金属离子
调节溶液极性使其沉淀,向CuSO4溶液中加入氨水至过量后加入无水乙醇产生深蓝色沉淀{Cu[NH3]4SO4·H2O}
加足量盐酸CaCO3+2H+===Ca2++H2O+CO2↑
CaCO3(s) ⇌ Ca2+(aq)+CO32-(aq)
FeS、MnS、NiS、ZnS:FeS + 2H+ == Fe2+ + H2S↑
2、盐溶解法:Mg(OH)2溶于NH4Cl溶液
3、氧化还原溶解法不溶于盐酸的硫化物CuS、Ag2S等溶于稀HNO3。4、配位溶解法:AgCl溶于氨水
沉淀转化的应用1、锅炉除水垢(除去水垢中的CaSO4 )
先加Na2CO3,再加盐酸
CaSO4+CO32- ⇌ CaCO3+SO42-,CaCO3+2HCl = CaCl2+H2O+CO2↑
2、矿物转化例如:原生铜硫化物变成CuSO4溶液,遇到深层闪锌矿(ZnS)和方铅矿(PbS)时,便慢慢地使之转变铜蓝(CuS)。
Cu2+(aq) + ZnS(s) = CuS(s) + Zn2+ (aq) Cu2+ (aq) + PbS(s) = CuS(s) + Pb2+ (aq) 。
3、利用沉淀转化原理,在工业废水的处理过程中,常用FeS(s) 、 MnS(s)等难溶物作为沉淀剂除去废水中的Cu2+、Hg2+、Pb2+等重金属离子。
FeS(s) + Hg2+(aq) ⇌ HgS(s) + Fe2+(aq)
将块状或颗粒状的物质磨成粉末或将液体分散成微小液滴,增大反应物接触面积,以加快反应速率或使反应更充分
与水接触反应或溶解(后过滤)
使用酸(HCl/HNO3/H2SO4)溶解固体:金属、金属氧化物(膜)、难溶弱酸盐(注意HNO3的氧化性,Fe3O4难溶于酸) 滤渣:SiO2、(注:H2SO4酸浸有CaSO4沉淀,Ca2+一般用CO32-、F-、C2O42-进行除去)
使用碱溶解固体:溶解金属表面油脂膜、酸性氧化物(SiO2)、Al2O3/Al、某些盐、非金属单质
固体溶解后,离子在溶液中的含量的多少
作用:①除去可燃物 ②是原料发生氧化、分解反应(如金属硫化物)③改变结构,使一些物质能溶解
固体加水(酸)溶解得到离子
例1、一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
2、常用的控制条件的方法
(2)控制温度:①低温(冷却):
b、防止挥发(如HCl、HNO3等收集AlCl3等)
c、防止分解(如H2O2、氨水、NaHCO3、NH4HCO3等铵盐)
d、增加气体溶解度,使气体充分吸收、防止气体挥发
②加热(升温):
a、提高物质的溶解或反应速率
b、减小气体的溶解度,使气体充分逸出
c、使固体充分气化、挥发、防止堵塞
d、使平衡正向移动,提高转化率r产率
a、确保催化剂活性最大 b、兼顾反应速率与化学平衡(特别是△H
相关课件
这是一份2024届高三化学高考备考一轮复习专题 化工流程题大题分析及备考建议课件,共3页。PPT课件主要包含了注重基础,图像推理分析能力,备考策略等内容,欢迎下载使用。
这是一份2024届高三化学高考备考一轮复习:化工流程中的Ksp计算与溶解平衡图像课件,共28页。
这是一份2023届高中化学一轮复习课件:无机化工流程题,共45页。PPT课件主要包含了氧化完全,Fe2+,Mn2+,Al3+和Fe3+,FeOH3,NH3,CO2,水浴加热,Ag+,分液漏斗等内容,欢迎下载使用。









