






所属成套资源:新人教版化学选择性必修1PPT课件全套
- 3.2《水的电离和溶液的pH》(第2课时)课件 课件 2 次下载
- 3.3《盐类的水解》(第1课时)课件 课件 4 次下载
- 3.4《沉淀溶解平衡》(第1课时)课件 课件 4 次下载
- 3.4《沉淀溶解平衡》(第2课时)课件 课件 2 次下载
- 4.1《原电池》(第1课时)课件 课件 3 次下载
人教版 (2019)选择性必修1第三节 盐类的水解完美版课件ppt
展开
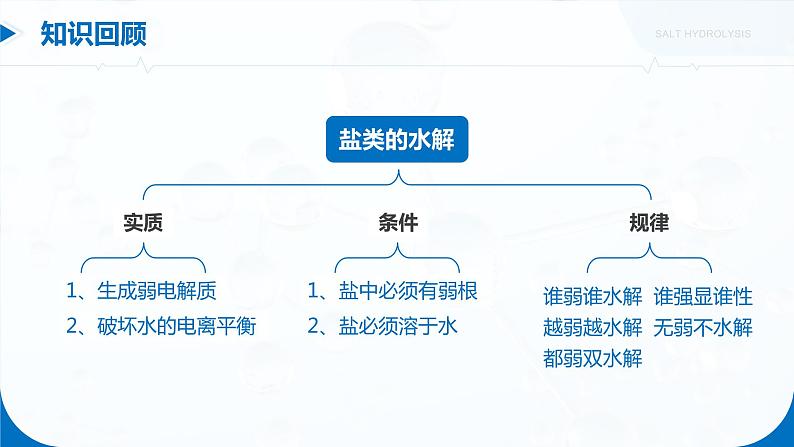
这是一份人教版 (2019)选择性必修1第三节 盐类的水解完美版课件ppt,共42页。PPT课件主要包含了生成弱电解质,破坏水的电离平衡,盐中必须有弱根,盐必须溶于水,知识回顾,HFHCN,HCN酸性弱,CN-水解程度大,生成的OH-浓度大,内因越弱越水解等内容,欢迎下载使用。
谁弱谁水解 谁强显谁性 越弱越水解 无弱不水解 都弱双水解
F- + H2O ⇌ HF + OH-
CN- + H2O ⇌ HCN + OH-
已知浓度相同的NaF和NaCN溶液, NaCN溶液的pH远大于NaF,分析其原因?
盐水解生成的弱酸或弱碱越弱,水解程度就越大,溶液相应的碱性或酸性就越强
NH4Cl < AlCl3
②比较等浓度 NH4Cl溶液与AlCl3溶液的酸性:
①已知酸性:CH3COOH>H2CO3>HClO>HCO3-,比较等浓度CH3COONa,Na2CO3,NaHCO3,NaClO碱性
Na2CO3 > NaClO > NaHCO3> CH3COONa
反应物的性质(越弱越水解)
一、影响盐类水解的因素
同物质的量浓度NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10,则相对应的酸:HX、HY、HZ的酸性比较。
盐类的水解程度受到盐的浓度、温度及溶液酸碱度的影响 --符合勒夏特列原理
水解是中和反应的逆反应,
是吸热反应(△H>0)。
升高温度,盐类水解平衡向正反应方向移动有利于盐类的水解。--越热越水解
2. 外因(外界条件)
a. 加水(减小浓度):
b. 加溶质(增大浓度):
即:酸可抑制阳离子水解,促进阴离子水解;碱可抑制阴离子水解,促进阳离子水解。
对强碱弱酸盐,加酸促进水解,加碱抑制水解。对强酸弱碱盐,加酸抑制水解,加碱促进水解。
水解情况相同的离子的水解相互抑制水解情况相反的离子的水解相互促进(双水解)
在0.01ml/LFeCl3溶液中:
Fe3++3H2O⇌Fe(OH)3 + 3H+
比较下列溶液的pH大小(填“>”“c(HCO3-)>c(CO32-)>c(H+)>c(OH-)(B)c(Na+)+c(H+)=c(OH-)+c(CO32-) +c(HCO3-)(C)c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)(D)c(Na+)=c(HCO3-)+c(H2CO3)+c(OH-)(E)c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-)
在0.2ml/L的NH4Cl溶液中,下列关系式正确的是( )A.c(Cl-)> c( NH4+ ) >c( H+ ) >c( OH- )B.c( NH4+ ) > c(Cl- ) >c( H+ ) >c( OH- )C. c(Cl- ) =c( NH4+ ) >c(H+ ) =c( OH- ) D.c( NH4+ ) =c(Cl- ) >c( H+ ) >c( OH- )
将10mL0.1ml/L氨水和10mL0.1ml/L盐酸混合后, 溶液里各种离子物质的量浓度的关系是 ( )A.C(Cl-)+C(OH-)=C(NH4+)+C(H+) B. C(Cl-)> C(NH4+)> C(H+) > C(OH-)C.C (H+) > C(OH-)>C (Cl-)>C(NH4+) D.C(Cl-)> C(H+) >C (NH4+)>C (OH-)
下列根据反应原理设计的应用,不正确的是( )A.CO32-+H2O⇌HCO3-+OH-热的纯碱溶液清洗油污B.Al3++3H2O ⇌ Al(OH)3+3H+明矾净水C.TiCl4+(x+2)H2O(过量) ⇌ TiO2·xH2O+4HCl用TiCl4制 备TiO2D.SnCl2+H2O ⇌ Sn(OH)Cl+HCl配制氯化亚锡溶液时加入氢氧化钠
1、决定因素(内因):
2、外界条件(外因):
(1)浓度:(2)温度:(3)外加酸、碱:
相关课件
这是一份人教版 (2019)选择性必修1第三节 盐类的水解教学ppt课件,共60页。PPT课件主要包含了呈酸性,呈碱性,呈中性,科学探究,①③④,课堂练习等内容,欢迎下载使用。
这是一份化学选择性必修1第三节 盐类的水解一等奖ppt课件,共28页。PPT课件主要包含了你知道吗,知识回顾,活动与探究,盐溶液的酸碱性,盐类的水解,如AlCl3,②完全双水解等内容,欢迎下载使用。
这是一份2021学年第三节 盐类的水解课堂教学课件ppt,共55页。PPT课件主要包含了你知道吗,生成的盐,强酸强碱盐,强酸弱碱盐,强碱弱酸盐,弱酸弱碱盐,③④⑦⑧,①⑤⑥⑩,相互作用,促进水的电离等内容,欢迎下载使用。










