



【新高考】2023年高考化学二轮题型精讲精练——专题13 反应微观机理分析
展开专题13 反应微观机理分析
目录
一、热点题型归纳………………………………………………………………………………………………………1
【题型一】普通化学反应历程分析……………………………………………………………………………………1
【题型二】化学反应历程图像分析……………………………………………………………………………………1
【题型三】无机循环历程图像分析……………………………………………………………………………………3
【题型四】有机循环历程图像分析……………………………………………………………………………………5
【题型五】能量反应过程图像分析……………………………………………………………………………………6
二、最新模考题组练……………………………………………………………………………………………………9
【题型一】普通化学反应历程分析
【典例分析】
【典例1】(江苏省百校大联考2022届高三上学期第二次考试)东南大学王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还原合成氨。
已知:
第一步:*+H+e-*H(快)(吸附在催化剂表面的物种用*表示);
第二步:N2+2*H中间体(吸附在催化剂表面)(慢);
第三步:……(快)。
下列说法不正确的是( )。
A.上述三步中的决定速率步骤为第二步
B.第三步可表示为2*NH+4H++4e-2NH3
C.该法在合成氨的过程中能量的转化形式是电能转化为化学能
D.该法较传统工业合成氨法,具有能耗小、环境友好的优点
【提分秘籍】
1.反应历程:由基元反应构成的反应序列,又称反应机理
(1)总反应:2NO+2H2N2+2H2O
(2)反应历程
①2NO+H2N2O+H2O(慢)
②2N2O2N2+O2(快)
③2H2+O22H2O(更快)
(3)决速反应:在反应历程中,反应速率最慢的基元反应
(4)决速浓度:最慢反应中反应物的浓度决定总反应的反应速率
2.简单的催化反应
(1)催化剂:第①步反应的反应物,第②步反应的生成物
(2)中间产物:第①步反应的生成物,第②步反应的反应物
【变式演练】
1.(2022·内蒙古赤峰高三2月模拟)已知温度不同,NO2和CO之间发生反应的机理不同。
①673K时,NO2和CO发生基元反应(即一步完成):NO2+CO=NO+CO2,其反应过程如图所示:
②473K时,则经过两步反应,反应机理是:NO2+NO2→NO+NO3(慢),CO+NO3→NO2+CO2(快)。
下列有关说法错误的是( )。
A.相同条件下,活化分子的能量比对应反应物分子的能量高
B.473K时,总反应速率由第一步决定
C.使用催化剂可增加活化分子百分数,提高NO2的平衡转化率
D.温度不同反应机理不同,但都经历氮氧键断裂和碳氧键生成的过程
2.(2022届辽宁省高三实战猜题卷)氧化亚氮在碘蒸气存在时的热分解反应:2N2O2N2+O2,其反应机理包含以下步骤:
第一步:I2(g)2I(g)(快反应)
第二步:I(g)+N2O(g)N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)N2(g)+O2(g)+I(g)(快反应)
下列说法错误的是( )。
A.第二步对分解反应速率起决定作用
B.I2浓度与N2O分解速率无关
C.慢反应的活化能高于快反应的活化能
D.第二步反应中I(g)作氧化剂
【题型二】化学反应历程图像分析
【典例分析】
【典例2】(2020·北京市等级考)硫酸盐(含SO42-、HSO4-)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是( )。
A.该过程有H2O参与
B.NO2是生成硫酸盐的氧化剂
C.硫酸盐气溶胶呈酸性
D.该过程没有生成硫氧键
【提分秘籍】
1.化学反应的本质
(1)宏观:有新物质生成
(2)微观:旧化学键的断裂,新化学键的形成
2.化学键与能量变化:成键放热,断键吸热
3.化学键的极性
(1)极性键:不同元素原子形成的共价键
(2)非极性键:同种元素原子形成的共价键
4.原子利用率
(1)原子利用率=×100%
(2)原子经济百分数=×100%
(3)原子利用率100%的反应类型
①无机反应:化合反应
②有机反应:加成反应和加聚反应
【变式演练】
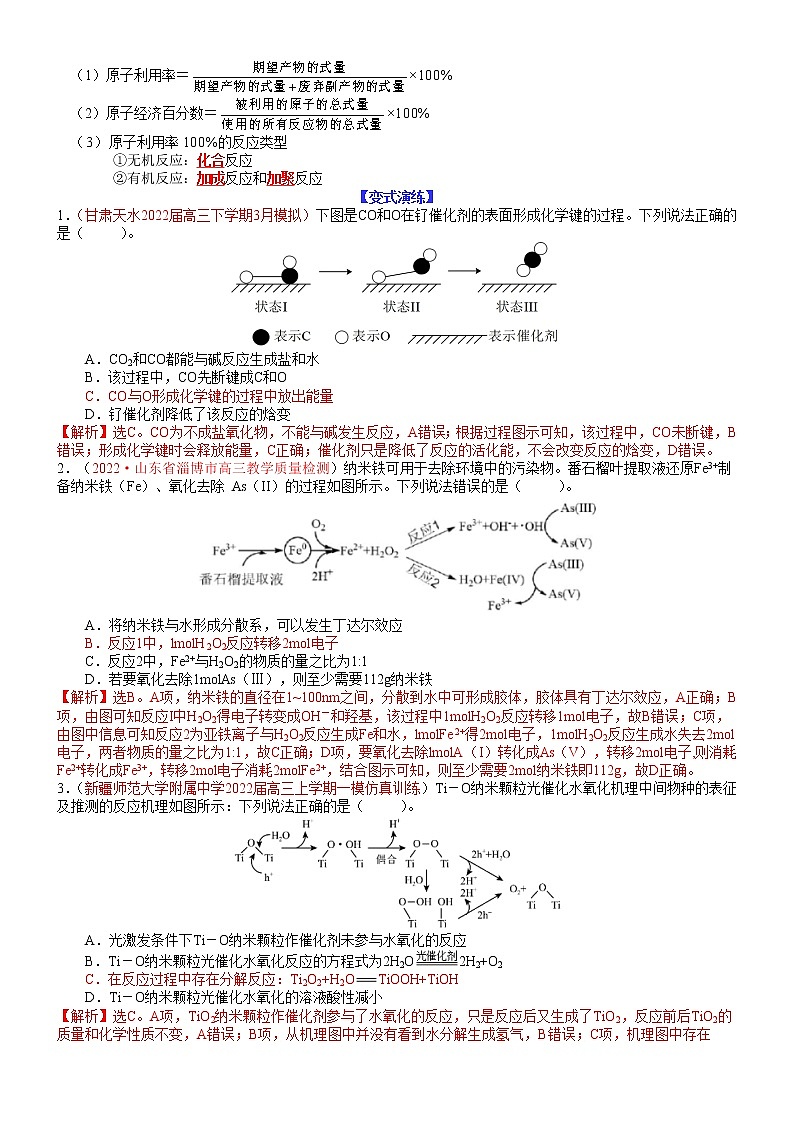
1.(甘肃天水2022届高三下学期3月模拟)下图是CO和O在钌催化剂的表面形成化学键的过程。下列说法正确的是( )。
A.CO2和CO都能与碱反应生成盐和水
B.该过程中,CO先断键成C和O
C.CO与O形成化学键的过程中放出能量
D.钌催化剂降低了该反应的焓变
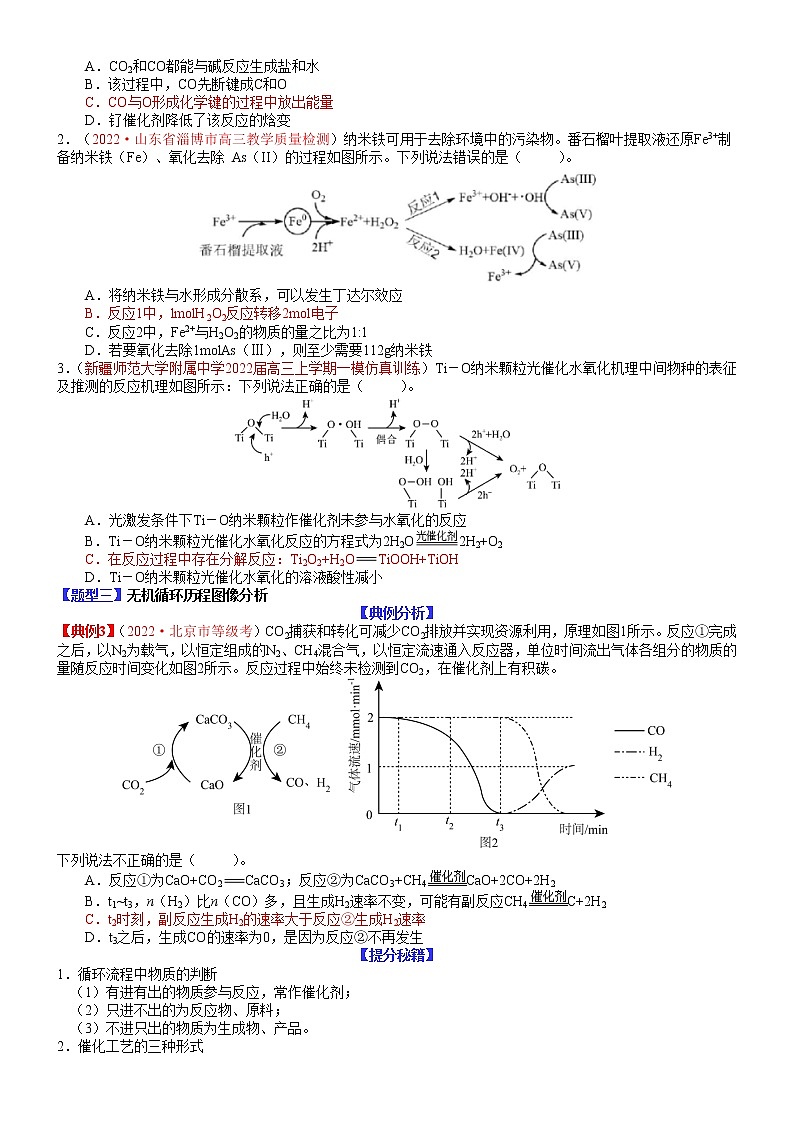
2.(2022·山东省淄博市高三教学质量检测)纳米铁可用于去除环境中的污染物。番石榴叶提取液还原Fe3+制备纳米铁(Fe)、氧化去除 As(II)的过程如图所示。下列说法错误的是( )。
A.将纳米铁与水形成分散系,可以发生丁达尔效应
B.反应1中,lmolH2O2反应转移2mol电子
C.反应2中,Fe2+与H2O2的物质的量之比为1:1
D.若要氧化去除1molAs(Ⅲ),则至少需要112g纳米铁
3.(新疆师范大学附属中学2022届高三上学期一模仿真训练)Ti-O纳米颗粒光催化水氧化机理中间物种的表征及推测的反应机理如图所示:下列说法正确的是( )。
A.光激发条件下Ti-O纳米颗粒作催化剂未参与水氧化的反应
B.Ti-O纳米颗粒光催化水氧化反应的方程式为2H2O2H2+O2
C.在反应过程中存在分解反应:Ti2O2+H2OTiOOH+TiOH
D.Ti-O纳米颗粒光催化水氧化的溶液酸性减小
【题型三】无机循环历程图像分析
【典例分析】
【典例3】(2022·北京市等级考)CO2捕获和转化可减少CO2排放并实现资源利用,原理如图1所示。反应①完成之后,以N2为载气,以恒定组成的N2、CH4混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO2,在催化剂上有积碳。
下列说法不正确的是( )。
A.反应①为CaO+CO2CaCO3;反应②为CaCO3+CH4CaO+2CO+2H2
B.t1~t3,n(H2)比n(CO)多,且生成H2速率不变,可能有副反应CH4C+2H2
C.t2时刻,副反应生成H2的速率大于反应②生成H2速率
D.t3之后,生成CO的速率为0,是因为反应②不再发生
【提分秘籍】
1.循环流程中物质的判断
(1)有进有出的物质参与反应,常作催化剂;
(2)只进不出的为反应物、原料;
(3)不进只出的物质为生成物、产品。
2.催化工艺的三种形式
(1)直接型
(2)微观型
(3)循环型
①反应物:A和F
②生成物:B和E
③催化剂:C或D,中间产物D或C
【变式演练】
1.(2020·全国Ⅱ卷)据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是( )。
A.OH-参与了该催化循环
B.该反应可产生清洁燃料H2
C.该反应可消耗温室气体CO2
D.该催化循环中Fe的成键数目发生变化
2.(北京市西城区2022届高三下学期一模)氮掺杂的碳材料可以有效催化燃料电池中O2的还原反应,其催化机理如图。
途径一:A→B→C→F;途径二:A→B→C→D→E。下列说法不正确的是( )。
A.途径一中存在极性共价键的断裂与形成
B.途径一的电极反应是2H++O2+2e-H2O2
C.途径二,1molO2得到4mol e-
D.氮掺杂的碳材料降低了反应的焓变
3.(福建省厦门市2022届高三下学期3月第二次质量检测)利用化学链将高炉废气中CO2转化为CO的示意图如下。下列说法不正确的是( )。
A.Fe3O4和CaO可循环利用
B.反应④为吸热反应
C.该化学链的总反应是CO2+H2H2O+CO
D.该方法可降低分离CO和N2所需的能耗
【题型四】有机循环历程图像分析
【典例分析】
【典例4】(2022·山东省等级考)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是( )。
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C3H8的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【变式演练】
1.(2022·广东省等级考)我国科学家进行了如图所示的碳循环研究。下列说法正确的是( )。
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C.1molCO中含有6.02×1024个电子
D.22.4LCO2被还原生成1molCO
2.(2021·湖北省选择考)甲烷单加氧酶(s-mmo)含有双核铁活性中心,是O2氧化CH4生成CH3OH的催化剂,反应过程如图所示。下列叙述错误的是( )。
A.基态Fe原子的核外电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH4+O2+2H++2e-CH3OH+H2O
3.(2020年·全国卷Ⅰ)铑的配合物离子[Rh(CO)2I2]-可催化甲醇羰基化,反应过程如图所示。
下列叙述错误的是( )。
A.CH3COI是反应中间体
B.甲醇羰基化反应为CH3OH+CO=CH3CO2H
C.反应过程中Rh的成键数目保持不变
D.存在反应CH3OH+HI=CH3I+H2O
【题型五】能量反应过程图像分析
【典例分析】
【典例5】(2021·山东省等级考)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
能量变化如图所示。已知为快速平衡,下列说法正确的是( )。
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH318OH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【提分秘籍】
1.反应热性质的判断
(1)放热反应:反应物的能量和大于生成物的能量和
(2)吸热反应:反应物的能量和小于生成物的能量和
2.反应热的判断:看反应物和生成物能量和的差值
(1)正反应的反应热:△H正=-(Ea′-Ea)kJ·mol-1
(2)逆反应的反应热:△H逆=+(Ea′-Ea)kJ·mol-1
3.微粒稳定性的判断:能量低的微粒稳定性强
4.催化剂和中间产物(过渡态物质)的判断
(1)催化剂:第一步反应的反应物,第二步反应的生成物
(2)过渡物:第一步反应的生成物_,第二步反应的反应物
5.曲线上的峰
(1)峰的个数表示中间反应的个数,不一定表示中间产物的种类
(2)峰谷
①峰前的峰谷:表示该中间反应反应物的能量
②峰后的峰谷:表示该中间反应生成物的能量
6.活化能
(1)正反应的活化能:反应物到最高点的能量差Ea正=EakJ·mol-1
(2)逆反应的活化能:生成物到最高点的能量差Ea逆=EakJ·mol-1
(3)活化能和反应热的关系
①放热反应:Ea正<Ea逆
②吸热反应:Ea正>Ea逆
(4)活化能和反应速率的关系:活化能越大,反应速率越慢
(5)催化剂对反应的影响
①催化剂参与反应,降低反应的活化能,加快反应速率
②催化剂不能改变反应热,可以降低反应所需的温度,减小反应的能耗
③总反应的活化能大于催化反应过程中各分反应的活化能
④催化剂具有选择性:相同反应物用不同催化剂生成物不同
A+BC A+BD
【变式演练】
1.(2020·天津等级考真题)理论研究表明,在101kPa和298K下,HCN(g)HNC(g)异构化反应过程的能量变化如图所示。下列说法错误的是( )。
A.HCN比HNC稳定
B.该异构化反应的△H=+59.3kJ•mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
2.(百师联盟2022届高三下学期二轮联考)CH3-CH=CH-COOCH3有两种立体异构体和,由CH3CHO和Ph3P=CHCOOCH3反应制取这两种异构体的历程中能量变化如图:
已知:在立体结构中,实线表示该键在纸平面上,实楔形线表示该键在纸前方,虚线表示该键在纸后方。下列说法正确的是( )。
A.比稳定
B.温度升高,CH3CHO的转化率减小
C.生成的过程中,速率最快的是由生成的反应
D.两个反应历程中,中间产物相同
3.(2022·黑龙江哈尔滨高三3月模拟)三甲胺(N(CH3)3)是重要的化工原料,最近我国科学家发明了使用铜催化剂将N,N-二甲基甲酰胺[N(CH3)2CHO,简称为DMF]转化为三甲胺的合成路线,单一DMF分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是( )。
A.该历程中决速步骤为:(CH3)2NCH2OH*=(CH3)2NCH2+OH*
B.该反应的原子利用率为100%,该历程中的最大能垒(活化能)为2.16eV
C.升高温度可以加快反应速率,并提高DMF的平衡转化率
D.若1molDMF完全转化为三甲胺,则会释放出1.02eV·NA的能量
1.(2022~2023学年河南漯河高三11月模拟)已知分解1molKClO3放出热量38.8kJ,在存在MnO2条件下加热,KClO3的分解机理为:
①2KClO3+4MnO22KCl+2Mn2O7(慢)
②2Mn2O74MnO2+3O2(快)
下列有关说法中不正确的是( )。
A.1molKClO3所具有的总能量高于1molKCl和1.5molO2所具有的总能量
B.KClO3分解速率快慢主要取决于反应①
C.1gKClO3、1gMnO2和0.1gMn2O7混合加热,充分反应后MnO2质量为1g
D.将固体二氧化锰碾碎,可加快KClO3的分解速率
2.(贵州省遵义市2022届高三4月统一模拟测试)冬季燃煤排放的大量活性溴化合物BrCl能通过光解释放溴自由基和氯自由基,从而影响大气中自由基(OH、HO2)的浓度,其循环原理如图所示。下列说法不正确的是( )。
A.NO2的排放会造成酸雨
B.向原煤中添加石灰石有利于实现“碳达峰、碳中和”
C.通过上述循环,大气中OH自由基的浓度升高
D.BrCl的排放会造成臭氧含量减小
3.(新疆师大附中2022届高三一模)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图,下列说法不正确的是( )。
A.该过程的总反应为H2+O2H2O2
B.生成1molH2O2的过程中,转移电子总数为4mol
C.[PdCl4]2-在此过程中作为催化剂
D.历程中发生了Pd+O2+2Cl-[PdCl2O2]2-
4.(2022届广东省广州市高三上学期12月调研)双碱法脱除烟气中SO2的过程如图所示。下列说法中不正确的是( )。
A.过程I中,SO2表现出还原性
B.过程II中,1molO2可氧化2molNa2SO3
C.脱除SO2的过程中,NaOH可以循环利用
D.总反应为:2SO2+2Ca(OH)2+O22CaSO4+2H2O
5.(保定市部分学校2022届高三上学期期中考试)实验室常用MnO4-标定(NH4)2Fe(SO4)2,同时使MnO4-再生,其反应原理如图。下列说法正确的是( )。
A.反应1中S2O82-中的硫元素被还原
B.只发生反应1或只发生反应2时溶液颜色均发生了变化
C.S2O82-和I-、SO32-能在水溶液中大量共存
D.将反应2设计成原电池,放电时Fe2+向正极迁移
6.(海安市2022届高三期初学业质量监测)硝酸盐污染已成为一个日益严重的环境问题,甲酸(HCOOH)在纳米级Pd表面分解为活性H2和CO2,再经下列历程实现NO3-的催化还原,进而减少污染。已知Fe(Ⅱ)、Fe(Ⅲ)表示Fe3O4中二价铁和三价铁。下列说法不正确的是( )。
A.Fe3O4参与了该循环历程
B.HCOOH分解时,碳氢健和氧氢健发生了断裂
C.H2在反应历程中生成的H+起到调节体系pH的作用
D.在整个历程中,每1mol H2可还原1molNO3-
7.(2022年1月浙江选考仿真模拟卷B)钒元素用途广泛,如图是一种钒的化合物催化某反应的反应机理。下列叙述错误的是( )。
A.H2O参与了该催化反应
B.过程①中反应的原子利用率为100%
C.该催化循环过程中有氢氧键的断裂和形成
D.每次循环的净反应为H2O2+2Cl-2HOCl+2e-
8.(湖南湘东名校2023届第一次联考)某科研人员研究得出,HCHO可在羟基磷灰石(HAP)表面催化氧化生成CO2和H2O,其历程示意图如图(图中只画出了HAP的部分结构)。
下列说法错误的是( )。
A.HAP不能提高HCHO与O2的平衡转化率
B.HCHO在反应过程中,有C-H键发生断裂
C.根据图示信息,CO2分子中的氧原子全部来自O2
D.该过程的总反应是HCHO+O2CO2+H2O
9.(河南省新未来2023届高三上学期9月联考)氮肥是保证粮食安全的重要物资,某种制备NH3的转化历程如图所示.下列说法错误的是( )。
A.步骤Ⅰ中发生的反应为4LiOH(熔融)4Li+O2↑+2H2O
B.该转化历程没有涉及置换反应
C.该转化历程的总反应为2N2+6H2O4NH3+3O2
D.O2的氧化性强于N2
10.(河南省十所名校2023届高三尖子生第一次考试)由Rh2VO1~3-簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。
下列说法错误的是( )。
A.Rh2VO1~3-在循环中起催化作用
B.该反应可用于制取合成气CO、H2
C.过程中包含反应Rh2VO1~3-Rh2VO-+CO↑+H2↑
D.反应过程中金属元素Rh、V的价态均不变
11.(湖南省三湘创新发展联合2022~2023学年高三上学期起点调研)硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、CuCl2和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是( )。
A.历程①发生反应S2-+Cu2+CuS↓
B.历程②中CuS作氧化剂
C.历程③中n(Fe2+)∶n(O2)=4∶1
D.若要吸收34gH2S,则至少要通入标准状况下56L空气(空气中氧气体积按20%计)
12.(湖南省永州市第一中学2022~20223学年高三下学期入学考试)在酸性环境中,纳米Fe/Ni复合材料去除污染水体的NO3-的反应过程(Ni不参与反应)如图所示:
下列表达反应过程或现象的方程式错误的是( )。
A.反应步骤ⅰ:NO3-+Fe+2H+NO2-+Fe2++H2O
B.反应步骤ⅱ:NO2-+3Fe+8H+3Fe2++NH4++2H2O
C.反应进行一段时间,过滤出水体中出现的白色絮状物,白色絮状物在空气中最终变成红褐色:4Fe(OH)2+O2+2H2O4Fe(OH)3
D.硝酸亚铁溶液中滴加稀硫酸发现溶液变黄:2Fe2++4H++SO42-2Fe3++SO2↑+2H2O
13.(山东威海乳山市2022~2023学年高三上学期期中)近期我国科技工作者开发了高效NO净化催化剂(用M表示),实现NO减排,其催化原理如图所示(□代表氧空位)。下列说法错误的是( )。
A.反应过程中有O-H的断裂和生成
B.反应过程中Ce的成键数目未发生改变
C.反应过程中Ti的化合价发生了改变
D.催化循环的总反应为:4NH3+4NO+O24N2+6H2O
14.(重庆市2022~2023学年高三上学期半期质量监测)向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜。其反应过程如图所示。
下列说法不正确的是( )。
A.Fe3+对该反应有催化作用
B.该过程中的Fe3+可由Fe(NO3)3提供
C.可用K3[Fe(CN)6]溶液区分Fe3+与Fe2+
D.制备CuCl2的总反应为2Cu+O2+4HCl2CuCl2+2H2O
15.(2023年1月浙江省选考仿真模拟卷C)我国科学家通过双功能催化剂催化水煤气变换反应:CO(g)+H2O(g)CO2(g)+H2(g)△H<0,此时该反应总熵变记作△S。低温即可获得高转化率和高反应速率,反应过程示意图如图:
下列说法不正确的是( )。
A.△H=△H1+△H2+△H3+△H4
B.△S=△S1+△S2+△S3+△S4
C.状态III→状态IV过程的△S3<0,△H3<0
D.催化剂的使用使反应放出热量增多,温度升高导致反应速率加快
16.(江西省赣抚吉名校2022届高三联考)亚硝酰氯在有机合成中有重要应用。2NO(g)+Cl2(g)=2NOCl(g)的反应历程如图所示。下列说法错误的是( )。
A.催化剂能提高反应物的相对能量
B.相对曲线II,曲线I表示加入催化剂
C.曲线II的正反应活化能为15.5kJ·mol-1
D.2NO(g)+Cl2(g)=2NOCl(g)△H=-77.1kJ·mol-1
17.(“超级全能生”2022高考全国卷地区5月联考)如图表示2-甲基-2-溴丙烷发生水解的反应历程,下列说法正确的是( )。
A.由图可知反应有两个过渡态无法判断反应的热效应
B.增大c(NaOH),总反应的速率会增大
C.反应中存在C-Br键的断裂和C-O键的形成
D.若第一阶段转化率为30%,第二阶段转化率为40%,则最终产物的产率为12%
18.(2022·黑龙江大庆高三3月模拟)如图是CH4与Zr形成过渡金属化合物的过程。下列说法不正确的是( )。
A.整个反应快慢,由CH2-Zr…H2→状态2反应决定
B.Zr+CH4→CH3-Zr…H活化能为213.6kJ·mol-1
C.在中间产物中CH3-Zr…H状态最稳定
D.Zr+CH4→CH-Zr…H3∆H=+39.54kJ·mol-1
19.(2022·湖南永州高三4月模拟)活泼自由基与氧气的反应一直是关注的热点。HNO自由基与O2反应过程的能量变化如图所示:
下列说法正确的是( )。
A.该反应为吸热反应
B.相同条件下,P1比P2更稳定
C.该历程中最大正反应的活化能Ea=215.49kJ·mol-1
D.相同条件下,由中间产物Z转化为产物的速率:v(P1)>v(P2)
20.(湖南省常德市2023届高三上学期期中)在超临界水中进行碳碳加成反应时存在两条不同的路径,其反应机理如图所示。下列有关说法错误的是( )。
A.比稳定
B.反应生成的活化能为54.0kJ·mol−1
C.和互为同分异构体
D.选择适当的催化剂,有可能改变不同路径产物的产量
21.(四川省遂宁市高2023届高三零诊)我国科学家合成了Y、Sc(Y1/NC,Sc1/NC)单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是( )。
A.相同条件下,Sc1/NC比Y1/NC催化剂更利于吸附氮气
B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率
C.使用Sc1/NC单原子催化剂,反应的快慢由生成*NNH的速率决定
D.工业合成氨与电化学催化还原氮气均涉及到共价键的断裂与形成
22.(重庆市2022~2023学年高三上学期半期质量监测)Ni可活化C2H6放出CH4,其反应历程如图所示。下列关于活化历程的说法正确的是( )。
A.决速步骤:中间体1→中间体2
B.在此反应过程中Ni的成键数目没有发生变化
C.涉及非极性键的断裂和生成
D.总反应为Ni(s)+C2H6(g)NiCH2(s)+CH4(g)ΔH=-6.57kJ/mol
23.(安徽A10联盟2023届高三开学摸底考)在Ni作用下,可将C2H6(g)转化为CH4(g),转化历程如下(NiCH2为固体)所示:
下列说法中错误的是( )。
A.总反应的热化学方程式为Ni(s)+C2H6(g)=NiCH2(s)+CH4(g)AH=-6.57kJ·mol-1
B.转化过程中的一段时间内,可存在中间体2的浓度大于另外两种中间体的浓度
C.转化中断裂与形成的共价键种类不同查
D.转化过程中Ni的成键数目未变化
24.(2022~2023学年甘肃省张掖市高三上学期第一次诊断)GeorgeA.Olah教授和其合作者使用Ru-PNPpincer络合物作催化剂,用五乙烯六胺(PEHA)多聚物来捕获二氧化碳,可以直接将空气中二氧化碳转化为甲醇,反应可能的过程如图所示。下列叙述错误的是( )。
A.甲醇可作为车用燃料
B.总反应方程式为CO2+3H2H2O+CH3OH
C.循环过程中催化剂参与中间反应
D.反应过程中只有极性键的断裂和形成
25.(河北省邯郸市2022~2023学年高三上学期摸底)(不定项)某科学家首次发现在温和的条件下利用LnPd和CuX做共同催化剂,卤代烃和炔烃发生偶联反应,其偶联反应机理如图。已知:R1、R2为烃基,X为卤素原子,下列说法正确的是( )。
A.Pd在此偶联反应的机理图中共呈现了3种价态
B.每步反应均存在极性键的断裂和形成
C.该偶联反应的总反应为R1-X+R2-C≡CHHX+R2-C≡C-R1
D.若R1、R2分别为甲基、乙基,反应除生成2-戊炔外,还能生成2-丁炔和2-己炔
26.(宁波市2023学年第一学期选考模拟)可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表)下列说法不正确的是( )。
A.反应I过程中有水生成
B.反应IV涉及加成反应和消去反应
C.该过程反应原料为硝基苯和苯甲醇
D.用CH3CH2CH2OH替代上述过程中的同类物质参与反应,可以合成
27.(2023年1月浙江省选考仿真模拟卷C)TRAP是一种温和的氧化剂,TRAP试剂中的RuO4-不会氧化碳碳双键,可以将醇仅氧化至醛,不会过度氧化为羧酸。TRAP氧化醇的反应机理如下图,下列说法不正确的是( )。
A.在上述6步反应中发生氧化还原反应的不至2步
B.步骤④⑤中NMO将RuO3-还原,生成TRAP试
C.步骤⑥的离子方程式为2RuO3-=RuO2+RuO42-
D.若R1为CH3CH=CH-,R2为-H,则TRAP氧化该醇的主产物为2-丁烯醛
28.(2023年1月浙江省选考仿真模拟卷B)铼的配合物(ReO3CH3,用MTO表示)可催化醛烯烃基化,反应过程如图所示。
下列叙述错误的是( )。
A.ReO2(CH3)=CR1R2是反应的中间体
B.醛烯烃基化反应为N2=CR1R2+R3CHO+P(C6H5)3R3CH=CR1R2+N2↑+O=P(C6H5)3
C.有机物N2=CR1R2中的N原子最外层满足8电子结构,则N与N原子之间是单键
D.存在反应:+3P(C6H5)3→O=P(C6H5)3+
29.(湖南永州市2023年高考第一次适应性考试)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。
下列说法错误的是( )。
A.催化剂BMO能降低反应的活化能,但不能改变反应的焓变
B.反应①和②中转移的e-数目相等
C.整个过程中参与反应的n(苯酚)∶n(O2)=1∶7
D.过程①的反应为:
30.(2022年江苏湖州高三3月模拟)(不定项)使用NC环金属化Ir(III)配合物催化甲酸脱氢的反应机理如下图。下列说法中错误的是( )。
A.甲酸脱氢过程的总反应为HCOOHCO2↑+H2↑
B.反应过程中,Ir(III)配合物A为催化剂,Ir(III)配合物B为中间产物
C.由D→E的过程,是甲酸协助转运H的过程
D.反应过程中,HCOOH中的C=O键发生断裂
题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用): 这是一份题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用),文件包含题型10反应微观机理分析速率方程及其应用原卷版docx、题型10反应微观机理分析速率方程及其应用解析版docx等2份试卷配套教学资源,其中试卷共79页, 欢迎下载使用。
【高考二轮复习】2023年高考化学精讲+精练+小测(全国通用)——专题10 化学反应机理与历程(讲)(原卷版+解析版): 这是一份【高考二轮复习】2023年高考化学精讲+精练+小测(全国通用)——专题10 化学反应机理与历程(讲)(原卷版+解析版),文件包含专题10化学反应机理与历程讲教师版docx、专题10化学反应机理与历程讲学生版docx等2份试卷配套教学资源,其中试卷共35页, 欢迎下载使用。
【高考二轮复习】2023年高考化学精讲+精练+小测(全国通用)——专题10 化学反应机理与历程(练)(原卷版+解析版): 这是一份【高考二轮复习】2023年高考化学精讲+精练+小测(全国通用)——专题10 化学反应机理与历程(练)(原卷版+解析版),文件包含专题10化学反应机理与历程练解析版docx、专题10化学反应机理与历程练原卷版docx等2份试卷配套教学资源,其中试卷共101页, 欢迎下载使用。












