
所属成套资源:2021-2022学年高中化学高一(下)月考化学试卷(含答案解析)真题合集
2021-2022学年湖南省岳阳四中高一(下)第一次月考化学试卷(含答案解析)
展开
这是一份2021-2022学年湖南省岳阳四中高一(下)第一次月考化学试卷(含答案解析),共17页。试卷主要包含了 下列物质中含有共价键的盐是, 有下列氧化还原反应, 下列说法正确的是等内容,欢迎下载使用。
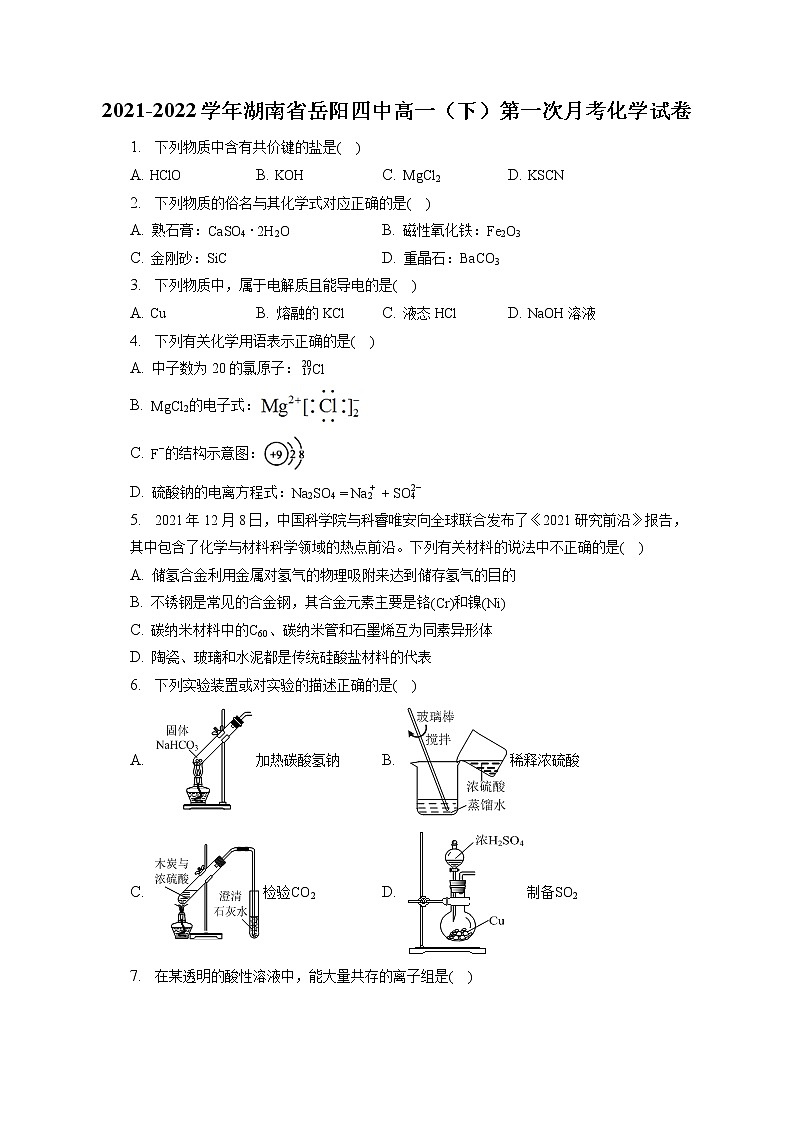
2021-2022学年湖南省岳阳四中高一(下)第一次月考化学试卷
1. 下列物质中含有共价键的盐是( )
A. HClO B. KOH C. MgCl2 D. KSCN
2. 下列物质的俗名与其化学式对应正确的是( )
A. 熟石膏:CaSO4⋅2H2O B. 磁性氧化铁:Fe2O3
C. 金刚砂:SiC D. 重晶石:BaCO3
3. 下列物质中,属于电解质且能导电的是( )
A. Cu B. 熔融的KCl C. 液态HCl D. NaOH溶液
4. 下列有关化学用语表示正确的是( )
A. 中子数为20的氯原子: 1720Cl
B. MgCl2的电子式:
C. F−的结构示意图:
D. 硫酸钠的电离方程式:Na2SO4=Na2++SO42−
5. 2021年12月8日,中国科学院与科睿唯安向全球联合发布了《2021研究前沿》报告,其中包含了化学与材料科学领域的热点前沿。下列有关材料的说法中不正确的是( )
A. 储氢合金利用金属对氢气的物理吸附来达到储存氢气的目的
B. 不锈钢是常见的合金钢,其合金元素主要是铬(Cr)和镍(Ni)
C. 碳纳米材料中的C60、碳纳米管和石墨烯互为同素异形体
D. 陶瓷、玻璃和水泥都是传统硅酸盐材料的代表
6. 下列实验装置或对实验的描述正确的是( )
A. 加热碳酸氢钠 B. 稀释浓硫酸
C. 检验CO2 D. 制备SO2
7. 在某透明的酸性溶液中,能大量共存的离子组是( )
A. Al3+、SO42−、Na+、Cu2+ B. K+、HCO3−、Mg2+、Cl−
C. SO32−、K+、Cl−、Na+ D. Fe2+、SO42−、K+、NO3−
8. 有下列氧化还原反应:①2I−+Cl2=I2+2Cl−;②2Fe3++2I−=2Fe2++I2;③2Fe2++Cl2=2Fe3++2Cl−;④2MnO4−+10Cl−+16H+=2Mn2++5Cl2+8H2O,根据上述反应,判断下列结论中正确的是( )
A. 要除去含有Fe2+、Cl−和I−的混合溶液中的杂质离子I−,应加入过量的新制氯水
B. 氧化性强弱顺序为:MnO4−>Cl2>Fe3+>I2
C. Mn2+是MnO4−的氧化产物,I2是I−的还原产物
D. 在溶液中不可能发生反应:MnO4−+5Fe2++8H+=Mn2++5Fe3++4H2O
9. 下列说法正确的是( )
A. pHI2;
②2Fe3++2I−=2Fe2++I2中,Fe元素的化合价升高,I元素的化合价降低,根据氧化剂的氧化性大于氧化产物,则氧化性Fe3+>I2;
③2Fe2++Cl2=2Fe3++2Cl−中,Cl元素的化合价升高,Fe元素的化合价降低,根据氧化剂的氧化性大于氧化产物,则氧化性Cl2>Fe3+;
④2MnO4−+10Cl−+16H+=2Mn2++5Cl2↑+8H2O中,Cl元素的化合价升高,Mn元素的化合价降低,根据氧化剂的氧化性大于氧化产物,则氧化性MnO4−>Cl2,据此分析解答。
A.由以上分析可知,氧化性强弱顺序为:MnO4−>Cl2>Fe3+>I2,则要除去含有Fe2+、Cl−和I−的混合溶液中的杂质离子I−,只能加三价铁溶液,不能加入过量的新制氯水,故A错误;
B.由以上分析可知,氧化性强弱顺序为:MnO4−>Cl2>Fe3+>I2,故B正确;
C.④2MnO4−+10Cl−+16H+=2Mn2++5Cl2↑+8H2O中,Mn元素的化合价降低,则Mn2+是MnO4−的还原产物,故C错误;
D.由B得,氧化性强弱顺序为:MnO4−>Cl2>Fe3+>I2,所以可能发生反应:MnO4−+5Fe2++8H+=Mn2++5Fe3++4H2O,故D错误;
故选B。
9.【答案】B
【解析】解:A.雨水因为溶有二氧化碳本来就是酸性,故pHF−>Na+。
20.【答案】H2O 将湿润的红色石蕊试纸伸到瓶口,试纸变蓝,证明是NH3 3Cu+8H++2NO3−=3Cu2++2NO↑+4H2O2NH4Cl+Ca(OH)2−△CaCl2+2NH3↑+2H2O
【解析】解:(1)二氧化氮能与水反应生成NO和硝酸,除去NO中的NO2所用的试剂为H2O,
故答案为:H2O;
(2)A为N2,其电子式为,
故答案为:;
(3)检验试管中盛装的是NH3的方法为:将湿润的红色石蕊试纸伸到瓶口,试纸变蓝,证明是NH3,
故答案为:将湿润的红色石蕊试纸伸到瓶口,试纸变蓝,证明是NH3;
(4)E→C的离子方程式为3Cu+8H++2NO3−=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3−=3Cu2++2NO↑+4H2O;
(5)实验室制备NH3的化学方程式为2NH4Cl+Ca(OH)2−△CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2−△CaCl2+2NH3↑+2H2O。
由A、B、C、D、E五种含氮物质的转化关系图,其中A、B、C、D常温下都是气体,B为红棕色,可知B为NO2,结合图中转化可知A为N2,C为NO,D为NH3,E为HNO3。
本题考查无机物的推断,为高频考点,B的颜色为推断的突破口,熟练掌握元素化合物知识,侧重分析与推断能力的考查,题目难度不大。
21.【答案】(1)检验装置气密性;饱和NaHSO3溶液
(2)Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
(3)D
(4)取少量C中溶液于试管中,先加盐酸酸化,再加入氯化钡,若产生白色沉淀则证明阴离子是硫酸根
【解析】
【分析】
本题考查综合性实验,难度不大,掌握常见非金属及其化合物性质为解答的关键,注意常见离子的检验方法。
【解答】
(1)任何制备气体的装置都要检验装置的气密性,试剂a作用是除去挥发的浓硫酸蒸气,同时不能溶解消耗SO2气体,该试剂是饱和NaHSO3溶液;
(2)浓硫酸和铜片在加热条件下产生二氧化硫、水及硫酸铜,相应的化学方程式为:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O;
(3)A.在加热条件下充分反应,A装置中由于其中水很少,因此溶液不呈蓝色,而是无色,故A错误;
B.二氧化硫通入水中,酸性本来就会增强,与氧化还原反应无关,故B错误;
C.二氧化硫也可以使高锰酸钾溶液褪色,故无法证明有亚铁离子生成,故C错误;
D.尾气要注意防倒吸,符合题意,故D正确;
故选:D;
(4)SO2气体通入C装置充分反应后生成硫酸根离子,取少量C中溶液于试管中,先加盐酸酸化,再加入氯化钡,若产生白色沉淀则证明阴离子是硫酸根。
22.【答案】0.0192;逸出的SO2中混有HCl,消耗NaOH标准溶液体积偏大
【解析】
【分析】
本题考查化学方程式的计算,涉及滴定原理的运用,试题培养了学生分析计算能力、灵活运用知识的能力。
【解答】
发生反应:SO2+H2O2=H2SO4,2NaOH+H2SO4=Na2SO4+2H2O,根据2NaOH∼H2SO4∼SO2,可知知SO2的质量为:12×(0.00600mol/L×0.02L)×64g/mol=0.00384g,该葡萄酒中的二氧化硫含量为:0.00384g0.2L=0.0192g/L,逸出的SO2中混有HCl,消耗NaOH标准溶液体积偏大,测定结果比实际值偏高。
相关试卷
这是一份2021-2022学年湖南省邵阳市洞口二中高一(下)第一次月考化学试卷(含答案解析),共14页。试卷主要包含了 化学与科技、生活密切相关, 下列关于硫的说法不正确的是, 下列关于氨的说法正确的是, 下列关于氮气的说法错误的是等内容,欢迎下载使用。
这是一份2021-2022学年湖南省长沙市明德中学高一(下)月考化学试卷(第一次)(含答案解析),共16页。试卷主要包含了 下列装置能达到实验目的的是,2mlCu与含0等内容,欢迎下载使用。
这是一份2021-2022学年湖南省名校联盟高一(下)月考化学试卷(3月份)(含答案解析),共19页。试卷主要包含了 下列化学用语不正确的是等内容,欢迎下载使用。









