




所属成套资源:新鲁科版高中化学必修第二册课件PPT+同步练习全册
化学第1节 原子结构与元素性质优质课件ppt
展开
这是一份化学第1节 原子结构与元素性质优质课件ppt,共12页。PPT课件主要包含了质子数,原子核,核外电子,原子是电中性的,质量数,AZ个,知识回顾,核外电子排布规律,原子结构示意图等内容,欢迎下载使用。
1.了解1~20号元素原子的核外电子排布。2.了解核外电子的排布规律。3.了解原子的最外层电子数与元素原子得失电子的能力和化合价的关系。
电子按能量高低在核外分层排布。
⑶最外层电子数不超过8个电子(K层为最外层时,电子数不超过2个),次外层不超过18个电子,倒数第三层不超过32个电子。
K→ L → M→N → O → P
2→ 8 →18→32→50→ 2n2
⑴电子总是尽先排布在离核最近、能量最低的电子层里。
⑵每个电子层最多只能排布2n2个电子。
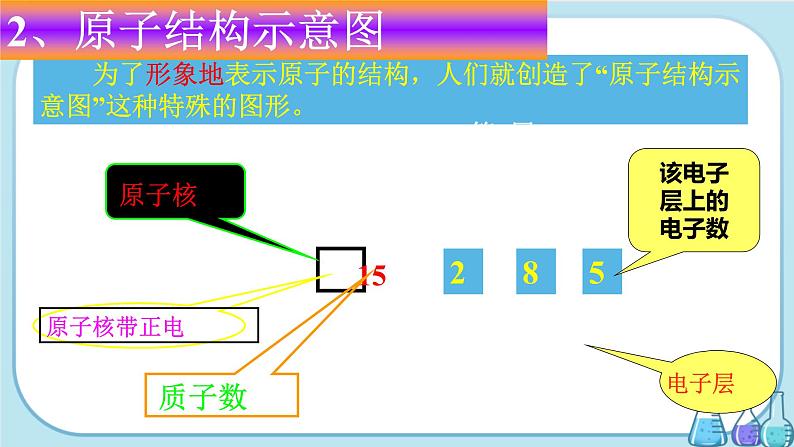
为了形象地表示原子的结构,人们就创造了“原子结构示意图”这种特殊的图形。
核电荷数为1~20的元素原子核外电子层排布
稀有气体元素原子电子层排布
3.元素的化学性质、化合价与原子的 最外层电子排布密切相关
3)非金属元素原子最外层电子数一般大于 或等于4,易获得电子而形成阴离子, 常见化合价为负价。
(1)稀有气体最外层电子达到稳定结构, 其化学性质稳定;常见化合价为0价
(2)金属元素原子最外层电子数一般小于4, 易失去而形成阳离子,常见化合价为正价。
1.下列原子结构示意图中,正确的是( )2.某元素原子的原子核外有三个电子层,最外层有4个电子,该原子核内的质子数为( )A.14 B.15 C.16 D.17
3.根据下列叙述,写出元素名称并画出原子结构示意图。
(1)A元素原子核外M层电子数是L层电子数的1/2;
(2)B元素原子的最外层电子数是次外层电子数的1.5倍;
(3)C元素的次外层电子数是最外层电子数的1/4
相关课件
这是一份化学苏教版 (2019)第三单元 人类对原子结构的认识一等奖ppt课件,共22页。PPT课件主要包含了学习目标,能量逐步升高,能量最低,原子核,最外层电子数等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修2第一节 原子结构评课课件ppt,共60页。PPT课件主要包含了课前·新知导学,概率密度,哑铃状,空间运动状态,微思考,单独分占,原子轨道,课堂·素养初培,情境导入,深化理解等内容,欢迎下载使用。
这是一份鲁科版 (2019)选择性必修2第2节 原子结构与元素周期表教学课件ppt,共60页。PPT课件主要包含了NO1,NO2,NO3等内容,欢迎下载使用。










