





鲁科版 (2019)必修 第二册第1节 化学键与物质构成优质ppt课件
展开1.理解离子化合物、共价化合物的分类依据并能进行正确判断。
一. 离子化合物和共价化合物
【注意】 1.离子化合物含有离子键,也可能同时含共价键 2. 大多数盐类物质属于离子化合物(但AlCl3例外,它属于共价化合物);活泼金属的氧化物、强碱均属于离子化合物。
注意:1.共价化合物只含有共价键;含有共价键的化合物不一定是共价化合物,如NaOH、Na2SO4 、NH4Cl等。只含共价键的物质也不一定是共价化合物,如H2 、O2 2.酸,非金属氧化物、非金属的氢化物、绝大多数的有机化合物均属于共价化合物。
1、Na2O 2、H2O 3、KCI 4、Na2S 5、CaCl2 6、KNO3 7、H2SO4 8、NaOH 9、CH4 10、NH4Cl
【针对练习】判断下列物质中是否含有离子键、共价键?哪些是离子化合物?哪些是共价化合物?
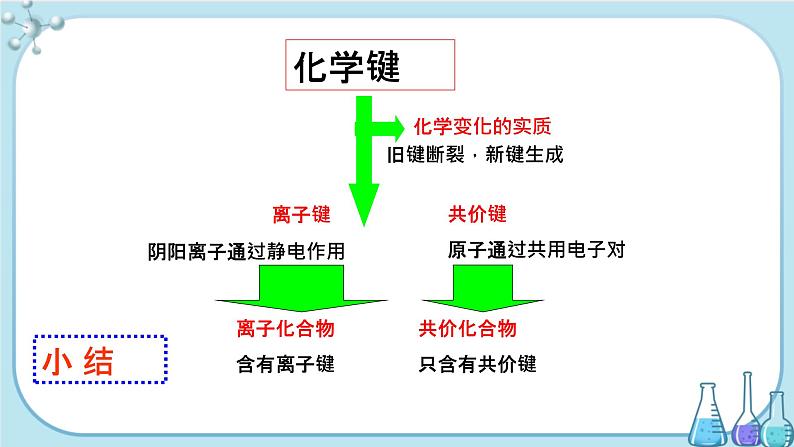
离子键阴阳离子通过静电作用
共价键原子通过共用电子对
共价化合物只含有共价键
1.离子化合物中一定含有金属元素吗?
3. 判断正误:①非金属元素间不可能形成离子键。
②两种非金属原子间只能形成共价键。
2.溶于水能电离出阴阳离子的化合物一定是 离子化合物吗?
熔融状态能导电的化合物一定是离子化合物。
二、电子式在元素符号周围用“ · ”或“×”来表示原子最外层电子的式子。
(1)原子的电子式:最外层电子用小黑点“.”或小叉“×”来表示。
(2)阳离子的电子式:即它的离子符号。
双核(或多核)离子的电子式
(3)阴离子的电子式:画出最外层电子数,还应用括号“[ ]”括起来,并在右上角标出“n-”电荷字样。
离子化合物的电子式:由阴、阳离子的电子式组成,但相同离子不能合并
⒈ AB型: NaCl: KBr: MgO: CaO:⒉ AB2型: MgCl2: CaBr2:⒊ A2B型: Na2O: K2S:NaOH:
常见共价化合物的电子式:
① NaCl: ② MgO: ③ MgCl2: ④ K2S:
用电子式表示离子化合物的形成过程
用电子式表示单质和共价化合物的形成过程
1.箭头左方相同的微粒可以合并,箭头右方相同的微粒不可以合并。2.反应物要用原子的电子式表示。生成物要用离子化合物或共价化合物的电子式表示。3.用于连结反应物和生成物的符号是 → 而不是=。
1.下列粒子的电子式错误的是:
2.下列化合物电子式书写正确的是:
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物评优课课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物评优课课件ppt,共60页。PPT课件主要包含了第一节硫及其化合物,第2课时硫酸,硫酸的性质,微判断,尝试解答,微训练,研习1硫酸的性质,课时作业二硫酸等内容,欢迎下载使用。
人教版 (2019)必修 第二册第一节 硫及其化合物优秀ppt课件: 这是一份人教版 (2019)必修 第二册第一节 硫及其化合物优秀ppt课件,共24页。PPT课件主要包含了硫酸的物理性质,硫酸的工业制法,硫酸的化学性质,根据元素组成分类,思考二,硫酸的用途,几种常见的硫酸盐,实验5-4,硫酸根离子的检验,待测液等内容,欢迎下载使用。
人教版 (2019)选择性必修3第一章 有机化合物的结构特点与研究方法第一节 有机化合物的结构特点图片ppt课件: 这是一份人教版 (2019)选择性必修3第一章 有机化合物的结构特点与研究方法第一节 有机化合物的结构特点图片ppt课件,共60页。PPT课件主要包含了随堂演练知识落实,课时对点练,内容索引,发生断裂,官能团,化学键,同分异构,同分异构体的类型,构造异构现象举例,正丁烷等内容,欢迎下载使用。













