




第15讲 铁盐和亚铁盐(讲义)-高一化学同步精品讲义(人教必修第一册 )
展开
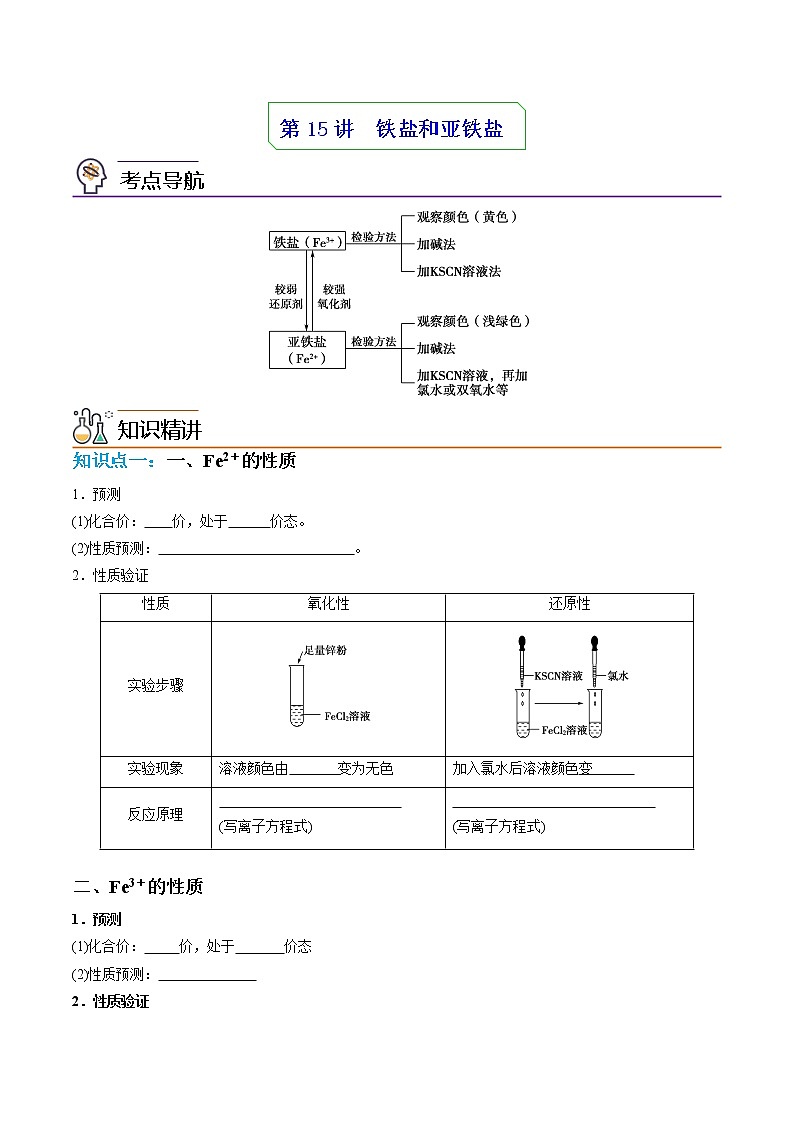
知识点一:一、Fe2+的性质1.预测(1)化合价: 价,处于 价态。(2)性质预测: 。2.性质验证性质氧化性还原性实验步骤实验现象溶液颜色由 变为无色加入氯水后溶液颜色变 反应原理 (写离子方程式) (写离子方程式) 二、Fe3+的性质1.预测(1)化合价: 价,处于 价态(2)性质预测: 2.性质验证实验步骤实验现象加入KSCN溶液: ;再加铁粉: 加入KSCN溶液: ;再加铜片: 反应原理2Fe3++Fe===3Fe2+2Fe3++Cu===2Fe2++Cu2+三、Fe3+和Fe2+的相互转化实验操作实验现象加适量铁粉振荡后,溶液变成 色,再加KSCN溶液颜色 ,再滴加氯水后,溶液变成 离子方程式 、 结论Fe3+遇到较强的 剂时,会被还原成 ,Fe2+在较强的 剂的作用下会被氧化成 微警示【即学即练1】1.下列离子方程式书写正确的是A.向FeO固体中加入少量稀硝酸:B.往溶液中通入少量的:C.向溶液中加入过量氨水:D.向溶液中加入氯水:2.下列说法不正确的是A.在工业上可用铁制槽车或铝制槽车运输浓硫酸B.金属钠着火时,应立刻用泡沫灭火器灭火防止火势蔓延C.配制FeSO4溶液时加入少量的铁粉D.钠保存在石蜡油或煤油中,实验后剩余的钠粒可放回原试剂瓶中3.下列有关铁及其化合物的性质与用途具有对应关系的是A.铁粉具有还原性,可用作食品保存的抗氧化剂B.纳米Fe3O4能与酸反应,可用作铁磁性材料C.FeCl3溶液呈酸性,可用于腐蚀印刷电路板上的CuD.聚合硫酸铁能水解并形成胶体,可用于自来水的消毒4.“类比”是一种重要的科学方法,下列结论正确的是选项已知结论A铁和氯气反应:铁和碘单质反应:B常温下Zn易溶于浓硫酸常温下Al易溶于浓硫酸C是酸性氧化物可与NaOH溶液反应是酸性氧化物可与NaOH溶液反应D向溶液中通入少量:向溶液中通入少量: A.A B.B C.C D.D知识点二: 1.Fe2+、Fe3+的检验(1)直接观察颜色(2)利用氢氧化物沉淀的颜色(3)利用显色反应(4)利用Fe2+的还原性(5)同时含有Fe2+和Fe3+的溶液Fe2+对检验Fe3+无干扰,可以滴加KSCN溶液检验Fe3+;Fe3+对检验Fe2+有干扰,不能采用加KSCN溶液检验Fe2+,通常向溶液中滴加适量酸性KMnO4溶液,溶液紫红色褪去说明含有Fe2+。(6)检验铁的氧化物中是否有+2价铁时,正确的思路为少量固体溶液紫红色褪去。①步骤a中不能选用盐酸,原因是酸性KMnO4溶液可以氧化盐酸。②步骤a中不能选用稀硝酸,原因是稀硝酸可以将Fe2+氧化为Fe3+。【即学即练2】1.下列实验操作、现象和结论均合理的是A.向20%蔗糖溶液中加入少量稀硫酸,加热,再加入银氨溶液,水浴加热,未出现银镜,说明蔗糖未水解B.用洁净的铂丝蘸取白色粉末在火焰上灼烧,火焰呈黄色,说明该白色粉末是钠盐C.某溶液中滴加氯水后再滴加KSCN溶液呈红色,说明原溶液含有D.某无色溶液中滴加氯水溶液呈棕色,再滴加淀粉溶液显蓝色,说明原溶液中含有2.用相同浓度的和溶液进行实验:下列说法不正确的是A.相同浓度的和溶液中,的浓度不同B.提供空轨道,提供孤电子对,两者以配位键结合成C.溶液2不显红色,说明与的结合力强于与的结合力D.由对比实验可知,用溶液检验溶液中的比用KSCN溶液更好3.下列关于溶液中所含离子检验的说法正确的是A.取少量某溶液于试管中,向其中先滴加稀硝酸,再滴加溶液,有白色沉淀生成,说明该溶液中含有B.取少量某溶液于试管中,向其中加入少量新制氯水,再滴加KSCN溶液,若溶液变红,说明该溶液中含有C.取少量某溶液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体,若红色石蕊试纸变蓝,说明该溶液中含有D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有4.向盛有2mLFeCl3溶液的试管中加入少量铁粉,进行如下实验。下列分析正确的是A.只加入KSCN溶液可检验试管1中是否含有Fe2+B.试管2中无现象,则表明试管1中溶液不含Fe3+C.试管3中的离子反应为:Fe2++Cl2=Fe3++2Cl-D.试管3中必定有红色沉淀生成 1.某溶液中加KSCN溶液,颜色无变化,再加氯水溶液变红,说明什么?发生的反应是什么?【细剖精析】说明原溶液中无Fe3+,有Fe2+,2Fe2++Cl2===2Fe3++2Cl-。2.某溶液中加KSCN溶液,溶液变红,然后加足量Fe粉,红色又褪去,说明什么?写出反应的离子方程式。【细剖精析】原溶液中有Fe3+,2Fe3++Fe===3Fe2+。3.如何通过实验证明Fe3O4中含有+2价铁?【细剖精析】取Fe3O4少许于试管中,加入稀H2SO4溶解,再向其中加入几滴酸性KMnO4溶液,若紫色褪去,证明Fe3O4中含Fe2+。4.Fe3+和Fe2+的检验:(1)铁粉和稀硫酸反应的实验,如何证明产物不是Fe3+?【细剖精析】向反应后的溶液中滴加KSCN溶液,若溶液不变红,说明产物中不含Fe3+。(2)检验某未知溶液中是否含Fe2+时,能否先滴加氯水,后滴加KSCN溶液?【细剖精析】不能。若未知溶液中含有Fe3+,滴加KSCN溶液时,溶液变成红色,会干扰Fe2+的检验。(3)如何检验Fe2(SO4)3溶液中是否有Fe2+?【细剖精析】取待测溶液,加入酸性KMnO4溶液,若紫色褪去,说明含Fe2+。5.为了检验Fe3O4中铁元素的价态,设计了以下实验:问题思考:(1)甲实验中可观察到什么现象?得出什么结论?【细剖精析】溶液紫色退去、棕黄色加深,证明溶液中存在Fe2+,Fe2+具有还原性。(2)乙实验中可观察到什么现象?能否证明Fe2+的存在?说明理由。【细剖精析】有红褐色沉淀产生;不能证明Fe2+的存在,因为Fe(OH)3的颜色掩盖了Fe(OH)2产生的实验现象。(3)丙实验可观察到什么现象?得出什么结论?【细剖精析】溶液由棕黄色变为红色,证明有Fe3+存在。向某未知酸性溶液中滴加KSCN溶液,无明显现象,但放置一段时间后,溶液慢慢变红色。可以说明什么?写出有关离子方程式。【细剖精析】可以说明溶液中含有Fe2+。4Fe2++4H++O2===4Fe3++2H2O。 1.“铁三角”转化关系(1)(2) (3) 2.含铁物质的分离与除杂主要物质杂质除杂方法Fe2+Fe3+加过量铁粉后过滤FeCl3FeCl2加氯水或通入Cl2Fe2+Cu2+加过量铁粉后过滤FeAl加NaOH溶液后过滤Fe2O3Al2O3加NaOH溶液后过滤3.离子的共存问题①Fe3+与I-、S2-等还原性离子不能大量共存。②Fe2+与MnO(H+)、ClO-等氧化性离子不能大量共存。 题组A 基础过关练1.在蒸发皿中蒸干并灼烧下列溶液,可以获得原溶液溶质固体的是A.溶液 B.溶液 C.溶液 D.溶液2.下列操作、现象和结论都正确的是选项操作现象结论A向酸性溶液中通入足量的乙烯紫色溶液变为无色乙烯具有漂白性B向新制的悬浊液中加入葡萄糖溶液并加热产生砖红色沉淀葡萄糖具有还原性C在酒精灯火焰上分别灼烧头发和丝织品有烧焦羽毛气味可区分丝织品和头发D向某溶液中依次滴加氯水、KSCN溶液溶液变为红色原溶液中一定含有 A.A B.B C.C D.D3.下列实验对应的化学用语正确的是A.溶液中滴加溶液,静置一段时间后:B.酸性氯化亚铁溶液中加入双氧水:C.足量二氧化硫与氢氧化钠溶液反应:D.澄清石灰水中加入过量溶液:4.硫酸亚铁是一种重要的化工原料,部分转化如下图所示。下列说法正确的是A.用酸性KMnO4溶液可以检验FeSO4是否变质B.制纳米Fe3O4时通入的O2需过量C.制FeCO3时应将FeSO4溶液加入Na2CO3溶液中D.生成(NH4)2Fe(SO4)2·6H2O的反应为非氧化还原反应5.下列铁的化合物的性质与用途具有对应关系的是A.易溶于水,可用作净水剂B.能与酸反应,可用作红色颜料C.溶液呈酸性,可用于蚀刻铜电路板D.具有强氧化性,能使蛋白质变性,可用于水体的消毒6.在指定条件 下,下列选项所示物质间转化能实现的是A.Fe(s) FeCl2(s)B.FeO(s)Fe(NO3)2(aq)C.Fe(OH)2(s) Fe(OH)3(s)D.FeCl3(aq) Fe(s)【答案】C7.把KMnO4溶液滴入一含有铁离子的酸性水溶液中,KMnO4颜色消失,试推断溶液中含有铁离子的种类,最可能的情况是A.含有Fe2+,但不能确定是否含有Fe3+B.只含有Fe2+C.Fe2+和Fe3+都有D.含有Fe3+,但不能确定是否含有Fe2+8.下列反应的离子方程式书写正确的是A.向H2O2溶液中滴加少量FeCl3溶液:2Fe3++H2O2=O2↑+2H++2Fe2+B.CuSO4溶液中滴加稀氨水:Cu2++2OH-=Cu(OH)2↓C.使用K3[Fe(CN)6]溶液检验Fe2+:2[Fe(CN)6]3-+3Fe2+=Fe3[Fe(CN)6]2↓D.将等浓度Ba(OH)2溶液与NaHSO4溶液按体积比1∶2混合:2Ba2++2SO+3H++3OH-=2BaSO4↓+3H2O题组B 能力提升练1.根据实验目的,下列实验及现象、结论都正确的是选项实验目的实验及现象结论A向溶液中滴加过量氯水,再加入淀粉溶液先变橙色,后变蓝色氧化性:B检验铁锈中是否含有二价铁将铁锈溶于浓盐酸,滴入溶液,紫色褪去铁锈中含有二价铁C探究氢离子浓度对、相互转化的影响向溶液中缓慢滴加硫酸溶液,黄色变为橙红色增大氢离子浓度,转化平衡向生成的方向移动D检验乙醇中是否含有水向乙醇中加入一小粒金属钠,产生无色气体乙醇中含有水 A.A B.B C.C D.D2.滴定法测铀时需添加VOSO4做催化剂,该物质易被氧化,实验室常用Fe2+去除VOSO4溶液中的(VO2)2SO4,实验装置如图所示。下列分析正确的是 A.VOSO4和(VO2)2SO4中V元素的化合价相同B.b中反应所生成气体的作用之一是将装置中的空气排尽C.用小试管在m处收集气体并验纯后,应先关闭K2,再打开K3D.实验完毕,可用氯水和KSCN溶液检验c中溶液是否含有Fe2+3.下列根据实验操作及现象进行的分析和推断中,不正确的是操作 现象一段时间后:①中,铁钉裸露在外的附近区域变红;②中…… A.NaCl的琼脂水溶液为离子迁移的通路B.①中变红是因为发生反应,促进了水的电离C.②中可观察到铁钉裸露在外的附近区域产生蓝色沉淀,铜丝附近区域变红D.①和②中发生的氧化反应均可表示为(M代表锌或铁)4.为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是A.加入溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现C.加入溶液无红色出现 D.加入溶液无蓝色沉淀生成5.以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血C.过滤步骤说明硫酸亚铁晶体难溶于水D.实验过程不直接蒸发结晶的原因是防止FeSO4水解生成Fe(OH)26.向NH4Fe(SO4)2(aq)中逐滴滴加Ba(OH)2(aq)至过量的过程中,有关离子反应错误的是A.2Fe3++3+3Ba2++6OH-→2Fe(OH)3↓+3BaSO4↓B.Fe3++5+4+4Ba2++8OH-→Fe(OH)3↓+5NH3·H2O+4BaSO4↓C.3Fe3+++5+5Ba2++10OH-→3Fe(OH)3↓+NH3·H2O+5BaSO4↓D.Fe3+++2+2Ba2++4OH-→Fe(OH)3↓+NH3·H2O+2BaSO4↓7.学习小组进行如下实验:序号实验操作实验现象Ⅰ将1mLpH=1的0.1mol·L-1 FeSO4溶液和2滴0.1mol·L-1KSCN溶液混合,接着向混合溶液中逐滴滴加0.5mL0.3mol·L-1的H2O2溶液滴入H2O2溶液,溶液立即变红,继续滴加,溶液红色变浅并逐渐褪去Ⅱ向i的混合溶液中滴入KSCN溶液溶液变红Ⅲ向1mL0.3mol·L-1的H2O2溶液中滴加2滴0.1mol·L-1KSCN溶液,继续加入0.5mLpH=1的H2SO4溶液,静置2min无明显现象Ⅳ向ⅲ的混合溶液中滴入2滴Fe2(SO4)3溶液滴入Fe2(SO4)3溶液,溶液立即变红,静置2min,溶液红色变浅并逐渐褪去 下列说法错误的是A.实验中溶液变红的原因是生成Fe(SCN)3B.实验i~ⅱ说明实验i中SCN-被H2O2全部氧化C.实验ⅲ~ⅳ说明酸性溶液中H2O2氧化KSCN的速度慢D.实验i~ⅳ说明Fe2+能加速H2O2氧化KSCN的反应8.能验证某溶液中含有,不含的实验事实是A.向溶液中滴加溶液,溶液变红B.向溶液中滴加溶液,无明显变化;再滴加几滴氯水,溶液变红C.向溶液中依次滴加氯水、溶液,溶液变红D.向溶液中滴加少量溶液,产生红褐色沉淀题组C 培优拔尖练1.某班同学用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液.在FeCl2溶液中需加入少量铁屑,其目的是____。(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为:___。(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是___。(4)丙组同学取l0mL0.lmol·L-1KI溶液,加入6mL0.lmol·L-1FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:①第一支试管中加入lmLCCl4充分振荡、静置,CCl4层显紫色;②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀:③第三支试行中加入1滴KSCN溶液,溶液变红。实验②检验的离子是(填离子符号)___;实验①和③说明:在I-过量的情况下,溶液中仍含有(填离子符号)____,由此可以证明该氧化还原反应为___。(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是___;生成沉淀的原因是(用平衡移动原理解释)____。(6)戊组同学模拟工业上用NaClO3氧化酸性FeCl2废液制备FeCl3。①若酸性FeCl2废液中:c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为___。②完成NaClO3氧化FeCl2的离子方程式:___。ClO+Fe2++___=Cl-+Fe3++___③FeCl3具有净水作用,其原理是___。2.某兴趣小组研究I2与FeCl2溶液的反应。配制FeCl2溶液:向0.1 mol·L-1FeCl3溶液中加入足量铁粉,充分振荡,备用。(1)FeCl3溶液与铁粉反应的离子方程式是________。(2)检验FeCl3完全反应的实验方案是____________。(3)设计如下实验,研究I2是否能够氧化FeCl2:实验现象:试管1溶液变红,试管2溶液呈现较浅的蓝色。实验结论:I2能够氧化FeCl2。①有的同学认为上述实验现象不足以得出上述结论,原因是________。②欲证实实验结论,再次设计对比实验。实验方案和相应的现象是________。(4)继续进行实验:实验 实验操作 实验现象 I向试管1中加入KI固体,充分振荡溶液红色完全褪去,变为黄色。 Ⅱ向I中所得的黄色溶液中加入0.5mL CCl4,充分振荡、静置水层仍为黄色,CCl4层几乎无色。 ①针对Ⅱ中现象,小组同学提出假设:在一定量KI的存在下,I-+I2I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):____________ ②应用化学平衡移动原理,结合离子方程式,解释实验I中溶液红色褪去的原因:_______________________。






