
《课题3 金属资源的利用与保护》第1课时示范课教案【人教版化学九年级下册】
展开课题3 金属资源的利用和保护
第1课时
一、教学目标
1.知道一些常见金属(如铁、铝、铜等)矿物,了解从铁矿石中将铁还原出来的方法。
2.了解实验室将氧化铁还原成铁的原理。
3.会根据化学方程式对含有某些杂质的反应物或生成物进行有关计算。
二、教学重难点
重点:实验室将氧化铁还原成铁的原理。
难点:根据化学方程式对含有某些杂质的反应物或生成物进行有关计算。
三、教学准备
多媒体课件
四、教学过程
教学环节 | 教师活动 | 学生活动 | 设计意图 |
环节一 创设情境 引入新课 | 【导入】目前人们生活中常使用的金属有哪些呢? 【总结】 | 观看,思考 | 通过提问生活中常使用的金属,引入新课,激发学生的求知欲。 |
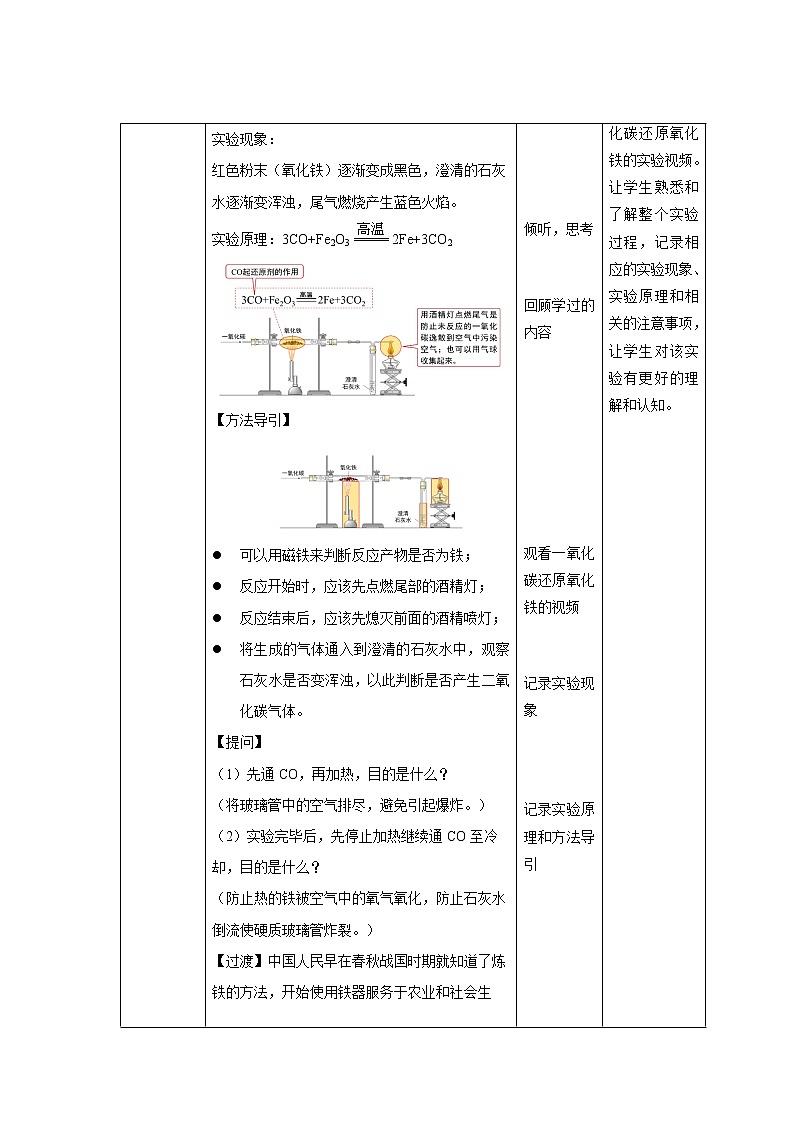
环节二 新课讲解 | 【过渡】地球上的金属资源广泛地存在于地壳和海洋中,除少数很不活泼的金属如金、银等有单质形式存在外,其余都以化合物的形式存在。 【讲解】极少数不活泼的金属以单质的形式存在,如铂、金、银等 【讲解】化学性质较活泼的金属以化合物的形式存在,如铁、锌、钠和钙等在自然界中以矿物的形式存在。 铁的矿物 铜的矿物 铝的矿物 【过渡】大自然向人类提供了丰富的金属矿物资源,人类每年要提取数以亿吨计的金属,用于工农业生产和其他领域。其中,提取量最大的是铁。 【提问】怎样把铁矿石变成铁呢? 【总结】把铁元素从铁矿石中提炼出来。 【提问】我们学过哪些能得到铁的化学方程式呢? 【总结】 【过渡】下面,我们一起来学习有关铁的冶炼的知识吧! 【播放视频】一氧化碳还原氧化铁 实验现象: 红色粉末(氧化铁)逐渐变成黑色,澄清的石灰水逐渐变浑浊,尾气燃烧产生蓝色火焰。 实验原理:3CO+Fe2O32Fe+3CO2 【方法导引】 可以用磁铁来判断反应产物是否为铁; 反应开始时,应该先点燃尾部的酒精灯; 反应结束后,应该先熄灭前面的酒精喷灯; 将生成的气体通入到澄清的石灰水中,观察石灰水是否变浑浊,以此判断是否产生二氧化碳气体。 【提问】 (1)先通CO,再加热,目的是什么? (将玻璃管中的空气排尽,避免引起爆炸。) (2)实验完毕后,先停止加热继续通CO至冷却,目的是什么? (防止热的铁被空气中的氧气氧化,防止石灰水倒流使硬质玻璃管炸裂。) 【过渡】中国人民早在春秋战国时期就知道了炼铁的方法,开始使用铁器服务于农业和社会生活。中国的现代钢铁工业蓬勃发展,涌现了一批特大钢铁企业如宝钢、首钢等。你知道它们的炼铁原理是什么?所用原料有哪些? 【总结与交流】 1.工业炼铁原料:铁矿石、焦炭、石灰石。 2.炼铁高炉内发生的化学反应: C+O2CO2、CO2+C2CO、3CO+Fe2O32Fe+3CO2 3.石灰石的主要作用是将矿石中的二氧化硅转变为炉渣。 CaCO3+SiO2CaSiO3 + CO2↑ 【交流讨论】高炉炼铁和实验室炼铁有什么区别?其产物是纯铁吗? 【总结与交流】 (1)两者的产物不同。工业炼铁得到的是生铁,实验室得到的是纯铁。 生铁:含有2%~4.3%的碳及少量磷和硫的铁合金,硬而脆,不利于加工,可经过吹氧冶炼等工序生产钢,含碳量降至0.03%~2%的铁合金。 (2)设备不同。工业炼铁设备是高炉,实验室用玻璃管。 (3)对环境影响不同。高炉炼铁对环境影响大,实验室对环境影响小。 (4)操作难易程度不同。高炉炼铁工艺复杂,实验室操作简单。 【过渡】在实际炼铁时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题。 【讲解】在进行化学方程式的计算中,一定要用纯物质的量来进行计算。 因此,含杂质的计算一般做法如下: 第一步,将含杂质的物质质量转化成纯物质的质量。即:纯物质质量=不纯物总质量×纯度,纯度=(纯物总质量÷不纯物质质量)× 100% 第二步,依据化学方程式,根据已知纯物质的质量计算未知纯物质的质量。 第三步,将纯物质转化成杂质物质的质量。即:不纯物质质量=纯物总质量÷纯度 下面我们通过一个例题来学习一下吧! 【例题】用1 000 t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少? 【总结】 方法一: 分析:带入化学方程式计算的数据应是纯净物的质量:赤铁矿石→氧化铁→铁→生铁 方法1:根据化学式: 矿石中Fe2O3的质量:1000 t×80%=800 t Fe2O3中铁元素的质量: 可得到生铁的质量:560 t ÷96%= 583.3 t 方法二: 方法2:根据化学方程式 解:设理论上可以炼出含铁96%的生铁的质量为x。 3CO+Fe2O32Fe+3CO2 160 2×56 1000 t×80% x·96% x =583.3 t 答:理论上可以炼出含铁96%的生铁的质量为583.3 t 。 |
倾听,思考并回答问题
倾听
倾听,记录笔记
倾听,记录笔记
倾听,思考
回顾学过的内容
观看一氧化碳还原氧化铁的视频
记录实验现象
记录实验原理和方法导引
分组讨论并回答问题
倾听,思考
倾听,记录笔记
思考,分组讨论
记录笔记
倾听
记录笔记
倾听,思考
分组练习
|
通过讲解和展示相应的图片让学生知道在地壳中元素的存在形式,拓展学生的知识面。
通过复习相关内容,以此来加强学生对相关内容的记忆和理解。
通过观看一氧化碳还原氧化铁的实验视频。让学生熟悉和了解整个实验过程,记录相应的实验现象、实验原理和相关的注意事项,让学生对该实验有更好的理解和认知。
让学生了解炼铁相关的历史。
通过讲解,让学生充分了解炼铁相关的内容。
通过对比高炉炼铁和实验室炼铁的区别,让学生对炼铁有更充分的认知。
引入含杂质相关的计算
让学生了解涉及杂质的计算的相关概念和计算步骤。
通过教师讲解,让学生了解第一种计算方法,同时让学生思考第二种解题方法。以此来发散学生的思维和强化学生对涉及杂质类型计算过程的熟练程度。
|
环节三拓展延伸 | 【展示】稀土的由来 | 观看 | 拓展学生的知识面。 |
随堂作业 | PPT展示 | 做题 | 通过习题巩固本节所学知识 |
环节四 课堂小结 | 展示PPT22页。 | 倾听并理解。 | 帮助学生梳理本节知识,便于学生记忆。 |
五、板书设计
课题3 金属资源的利用和保护
第1课时
一、金属资源的存在形式及常见的矿石
二、铁的冶炼
1.冶炼原理:Fe2O3+3CO3CO2+2Fe
2.业炼铁设备:炼铁高炉
3.工业炼铁原料:铁矿石、焦炭、石灰石
三、有关杂质问题的计算









