



所属成套资源:【讲通练透】中考化学二轮复习(全国通用)
初中化学二轮复习【讲通练透】专题13 化学工艺流程专题(讲通)
展开
这是一份初中化学二轮复习【讲通练透】专题13 化学工艺流程专题(讲通),文件包含专题13化学工艺流程专题精讲讲义教师版docx、专题13化学工艺流程专题精讲讲义学生版docx等2份试卷配套教学资源,其中试卷共28页, 欢迎下载使用。
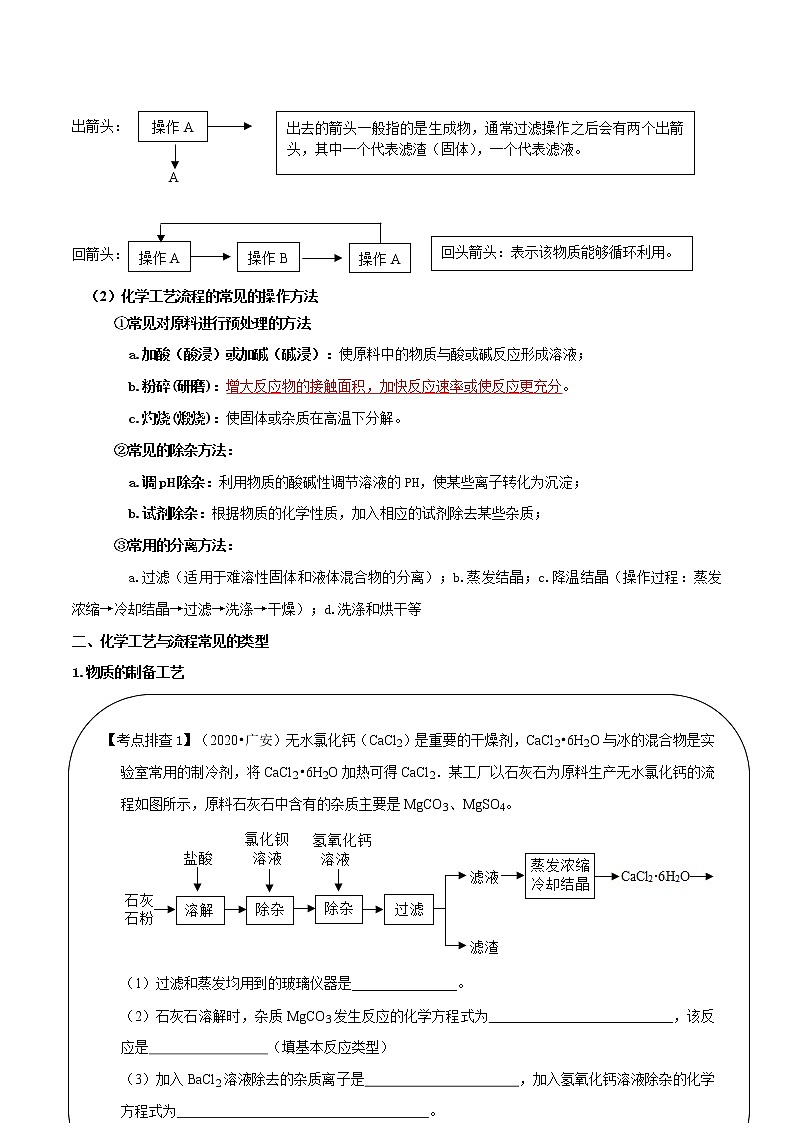
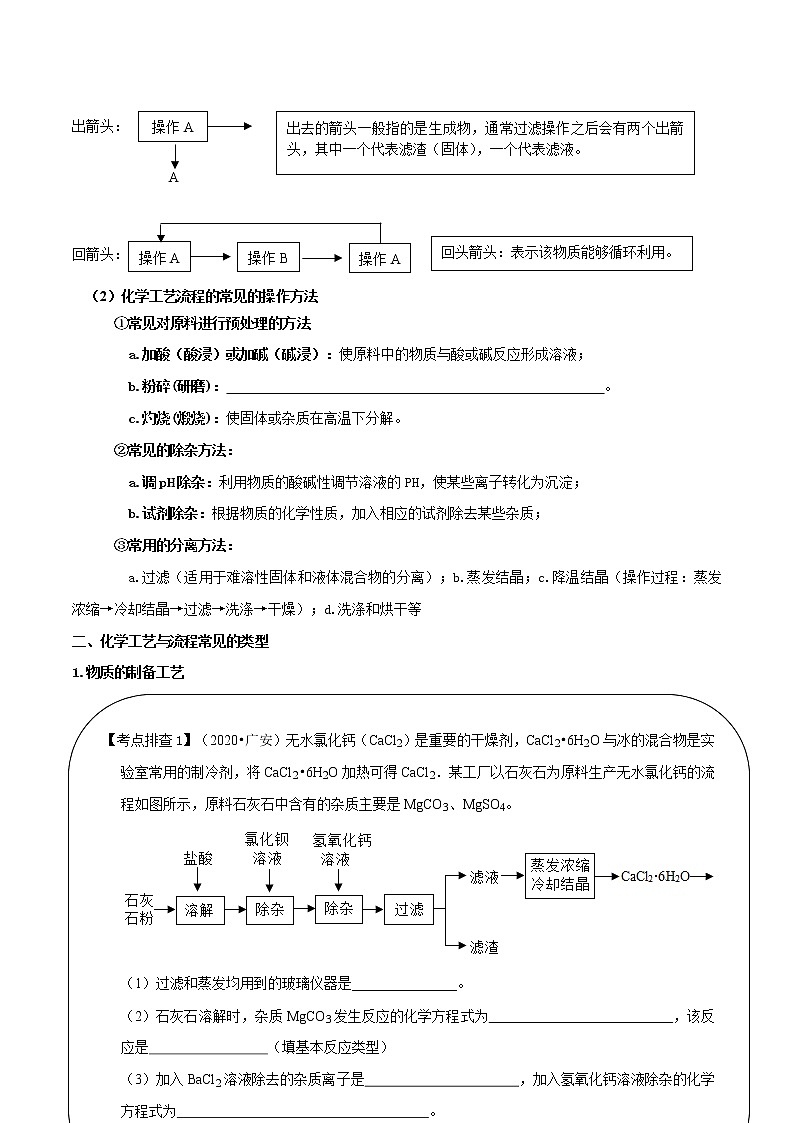
中考化学第二轮复习策略一、重视知识的综合运用在第二轮复习过程中,考生需要重视知识的综合运用,关注实验探究、联系实际,逐步提高所学技能,能解决一些需要查阅资料解决的实际问题。中考试卷中,重点知识反复考,核心知识重点考,近三年中考都有燃烧条件的探究、实验基本操作的考查、溶解度曲线、气体的制取收集方法等,比如:非选择题中,考查了考生对微粒观、元素观的认识,属于初中化学课程标准的一级主题——物质构成的奥秘。 二、合理选取备考资料关于试题的筛选,如果是巩固练习,可以用模拟试题,由于区模拟卷难易度适中,知识覆盖较为全面,部分非选择题综合度也较高,锻炼考生的审题能力和对各章知识的统筹综合应用能力。如果是进行自我评测或进行周测,建议更多选择近三年辽宁地区的中考真题。通过多年经验分析,考生在试卷中的错误整体分为以下几种情况:(1)审题问题;(2)概念知识不清;(3)概念知识不会综合应用;(4)由于学习方法和习惯问题,复习时间安排不合理,不会让知识做到有序多次呈现;(5)主观学习态度、情绪控制问题;(6)理化答题时间分配问题。考生需对号入座,有针对性地发现问题、解决问题。 专题13 化学工艺流程专题(精讲讲义)一、工艺流程图的解读1.解题思路分析①总览全题,找出原料和目标产物;②在流程图上找主线;③围绕主线精读流程(重点是对原料进行预处理和物质的分离方法),推断相关物质,并写出相关的化学方程式;④若有陌生的内容,尝试回归题目,在题目中寻找答案。2.认识工艺与流程图(1)化学工艺流程箭头解析 入箭头: 出箭头: 回箭头: (2)化学工艺流程的常见的操作方法①常见对原料进行预处理的方法a.加酸(酸浸)或加碱(碱浸):使原料中的物质与酸或碱反应形成溶液; b.粉碎(研磨): 。
c.灼烧(煅烧):使固体或杂质在高温下分解。②常见的除杂方法:a.调pH除杂:利用物质的酸碱性调节溶液的PH,使某些离子转化为沉淀; b.试剂除杂:根据物质的化学性质,加入相应的试剂除去某些杂质;③常用的分离方法:a.过滤(适用于难溶性固体和液体混合物的分离);b.蒸发结晶;c.降温结晶(操作过程:蒸发浓缩→冷却结晶→过滤→洗涤→干燥);d.洗涤和烘干等二、化学工艺与流程常见的类型1.物质的制备工艺 2.海水提取工艺 主要包括海水中提取食盐、金属镁、溴等物质。(1)粗盐的提纯:粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+、Mg2+、SO42-等可溶性杂质。·不溶性杂质可以用过滤的方法除去,步骤为: 、 、 ;·可溶性杂质中的SO42-、Ca2+、Mg2+则可通过加入BaCl2、NaOH和Na2CO3溶液生成沉淀而除去,最后蒸发水分得到较纯净的精盐。提纯步骤如下: ①溶解; ②加入过量BaCl2溶液去除SO42-,化学方程式为: ; ③加入过量NaOH溶液去除Mg2+,化学方程式为: ; ④加入过量Na2CO3溶液去除Ca2+及BaCl2中的钡离子(加入BaCl2溶液和Na2CO3溶液的顺序不能颠倒),化学方程式为: 、 ; ⑤过滤; ⑥向滤液中加入适量HCl除去过量NaOH、Na2CO3,化学方程式为: 、 ; ⑦蒸发结晶。(2)海水提镁•Ca(OH)2的生成:CaCO3===CaO+CO2↑ (分解反应) CaO+H2O==Ca(OH)2 (化合反应) •MgCl2+Ca(OH)2 ===Mg(OH)2↓+CaCl2 (复分解反应)•Mg(OH)2+2HCl===MgCl2+2H2O (复分解反应)•MgCl2Mg+Cl2↑ (分解反应) 3.废旧金属的回收利用工艺 [相关知识](1)金属活动性顺序及应用 K Ca Na Al Zn Sn Pb(H) Hg Ag Pt Au
金属活动性:由强到弱(2)金属的化学性质①活泼金属与酸反应:金属+酸→盐+氢气条件:金属在金属活动性顺序中排在氢之 ;酸指的是 和 。②与盐反应:金属+盐溶液→新盐+新金属条件:金属(钾、钙、钠除外)的活动性强于盐中金属阳离子对应的金属;盐必须可溶于水。在金属活动顺序表中排名越靠后的金属越容易从其盐溶液中置换出来。 中考题型1 物质的制备工艺【例1】(2020•昆明)工业上利用氟碳铈矿(主要成分为CeFCO3)提取CeCl3的一种工艺流程如图:(1)流程中Ce(BF4)3转化成KBF4的基本反应类型是 。(2)在足量氧气中高温焙烧CeFCO3,化学方程式为 。(3)流程涉及的化合物中,铈元素的化合价为 价。(4)酸浸过程中,CeO2与盐酸反应有刺激性气味的气体单质生成,且化学方程式中CeO2与盐酸的化学计量数之比为1:4,则化学方程式为 。【例2】(2020•大庆)以黄铁矿(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:(1)将黄铁矿粉碎,目的是 。(2)沸腾炉中发生反应的化学方程式是 。(3)若硫酸厂产生的废气未经处理就排放到空气中,可能形成酸雨,我们把pH< 的降雨称为酸雨。(4)炉渣Fe2O3可回收冶炼成铁,生活中防止铁生锈的常见方法 (答出一条即可)。中考题型2 海水提纯工艺【例3】(2020•呼和浩特)在抗击“新冠肺炎病毒”期间,消毒剂在公共场所进行卫生防疫时发挥着重要作用。二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质MgSO4、CaCl2)为原料,制取ClO2的工艺流程如图:(1)试剂A为 。(2)加入过量Na2CO3溶液的作用是 。(3)步骤④中发生反应的化学方程式为 。(4)步骤⑤涉及的物质中含氯元素化合价最高的物质是 。(5)如图流程中可循环利用的物质有 。【例4】(2020•桂林)目前世界上60%的镁是从海水中提取的,综合利用海水制备镁的流程如图所示。根据上述流程回答下列问题。(1)气体A是 。操作①的名称是 。(2)“水浸”过程中发生反应的化学方程式是 ;“沉淀池”中发生的主要反应的化学方程式是 。(3)上述流程所发生的化学反应中,没有涉及的基本反应类型是 。中考题型3 废旧金属的回收利用工艺【例5】(2020•怀化)某种手机电路板主要含有Fe、Cu、Ag(银)、Ni(镍)等金属及非金属基材,如图是某工厂回收金属铜的工艺流程图。已知:2Cu+O2+2H2SO42CuSO4+2H2O。(1)电路板不直接焚烧而采取热风处理的主要目的是 。(2)操作①的名称是 。(3)写出滤液③与铁粉反应的化学方程式 。(4)Fe、Cu、Ag、Ni在溶液中的金属活动性顺序由强到弱依次为 。(5)写出⑤得到纯铜的一种方法 。【例6】(2020•镇江)用除铁锈后的废液(主要含FeCl3、FeCl2、HCl)制备污水处理剂FeSO4•7H2O的流程如图。(1)“操作1”“操作2”用到的玻璃仪器有烧杯、玻璃棒、 等。“操作1”所得固体需洗涤。取最后一次洗涤后的滤液,向其中滴加 ,无明显现象,则固体已洗净。(2)试剂X可用 (填序号)。a.稀HClb.稀HNO3c.稀H2SO4(3)“系列操作”包括:蒸发浓缩、 、过滤等。 1.(2021•玄武区一模)以CuSO4为原料制备碱式碳酸铜[Cu2(OH)2CO3]的过程如图,下列说法错误的是( )A.“沉淀”时的反应为:2CuSO4+2Na2CO3+H2O═Cu2(OH)2CO3↓+2Na2SO4+CO2↑ B.若过滤时滤纸破损会导致产率偏低 C.可选用试剂BaCl2溶液检验是否将沉淀洗涤干净 D.若“沉淀”时有少量5Cu(OH)2•2CuCO3生成,则产品中铜元素的质量分数会偏低2.(2021•江宁区一模)黄铜渣中约含Cu 50%、CuO 5%、Zn 7%、ZnO 31%,其余为杂质。处理黄铜渣可得到铜和硫酸锌,其主要流程如图(杂质不溶于水、不参与反应)。下列说法不正确的是( )A.上述三处操作中均需要进行过滤 B.溶液A中ZnSO4的质量大于CuSO4的质量 C.溶液A的质量大于溶液B的质量 D.溶液C中溶质的质量分数大于或等于溶液B中溶质的质量分数3.(2021•南阳模拟)粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如图所示:(1)写出Ⅰ中发生反应的化学方程式 ;(2)加入过量Na2CO3的作用是 。4.(2021•江西模拟)高纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产。某兴趣小组按如图所示实验步骤,模拟工业流程制备高纯碳酸钙。(1)“操作1”和“操作2”的名称是 。(2)“酸溶”过程中,将一定浓度的盐酸缓慢加入粉碎后的优质石灰石中,同时搅拌。搅拌的目的是 。(3)“转化”过程中除氯化钙、氨气、二氧化碳外水也参与了反应,反应的化学方程式为 。(4)上述工艺流程中可以循环使用的物质是 。5.(2021•官渡区一模)2020年是北京故宫建成600周年。红墙黄瓦是故宫的标志,涂制故宫的红墙使用的是铁红颜料,其主要成分为Fe2O3。工业上以硫酸亚铁为原料生产铁红颜料和副产品K2SO4固体的主要工艺流程如图。已知:①反应Ⅰ的化学方程式为FeSO4+2NH4HCO3═FeCO3↓+CO2↑+(NH4)2SO4+H2O。②NH4HCO3的分解温度为35℃。(1)反应Ⅰ需控制反应温度在35℃以下的目的是 。(2)反应Ⅲ中高温煅烧FeCO3的化学方程式为 。(3)反应Ⅳ中涉及到的物质在20℃时的溶解度如下表所示:物质(NH4)2SO4NH4ClK2SO4KCl溶解度/g75.437.211.134.2反应Ⅳ中发生反应的化学方程式为 。(4)滤液Ⅱ中的阴离子除含有SO42﹣之外还含有 (填离子符号)。6.(2021•赣州模拟)金属镉广泛用于合金制造及电池生产等,一种用铜镉废渣(含Cd、Zn、Cu、Fe及Co等单质)制取海绵镉的工艺流程如图(提示:Cd能与硫酸反应生成+2价,Co不反应)。(1)粉碎的目的是 。(2)操作①的名称是 。(3)除铁中发生的反应是6FeSO4+2KMnO4+4H2SO4═2 +3Fe2(SO4)3+K2SO4+4H2O。(4)沉镉中得到海绵镉发生反应的化学方程式: 。(5)流程中可循环利用的物质是 。
相关试卷
这是一份初中化学二轮复习【讲通练透】专题15 化学计算(讲通),文件包含专题15化学计算精讲讲义教师版docx、专题15化学计算精讲讲义学生版docx等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。
这是一份初中化学二轮复习【讲通练透】专题13 化学工艺流程专题(练透),文件包含专题13化学工艺流程专题专题跟踪检测教师版docx、专题13化学工艺流程专题专题跟踪检测学生版docx等2份试卷配套教学资源,其中试卷共28页, 欢迎下载使用。
这是一份初中化学二轮复习【讲通练透】专题11 化学实验专题(讲通),文件包含专题11化学实验专题精讲讲义教师版docx、专题11化学实验专题精讲讲义学生版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。








