

2022天津南开区高三上学期期末考试化学试卷含答案
展开本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 100 分,考试用时 60
分钟。第Ⅰ卷 1 至 4 页,第Ⅱ卷 5 至 8 页。
答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并在规定位置粘贴考试用条形码。答题时,务必将答案涂写在答题卡上,答在试卷上无效。
第Ⅰ卷(选择题,共 36 分)
注意事项:
每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
可能用到的相对原子质量:H 1C 12N 14O 16Al 27P 31Cl 35.5Cr 52
一、选择题(本题包括 12 小题,每小题 3 分,共 36 分。每小题只有一个选项符合题意)
我国提出争取在 2030 年前实现碳达峰,2060 年前实现碳中和,这对于改善环境,实现绿色发展至关重要。“碳中和”是指 CO2 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效的是
A.开采可燃冰作为新能源B.研发催化剂将 CO2 还原为甲醇
C.将重油裂化为汽油作为燃料 D.通过清洁煤技术减少煤燃烧污染
某白色固体混合物由 NaCl、KCl、MgSO4、CaCO3 中的两种组成,进行如下实验:①混合物溶于水,得到澄清透明溶液;②做焰色试验,透过钴玻璃可观察到紫色;③向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为
A.KCl、CaCO3B.KCl、NaCl
C.MgSO4、NaClD.KCl、MgSO4 3.下列说法正确的是
A.电负性:Se > AsB.离子半径:Na+ > Cl−
C.第一电离能:Al > MgD.键长:Cl−Cl > Br−Br
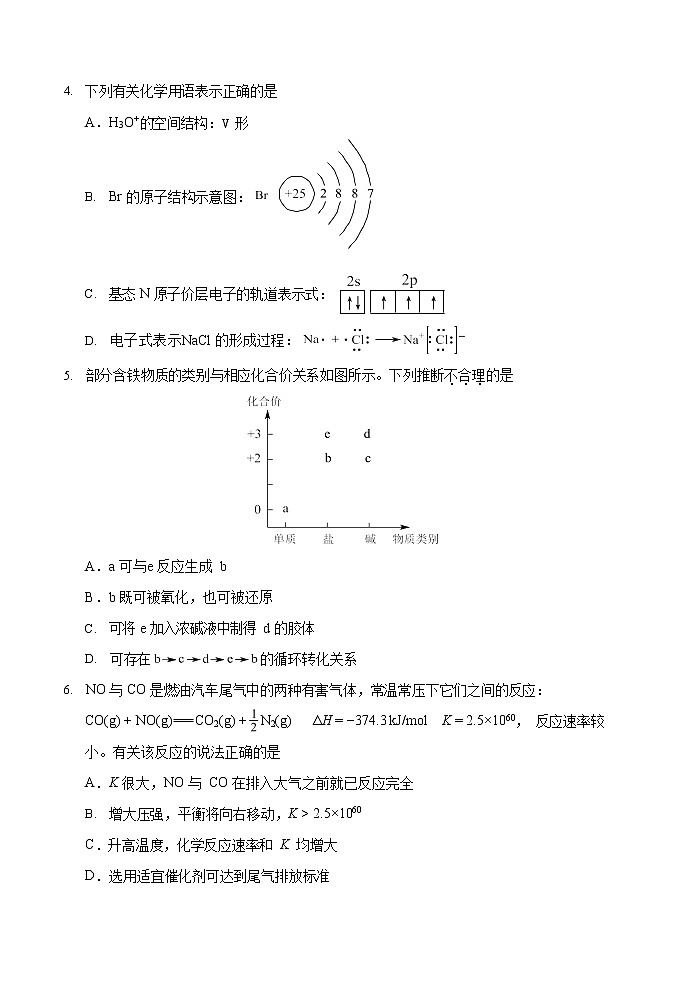
下列有关化学用语表示正确的是A.H3O+的空间结构:V 形
Br 的原子结构示意图:
基态 N 原子价层电子的轨道表示式:
电子式表示NaCl 的形成过程:
部分含铁物质的类别与相应化合价关系如图所示。下列推断不.合.理.的是
A.a 可与e 反应生成 b
B.b 既可被氧化,也可被还原
可将 e 加入浓碱液中制得 d 的胶体
可存在的循环转化关系
NO 与 CO 是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
CO(g) + NO(g)CO2(g) +N2(g)ΔH = −374.3 kJ/mlK = 2.5×1060, 反应速率较
小。有关该反应的说法正确的是
A.K 很大,NO 与 CO 在排入大气之前就已反应完全
增大压强,平衡将向右移动,K > 2.5×1060 C.升高温度,化学反应速率和 K 均增大D.选用适宜催化剂可达到尾气排放标准
下列有关物质性质与用途具有对应关系的是A.NH3 极易溶于水,可用作制冷剂B.SiO2 熔点高硬度大,可用于制光导纤维
NaHCO3 受热易分解,可用于制胃酸中和剂
ClO2 具有强氧化性,可用于自来水的杀菌消毒
下列指定反应的离子方程式正确的是
3
A.向碳酸氢铵溶液中加入足量石灰水:Ca2+ + OH−+ HCO3− CaCO3↓+ H2O B.向NaIO3 酸性溶液中加入 NaI 溶液:IO − + 5I− + 6H+ 3I2 + 3H2O
3
C.向稀硝酸中加入Na2SO3 溶液:SO 2− + 2H+ SO2↑ + H2O
D.钠与水反应:Na + H2ONa+ + OH−+ H2↑
W、X、Y、Z 均为短周期主族元素,原子序数依次增加,且原子核外 L 电子层的电子数分别为 0、5、8、8,它们的最外层电子数之和为 18。下列说法一定正确的是
单质的熔点:Y > Z
阴离子的还原性:X > Y
C.W 与 Z 可形成离子化合物
D.氧化物的水化物的酸性:Z > Y
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示。
① H2(g) + I2(?)2HI(g)ΔH = −9.48 kJ/ml
② H2(g) + I2(?)2HI(g)ΔH = +26.48 kJ/ml
下列判断正确的是
A.HI(g)比 HI(s)热稳定性更好B.1ml 固态碘升华时将吸热 17 kJ
①中的 I2 为固态,②中的 I2 为气态
①的反应物总能量比②的反应物总能量高
有氧条件下,NO 在催化剂作用下可被 NH3 还原为 N2,反应机理如下图所示。
下列说法不.正.确.的是
A.V5+ =O 在反应中起到催化剂的作用
该转化过程中,仅O2 体现了氧化性
该转化过程中若O2 过量不利于 NO 转化为N2
D.该转化过程的总反应:4NH3 + 4NO + O24N2 + 6H2O
12.已知:A(g) + 2B(g)3C(g)ΔH ˂ 0,向一恒温恒容的密闭容器中充入 1 ml A 和
2 ml B 发生反应,t1 时达到平衡状态I,在 t2 时改变某一条件,t3 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如下图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡B.平衡时A 的体积分数 φ:φ(I) > φ(Ⅱ)
t2 时改变的条件:向容器中加入C
平衡常数 K:K(Ⅱ) ˂ K(I)
2021~2022 学年度第一学期南开区期末考试试卷
高三年级化学学科
第Ⅱ卷(非选择题,共 64 分)
注意事项:
用黑色墨水的钢笔或签字笔将答案写在答题卡上。
本卷共 4 题,共 64 分。
可能用到的相对原子质量:H 1C 12N 14O 16Al 27P 31Cl 35.5Cr 52
二、(本题包括 1 小题,共 16 分)
13.(16 分)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
Cr 是第 周期第 族元素。
基态 Cr 原子的核外电子有 种空间运动状态,有 个未成对电子。
Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为
。
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是 ,H2O 的键角小于 NH3,原因是 。
a nm
c nm
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是 原子。若 NA 表示阿伏加德罗常数的值,则该晶体的密度为 g∙cm−3(用含 a、c 和 NA 的代数式表示)。
三、(本题包括 1 小题,共 14 分)
14.(14 分)已知 X、Y、Z 为常见的单质,其它为化合物,X 的组成元素是地壳中含量最多的金属元素。B 是一种能使湿润的红色石蕊试纸变蓝的气体,D 是一种常见的两性氢氧化物。各物质间的转化关系如下图所示(部分条件与产物已略去)。
回答下列问题:
(1)E 是一种高能燃料,其组成元素与B 相同,1ml E 分子中不同原子的数目比为
1 : 2,且含有 18 ml 电子,则E 的化学式为 。
(2)NaClO 的电子式为 。
(3)X 的原子核外电子占据最高能级的电子云轮廓图为 形。
(4)A 与 H2O 反应的化学方程式为 。
(5)D 与强碱溶液反应的离子方程式为 。
(6)B 与NaClO 反应时,1 ml NaClO 参加反应,转移 2 ml 电子,该反应的化学方程式为。
(7)一定条件下,X 与 TiO2、C(石墨)反应只生成 F 和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成 1ml F 时放出 526 kJ 热量,其热化学方程式为 。
四、(本题包括 1 小题,共 18 分)
15.(18 分)化学是一门以实验为基础的学科,回答下列问题:
I.[Cu(NH3)4]SO4·H2O 晶体制备。
向盛有 4 mL 0.1 ml/L CuSO4 溶液的试管里滴加几滴 1 ml/L 氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为 ,
写出难溶物与氨反应的离子方程式: 。
再向试管中加入极性较 的试剂乙醇(填“大”或“小”),并用玻璃棒摩擦试管
壁,可以观察到有 色的[Cu(NH3)4]SO4·H2O 晶体析出。
4
检验晶体中是否含有 SO 2−的方法是 。
温度对化学反应速率的影响。
不同温度下分别进行硫代硫酸钠与硫酸的反应,写出该反应的化学方程式:
,可以通过比较 ,
判断该反应进行的快慢。
压强对化学平衡的影响。
如上图所示,用 50 mL 注射器吸入 20 mL NO2 和N2O4 的混合气体(使注射器的活塞位于 I 处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色先变
(填“深”或“浅”),又逐渐变 (填“深”或“浅”),气体颜色变化的原因是
。
五、(本题包括 1 小题,共 16 分)
16.(16 分)氮元素的单质及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
(1)已知:反应 i: N2(g) + 3H2(g)2NH3(g)ΔH1 = − 92.4 kJ/ml
反应 ii:2H2(g) + O2(g)2H2O(g)ΔH2 = − 483.6kJ/ml
则氨气完全燃烧生成氮气和水蒸气的热化学方程式为 。
已知反应 i 断开 1 ml 化学键所需的能量如下表。
则断开 1 ml N−H 键所需的能量是 kJ。
一定温度下,向 2 L 密闭容器中加入 1ml NH3,发生反应 i,H2 物质的量随时间的变化如图 1 所示。2min 内的平均反应速率 υ(NH3)= ,该反应的化学平衡常数 K 的表达式为 。相同温度下, 若开始加入 NH3 的物质的量是原来的 2 倍,则 H2 平衡时的物质的量 0.12 ml(填“>”、“=”或“<”)。
图 2 表示反应 i 在 500℃、60.0 MPa 条件下,原料气投料比与平衡时 NH3 体积分数的关系。根据图中 M 点数据计算 N2 的平衡体积分数是 。
图 3 表示反应 i 平衡时 NH3 体积分数随温度或压强变化的曲线,图中 L(L1、L2)、 X 分别代表温度或压强。其中 X 代表的是 (填“温度”或“压强”),试判断 L1 L2
(填“>”、“=”或“<”)。N≡N
H−H
N−H
键能/kJ·ml −1
945
436
?
2023年天津南开区高三二模化学试卷含答案解析: 这是一份2023年天津南开区高三二模化学试卷含答案解析,共10页。
2023年天津南开区高三一模化学试卷含答案解析: 这是一份2023年天津南开区高三一模化学试卷含答案解析,共12页。
2022天津南开区高二上学期期末考试化学试题含解析: 这是一份2022天津南开区高二上学期期末考试化学试题含解析,文件包含天津市南开区2021-2022学年高二上学期期末考试化学试题含解析docx、天津市南开区2021-2022学年高二上学期期末考试化学试题docx等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。












