




化学专题5 药物合成的重要原料——卤代烃、胺、酰胺第三单元 有机合成设计评优课ppt课件
展开核心素养 发展目标
1.根据有机物分子中的化学键和官能团,理解碳骨架的变化及官能团衍变的反应规律,掌握官能团引入、转化及消除的方法。
2.形成对有机反应多角度认识的基本思路;建立分析有机物分子结构的思维模型,并利用模型进一步掌握有机合成和推断的基本方法和步骤。
一、重要有机物之间的相互转化
二、有机合成的一般过程
重要有机物之间的相互转化
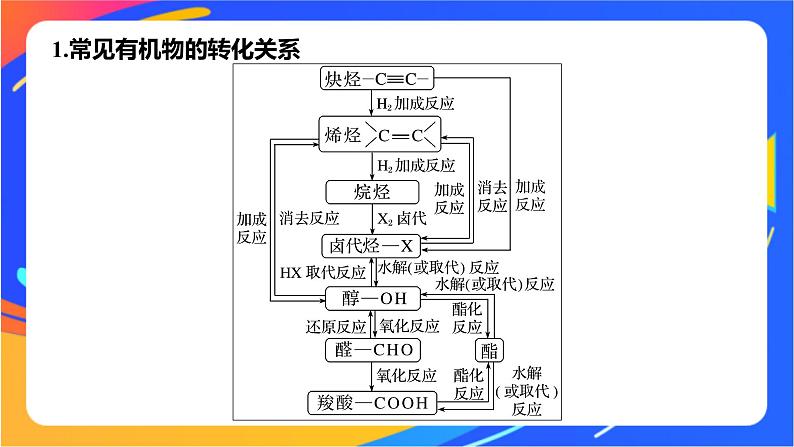
1.常见有机物的转化关系
2.常见官能团引入或转化的方法(1)碳碳双键①醇的消去反应CH3CH2OH __________________。②卤代烃的消去反应CH3—CH2—Br+NaOH _________________________。③炔烃的不完全加成反应CH≡CH+HCl ____________。
CH2==CH2↑+H2O
CH2==CH2↑+NaBr+H2O
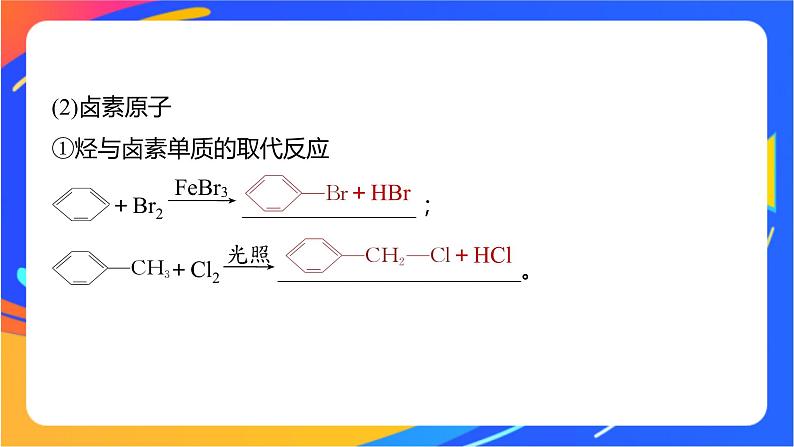
(2)卤素原子①烃与卤素单质的取代反应 +Br2 _______________; +Cl2 _____________________。
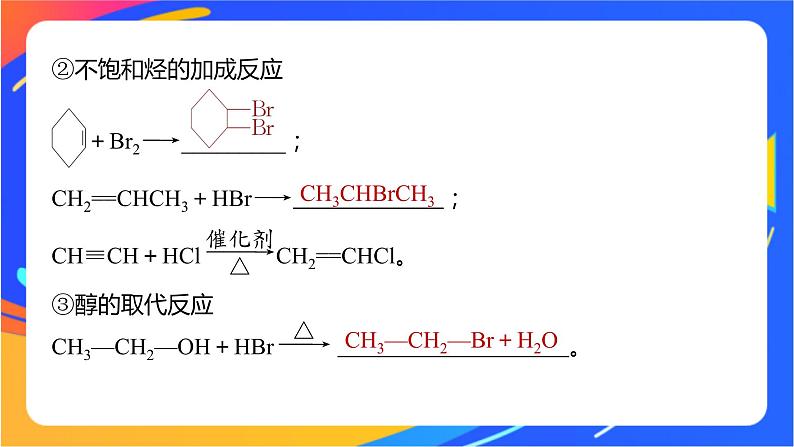
②不饱和烃的加成反应 +Br2―→_________;CH2==CHCH3+HBr―→ ;CH≡CH+HCl CH2==CHCl。③醇的取代反应CH3—CH2—OH+HBr 。
CH3—CH2—Br+H2O
(3)羟基①烯烃与水的加成反应CH2==CH2+H2O 。②卤代烃的水解反应CH3—CH2—Br+NaOH 。
CH3CH2—OH+NaBr
③醛或酮的还原反应CH3CHO+H2 ; +H2 ______________。
④酯的水解反应CH3COOCH2CH3+H2O ;CH3COOCH2CH3+NaOH 。熟悉烃及其衍生物之间的相互转化是有机合成的基础。
CH3COOH+CH3CH2OH
CH3COONa+CH3CH2OH
3.医药工业合成“扑热息痛”的过程
氯苯 对硝基氯苯 对硝基苯酚 对氨基苯酚 对乙酰氨基酚
其中的母体 不变,苯环上的 发生变化,也就是说有机化合物之间的转化,实质就是在一定条件下 发生的变化。
1.结合官能团的引入和转化方法,分析如何由乙烯合成乙酸乙酯?写出转化过程,并指明每步反应的反应类型。
2.结合官能团的转化关系分析由2-丁烯制备1,3-丁二烯的转化过程。
提示 CH3CH==CHCH3 CH2==CHCH==CH2。
3.有机化合物的性质主要取决于它所具有的官能团,有机化合物的反应往往围绕官能团展开,了解官能团之间的相互转化,能帮助我们进一步掌握有机化合物的内在联系:写出各有机物之间转化的化学方程式:①________________________________;②____________________________;③____________________________________________;
CH3CH3+Br2 CH3CH2Br+HBr
CH2==CH2+HBr―→CH3CH2Br
CH3CH2Br+KOH CH2==CH2↑
④___________________________;⑤________________________________________;⑥___________________________________;⑦__________________________________________;
CH2==CH2+H2 CH3CH3
CH2==CH2+H2O
CH3CH2OH CH2==CH2↑
2CH3CH2OH+O2 2CH3CHO+2H2O
⑧__________________________________________;⑨__________________________________________;⑩______________________________;⑪__________________________________________;
CH≡CH+H2 CH2==CH2
CH3COOC2H5+H2O CH3COOH+C2H5OH
⑫__________________________________________________;⑬_______________________________________________;⑭_____________________________________。
CH3COOCH2CH3+H2O
CH3CH2Br+NaOH
CH3CH2OH+NaBr
CH3CH2OH+HBr CH3CH2Br+H2O
4.将 直接氧化能得到 吗?如果不能,请写出合理的转化过程。
提示 不能。该转化的要求是只将醇羟基转化为羧基,但是在此过程中酚羟基也易被氧化,因此需要先对酚羟基实施保护。具体的转化过程可以为
1.富马酸(反式丁烯二酸)与Fe2+形成的配合物为富马酸铁,又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线:
回答下列问题:(1)A的化学名称为_______;由A生成B的反应类型为_________。
环己烷 取代反应
(2)C的结构简式为__________。
(3)富马酸的结构简式为________________。
由框图转化信息可知A、B、C分子的碳骨架无变化,可知B为 、C为 ;由强酸制弱酸可知,丁烯二酸钠酸化可得富马酸( )。
2.已知:①环己烯可以通过丁二烯与乙烯发生环化加成反应得到:
(也可表示为 )
②实验证明,下列反应中反应物分子的环外双键比环内双键更容易被氧化:
③R—CHO+H2―→R—CH2OH现仅以丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
请按要求填空:(1)A的结构简式是_______________;B的结构简式是___________。
(2)写出下列反应的化学方程式和反应类型:反应④:__________________________,反应类型:__________。反应⑤:___________________,反应类型:__________。
理解题给信息是解决本题的关键,因为原料是丁二烯,通过碳碳双键之间的环化加成反应可以得到六元碳环。目标产物的六元环的支链为甲基,由信息②及C的分子式知,可先将支链中的碳碳双键氧化,得到醛基,从醛基得到甲基的理想途径是醛基被还原得到醇羟基,通过醇的消去反应得到碳碳双键,再与氢气加成得到甲基。故其合成路线如下:
1.已知起始原料和目标产物的有机合成(1)有机合成过程示意图
(2)应用例析①一元化合物合成路线(以酯的合成为例)
③芳香族化合物合成路线a.
2.逆合成分析法它是将目标化合物倒退一步,寻找上一步反应的中间原料,即前体,依次倒推,最后确定最适宜的__________和最终的合成路线。其基本思路是,将目标分子中的化学键切断或转换官能团,推出拟合成目标分子的前体,再根据前体推出最初的原料。(1)基本思路
(2)基本原则①确定合成路线中的各步反应时,应尽可能选择反应条件温和、产率高的反应。②所使用的基础原料和辅助原料应该是 、 、易得和廉价的。
(3)应用例析由“逆合成分析法”分析由乙烯合成草酸二乙酯的具体步骤如下:①草酸二乙酯分子中含有两个酯基,按酯化反应规律将酯基断开,得到 和 ,说明目标化合物可由 和 通过酯化反应得到:
②羧酸可由醛氧化得到,乙二酸的前体应该是乙二醛: ⇒________;
③乙二醛的前体是乙二醇: ⇒ ;④乙二醇的前体是1,2-二氯乙烷。1,2-二氯乙烷可通过乙烯的加成反应而得到: ⇒__________⇒ ;⑤乙醇可以通过乙烯与水的加成得到。
根据以上分析,合成步骤如下(用化学方程式表示):ⅰ:CH2==CH2+H2O CH3CH2OHⅱ:CH2==CH2+Cl2ⅲ: +2NaOH +2NaCl
ⅳ:ⅴ: +2CH3CH2OH +2H2O根据以上逆合成分析,合成步骤如下:
1.(2022·长沙质检)请用合成反应流程图表示出由 和其他无机物合成 最合理的方案(不超过4步)。例:
可采取逆合成分析法。由于目标产物为二元醇,且羟基位于相邻碳原子上,逆推其为碳碳双键与氯气加成后水解所得;碳碳双键可由卤代烃消去而得;而已知原料恰好为卤代烃,故只要将苯环加氢即可。
2.如何利用 合成 ?注:氨基与苯环直接相连,具有较强的还原性,易被氧化。
提示 应先把—CH3氧化成—COOH,再把—NO2还原为—NH2,防止当KMnO4氧化—CH3时,—NH2也被氧化。
1.由CH3CH==CH2和CH3COOH合成CH2(OOCCH3)CH(OOCCH3)CH2(OOCCH3)时,需要经过的反应是A.加成→取代→取代→取代B.取代→加成→取代→取代C.取代→取代→加成→取代D.取代→取代→取代→加成
根据有机物的结构简式可知,化合物是由丙三醇和乙酸通过酯化反应生成的;要生成丙三醇,需要1,2,3-三氯丙烷通过水解反应生成;生成1,2,3-三氯丙烷需要利用CH2ClCH==CH2和氯气通过加成反应生成;丙烯通过取代反应即生成CH2ClCH==CH2。
2.以 和 为原料合成 ,请用合成反应的流程图表示出最合理的合成方案(注明必要的反应条件)。提示:①②RCH2CH==CH2+Cl2 RCHClCH==CH2+HCl;③合成反应流程图示例如下(无机试剂可任选):
3.香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎的作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和乙二酸。
提示:Ⅰ.CH3CH==CHCH2CH3 CH3COOH+CH3CH2COOH;Ⅱ. R—CH==CH2 R—CH2—CH2Br。请回答下列问题:
(1)写出化合物C的结构简式:_________________________。
A是芳香内酯,其分子式为C9H6O2。由A→B是酯的水解反应。由B的分子式为C9H8O3结合题给信息Ⅰ和C被氧化的产物,可以推出A的结构简式为 ;从而推出水解产物B的结构简式为 ;由C的分子式,结合B C,则推出C的结构简式为 。
(2)在上述转化过程中,反应步骤B―→C的目的是____________________________。
B→C 的目的是把酚羟基保护起来,防止下一步C的氧化破坏酚羟基。
(3)请设计合理方案由 合成 (用反应流程图表示,并注明反应条件)。例:由乙醇合成聚乙烯的反应流程图可表示为CH3CH2OH CH2==CH2 CH2-CH2
由 ,采用逆合成分析法则有:←―― ;正向分析则要把 转变成—CH2CH2—OH。通过消去、加成、水解等过程,结合题给信息R—CH==CH2R—CH2—CH2—Br完成转变。最后再进行酯化成环反应,生成目标产物内酯。
(1)逆合成分析法设计有机合成路线的思维程序①观察目标分子结构,即目标分子的碳骨架特征,以及官能团的种类和位置。②由目标分子逆推原料分子,并设计合成路线,即目标分子碳骨架的构建,以及官能团的引入和转化。③依据绿色合成的思想,对不同的合成路线进行优选。
(2)有机合成中常见官能团的保护①酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH溶液反应,把—OH变为—ONa(或使其与CH3I反应,把—OH变为—OCH3)将其保护起来,待氧化后再酸化将其转变为—OH。②碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。
③氨基(—NH2)的保护:如在对硝基甲苯 对氨基苯甲酸的过程中应先把—CH3氧化成—COOH之后,再把—NO2还原为—NH2。防止当KMnO4氧化—CH3时,—NH2(具有还原性)也被氧化。
1.已知酸性: >H2CO3> ,综合考虑反应物的转化率和原料成本等因素,将 转变为 的最佳方法是A.与稀H2SO4共热后,加入足量NaOH溶液B.与稀H2SO4共热后,加入足量Na2CO3溶液C.与足量的NaOH溶液共热后,再加入适量H2SO4D.与足量的NaOH溶液共热后,再通入足量CO2
先在氢氧化钠溶液中水解,转化为 ,因为酸性 >H2CO3> ,故再通入足量CO2转变为 。
2.已知苯与一卤代烷在催化剂作用下发生反应生成苯的同系物, +CH3X +HX。在催化剂存在的条件下,应选择苯和下列哪组物质为原料合成乙苯A.CH3—CH3和Cl2 B.CH2==CH2和Cl2C.CH2==CH2和HCl D.CH3—CH3和HCl
根据题给信息,合成乙苯应该选择的原料是苯和氯乙烷。乙烷与氯气在光照下发生取代反应,生成一氯乙烷、二氯乙烷等多种取代产物,既难得到纯净的乙苯,又浪费了原料,A项错误;乙烯与氯气反应生成1,2-二氯乙烷,与苯反应不能得到乙苯(产物比较复杂),B项错误;乙烯与氯化氢反应生成一氯乙烷,它与苯反应只能生成乙苯和氯化氢,合成过程中,氯化氢可以循环使用,C项正确;乙烷与氯化氢不反应,得不到氯乙烷,D项错误。
题组二 有机官能团的引入和转化3.下列有关说法错误的是A.通过还原反应可以消去醛基B.消去反应不能改变官能团的种类C.酯的水解可以产生羧基D.通过取代反应可以引入卤素原子
4.在有机合成中,常会将官能团消除或增加,下列相关过程中反应类型及相关产物不合理的是A.乙烯→乙二醇:CH2==CH2
D.乙烯→乙炔:CH2==CH2 CH≡CH
B项,由溴乙烷→乙醇,只需溴乙烷在碱性条件下水解即可,路线不合理,且由溴乙烷→乙烯为消去反应。
5.(2022·北京高二期中)在有机合成中官能团的引入或改变是极为重要的,下列说法正确的是A.甲苯在光照下与Cl2反应,主反应为苯环上引入氯原子B.引入羟基的方法常有卤代烃和酯的水解、烯烃的加成、醛类的还原C.将CH2==CH—CH2OH与酸性KMnO4溶液反应即可得到CH2==CH—COOHD.HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化 反应即可得到
甲苯在光照下与Cl2反应,主反应为甲基上引入氯原子,故A错误;卤代烃水解为醇,酯水解为酸和醇,烯烃与水发生加成反应生成醇,醛与氢气发生还原反应生成醇,故B正确;碳碳双键、羟基都能被酸性高锰酸钾溶液氧化,CH2==CH—CH2OH与酸性KMnO4溶液反应不能得到CH2==CH—COOH,故C错误;HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化、加聚反应可得到 ,故D错误。
题组三 有机合成路线的设计与选择6.在有机合成中,若制得的有机化合物较纯净且易分离,在工业生产上才有实用价值。据此判断下列有机合成一般不适用于工业生产的是A.酚钠与卤代烃作用合成酚醚: + +NaBrB.乙烷与氯气在光照下制备氯乙烷:CH3CH3+Cl2 CH3CH2Cl+HClC.萘与浓硫酸制备萘磺酸: +HO—SO3H +H2OD.乙烯水化制乙醇:CH2==CH2+H2O CH3CH2OH
乙烷与氯气在光照下发生取代反应,反应生成的有机物是多种氯代乙烷的混合物。
7.以溴乙烷为原料制备乙二醇,下列方案最合理的是
题干中强调的是最合理的方案,A项与D项相比,步骤多一步,且在乙醇发生消去反应时,容易发生分子间脱水、氧化反应等副反应;B项步骤最少,但取代反应不会停留在“CH2BrCH2Br”阶段,副产物多,分离困难,原料浪费;C项比D项多一步取代反应,显然不合理;D项相对步骤少,操作简单,副产物少,较合理。
题组四 有机合成方法的分析与应用8.以乙醇为原料,用下述6种类型的反应:①氧化;②消去;③加成;④酯化;⑤水解;⑥加聚来合成乙二酸乙二酯( )的正确顺序是A.①⑤②③④ B.①②③④⑤C.②③⑤①④ D.②③⑤①⑥
以乙醇为原料合成乙二酸乙二酯,经过以下几步:第一步,乙醇发生消去反应生成乙烯;第二步,乙烯发生加成反应生成二卤代烃;第三步,二卤代烃水解生成乙二醇;第四步,乙二醇氧化生成乙二酸;第五步,乙二醇与乙二酸发生酯化反应生成乙二酸乙二酯。涉及的反应类型按顺序依次为②③⑤①④,C项正确。
9.(2022·天津高二期中)下面是以环戊烷为原料制备环戊二烯的合成路线,下列说法正确的是
A.A的结构简式为B.反应④的反应试剂和反应条件是浓H2SO4、加热C.①②③的反应类型分别为卤代、水解、消去D.环戊二烯与Br2以物质的量之比为1∶1加成可生成
根据上述分析可知A是环戊烯( ),A错误;反应④是 转化为 的反应,反应条件是NaOH的乙醇溶液、加热,B错误;根据前面分析可知①是取代反应,②是消去反应,③是加成反应,C错误;环戊二烯与Br2以物质的量之比为1∶1加成时,若发生1,4-加成反应,可生成 ,D正确。
10.食品香精菠萝酯的生产路线(反应条件略去)如下:
下列叙述错误的是A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应D.步骤(2)产物中残留的烯丙醇可用溴水检验
A项中利用 的显色反应可进行检验,正确;B项中 和菠萝酯中的 均可以被酸性KMnO4氧化,正确;
C项中苯氧乙酸中的羧基、菠萝酯中的酯基都可与NaOH溶液反应,正确;D项中步骤(2)的产物也含 ,能使溴水褪色,错误。
11.我国自主研发对二甲苯的绿色合成路线示意图如下:下列说法正确的是A.过程①发生了取代反应B.中间产物M的结构简式为C.利用相同原料、相同原理也能合成邻二甲苯D.该合成路线理论上碳原子的利用率为100%
异戊二烯与丙烯醛发生加成反应,生成4-甲基-3-环己烯甲醛,A错误;通过M的球棍模型可以看出六元
环上甲基的邻位有一个双键,所以M的结构简式为 ,B错误;根据合成路线,可以合成对二甲苯和间二甲苯,不能合成邻二甲苯,C错误;该合成路线包含两步,第一步为加成反应,第二步为脱水反应,两步的碳原子利用率均为100%,D正确。
12.对氨基苯甲酸可用甲苯为原料合成,已知苯环上的硝基可被还原为氨基: ,产物苯胺还原性强,易被氧化。已知—CH3为邻、对位取代定位基,而—COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是
由甲苯制取产物时,需发生硝化反应引入硝基,再还原得到氨基,将甲基氧化才得到羧基;但氨基易被氧化,故甲基氧化为羧基应在硝基还原前,否则生成的氨基也被氧化,故先进行硝化反应,再将甲基氧化为羧基,再将硝基还原为氨基,故A正确、D错误;另外还要注意—CH3为邻、对位取代定位基,而—COOH为间位取代定位基,所以B错误。
13.(2022·新乡高二月考)化合物F是合成心脏病治疗药法西多曲的中间体,其合成路线如图所示:(1)C中含氧官能团的名称为______和______。
C的结构简式为 ,其中含氧官能团的名称为醚键、酯基。
(2)A→B的反应类型为____________。
反应中A中的羟基变为B中的醚键,则A→B的反应类型为取代反应。
(3)写出同时满足下列条件的B的一种同分异构体的结构简式:___________________________________________。①能与FeCl3溶液发生显色反应,不能发生银镜反应;②苯环上有4个取代基,分子中只有4种不同化学环境的氢原子。
(或 )
能与FeCl3溶液发生显色反应,不能发生银镜反应,因此B的同分异构体中含有酚羟基,不含醛基,B的分子式为C8H6O3,不饱和度为6,苯环的不饱和度为4,剩下2个不饱和度为碳
碳三键,且苯环上有4个取代基,分子中只有4种不同化学环境的氢原子,分子中共有6个氢原子,则该分子结构对称,符合条件的结构简式为 或 。
(4)请写出以H2C==CH2、H2C(COOC2H5)2、 为原料制备 的合成路线流程图(无机试剂和有机溶剂任选,合成路线流程图示例见本题题干)。
以H2C==CH2、H2C(COOC2H5)2、 为原料制备 ,根据F的合
成路线可知,H2C==CH2和氯气发生加成反应生成1,2-二氯乙烷, 发生水解反应经酸化后再和1,2-二氯乙烷发生取代反应,再经氧化反应、取代反应生成目标产物。
14.(2022·合肥高二期中)M是一种重要材料的中间体,其结构简式为 。合成M的一种途径如下: A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。已知:①Y的1H核磁共振谱只有1组峰;②RCH==CH2 RCH2CH2OH;③两个羟基连接在同一个碳原子上不稳定,易脱水。
请回答下列问题:(1)D中官能团的名称是_____,Y的结构简式是______________。(2)步骤①的反应类型是__________。
(3)下列说法不正确的是__(填字母)。a.A和E都能发生氧化反应b.1 ml B完全燃烧需6 ml O2c.C能与新制的氢氧化铜反应d.1 ml F最多能与3 ml H2反应
反应⑤为取代反应,可推知E为 。反应⑥为卤代烃的水解反应,酸化得到F为 ,由M的结构可知D为(CH3)2CHCOOH,逆推可知C为(CH3)2CHCHO、B为(CH3)2CHCH2OH,结合信息②可知A为
(CH3)2C==CH2,Y发生消去反应得到A,而Y的1H核磁共振谱只有1组峰,则Y为 。
A为(CH3)2C==CH2,E为 ,均可以燃烧,碳碳双键、酚羟基都易被氧化,均可以发生氧化反应,故a正确;B为(CH3)2CHCH2OH,1 ml B完全燃烧需要6 ml O2,故b正确;
C为(CH3)2CHCHO,含有醛基,能与新制的氢氧化铜反应,故c正确;F为 ,苯环、醛基均与氢气发生加成反应,1 ml F最多能与4 ml H2反应,故d错误。
(4)步骤⑦的化学方程式是________________________________________________________________________。
(5)M经催化氧化得到X(C11H12O4),X的同分异构体中同时满足下列条件的结构简式为_____________________________________。a.苯环上只有两个取代基,苯环上的一氯代物有2种;b.水解只生成芳香醇和二元酸,且二元酸的1H核磁共振谱只有2组峰。
M[ ]经催化氧化得到X(C11H12O4),则X为 ,X的同分异构体中同时满足下列条件:a.苯环上只有两个取代基,苯环上的一氯代物有2种,说明含有2个不同的取代基,且处于对位;b.水解只生成芳香醇和二元酸,且二元酸的1H核磁共振谱只有2组峰,符合条件的同分异构体为 。
15.(2022·乐山高二检测)格氏试剂是一种比较常见的C—C偶联试剂,其合成方法及偶联反应如下:RX+Mg RMgX(X=Cl、Br、I);RMgBr+R′CHO―→ +HOMgBr。根据以下合成路线回答问题:
(1)B的化学名称是_______;C中含有官能团的名称为_____。(2)由A生成B和由C生成D的反应类型分别是_________、_________。(3)E中含有两个苯环结构,则E的结构简式为______________。
苯乙醛 羟基
氧化反应 消去反应
(4)写出C→D的化学方程式:_____________________________________________________。
(5)A的所有同分异构体中,其中属于芳香族的种类为_____种。
结合合成路线及已知信息分析如下:由已知信息分析 →A,故A的结构简式为 ,A→B是氧化反应,故B的结构简式为 ,
简式为 ,结合已知信息分析,E的结构简式为 。
由已知信息分析B→C,故C的结构简式为 ,C→D是消去反应,故D的结构
醚官能团异构可分析, 的苯环一元取代同分异构体有3种,苯环二元取代同分异构体有9种,苯环三元取代同分异构体有6种,共18种。
由题可知,若想知道A的所有同分异构体中属于芳香族的种类,则写出 含苯环的同分异构体即可,从位置异构和醇、
(6)请根据题给的有关物质间的转化信息,写出以正丙醇和甲醛为原料制备化合物 的合成路线(无机试剂任选)。
高中化学苏教版 (2019)选择性必修3第三单元 有机合成设计作业ppt课件: 这是一份高中化学苏教版 (2019)选择性必修3第三单元 有机合成设计作业ppt课件,共35页。
化学选择性必修3第三单元 有机合成设计图片课件ppt: 这是一份化学选择性必修3第三单元 有机合成设计图片课件ppt,共30页。
高中第三单元 有机合成设计优秀ppt课件: 这是一份高中第三单元 有机合成设计优秀ppt课件,共9页。PPT课件主要包含了3形成环醚等内容,欢迎下载使用。













