








沪教版化学九上·5.3《金属防护和废金属回收》(课件+教案含练习)
展开第5章 金属的冶炼与利用
第3节 金属防护和废金属回收
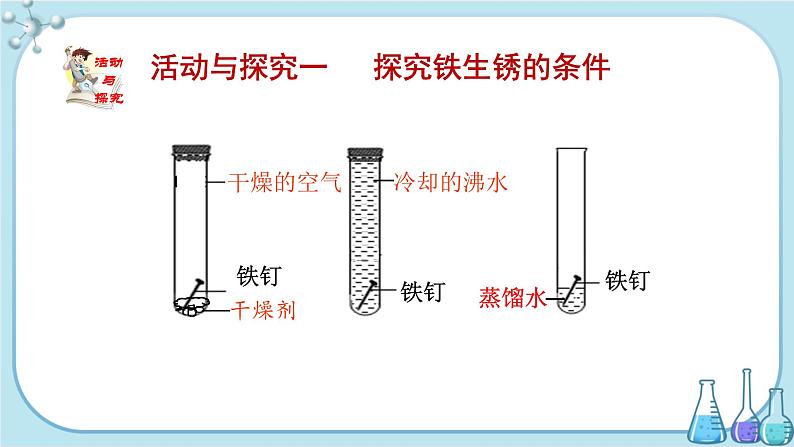
设计说明 本课题分三部分。第一部分通过铁钉生锈的对比实验探究钢铁锈蚀的条件;第二部分通过钢铁锈蚀条件及对生产生活中防锈的实例和图片的交流讨论,总结得出防锈的简单方法;第三部分自主学习,知道废弃金属对环境的污染,认识回收金属的重要性。 在教学中,利用课件中图片将大量的生活信息形象、真切地展示给学生。通过教师所做对比实验,学生分析归纳得出钢铁锈蚀的条件。通过生活实例及根据钢铁锈蚀的条件分析得出防止金属锈蚀的简单方法。使学生在讨论交流中取长补短,培养学生的合作意识。 通过创设教学情境,符合学生已有思维模式和知识结构,使钢铁生锈条件和燃烧条件、金属防锈方法和灭火方法,形成新旧知识之间关于学习方法的联系,帮助学生形成新的知识体系。 教学目标 【知识与技能】 1.知道钢铁锈蚀的条件。 2.了解防止金属锈蚀的简单方法。 3.知道废弃金属对环境的污染,认识回收金属的重要性。 【过程与方法】 1.通过关于对钢铁锈蚀的条件的探究,掌握对比实验的设计思路及控制变量法的具体操作。 2.通过对实验的观察和分析,学习对事实进行分析得出结论的科学方法。 【情感、态度与价值观】 认识处理废金属,回收废金属的价值,提高资源意识和环保意识。 重点难点 教学重点 铁生锈的原因及防止铁生锈的办法。 教学难点 铁生锈的原因。 教学方法 探究法:通过学生的探究实验,引导学生正确推理,概括出铁锈蚀的条件。 讨论法:通过分析讨论、归纳总结出科学合理的防锈方法。 教具、学具 1.计算机多媒体教学系统、CAI课件等。 2.稀盐酸、试管、纸槽、剪刀、磁铁、食品中“双吸剂”。 授课时数 1课时 教学过程 导入新课 【复习导入】教师多媒体展示金属腐蚀的图片。 我们知道金属腐蚀会造成危害,并且金属腐蚀每年都会给世界造成巨大的经济损失。而且人们每年都会向自然界索取大量的矿产资源,提炼金属。所以金属的腐蚀和防护已成为我们重要的课题。本节课我们就来学习金属腐蚀的原理以及如何进行防护 讲授新课 一、钢铁的锈蚀及其防护 【教师导入】钢铁是最常用的金属材料,根据生活经验,钢铁在干燥的空气中不易生锈,在潮湿的空气中容易生锈。那我们如何通过实验来探究铁生锈的条件? 【实验探究】引入课题并让学生看课本第127页的活动与探究。给出适当提示:看清5支试管中的铁钉分别处于什么样的环境中,是否与水接触。 【图片展示】图片展示一天、三天、一周后5枚铁钉的变化情况,学生观察现象,并根据表格汇总情况回答。
【学生质疑】①②两支试管中的铁钉为什么没有生锈,而③中的铁钉会生锈呢? 【教师总结】通过对比分析,钢铁生锈的原因实际上是铁跟氧气、水等物质相互作用,发生一系列复杂的化学反应,使铁转化为铁的化合物的过程。 【教师提问】为什么④⑤两支试管中的铁钉锈蚀严重呢?和哪些物质有关呢? 【教师总结】在氧气、水存在的环境中,稀硫酸、氯化钠溶液等能加快铁的锈蚀。 【教师导入】根据所做的实验的现象,你们认为铁生锈与哪些因素有关? 【教师总结】铁制品锈蚀的过程实质是铁跟氧气、水等物质作用,发生一系列复杂的化学反应,转化为铁的化合物的过程。稀硫酸、醋酸溶液和氯化钠溶液等物质存在时,能加快铁的锈蚀。 由此可见,金属的锈蚀是需要条件的,如要有能够发生反应的物质,反应物要能相互接触,生成物不会对反应起阻碍作用等。 【学生讨论】1.铁锈的主要成分是什么?它是纯净物吗? 铁锈能像氧化铝膜一样阻止铁继续生锈吗? 请同学们看第128页并描述铁锈的结构及主要成分。阅读第129页拓展视野了解铝的“自我保护”。 【教师总结】铁锈是混合物,成分复杂,主要是Fe2O3。铁锈的结构很疏松。不能阻碍里层的铁继续与氧气、水分等反应,因此铁制品可以完全锈蚀。 【教师展示】教师展示不同环境下铁钉的锈蚀,学生了解不同环境下铁钉的锈蚀情况不同。 不同环境下铁钉的锈蚀 【教师导入】我们知道了铁锈蚀原理。那自然就会想到,如果要防止铁生锈,它的原理是什么呢? 【教师总结】防止铁生锈的原理是要阻止铁同时与氧气、水接触。 【合作讨论】1.通过对铁制品锈蚀条件的探究,你对防止铁制品锈蚀有什么建议。 2.自行车的构件如支架、链条、车圈等,分别采用了什么防锈措施。 【师生总结】常用的防锈方法 1.保持铁制品表面的洁净和干燥。 2.在铁制品表面涂覆保护层,例如涂油、刷漆、搪瓷、烤蓝等。 3.涂上一层不易锈蚀的金属——电镀。 4.改变铁制品的内部结构,将其制成不锈钢。 【教师展示】教师多媒体展示镀铬、镀锌、涂防锈油、涂漆的物品,拓展知识。 镀铬 镀锌 涂防锈油 涂漆 二、废金属的回收利用 【教师导入】由于金属制品长期使用以及更新换代,产生了许多废弃的金属,面对这些废金属我们该如何处理呢?展示相关废金属的图片,这些废金属有哪些危害呢? 我国在回收某些废金属方面有哪些成就。 【合作讨论】学生阅读教材第129页内容,讨论问题。 1.废金属回收利用的好处有哪些? 2.保护金属资源的方法有哪些? 【师生总结】废金属回收利用的好处:保护环境,节约资源和能源。 保护金属资源的方法:防止金属腐蚀,回收利用废金属,有计划、合理地开采矿物。 【课外拓展】城市中废金属的处理回收过程。 【教师展示】教师展示城市矿山的图片,拓展知识。 城市矿山 典型例题 例1.现在,由于城市道路经常出现拥堵现象,于是人们改用骑自行车出行,既体现了健康的生活方式又体现了绿色环保,下列有关说法正确的是( ) A.自行车车架用锰钢制造,具有韧性好、强度大的优点 B.自行车有些部件用铝合金制成,铝合金具有密度小、熔点高、抗腐蚀性好的性质 C.自行车链条是用喷漆来进行防锈 D.自行车在南方比北方更耐用 解析:自行车车架用锰钢制造,具有韧性好、强度大的优点,A正确;自行车有些部件用铝合金制成,铝合金具有密度小、熔点低、抗腐蚀性好的性质,B错误;自行车链条不能用喷漆来进行防锈,应用涂油的方法进行防锈,C错误;自行车在北方比南方更耐用,D错误。 答案:A 例2.下列关于铁的说法正确的是( ) A.铁锈的主要成分是Fe3O4,铁丝燃烧的产物是Fe2O3 B.铁元素是地壳中含量最多的金属元素 C.铁锈很致密,能防止铁进一步氧化 D.铁丝生锈是缓慢氧化 解析:铁锈的主要成分是Fe2O3,铁丝燃烧的产物是Fe3O4,A错误;铝元素是地壳中含量最多的金属元素,B错误;铁锈是一种疏松多孔的物质,不能防止铁进一步氧化,C错误;铁丝生锈是缓慢氧化,D正确。 答案:D 例3.为保证航母的使用寿命,下列防锈措施,不可行的是( ) A.用抗锈蚀性能优异的合金制造航母零部件 B.刷防锈漆 C.船体表面镀一层金或其他不活泼贵金属 D.给某些部位涂油 解析:用抗锈蚀性能优异的合金制造航母零部件,能防止零部件生锈,A正确;刷防锈漆,能隔绝氧气和水,能防止生锈,B正确;船体表面镀一层金或其他不活泼贵金属,不活泼贵金属资源有限、价格太高,这种方法是不现实的,防锈措施不可行,C错误;给某些部位涂油,能隔绝氧气和水,能防止生锈,D正确。 答案:C 例4.下列关于金属的说法正确的是( ) A.回收废金属只是为了减少污染 B.铜的化学性质不活泼,所以铜制品不会生锈 C.篮球架的表面喷涂油漆,主要是为了美观 D.“真金不怕火炼”说明金的化学性质稳定 解析:回收废金属既节约了资源,又减少了环境污染,A错误;铜在潮湿的空气中,在空气中的氧气、二氧化碳和水共同作用下发生反应,生成绿色的铜锈(碱式碳酸铜),B错误;篮球架的表面喷涂油漆,主要是为了防锈,C错误;“真金不怕火炼”说明金的化学性质稳定,在高温下也不易发生反应,D正确。 答案:D 课堂小结 铁生锈的主要条件是与空气和水(或水蒸气)直接接触,稀硫酸、醋酸溶液和氯化钠溶液等物质能加快铁的锈蚀。如果隔绝了空气和水,就能在一定程度上防止钢铁生锈。在钢铁表面涂油、刷漆、镀铬、镀锌、镀锡及制造耐腐蚀的合金,如不锈钢等,都能防止钢铁生锈。 保护金属资源的有效途径是防止金属腐蚀、回收利用废金属等。 当堂达标 1.下列关于金属的说法正确的是( ) A.铜质插头利用了铜的导电性 B.硬铝的硬度比铝小 C.在金属表面喷涂油漆是防止其锈蚀的唯一方法 D.Ag能将硝酸铜溶液中的铜置换出来 答案:A 2.如图所示,将足量的生铁粉用水均匀地粘在试管内壁上,将试管倒立在装有水的烧杯中。实验过程中,观察到试管内液面缓慢上升。下列分析正确的是( ) A.若在生铁粉中加入少量NaCl,不会加快铁粉生锈 B.水能进入试管的最大体积约为试管容积的 C.该实验中涉及反应的反应物只有铁、氧气 D.如把该铁粉改为木炭粉,两者的现象完全相同 答案:B 3.下列说法正确的是( ) A.酒精灯中的酒精洒了,在桌上燃烧起来,不要惊慌,应立即用水浇灭 B.把铁粉和炭粉混合均匀后就得到了铁的合金 C.保护金属资源的有效途径只有三种 D.被雨水淋湿的自行车须先用干布擦净后才能用带油的布擦 答案:D 4.下列有关金属资源的利用与防护解释不合理的是( ) A.在航母金属外壳覆盖涂料,主要是为了美观 B.用“烤蓝”的方法处理钢铁表面,可减缓钢铁的腐蚀 C.用铝合金制造飞机机壳,是利用铝合金强度大、质量轻、抗腐蚀的性质 D.切菜后的菜刀用清水洗净擦干,可减缓菜刀生锈 答案:A 5.下列有关金属和金属材料的说法不正确的是( ) A.钢铁是使用最多的金属材料 B.高炉为工业炼铁使用的主要设备 C.铁制品在潮湿的空气中易生锈 D.“金银铜铁锡”俗称五金,在这五种金属中,金属活动性最强的是锡 答案:D 6.下列金属防护措施不正确的是( ) A.在金属制品表面镀保护层 B.改变金属结构制成合金使用 C.在金属制品表面涂油漆 D.用稀盐酸定期清洗金属制品 答案:D 7.(1)航母的甲板要求承受舰载机起落强烈的撞击和摩擦,制作甲板的钢材应具有的性质是 。 (2)为验证铝与镁的金属活动性顺序,分别将打磨过的铝条和镁条插入稀盐酸中,观察到镁比铝反应激烈。镁与稀盐酸反应的化学方程式是 。 (3)航母外壳用涂料覆盖是为了防止其与 接触而锈蚀。 答案:(1)韧性好、熔点高、硬度大 (2)Mg+2HCl═MgCl2+H2↑ (3)水和氧气 板书设计 第5章 金属的冶炼与利用 第3节 金属防护和废金属回收 一、钢铁的锈蚀及其防护 1.铁生锈的条件:铁与氧气、水同时接触,稀硫酸、醋酸溶液和氯化钠溶液等物质能加快铁的锈蚀。 2.钢铁的防护方法: ①保持表面洁净、干燥; ②在表面覆盖一层保护膜; ③改变金属的内部结构。 二、废金属的回收利用 | ||||||||||||||||||||||||||||||||||||||||||||









