





所属成套资源:科粤版化学九年级上册课件PPT+教案(内含练习)全套
科粤版化学九上·2.3《 构成物质的微粒(II)——原子和离子 (课时2)》(课件+教案含练习)
展开
这是一份科粤版化学九上·2.3《 构成物质的微粒(II)——原子和离子 (课时2)》(课件+教案含练习),共21页。
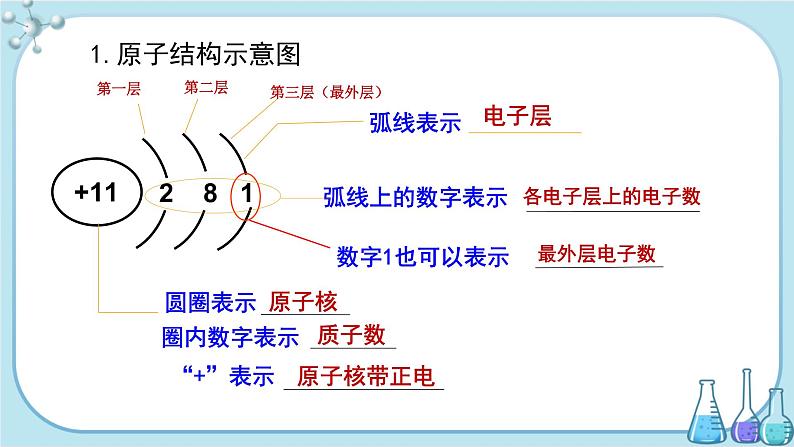
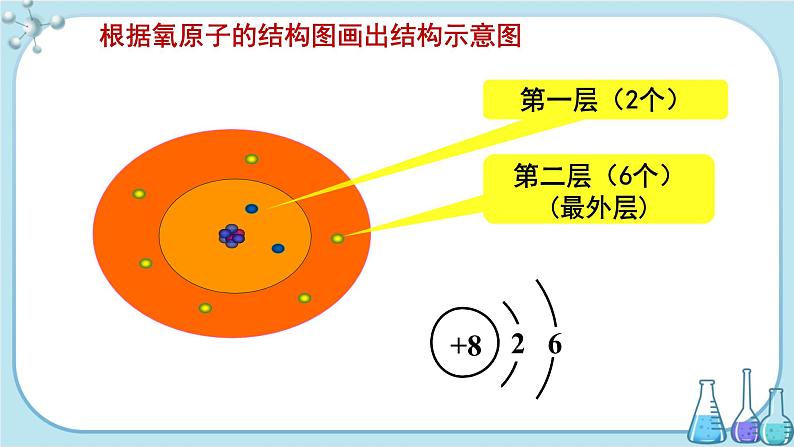
第二章 空气、物质的构成2.3 构成物质的微粒(Ⅱ)——原子和离子第二章 空气、物质的构成第2课时1.了解原子结构示意图的涵义,能表示前20种常见元素的原子结构示意图。2.知道原子核外电子排布与原子性质的关系3.了解原子质量的概念、能描述相对原子质量的含义。思考?电子在核外的空间里做高速的运动,它们会相互碰撞打架吗?电子在核外的排布会有什么特点?三、原子核外电子排布+11电子层原子核质子数各电子层上的电子数原子核带正电最外层电子数 2 8 11.原子结构示意图第一层(2个)第二层(6个)(最外层)根据氧原子的结构图画出结构示意图⑴第一层最多容纳___个电子,第二层最多容纳___个电子。2 (2)最外层不超过 个电子,只有1层的不超过___个电子。8 8 ⑶电子先排满第___层,再排第___层,排满第___层,再排第___层。(按照能量由低到高的顺序分层排布)2 3 21 2 2.原子核外电子排布核外电子排布的特点(1)各层最多能容纳的电子数为2n2个;(2)第一层最多容纳2个电子,第二层最多容纳8个电子,最外层不超过8个电子(若第一层为最外层时,不超过2个电子);(3)能量低的优先排满,依次再排能量逐步升高的电子层里。思考?金属元素和非金属元素的原子结构示意图有什么特点?3.原子结构与元素分类和元素化学性质的关系(1)金属元素:最外层一般少于4个电子,易失去最外层电子,化学性质活泼。(2)非金属元素:最外层一般等于或大于4个电子,易得到电子,化学性质活泼。(3)稀有气体元素:最外层8个电子(氦2个),称稳定结构,化学性质不活泼。结论:1.元素的化学性质与原子的最外层电子数有着密切关系。2.最外层电子数决定元素的化学性质。 原子核虽小,但整个原子的质量几乎都集中在核上,这是因为每个质子和每个中子的质量,都大约等于1个氢原子的质量,而电子的质量仅仅约等于质子质量的1/1836。这样小的数字,书写、记忆和使用起来都很不方便,就像用吨做单位来表示一粒稻谷或小麦的质量一样,能不能用一种好写、好记、好用的方法来表示原子的质量呢?不同原子的质量各不相同,可以用现代科学仪器精确地测量出来。如:一个氢原子的质量是:1.67×10-27㎏,一个氧原子的质量是:2.657×10-26㎏,一个铁原子的质量是:9.288×10-26㎏。四、相对原子质量1.概念 以一种碳原子(C-12)的质量的1/12作为标准,把其他原子的质量跟这个标准相比较所得到的比值,叫做这种原子的相对原子质量。 2.计算公式 碳原子有多种,它们的质子数都是6,但中子数不同,可能是6或7或8等。这里所说的“一种碳原子”是指含有6个质子和6个中子的碳原子,其质量的1/12约为1.661×10-27 kg,近似等于一个质子或一个中子的实际质量。=相对原子质量于原子的质量的比较氧的相对原子质量=≈ 16氧原子质量标准已知:氧原子的质量=2.657×10-26kg≈ 1.66×10-27kg注意: 1.相对原子质量不是原子的实际质量,是一个比值。2.单位:为1(一般不写)。练一练解:氢原子的相对原子质量= 1.6726×10- 27 kg÷ 1.66×10- 27 kg ≈ 1 C-12的十二分之一的质量已知:C-12原子的质量=1.993X10-26 kg,氢原子的质量=1.6726×10- 27 kg。求:氢原子的相对原子质量?思考:质子和中子的近似相对质量是多大? 相对原子质量 ≈质子数 + 中子数3.相对原子质量和质子数、中子数之间的关系 尝试查阅一下如下几种元素的相对原子质量:磷、铝、氮、钠、硫、镁 看谁查得又快又准! 磷——31 铝——27 氮——14 钠——23 硫——32 镁——24 1.根据第51页表中数据,计算氢、碳、氧、铁的相对原子质量,并把结果填进该表空栏检查站2.下列说法正确的是( )A.一个碳原子的质量为1.993×10-26kg,所以碳的相对原子质量为1.993×10-26kgB.氢的相对原子质量为1,所以氢的原子质量为1gC.相对原子质量和原子质量间没有相互联系D.相对原子质量是一个比值1121656D191.右图为氯原子的结构示意图,下列有关说法错误的是( )A.氯原子的核电荷数为17B.氯原子最外层有7个电子C.氯原子的质子数为17D.在化学反应中氯原子容易失去电子D2.已知1个C-12原子的质量为akg,则实际质量为bkg的另一种原子的相对原子质量为( )A.12b/a kg B.12b/aC.12a/b D.12a/b kg3.氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( ) A.50 B.86 C.136 D.222B B4.俄罗斯科学家最近合成了核电荷数为114的元素的原子,经测定该原子的近似相对质量为289,则其中子数是____________。175谢 谢 观 看





