2023年高考第二次模拟考试卷-化学(广东A卷)(考试版)A3版
展开2023年高考化学第二次模拟考试卷(广东A卷)
高三化学
本卷满分100分,考试时间75分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32
第Ⅰ卷(选择题 共44分)
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
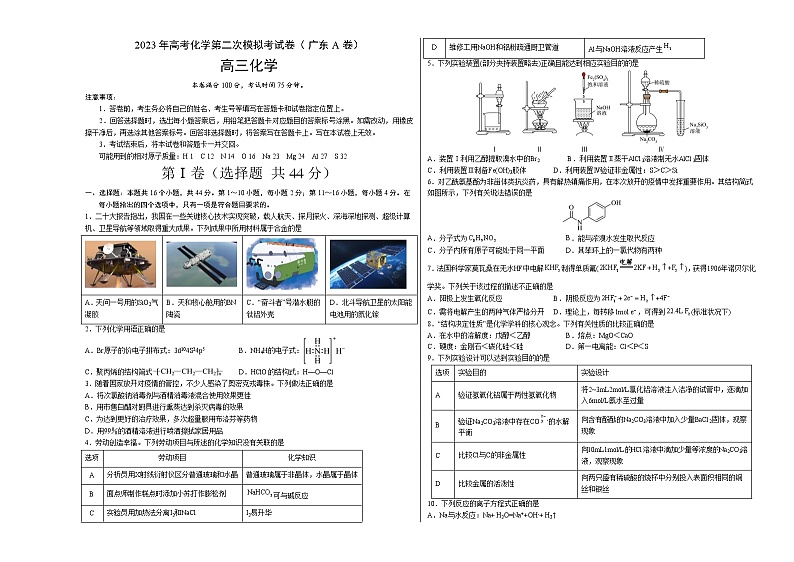
1.二十大报告指出,我国在一些关键核心技术实现突破,载人航天、探月探火、深海深地探测、超级计算机、卫星导航等领域取得重大成果。下列成果中所用材料属于合金的是
A.天问一号用的SiO2气凝胶 | B.天和核心舱用的BN陶瓷 | C.“奋斗者”号潜水艇的钛铝外壳 | D.北斗导航卫星的太阳能电池用的氮化镓 |
2.下列化学用语正确的是
A.Br原子的价电子排布式:3d104S24p5 B.NH4H的电子式:
C.聚丙烯的结构简式 D.HClO的结构式:H—O—Cl
3.随着国家放开对疫情的管控,不少人感染了奥密克戎毒株。下列做法正确的是
A.将次氯酸钠消毒剂与酒精消毒液混合使用效果更佳
B.用市售白醋对厨具进行熏蒸达到杀灭病毒的效果
C.为达到更好的治疗效果,多次超量服用布洛芬等药物
D.用99%的酒精溶液进行喷洒擦拭家居用品
4.劳动创造幸福。下列劳动项目与所述的化学知识没有关联的是
选项 | 劳动项目 | 化学知识 |
A | 分析员用X射线衍射仪区分普通玻璃和水晶 | 普通玻璃属于非晶体,水晶属于晶体 |
B | 面点师制作糕点时添加小苏打作膨松剂 | 可与碱反应 |
C | 实验员用加热法分离I2和NaCl | I2易升华 |
D | 维修工用NaOH和铝粉疏通厨卫管道 | Al与NaOH溶液反应产生 |
5.下列实验装置(部分夹持装置略去)正确且能达到相应实验目的的是
A.装置Ⅰ利用乙醇提取溴水中的Br2 B.利用装置Ⅱ蒸干AlCl3溶液制无水AlCl3固体
C.利用装置Ⅲ制备Fe(OH)3胶体 D.利用装置Ⅳ验证非金属性:S>C>Si
6.对乙酰氨基酚为非甾体类抗炎药,具有解热镇痛作用,在本次放开的疫情中发挥重要作用。其结构简式如图所示,下列有关说法错误的是
A.分子式为 B.能与浓溴水发生取代反应
C.分子内所有原子可能处于同一平面 D.其苯环上的一氯代物有两种
7.法国科学家莫瓦桑在无水HF中电解制得单质氟(),获得1906年诺贝尔化学奖。下列关于该过程的描述不正确的是
A.阳极上发生氧化反应 B.阴极反应为
C.需将电解产生的两种气体严格分开 D.理论上,每转移,可得到(标准状况下)
8.“结构决定性质”是化学学科的核心观念。下列有关性质的比较正确的是
A.在水中的溶解度:戊醇<乙醇 B.熔点:MgO<CaO
C.硬度:金刚石<碳化硅<硅 D.第一电离能:Cl<P<S
9.下列实验设计可以达到实验目的的是
选项 | 实验目的 | 实验设计 |
A | 验证氢氧化铝属于两性氢氧化物 | 将2~3mL2mol/L氯化铝溶液注入洁净的试管中,逐滴加入6mol/L氨水至过量 |
B | 验证Na2CO3溶液中存在CO-的水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,观察现象 |
C | 比较Cl与C的非金属性 | 向10mL1mol/L的HCl溶液中滴加少量等浓度的Na2CO3溶液,观察现象 |
D | 比较金属的活泼性 | 向两只盛有稀硫酸的烧杯中分别投入表面积相同的铜丝和银丝 |
10.下列反应的离子方程式正确的是
A.Na与水反应:Na+ H2O=Na++OH-+ H2↑
B.硫化钠水解反应:S2-+ H3O+ ⇌HS-+H2O
C.稀醋酸滴入NaOH溶液中:H++OH-= H2O
D.氢氧化钠溶液中通入足量二氧化碳:CO2+OH-=
11.工业烟气含有,可以用溶液进行绿色化处理后再排放。设为阿伏加德罗常数的值,下列说法正确的是
A.6.4 g 含有的电子数目为0.3
B.1 L 1 溶液中的数目为2
C.22.4 L(标准状况)与足量氧气反应,转移电子数目为2
D.1溶液最多能吸收的分子数目为0.1
12.用浓硫酸与乙醇共热制备乙烯时,常因温度过高发生副反应,使制备的乙烯气体中可能存在和等杂质气体,某同学将上述混合气体通入下列装置中以验证其成分,下列说法不正确的是
A.品红溶液a褪色证明气体中有
B.品红溶液b不变色且澄清石灰水变浑浊证明原乙烯气体中有
C.的生成体现了浓硫酸的氧化性
D.酸性高锰酸钾溶液可以氧化乙烯和
13.用方法可将汽车尾气中的和转化为无污染的气体。下列说法正确的是
A.过程中作催化剂
B.过程Ⅰ只发生还原反应,过程Ⅱ只发生氧化反应
C.为直线型非极性分子,一个分子内存在4个键
D.该过程的总反应为:
14.X、Y、Z、W、Q为原子序数依次递增的短周期主族元素。基态X原子价电子层有3个单电子,Z与Y可形成原子个数比为1∶1的含非极性共价键的离子化合物。W、Q的最外层电子数之和等于Z的原子序数。下列说法正确的是
A.简单离子半径:Z>Y B.X、W单质的晶体类型一定相同
C.简单氢化物的稳定性:X>Y D.Q的最高价含氧酸根离子的空间结构为正四面体形
15.一款低成本高能效的新型无隔膜铈铅单液流电池装置如图所示,该电池用石墨毡做电极,可溶性铈盐和铅盐的混合酸性溶液作电解液。已知电池反应为:。下列相关说法正确的是
A.放电时,在b电极发生还原反应
B.该电池可用稀硫酸酸化电解质溶液
C.充电过程中,a电极发生的反应为
D.放电过程中,电解质溶液中的向a电极移动
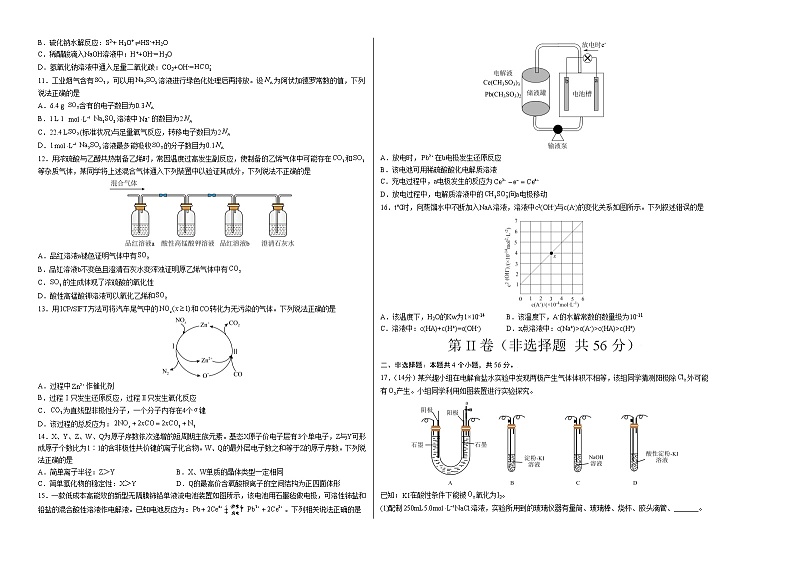
16.t℃时,向蒸馏水中不断加入NaA溶液,溶液中c2(OH-)与c(A-)的变化关系如图所示。下列叙述错误的是
A.该温度下,H2O的Kw为1×10-14 B.该温度下,A-的水解常数的数量级为10-11
C.溶液中:c(HA)+c(H+)=c(OH-) D.x点溶液中:c(Na+)>c(A-)>c(HA)>c(H+)
第II卷(非选择题 共56分)
二、非选择题:本题共4个小题,共56分。
17.(14分)某兴趣小组在电解食盐水实验中发现两极产生气体体积不相等,该组同学猜测阳极除外可能有产生。小组同学利用如图装置进行实验探究。
已知:在酸性条件下能被氧化为I2。
(1)配制溶液,实验所用到的玻璃仪器有量筒、玻璃棒、烧杯、胶头滴管、_______。
(2)利用上述装置检验阳极是否产生,其连接顺序为_______:A→_______→_______→_______。实验前从a处通入氮气的目的为_______。
(3)小组同学根据实验现象判断有产生,用电极反应式表示产生的原因_______。
(4)该小组在恒定电压下进行电解实验,探究不同、不同浓度的溶液对产生的影响,用传感器测得在时间内阳极区溶解氧的浓度变化,装置如图所示,数据记录如下表。
编号 | 溶解氧的浓度 | ||||
1 | 50.0 | 0 | 0 | 0 | 8.3~7.3 |
2 | 5.0 | 0 | 45.0 | 0 | 8.3~10.5 |
3 | 5.0 | 5.0 | x | 0 | 8.3~15.0 |
4 | 0 | 0 | 50.0 | 0 | 8.3 |
5 | 0 | 0 | 0 | 50.0 | 8.3~15.5 |
①实验2、3是判断相同浓度在不同下是否有氧气产生,其中_______。
②实验2和5条件下,测得溶解氧的曲线如图中Ⅰ、Ⅱ所示,分析实验2溶解氧先降低后升高的原因是_______。
③实验3中时间段内溶液溶解氧逐渐增大,电解后取阳极区溶液于试管a,加入淀粉溶液,没有明显现象;然后滴加稀硫酸,溶液变蓝。电解后另取阳极区溶液于试管b,加入淀粉溶液,溶液变蓝。由上述实验现象可获得的实验结论是_______。
④工业上在一定条件下电解食盐水制备较纯净的,除了控制一定的电压,采用活性电极外,可采取的措施有_______(写一种)。
18.(14分)钒(V)广泛应用于冶金、化工、航天等领域。一种以钒渣(主要成分是、、等)为原料制取金属钒的工艺流程如图所示:
已知:①具有强氧化性,主要存在于的溶液中,时转化成酸式多钒酸盐。
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | ||||
开始沉淀时()的pH | 1.9 | 7.0 | 8.1 | 8.9 |
沉淀完全时()的pH | 3.2 | 9.0 | 10.1 | 10.9 |
回答下列问题:
(1)中Fe为+2价,V的化合价为_______。
(2)“焙烧I”中转化为和的化学方程式为_______。
(3)“酸浸”所得浸出液中除含有、外,还含有的金属阳离子有_______。
(4)“沉钒”可得到沉淀,“焙烧II”中发生反应的化学方程式为_______。
(5)“沉钒”所得滤液中加入氨水调节溶液,过滤得到沉淀和溶液A,溶液A中浓度为,为尽可能多地回收,并避免中混入,应控制_______。溶液A经加氨沉淀除镁后,溶液中的溶质可再生循环到_______工序使用。
(6)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如下图所示:
①该钒的硫化物的化学式是_______
②该钒的硫化物的晶体中,与每个V原子最近且等距的S原子的个数是_______。
19.(14分)苯乙烯是生产塑料与合成橡胶的重要原料。氧化乙苯脱氢制苯乙烯的反应为:
反应I:
已知:
反应II:
反应III:
回答下列问题:
(1)反应I的__________。
(2)下列关于反应I~III的说法正确的是______(填标号)。
A.及时分离出水蒸气,有利于提高平衡混合物中苯乙烯的含量
B.保持恒定时,说明反应I达到化学平衡状态
C.其他条件相同,反应II分别在恒容和恒压条件下进行,前者乙苯的平衡转化率更高
D.反应III正反应的活化能小于逆反应的活化能
(3)在催化剂作用下,氧化乙苯脱氢制苯乙烯可能存在如下图所示反应机理:
该机理可表示为以下两个基元反应,请补充反应ⅱ:
ⅰ:;
ⅱ:__________.
(4)常压下,乙苯和经催化剂吸附后才能发生上述反应I。控制投料比[∶n(乙苯)]分别为1∶1、5∶1和10∶1,并在催化剂作用下发生反应,乙苯平衡转化率与反应温度的关系如图所示:
①乙苯平衡转化率相同时,投料比越高,对应的反应温度越______(填“高”或“低”)。
②相同温度下,投料比远大于10∶1时,乙苯的消耗速率明显下降,可能的原因是:
ⅰ.乙苯的浓度过低;
ⅱ.__________。
③850K时,反应经t min达到图中P点所示状态,若初始时乙苯的物质的量为n mol,则v(苯乙烯)=______。
(5)700K时,向恒容密闭容器中加入过量和一定量乙苯,初始和平衡时容器内压强分别为和,则平衡时苯乙烯的分压为______kPa(用含有、、p的代数式表示)。[已知:①混合气体中某组分的分压等于总压与该气体物质的量分数之积;以平衡分压代替平衡浓度进行计算,可得反应的分压平衡常数。② ]
20.(14分)水杨酸A具有解热镇痛的功效,其可作为医药工业的原料,用水杨酸制备平喘药沙丁胺醇的路线如下(表示;表示)
(1)化合物B的分子式为_______;E→F的反应类型为_______。
(2)化合物D中含有四种官能团,任选两种官能团进行检验。
限选试剂:溶液、稀硝酸、稀硫酸、新制氢氧化铜悬浊液、饱和溴水、硝酸银、溶液、溶液。
官能团名称 | 所选试剂 | 实验现象 |
_______ | _______ | _______ |
_______ | _______ | _______ |
(3)化合物M()是化合物A的同分异构体,其沸点M_______(填“高于”或“低于”)A,请解释原因_______
(4)化合物C有多种同分异构体,写出其中2种能同时满足下列条件的芳香族化合物的结构简式:_______、_______。
条件:①能发生水解反应且最多能与4倍物质的量的反应;
②核磁共振氢谱有四组峰,峰面积之比为。
(5)水杨酸因其酸性很强,对人的肠胃有刺激性,科学家对其结构进行一系列改造,研制出长效缓释阿司匹林(),不仅能减少对肠胃的刺激,且疗效更长,效果更佳。请设计出以水杨酸、乙二醇以及甲基丙烯酸为原料制备长效缓释阿司匹林的路线_______。
2023年高考第二次模拟考试卷-化学(湖南A卷)(考试版)A3版: 这是一份2023年高考第二次模拟考试卷-化学(湖南A卷)(考试版)A3版,共5页。试卷主要包含了下列说法错误的是等内容,欢迎下载使用。
2023年高考第二次模拟考试卷-化学(湖北A卷)(考试版)A3版: 这是一份2023年高考第二次模拟考试卷-化学(湖北A卷)(考试版)A3版,共5页。
2023年高考第二次模拟考试卷-化学(河北A卷)(考试版)A3: 这是一份2023年高考第二次模拟考试卷-化学(河北A卷)(考试版)A3,共5页。试卷主要包含了下列说法中错误的是等内容,欢迎下载使用。












