









化学必修 第一册第二节 离子反应优秀ppt课件
展开高中化学新教材特点分析及教学策略
(一)化学基本概念和化学基本理论:全套教材的知识安排,注意各年级内及各年级间的联系,在保证知识结构的系统性和完整性的同时,对内容的安排采用了将各部分知识分散处理,相对集中的方法。
(二)元素化合物知识:关于元素化合物知识,高一教材首先介绍了碱金属和卤素两个最典型的金属族和非金属族。
(三)化工基础知识:高一介绍了硅酸盐工业和环境保护知识。高二主要介绍合成氨工业,删掉了硝酸工业、钢铁工业和铝的冶炼。重点突出了合成氨工业中合成氨条件的选择。
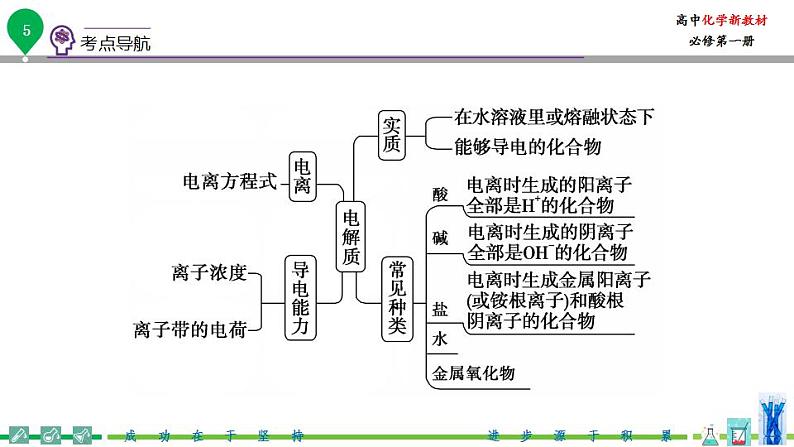
知识点一:一、电解质与导电原理
1.电解质
(1)导电实验
⇒
微提醒
(2)电解质与非电解质的比较
| 前提 | 条件 | 现象 | 实质 | 实例 |
电解质 | ① | 水溶液中或熔融状态下 | ② | ③ | HCl、NaOH、 BaSO4、Na2O等 |
非电解质 | 化合物 | ④ | 都不导电 | ⑤ | 酒精、蔗糖、NH3、SO3、CO2等 |
微提醒
(3)强电解质与弱电解质的比较
| 强电解质 | 弱电解质 |
定义 | 在水溶液中能① | 在水溶液中② |
电离平衡 | ③ | ④ |
溶液中存在微粒种类 | 离子、⑤ | 离子、⑥ |
电离过程 | ⑦ | ⑧ |
举例 | ①强酸:HCl、H2SO4、HNO3、HClO4、HBr、HI等; ②强碱:KOH、NaOH、Ba(OH)2等; ③绝大部分盐:BaSO4、BaCl2等 | ①弱酸:CH3COOH、HF、H2S、H2CO3等; ②弱碱:NH3·H2O、Cu(OH)2等; ③水(H2O) |
微提醒
2.电解质导电的分析
(1)能导电物质必须具备的条件是具有能 的、 的粒子。
(2)NaCl溶液导电的探究
①NaCl固体中含有带正电荷的离子 和带负电荷的离子 ,由于带相反电荷的离子间的相互作用,Na+和Cl-按一定规则紧密地排列着。这些离子不能 ,故干燥的NaCl固体不导电。
②NaCl固体加入水中,在水分子的作用下, 和 脱离NaCl固体的表面,进入水中,形成能够自由移动的 和 。
③在NaCl溶液中插入电极并接通电源,水合钠离子向与电源 极相连的电极移动,水合氯离子向与电源
极相连的电极移动,故NaCl溶液能够导电。
(3)NaCl熔融状态导电的探究
NaCl固体受热熔化,离子的运动随温度升高而加快,克服了离子间的相互作用,产生能够自由移动的
和 ,故熔融NaCl也导电。
微提醒
(4)电解质导电的两种模型认知
①电解质水溶液导电模型
②部分电解质熔融状态导电模型
【即学即练1】
1.秒判正误(正确的打“√”,错误的打“×”)
(1)金属与电解质溶液均可导电。( )
(2)铁丝、NaCl溶液和盐酸都能导电,所以三者都是电解质。( )
(3)KNO3溶液导电的原因是溶液中K+、NO在电场作用下可以定向移动。( )
(4)CO2溶于水能导电,因此CO2是电解质( )
(5)KHSO4只有在电流作用下才能电离成K+、H+和SO( )
(6)强电解质溶液的导电能力不一定都强,弱电解质溶液的导电能力不一定弱( )
(7)AgCl难溶于水,所以AgCl是弱电解质;醋酸铅易溶于水,所以醋酸铅是强电解质( )
(8)液态H2SO4、固态NaCl均不导电,所以H2SO4、NaCl均不是电解质。( )
(9)不含金属的化合物一定不是盐。 ( )
(10)强电解质饱和溶液一定比弱电解质饱和溶液的导电性强。( )
(11)Na2O溶于水和水反应生成NaOH,NaOH电离出离子,所以NaOH是电解质,Na2O是非电解质。( )
(12)BaSO4投入水中,导电性较弱,故它是弱电解质。( )
(13)强电解质都是离子化合物,弱电解质都是共价化合物。( )
(14)CaO是强电解质,是因为它的水溶液能导电。( )
(15)在溶于水或熔融状态下能够自身发生电离的化合物一定是电解质。( )
知识点二: 二、电解质的电离
1.电解质的电离
(1)强电解质的电离方程式中用“===”连接。
如Na2SO4:Na2SO4===2Na++SO
(2)弱电解质部分电离,用“”表示。
如HClO:
①多元弱酸分步电离,且电离程度逐步减弱,以第一步电离为主。
如H2CO3: 、
②多元弱碱分步电离,但通常一步写出。如Fe(OH)3的电离方程式为 。
③两性氢氧化物双向电离。如Al(OH)3的电离方程式为 。
(3)酸式盐的电离。
①强酸酸式盐完全电离,一步写出。如NaHSO4在水溶液中的电离方程式为 ,在熔融状态下的电离方程式为 。
②多元弱酸酸式盐,第一步完全电离,其余的部分电离。如NaHCO3在水溶液中的电离方程式为: 、 。
微提醒
2.从电离角度认识酸、碱、盐的本质
(1)酸:电离时生成的阳离子 的化合物。
(2)碱:电离时生成的阴离子 的化合物。
(3)盐:电离时生成 的化合物。
【即学即练2】
2.秒判正误,不正确的加以改正。
(1)HNO3===H+1+NO
(2)Ba(OH)2===Ba2++(OH-)2
(3)Na2SO4===Na+SO
(4)Al2(SO4)3===Al3++SO
(5)NaHSO4===Na++HSO
(6)NaHCO3===Na++H++CO
1.CO2、NH3的水溶液能导电,那么CO2、NH3是电解质吗?
【细剖精析】
2.BaSO4难溶于水,水溶液几乎不导电,BaSO4是非电解质,对吗?为什么?
【细剖精析】
3.液态HCl、H2SO4均不导电,故二者为非电解质对吗?为什么?
【细剖精析】
4.①NaCl晶体、液态HCl均不导电,则NaCl与HCl都不是电解质吗?②电解质导电的条件是什么?
【细剖精析】
5.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:
A B C
(1)灯泡不亮的原因是什么?在哪个烧杯中加水灯泡会变亮,变亮原因是什么?
【细剖精析】
(2)向烧杯C中加适量A(不过量)中的溶液后,溶液的导电性强弱如何变化?为什么?
【细剖精析】
【典例1】
如图所示,两烧杯中分别有同体积同物质的量浓度的盐酸和CH3COOH溶液,甲灯泡比较亮,乙灯泡比较暗。
问题思考:
(1)溶液的导电能力受哪些因素的影响?
(2)物质的量浓度相同的盐酸和CH3COOH溶液为何导电能力不同?
(3)小明从实验中得出结论“强电解质导电能力强,弱电解质导电能力弱”,这种说法对吗?为什么?
【典例2】
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。如图是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图。下列示意图中,能正确表示用NH3·H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是( )
题组A 基础过关练
1.(2022·浙江)下列物质能导电且属于电解质的是
A.Cu B.盐酸 C.熔融NaOH D.
2.(2022·全国)下列说法正确的是
A.蔗糖、硫酸钡均属于电解质
B.NH4Cl是电解质,所以NH4Cl溶液是电解质
C.电解质未必能导电,能导电的未必是电解质
D.Cl2的水溶液能导电,所以Cl2是电解质
3.(2022·全国·高一)下列说法正确的是
A.熔融NaCl能导电,是因为通电时NaCl发生了电离
B.NaCl固体不导电,因为NaCl固体中无带电微粒
C.NH4NO3电离时产生了NH、NO,无金属离子,所以NH4NO3不是盐
D.NaHSO4在水溶液中电离生成了Na+、H+、SO三种离子
4.(2022·浙江)下列物质属于非电解质的是
5.下列属于强电解质的是
A.H2SO3 B.HClO C.MgCl2 D.NH3·H2O
6.(2022·浙江杭州)下列物质的水溶液和熔融状态均能导电的是
A.Cl2 B.NaCl C.CH3CH2OH D.H2SO4
7.(2022·上海市)下列物质中是非电解质的是
A.NaCl B.HCl C.Cu D.SO3
8.(2022·吉林)下列说法正确的是
A.硫酸的导电能力比盐酸溶液强
B.氨气溶于水能导电,所以氨气是电解质
C.BaSO4、AgCl均不溶于水,所以BaSO4、AgCl不是电解质
D.碳酸氢钠在水中的电离方程式为NaHCO3=Na++
9.(2022·全国·高一)下列物质在水中的电离方程式正确的是
A.K2SO4=2K++SO
B.NaHSO4=Na++H++SO
C.NaHCO3=Na++H++CO
D.BaCl2=Ba2++Cl-
10.(2022·全国·高一)物质M在水中发生电离:M=X2++2Y-,则下列判断正确的是
A.M可能是酸 B.X2+一定是金属离子
C.Y-是OH- D.M一定属于盐
11.下列说法正确的是
A.在熔化状态下能导电的化合物为离子化合物
B.根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
C.非金属氧化物不一定是酸性氧化物
D.氨水能导电,所以氨水是电解质
12.(2022·吉林)下列关于电解质的说法正确的是
A.强电解质的导电能力一定比弱电解质导电能力强
B.CO2溶于水形成的溶液能导电,所以CO2是电解质
C.BaSO4难溶于水,所以是非电解质
D.NH4Cl在水溶液中完全电离,所以NH4Cl是强电解质
题组B 能力提升练
1.(2022·四川省内江市)分类法在化学学科的发展中起到了非常重要的作用,下列分类标准不合理的是
A.根据氧化物中是否含有金属元素,将氧化物分为酸性氧化物和碱性氧化物
B.根据电解质在水溶液中能否完全电离,将电解质分为强电解质和弱电解质
C.根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应
D.根据化合物在水溶液或熔融状态下能否导电,将化合物分为电解质和非电解质
2.(2022·云南·昆明一中高一期末)下列说法正确的是
A.溶于水能够导电,所以是电解质 B.液态HCl不导电,所以HCl是非电解质
C.电解质在通电的条件下才能发生电离 D.均属于电解质
3.(2022·吉林)下列关于电解质的说法正确的是
A.强电解质的导电能力一定比弱电解质导电能力强
B.CO2溶于水形成的溶液能导电,所以CO2是电解质
C.BaSO4难溶于水,所以是非电解质
D.NH4Cl在水溶液中完全电离,所以NH4Cl是强电解质
4.(2021·湖南)下列电离方程式正确的是
A. B.
C. D.
5.(2022·湖北·武汉东湖新技术开发区教育发展研究院高一期末)下列关于物质的分类组合正确的是
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 |
A | 超级钢 | 铁红 | 硫酸钡 | 食盐 | 氧化钠 |
B | 液氯 | 陨铁 | 碘化氢 | 次氯酸 | 酒精 |
C | 冰水 | 纯碱 | 氢氧化铁 | 氢氧化铝 | 二氧化硫 |
D | 硬铝 | 云雾 | 碳酸 | 氨气 | 氯化铜 |
A.A B.B C.C D.D
6.(2021·河北·石家庄市)下列说法不正确的是
①将BaSO4放入水中不能导电,所以BaSO4是非电解质
②氨溶于水得到的氨水能导电,所以氨水是电解质
③固态酸不导电,熔融态的酸可以导电
④固态的盐不导电,熔融态的盐也不导电
⑤强酸溶液的导电能力一定比弱酸溶液的导电能力强
⑥钠反应时失1个电子,镁失2个电子所以镁的还原性比钠强
A.①②③④⑤⑥ B.①④⑤ C.①②③④ D.①④⑥
7.(2022·全国·高一)现有下列物质:①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体⑨熔融氯化钠 ⑩胆矾晶体
请用序号填空:
(1)上述状态下,可导电的是_______。
(2)上述状态下,属于电解质但不能导电的是_______。
(3)属于电解质的是_______。
(4)属于非电解质的是_______。
8.回答下列问题:
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是_______(填序号)。
①硫酸钠溶液、②碳酸氢钠溶液、③氯化铵晶体、④氢氧化钡溶液、⑤干燥的氯化钠晶体、⑥蔗糖、⑦干燥的氢氧化钠固体、⑧稀硫酸。
(2)请写出下列物质电离方程式
NH4Cl:_______
Ba(OH)2:_______
NaHCO3:_______
题组C 培优拔尖练
1.以下11种物质为中学化学中常见的物质:
①Cu ②NaCl ③NaHSO4 ④SO3 ⑤H2SO4
⑥C2H5OH ⑦CaCO3 ⑧BaSO4 ⑨HCl
⑩NaOH ⑪NH3·H2O
请按下列要求回答问题。(注意:答案填序号)
(1)属于电解质的是____________________,非电解质的是____________________ 。
(2)在水溶液中能电离出H+的是________,属于酸的是________。
(3)属于碱的是________________,其中属于弱碱的是________。
(4)属于难溶性盐的是________,属于易溶性盐的是___________。
(5)属于强电解质的是________,属于弱电解质的是___________。
2.在两份相同的溶液中,分别滴入物质的量浓度相等的、溶液,其导电能力随滴入溶液体积变化的曲线如图所示.
请回答下列问题
写出溶液中,的电离方程式______.
图中①、②分别代表滴加哪种溶液的变化曲线①______②______
点,溶液中大量存在的离子是______.
、b两点对应的溶液均显______填“酸性”“中性”或“碱性”
曲线②中d点导电能力最弱的原因是______用化学方程式表示
点,两溶液中含有相同量的哪种离子______.
鲁科版 (2019)必修 第一册第2节 电解质的电离 离子反应评课ppt课件: 这是一份鲁科版 (2019)必修 第一册<a href="/hx/tb_c4002542_t3/?tag_id=26" target="_blank">第2节 电解质的电离 离子反应评课ppt课件</a>,共60页。
人教版 (2019)第一章 物质及其变化第一节 物质的分类及转化课文内容ppt课件: 这是一份人教版 (2019)第一章 物质及其变化第一节 物质的分类及转化课文内容ppt课件,文件包含高中化学新教材同步必修第一册第02讲物质的转化二教师版docx、高中化学新教材同步必修第一册第02讲物质的转化二学生版docx、高中化学新教材同步必修第一册第02讲物质的转化二pptx等3份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
化学第一节 物质的分类及转化背景图课件ppt: 这是一份化学第一节 物质的分类及转化背景图课件ppt,文件包含高中化学新教材同步必修第一册第01讲物质的分类与转化一pptx、高中化学新教材同步必修第一册第01讲物质的分类与转化一教师版docx、高中化学新教材同步必修第一册第01讲物质的分类与转化一学生版docx等3份课件配套教学资源,其中PPT共47页, 欢迎下载使用。












