

广东省汕头市金山中学2022-2023学年高一化学下学期3月阶段性考试试题(Word版附答案)
展开2022级高一第二学期阶段性考试
化学科试卷
可能用到的相对原子质量:H:1 C:12 N:14 O:16 S:32 Ba:137
一、单选题(本题包括18小题,每小题3分,共54分。请将答案填涂到答题卡上。)
1.古诗词是我们宝贵的精神财富。下列诗句中不涉及氧化还原反应的是
A.泉眼无声惜细流,树阴照水爱晴柔 B.春蚕到死丝方尽,蜡炬成灰泪始干
C.野火烧不尽,春风吹又生 D.爆竹声中一岁除,春风送暖入屠苏
2.下列化学用语或图示表达正确的是
A.2的电子式: B.HClO的结构式:H-Cl-O
C. 的电子式: D. 的结构式:N=N
3.下列物质在给定条件下不能一步转化的是
A.NaNa2O B.SSO3 C.CCO D.Cl2FeCl3
4. 设NA为阿伏伽德罗常数的值,下列叙述中正确的是
A. 常温常压下,28 g CO和N2的混合气体中含有原子数为2 NA
B. 1molCl2与1molFe完全反应时转移的电子数为3NA
C. 标准状况下,18 g水的体积为22.4L
D. 32 g S8单质(S8分子结构:)中,S—S共价键的数目为8NA
5.下列关于硫酸的叙述中,正确的一项是
A.常温下浓硫酸可以用铝罐或铁罐贮存,说明常温下铝、铁与浓硫酸不会反应
B.浓硫酸使蔗糖变黑,并产生大量气体,主要体现了浓硫酸的吸水性和强氧化性
C.浓硫酸能使胆矾由蓝色变为白色,体现浓硫酸的脱水性
D.将过量的铜加入到少量浓硫酸中加热充分反应,硫酸仍会有剩余
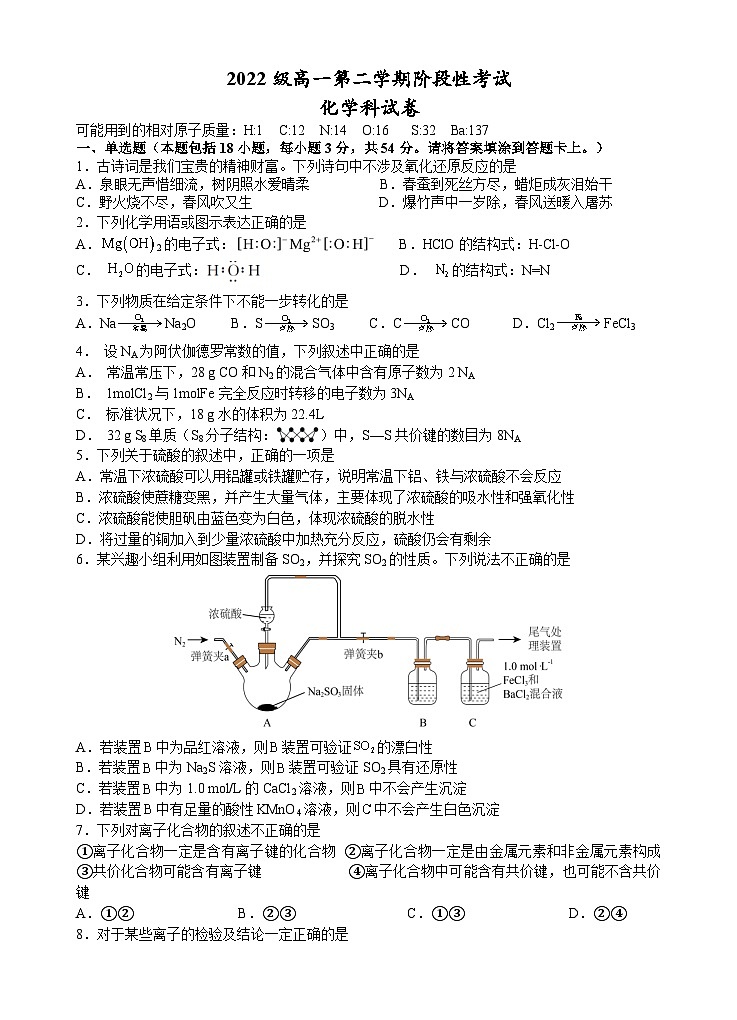
6.某兴趣小组利用如图装置制备SO2,并探究SO2的性质。下列说法不正确的是
A.若装置中为品红溶液,则装置可验证的漂白性
B.若装置中为Na2S溶液,则装置可验证SO2具有还原性
C.若装置中为1.0 mol/L的CaCl2溶液,则中不会产生沉淀
D.若装置中有足量的酸性KMnO4溶液,则中不会产生白色沉淀
7.下列对离子化合物的叙述不正确的是
①离子化合物一定是含有离子键的化合物 ②离子化合物一定是由金属元素和非金属元素构成 ③共价化合物可能含有离子键 ④离子化合物中可能含有共价键,也可能不含共价键
A.①② B.②③ C.①③ D.②④
8.对于某些离子的检验及结论一定正确的是
A.加入盐酸产生无色气体,将气体通入石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠并加热,产生气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
9. 下列离子能大量共存的是
A. 使无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、CO32-
B. 无色透明的溶液中:Cu2+、K+、SO42-、NO3-
C. 含有大量Ba(NO3)2的溶液中:Mg2+、NH4+、SO42-、Cl—
D. 使紫色石蕊试液呈红色的溶液中:Na+、K+、SO32-、NO3-
10.下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评价 |
A | 少量NaHSO4溶液与过量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | 正确 |
B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O=Fe(OH)3↓+3H+ | 正确 |
D | NaOH溶液中通入少量CO2:OH-+CO2=HCO3- | 正确 |
11.X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图,下列叙述正确的是
A.R的氧化物均为离子化合物
B.简单气态氢化物的稳定性:Y>Z
C.Y的氧化物均为酸性氧化物
D.含氧酸酸性:Z>M
12.用化学沉淀法去除粗盐中的Ca2+、Mg2+、SO42- 制精盐。实验室用下述方案模拟粗盐的精制:
下列说法不正确的是
A.溶解操作中需用玻璃棒搅拌,其目的是加速粗盐溶解
B.滤液中滴加盐酸直到没有气泡冒出,使滤液呈中性或微酸性
C.蒸发结晶时,当蒸发皿中出现较多固体时,停止加热,用余热使滤液蒸干
D.试剂1、试剂2、试剂3依次可选用Na2CO3溶液、NaOH溶液、BaCl2溶液
13.从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如图。下列说法错误的是
已知:I2+5Cl2+6H2O═2HIO3+10HCl,pH=2时,NaNO2溶液只能将I﹣氧化为I2,同时生成NO。
A.方案甲中,根据I2的特性,操作1的方法是升华
B.操作2中的萃取操作用到的主要仪器为分液漏斗
C.反应②的离子方程式是3I2+3CO32﹣═5I﹣+IO3﹣+3CO2↑
D.可用Cl2、酸性KMnO4等强氧化剂代替NaNO2
14.用黄铁矿为原料制硫酸产生的硫酸渣(含Fe2O3、SiO2、Al2O3、MgO等)提取铁红(Fe2O3)的过程如图所示。下列有关离子方程式判断和书写错误的是
A.酸溶过程中Fe2O3溶解的离子反应
方程式为
B.滤渣A(SiO2)溶解于NaOH溶液的离子方程式为
C.“还原”过程发生的离子反应方程式为
D.“氧化”过程发生的离子反应方程式为
15.下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。下列说法中不正确的是
A.当 X 是强酸时,A、B、C、D、E、F 中均含同一种元素,F 可能是 H2SO4
B.当 X 是强碱时,A、B、C、D、E、F 中均含同一种元素,F 是 HNO3
C.当 X 是强酸时,用 O2 代替 Cl2, 也能与 B 反应生成 C 物质
D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体
16. 实验室探究SO2与Fe(NO3)3溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
A.滴加浓硫酸之前应进行的操作是打开弹簧夹,
通入一段时间N2
B.Y中产生的白色沉淀是BaSO3
C.在X装置中浓硫酸不体现氧化性
D.若将Fe(NO3)3换成氨水,Y中也能产生白色沉淀
17.将n mol K2SO3和m mol Na2S溶于水,用稀硫酸酸化后,若生成物分别是:
①SO2和S ②H2S和S ③只有S,
则n与m之比值从(Ⅰ)1∶2,(Ⅱ)大于1∶2;(Ⅲ)小于1∶2中选出符合上述情况的组合是
A.(Ⅰ)(Ⅱ)(Ⅲ) B.(Ⅱ)(Ⅰ)(Ⅲ) C.(Ⅲ)(Ⅱ)(Ⅰ) D.(Ⅱ)(Ⅲ)(Ⅰ)
18.工业废气中氮氧化物是造成污染的主要来源。为了治污,工业上通常通入NH3与之发生下列反应:NOx+NH3→N2+H2O。现有NO、NO2的混合气体3 L,可用同温同压的3.5 L NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为
A.1∶1 B.2∶1 C.1∶3 D.1∶4
二、非选择题(本题共3道题,共46分。请将答案填写到答题卡上。)
19.(15分)按要求写出下列方程式。
(1)Cu与浓硫酸反应的化学方程式________________________________________________.
(2)碳与热浓硫酸反应的化学方程式_____________________________________________.
(3)亚硫酸钠溶液与稀硝酸反应的离子方程式_______________________________________.
(4)二氧化硫与硫酸铁溶液反应的离子方程式__________________________________.
(5)双氧水与酸性高锰酸钾溶液反应的离子方程式______________________________________.
20.(14分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。回答下列问题:
(1)A中发生反应的化学方程式是 .
(2)B中加入的物质是 ,
其作用是 .
(3)实验时在C中观察到得现象是 ,
发生反应的化学方程式是 .
(4)实验时在D中观察到的现象是 ,收集到的物质是 .
21.(17分)工业上由含铜废料(含有、、等)制备硝酸铜晶体的流程如图:
(1)写出CuS“焙烧”生成SO2和CuO的化学反应方程式:____________________________.
(2)“过滤”后需洗涤沉淀,请设计实验证明已洗涤干净_______________________________.
(3)“淘洗”所用的溶液A应选用____(填序号)a.稀硫酸b.浓硫酸c.稀硝酸d.浓硝酸
(4)“反应”步骤加10%H2O2可以避免污染性气体的产生,写出该反应的离子方程式:_______,
也可以用气体_______(填化学式)代替双氧水.
(5)大量排放SO2容易造成酸雨等环境问题,工业上
可用双碱脱硫法处理废气,过程如图所示,写出
双碱脱硫法的总反应方程式:_______.
(6)已知:混合气体为SO2与N2的混合气体,为测定
SO2在混合气体中的体积分数,实验小组设计了如图实验方案:
①W溶液可以是 (填标号)。
a.H2O2溶液 b.酸性KMnO4溶液 c.氯水
②该混合气体中气体SO2的体积分数为 (用含V、m的式子表示).
2022级高一第二学期阶段性考试 答案
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
答案 | A | C | B | A | D | B | B | C | A | B | A | D | D | C | D | B | D | C |
19.(每小题3分,共15分)
(1)
(2)
(3)3SO32-+2NO3-+2H+=3SO42-+2NO↑+H2O
(4)2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
(5)5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O
20.(每空2分,共14分)
(1)2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
(2)碱石灰(或CaO或NaOH) 除去NH3气流中的水汽(或干燥NH3)
(3)黑色粉末部分逐渐变为红色 2NH3+3CuON2+3H2O+3Cu
(4)出现无色液体 氨水
21.(除标记的外每空2分,共17分)
(1)
(2)取最后一次洗涤液于试管中,加入盐酸酸化的氯化钡溶液,若无白色沉淀产生,则沉淀已经洗涤干净(用铁氰化钾也可)
(3)a
(4)
(5)(3分)
(6)①ac ② ✕100%
广东省汕头市金山中学2023-2024学年高一化学上学期期中考试试题(Word版附答案): 这是一份广东省汕头市金山中学2023-2024学年高一化学上学期期中考试试题(Word版附答案),共8页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
广东省汕头市金山中学2022-2023学年高一化学下学期期中试卷(Word版附解析): 这是一份广东省汕头市金山中学2022-2023学年高一化学下学期期中试卷(Word版附解析),共17页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
广东省汕头市金山中学2022-2023学年高二化学下学期期中考试试题(Word版附答案): 这是一份广东省汕头市金山中学2022-2023学年高二化学下学期期中考试试题(Word版附答案),共8页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。












