
山东省滨州市2023届高三二模化学试题
展开试卷类型:A
高三化学试题
2023.5
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,共12页,满分100分,考试时间90分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上。将条形码横贴在答题卡对应位置“条形码粘贴处”。
2.第I卷每小题选出答案后,用2B铅笔在答题卡上将对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,不能答在试卷上。
3.第II卷所有题目的答案,考生须用0.5毫米黑色签字笔答在答题卡规定的区域内,在试卷上答题不得分。
4.考试结束,监考人员将答题卡收回。
可能用到的相对原子质量:H 1 C 12 O 16 P 31 Cl 35.5
第I卷 选择题(共40分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.2022年我国科技创新成果丰硕,下列有关说法正确的是( )
A.量子通信的光纤和超算“天河一号”的芯片主要材料均为
B.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
C.“北斗卫星”授时系统的“星载铷钟”含铷元素,其单质遇水能缓慢反应放出
D.C919民航客机机身材料中的复合纤维属于天然有机高分子
2.下列实验仪器的使用或实验操作正确的是( )
A.容量瓶和分液漏斗使用前均需检查是否漏水
B.用氨水清洗做过银镜反应的试管
C.滴定实验中,需用待装液分别润洗滴定管和锥形瓶
D.蒸发操作中,将蒸发皿放在铁架台的铁圈上,垫石棉网加热
3.卡塔尔足球世界杯处处体现“化学元素”,下列有关描述正确的是( )
A.局部麻醉剂中的氯乙烷有2种同分异构体
B.人造草坪中的聚乙烯和聚丙烯互为同系物
C.看台材料中的聚碳酸酯可通过缩聚反应制得
D.运动衣的主要材料,其两种单体的核磁共振氢谱峰数、峰面积均相同
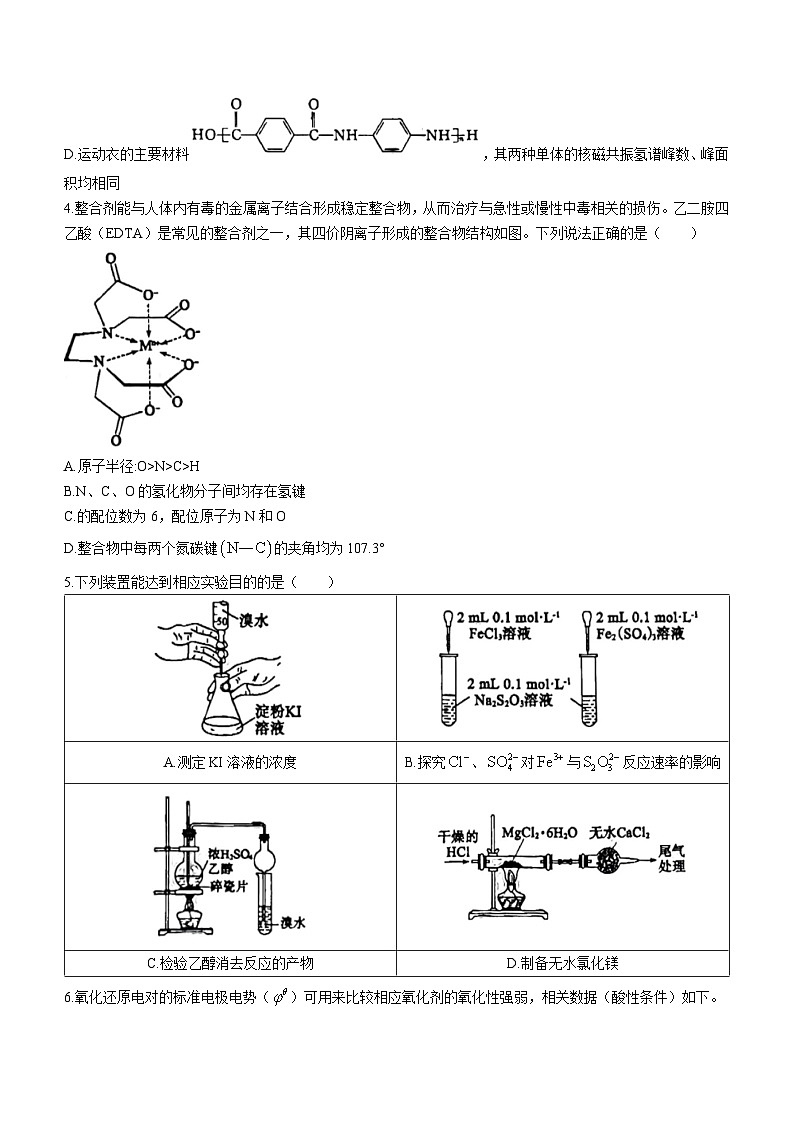
4.整合剂能与人体内有毒的金属离子结合形成稳定整合物,从而治疗与急性或慢性中毒相关的损伤。乙二胺四乙酸(EDTA)是常见的整合剂之一,其四价阴离子形成的整合物结构如图。下列说法正确的是( )
A.原子半径:O>N>C>H
B.N、C、O的氢化物分子间均存在氢键
C.的配位数为6,配位原子为N和O
D.整合物中每两个氮碳键的夹角均为107.3°
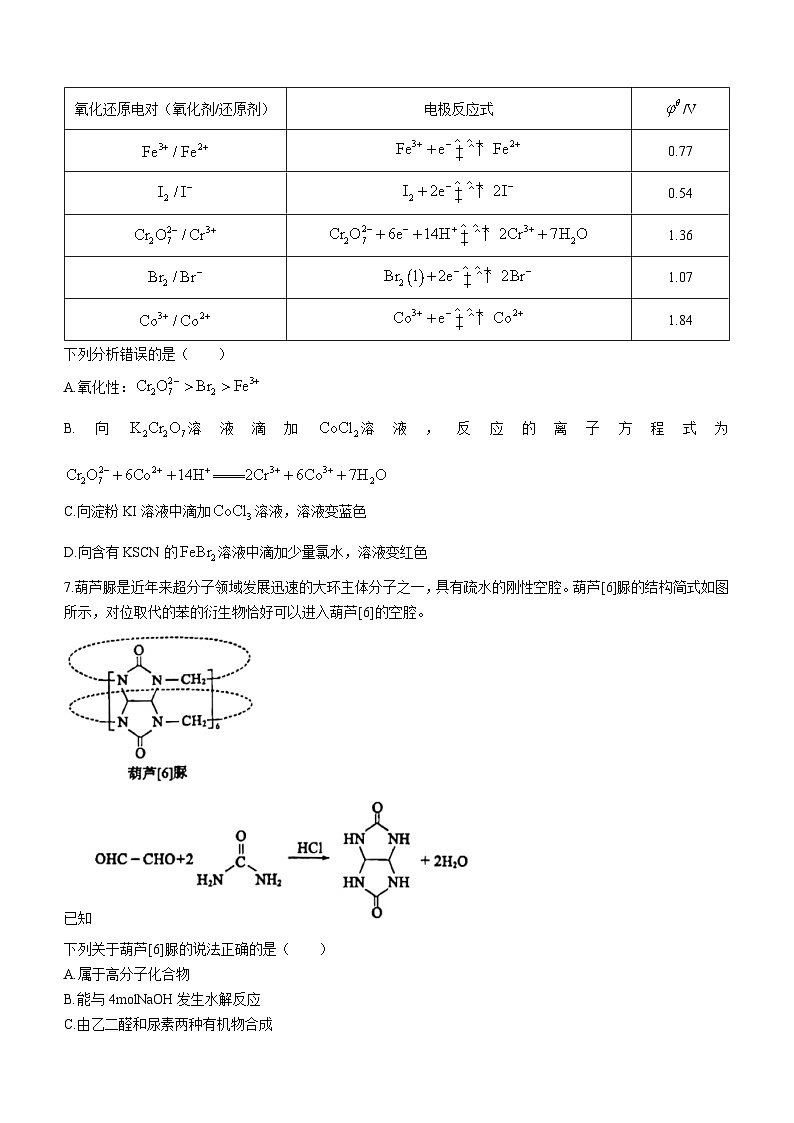
5.下列装置能达到相应实验目的的是( )
A.测定KI溶液的浓度 | B.探究、对与反应速率的影响 |
C.检验乙醇消去反应的产物 | D.制备无水氯化镁 |
6.氧化还原电对的标准电极电势()可用来比较相应氧化剂的氧化性强弱,相关数据(酸性条件)如下。
氧化还原电对(氧化剂/还原剂) | 电极反应式 | /V |
0.77 | ||
0.54 | ||
1.36 | ||
1.07 | ||
1.84 |
下列分析错误的是( )
A.氧化性:
B.向溶液滴加溶液,反应的离子方程式为
C.向淀粉KI溶液中滴加溶液,溶液变蓝色
D.向含有KSCN的溶液中滴加少量氯水,溶液变红色
7.葫芦脲是近年来超分子领域发展迅速的大环主体分子之一,具有疏水的刚性空腔。葫芦[6]脲的结构简式如图所示,对位取代的苯的衍生物恰好可以进入葫芦[6]的空腔。
已知
下列关于葫芦[6]脲的说法正确的是( )
A.属于高分子化合物
B.能与4molNaOH发生水解反应
C.由乙二醛和尿素两种有机物合成
D.4-甲基苯甲醛可进入葫芦[6]脲的空腔
8.是一种重要的无机化合物,能溶于水、稀硫酸,不溶于乙醇,受热易分解。利用“氧化法”制备的工艺流程如下:
“酸化反应”所得产物有、和KCl。
下列说法错误的是( )
A.“升温回流”的目的是使氯气逸出
B.“结晶过滤”所得滤液的主要成分是KCl
C.“系列操作”为蒸发结晶、过滤、乙醇洗涤
D.还可以通过电解KI溶液制备,电解前后溶液的pH不变
9.将(四氟硝酸锌)溶于[EMIM](1-乙基-3-甲基咪唑四氟硼酸盐)后形成的混合液,能替代锌离子电池中的常规水系电解液,避免水对锌的腐蚀。[EMIM]制备原理如下:
①
②
;;;
已知是类似于苯的芳香族化合物。下列说法错误的是( )
A.固态[EMIM]的为离子晶体,熔点低
B.分子中的C、N原子均在同一平面
C.为正四面体结构,四个B—F键键长相同
D.中存在大π键
10.水系锌离子电池(AZIBs)应用前景广阔。一种AZIBs电池示意图如下所示,钒基氧化物有利于Zn2+的扩散及嵌入/脱出,常被用做AZIBs正极材料,TMP(磷酸三甲酯)有良好的化学稳定性和宽的液态温度范围,适合做安全电解液。下列说法错误的是( )
A.在充放电过程中,锌箔侧发生与Zn的沉积或溶解
B.充电过程中,向侧移动
C.放电时正极电极反应可能为
D.TMP促进了水系锌离子电池宽温域范围内的应用
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.由实验操作和现象,可得出相应正确结论的是( )
选项 | 实验操作和现象 | 结论 |
A | 在火焰上灼烧搅拌过某无色溶液的玻璃棒,火焰出现黄色 | 溶液中含Na元素 |
B | 向某补铁口服液中滴加几滴酸性溶液,紫色褪去 | 该补铁口服液中有 |
C | 石蜡油加强热,将产生的气体通入的溶液,溶液变无色 | 气体中含有不饱和烃 |
D | 分别测浓度均为和溶液的pH,后者大于前者 |
12.炼油、石化等工业会产生含硫(价)废水。一种在碱性条件下处理含硫废水的反应过程如图,其中为催化剂,附着在催化剂载体聚苯胺的表面。下列说法错误的是( )
A.转化a中化合价发生变化的元素仅有S和O
B.转化c是该过程的第一步反应
C.一段时间后催化效率会下降,原因可能是生成的S覆盖在催化剂表面或进入催化剂空位处
D.该反应过程的总方程式为:
13.是一种白色晶体,易溶于水,常用于机械设备的磷化处理。以软锰矿(主要成分为,还含有少量的,FeO和)为原料制备的流程如下:
已知还原焙烧的主要反应为
25℃时相关物质的见下表(当溶液中某离子浓度时,可认为该离子沉淀完全)。
物质 | ||||
下列说法错误的是( )
A.“氧化”过程中所加试剂X为,也可以用代替
B.“调pH并过滤”中的pH理论最佳值为2.8
C.“沉锰”过程中,应将溶液逐量加入锰盐溶液中,如果颠倒试剂混合顺序可能会有生成
D.“反应”中主要发生
14.全钒液流电池储能容量大,使用寿命长,是电化学储能领域研究热点。一种简单钒液流电池工作原理如图,其电解液储存在储液罐中,使用时分别泵入正极室和负极室中,电池充放电总反应为。
下列说法错误的是( )
A.正极电解液和负极电解液所含离子对分别为和
B.充电时正极室的电极反应式为
C.将质子交换膜更换为硫酸根离子交换膜,电极反应式不变
D.当电路中通过n mol电子,两极室溶液质量差为2ng
15.硫酸工业中用NaOH溶液吸收尾气得到硫酸盐的过程如图。室温下,用溶液吸收(忽略溶液体积变化),所得溶液中含硫物种的浓度。室温下,,,。
下列说法正确的是( )
A.若“吸收”所得溶液中含硫物种的浓度,则溶液呈酸性
B.若“吸收”所得溶液,则溶液中
C.若“吸收”所得溶液,则“氧化”时主要反应的离子方程式为
D.将“氧化”所得溶液用溶液调节至,再与溶液等体积混合,最终溶液中
第II卷(非选择题 共60分)
三、非选择题:本题共5小题,共60分。
16.(12分)太阳能的开发利用在新能源研究中占据重要地位。
(1)我国科学家制备了一种太阳能电池,其结构示意图如下,其中是光电转换层,ITO玻璃为导电玻璃。
①基态的价电子排布式为______。
②C、N、O、F的第一电离能从大到小的顺序为______。
(2)钙钛矿材料是与钛酸钙()具备相同品体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式一般为,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA()、FA()、,等,其中MA中N原子的杂化轨道类型是______,1molFA中存在______个σ键(表示阿伏加德罗常数的值)。
(3)一种立方钙钛矿型晶体有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。
图a 图b
①图a晶胞中O的位置为______(填“体心”“顶点”“面心”“棱心”,下同);图b晶胞中O的位置为______。图a的晶胞参数为393.9pm,则O与O的最小核间距为______pm。
②晶胞经掺杂后能提高红外辐射效率。若图a晶胞的超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为______;掺杂Sr后O与O的最小核间距略有减小,其可能的原因是______。
17.(12分)磷酸亚铁锂电池是新能源汽车的动力电池之一。用含锂废渣(主要金属元素有Li、Ni、Ca,Mg)制得,纯化后用其制备电池的正极材料,工艺流程如下:
已知:①EDTA能与某些二价金属离子形成稳定的水溶性配合物。
②滤液1、滤液2中部分离子的浓度()见下表。
| ||||
滤液1 | 22.72 | 20.68 | 0.36 | 60.18 |
滤液2 | 21.94 | 0.08 |
③某些物质的溶解度(S)见下表。
T/℃ | 20 | 40 | 60 | 80 | 100 |
1.33 | 1.17 | 1.01 | 0.85 | 0.72 | |
34.7 | 33.6 | 32.7 | 31.7 | 30.9 |
回答下列问题:
(1)为加快“浸出”速率,本工艺中采取的措施有______。
(2)滤渣2的主要成分有______和(填化学式)。
(3)“沉锂”中,先加入EDTA,其作用是______;再加入饱和溶液,控制温度在95℃充分反应后,分离出粗的操作是______。
(4)生成纯的离子方程式为______。
(5)纯和足量碳、高温下反应,生成和一种可燃性气体,该反应的化学方程式为______。
18.(12分)是重要的化工原料,实验室利用红磷制取粗的装置如图,夹持装置略去,已知红磷与少量反应生成,与过量反应生成,遇水会强烈水解生成,遇会生成。、的熔沸点见下表。
物质 | 熔点/℃ | 沸点/℃ |
75.5 | ||
1.3 | 105.3 |
回答下列问题:
(1)A、C中所盛试剂为______,装置中a的作用是______。
(2)实验时,检查装置气密性后,先打开通入,再迅速加入红磷,通入的作用是______。
(3)装置B中的反应需要65~70℃,较适合的加热方式为______,装置E中盛有碱石灰,其作用为______。
(4)实验结束后,装置B中制得的粗产品中常混有、等。加入过量红磷加热可将转化为,通过______(填操作名称),即可得到较纯净的产品。
(5)纯度测定
步骤I:取ag上述所得产品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成250mL溶液;
步骤II:取25.00mL上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入mL溶液(过量),使完全转化为AgCl沉淀(可溶于稀硝酸);
步骤III:加入少硝基苯,振荡,使沉淀表面被有机物覆盖。以硫酸铁溶液为指示剂,用KSCN溶液滴定过量的溶液(难溶于水),达到滴定终点时,共用去mLKSCN溶液。
步骤I中发生反应的化学方程式为______,产品中的质量分数为______%,若测定过程中没有加入硝基苯,则所测的含量会______(填“偏大”“偏小”或“不变”)。
19.(12分)有机药物合成中常利用羰基-H活泼性构建碳骨架,M是一种药物中间体,其合成路线如下(部分反应条件已简化,忽略立体化学)。
已知:I.Et代表
II.
回答下列问题:
(1)A的化学名称是______;B的结构简式为______。
(2)由D生成E的第2步反应类型为______;M中含氧官能团的名称为______。
(3)写出由E生成F反应的化学方程式__________________。
(4)在B的同分异构体中,同时满足下列条件的总数为______种。
①能发生银镜反应;②分子中含有不对称碳原子。
(5)综合上述信息,写出由丙烯,、制备的合成路线(无机试剂任选)。
20.(12分)为减少含氮物质的排放对环境造成的污染,研究含氮物质的转化有重大意义。
(1)在进行低温下消除氯氧化物的机理研究时,某科研团队发现NO在转化过程中存在以下核心历程:
①
②
③
当温度为2.4K时,反应最终产物中,若使反应最终产物中,则温度应该______2.4K(填“高于”或“低于”)。
(2)为实现氮氢化物转化为氢气,我国科技人员计算了下列反应在一定温度范围内的压强平衡常数,并绘制和的线性关系如图所示()。
①
②
则反应的______(用、表示);由图可知该反应的______0(填“>”或“<”),写出推理过程______。
(3)原煤经热解、冷却得到的煤焦可用于NO的脱除。热解温度为500℃、900℃得到的煤焦分别用S-500、S-900表示,相关信息如下表。
煤焦 | 元素分析(%) | 比表面积() | |
C | H | ||
S-500 | 80.79 | 2.76 | 105.69 |
S-900 | 84.26 | 0.82 | 8.98 |
将NO浓度恒定的废气以固定流速通过如下反应器,不同温度下进行多组平行实验,测定相同时间内NO的出口浓度,可得NO的脱除率与温度的关系如下图所示[已知NO的脱除主要含吸附和化学还原()两个过程]。
①已知煤焦表面存在的官能团有利于NO的吸附,其数量与煤焦中氢碳质量比的值密切相关。由图可知,相同温度下,S-900对NO的脱除率比S-500的低,结合表格数据分析其原因可能是______、______。
②350℃后,随着温度升高,NO的脱除率增大的原因是______。
(4)电厂烟气中的氮氧化物进行脱硝处理时,通常采用以下反应原理:;。373℃下,在容积固定的密闭容器中通入1mol、1molNO和0.7mol,初始压强为,达到平衡后测得转化率为88%,体系中,此时容器中压强p=______(结果保留两位小数),NO转化率为______。
高三化学试题参考答案
2023.5
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.B 2.A 3.C 4.C 5.D 6.B 7.D 8.C 9.D 10.B
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.C 12.A 13.B 14.BD 15.BC
三、非选择题:本题共5小题,共60分。
16.(12分)
(1)①(1分) ②(1分)
(2)(1分) (1分)
(3)①棱心(1分) 面心(1分)(或278.5)(2分)
②(或)(2分) Sr原子半径小于La(2分)
17.(12分,每空2分)
(1)研磨、70℃
(2)、
(3)与、、形成稳定的水溶性配合物,防止其生成碳酸盐沉淀 趁热过滤
(4)
(5)
18.(12分)
(1)浓硫酸(1分) 使F与D压强相同,便于浓盐酸顺利滴出(1分)
(2)赶尽A、B装置中空气,防止被氧化(1分)
(3)水浴加热(1分)
吸收未反应的氯气,防止污染空气;防止空气中水蒸气进入,使发生水解(2分)
(4)蒸馏(1分)
(5)(2分) (2分) 偏小(1分)
19.(12分)
(1)3-戊酮(1分) (2分)
(2)取代反应(1分) 酰胺基(1分)
(3)(2分)
(4)9(2分)
(5)(3分)
20.(12分)
(1)低于(1分)
(2)(1分) <(1分)
T越大,的值越大,即越小,因此该反应为放热反应(2分)
(3)①热解温度高,煤焦H/C比值小,表面官能团少(1分)
S-900的比表面积小,吸附能力弱(1分)
②温度升高,反应速率增大(1分)
(4)1.08(2分) 72%(2分)
山东省滨州市2023届高三二模化学试题(含答案): 这是一份山东省滨州市2023届高三二模化学试题(含答案),共17页。试卷主要包含了单选题,多选题,结构与性质,工业流程题,实验题,有机推断题,原理综合题等内容,欢迎下载使用。
山东省滨州市2023届高三二模化学试题(含解析): 这是一份山东省滨州市2023届高三二模化学试题(含解析),共28页。试卷主要包含了单选题,多选题,结构与性质,工业流程题,实验题,有机推断题,原理综合题等内容,欢迎下载使用。
2023届山东省滨州市高三二模化学试题(Word版含答案): 这是一份2023届山东省滨州市高三二模化学试题(Word版含答案),共27页。试卷主要包含了考试结束,监考人员将答题卡收回,3°,77等内容,欢迎下载使用。












