山东省淄博市部分学校2023届高三下学期二模化学试题(含答案)
展开山东省淄博市部分学校2023届高三下学期二模化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学与生产、生活、科研密切相关。下列说法错误的是
A.食用油中添加叔丁基对苯二酚作抗氧化剂
B.谷物酿酒是利用淀粉水解产生乙醇的原理
C.“杯酚”分离是利用分子识别原理
D.将模具干燥后再注入铁水防止高温下铁与水反应
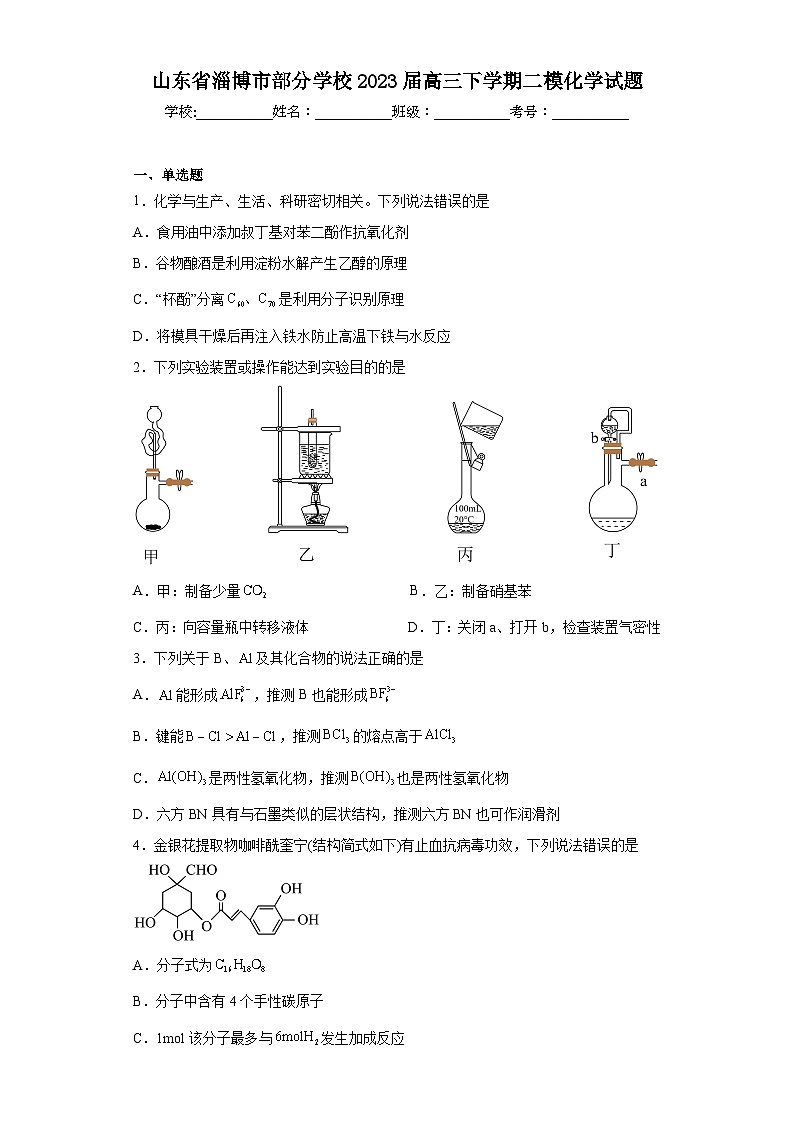
2.下列实验装置或操作能达到实验目的的是
A.甲:制备少量 B.乙:制备硝基苯
C.丙:向容量瓶中转移液体 D.丁:关闭a、打开b,检查装置气密性
3.下列关于B、及其化合物的说法正确的是
A.能形成,推测B也能形成
B.键能,推测的熔点高于
C.是两性氢氧化物,推测也是两性氢氧化物
D.六方BN具有与石墨类似的层状结构,推测六方BN也可作润滑剂
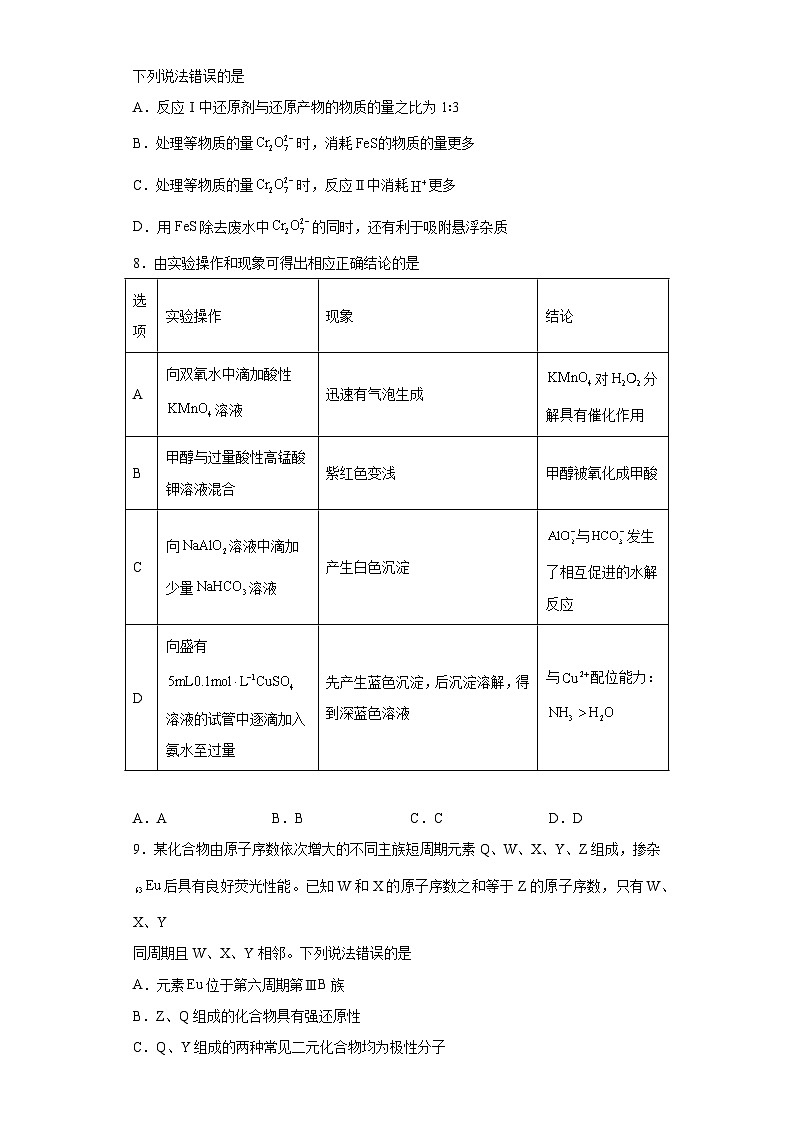
4.金银花提取物咖啡酰奎宁(结构简式如下)有止血抗病毒功效,下列说法错误的是
A.分子式为
B.分子中含有4个手性碳原子
C.1mol该分子最多与发生加成反应
D.其酸性水解产物羧酸分子中所有原子可能共平面
二、实验题
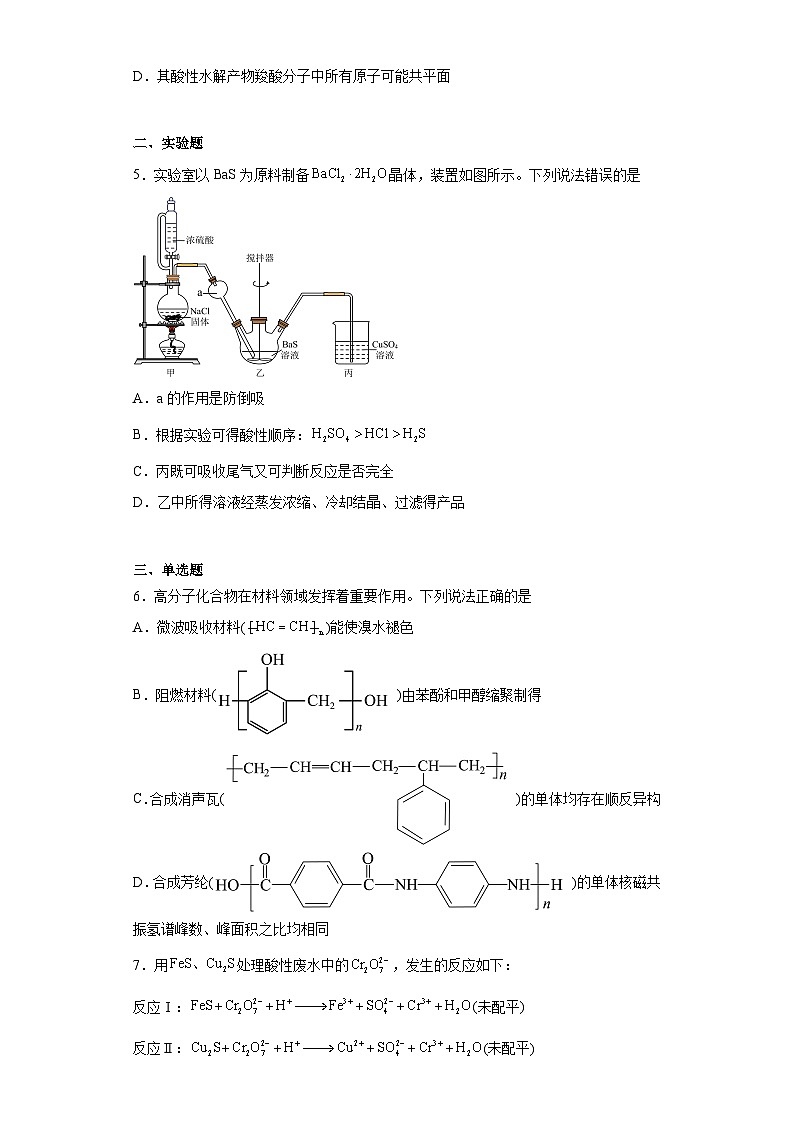
5.实验室以BaS为原料制备晶体,装置如图所示。下列说法错误的是
A.a的作用是防倒吸
B.根据实验可得酸性顺序:
C.丙既可吸收尾气又可判断反应是否完全
D.乙中所得溶液经蒸发浓缩、冷却结晶、过滤得产品
三、单选题
6.高分子化合物在材料领域发挥着重要作用。下列说法正确的是
A.微波吸收材料()能使溴水褪色
B.阻燃材料( )由苯酚和甲醇缩聚制得
C.合成消声瓦( )的单体均存在顺反异构
D.合成芳纶( )的单体核磁共振氢谱峰数、峰面积之比均相同
7.用处理酸性废水中的,发生的反应如下:
反应Ⅰ:(未配平)
反应Ⅱ:(未配平)
下列说法错误的是
A.反应Ⅰ中还原剂与还原产物的物质的量之比为1∶3
B.处理等物质的量时,消耗的物质的量更多
C.处理等物质的量时,反应Ⅱ中消耗更多
D.用FeS除去废水中的同时,还有利于吸附悬浮杂质
8.由实验操作和现象可得出相应正确结论的是
选项 | 实验操作 | 现象 | 结论 |
A | 向双氧水中滴加酸性溶液 | 迅速有气泡生成 | 对分解具有催化作用 |
B | 甲醇与过量酸性高锰酸钾溶液混合 | 紫红色变浅 | 甲醇被氧化成甲酸 |
C | 向溶液中滴加少量溶液 | 产生白色沉淀 | 与发生了相互促进的水解反应 |
D | 向盛有溶液的试管中逐滴加入氨水至过量 | 先产生蓝色沉淀,后沉淀溶解,得到深蓝色溶液 | 与配位能力: |
A.A B.B C.C D.D
9.某化合物由原子序数依次增大的不同主族短周期元素Q、W、X、Y、Z组成,掺杂后具有良好荧光性能。已知W和X的原子序数之和等于Z的原子序数,只有W、X、Y
同周期且W、X、Y相邻。下列说法错误的是
A.元素位于第六周期第ⅢB族
B.Z、Q组成的化合物具有强还原性
C.Q、Y组成的两种常见二元化合物均为极性分子
D.W、Q组成的化合物沸点均比Y、Q组成的化合物沸点低
10.微生物燃料电池碳氮联合去除的氮转化系统原理如图所示。下列说法错误的是
A.a极电势低于b极
B.离子交换膜是质子交换膜
C.a、b两极生成和的物质的量之比为5∶4
D.好氧微生物反应器中反应的离子方程式为
11.某温度下,在金表面发生反应:,其速率方程式为(k为速率常数)。反应过程中,与S(催化剂)及时间关系如图所示。已知(半衰期)为反应物消耗一半所用的时间,下列叙述错误的是
A.,Ⅰ条件下
B.其他条件相同,S(催化剂)越大,k越大
C.其他条件相同,增大,反应速率不变
D.该温度下,当S(催化剂),时,为
12.探究铜与硝酸反应的生成时的硝酸浓度。如图所示,先通一段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至,取,用的溶液滴定至终点时消耗(忽略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是
A.可用盛有溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成时的硝酸浓度不大于
C.若不通,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉的干扰)进行求算,所得实验结果偏低
四、多选题
13.用精炼铜漂浮阳极泥(主要成分为,含有少量)制备的工艺流程如下:
已知:①“转化”分两步进行,其第一步转化为。
②常温下,,。
下列说法错误的是
A.“滤渣1”的主要成分是,含砷废水主要成分是
B.“水解”分离和的原理是的水解高于水解的
C.“转化”的总反应方程式为
D.当恰好完全转化成时,溶液,此时溶液
五、单选题
14.甲苯与在无水存在下发生反应,其反应机理及部分能量示意图如下。下列说法错误的是
A.是该反应的催化剂
B.步骤Ⅱ是该反应的决定步骤
C.(l)+ (l)→(l)+HCl(g) ΔH=(b-a)kJ/mol
D.虚线L可表示与的反应中能量的变化
15.是一元弱酸,难溶盐的悬浊液中,不发生水解。实验发现,时,、的关系如图所示:
下列说法错误的是
A.表示的关系 B.
C. D.
六、结构与性质
16.磷、钠、铁等元素形成的化合物在生产、科研中应用广泛。回答下列问题:
(1)基态原子未成对电子数与基态P相同,且与同周期的元素有___________种;第三周期主族元素部分电离能如图所示,其中a、b和c分别代表___________(填标号)。
A.a为、b为、c为 B.a为、b为、c为
C.a为、b为、c为 D.a为、b为、c为
(2)锂离子电池正极材料,结构中八面体与四面体共用氧原子形成稳定的三维通道,有利于快速传输。与结构相似,但不能用作钠离子电池正极材料,从原子结构角度分析可能的原因是___________。
(3)能在有机溶剂中发生电离,生成空间结构相同的阴、阳离子,阳离子的化学式为___________,阴离子中心原子的杂化方式为___________。
(4)常温下黏度很大,温度升高,黏度降低,原因是___________。
(5)在超高压下,金属钠和氮可形成化合物。该化合物中,按简单立方排布,形成立方体空隙(部分结构如图所示),和交替填充在立方体的中心。晶体中配位的原子数为___________:晶胞中间距为,该晶体的密度为___________;若将取在晶胞顶点,在晶胞中的分数坐标为(0,0,)、(,0,0)、___________和___________。
七、工业流程题
17.回收稀土元素对促进稀土资源循环利用有十分重要的意义。利用钕铁硼合金废料制备和的工艺流程如下:
已知:①钕能与盐酸发生反应,硼不与盐酸反应;钕离子可与生成可溶性配合物。
②25℃,相关物质的见下表
物质 | ||||
回答下列问题:
(1)探究不同条件下,“酸浸”操作中钕、铁元素的浸出率,如下表所示。
序号 | 温度(℃) | 盐酸(mol/L) | 酒石酸浓度(g/L) | 的浸出率(%) | Nd的浸出率(%) |
Ⅰ | 40 | 4 | 0 | 69.15 | 87.22 |
Ⅱ | 50 | 4 | 0 | 65.35 | 83.45 |
Ⅲ | 40 | 6 | 0 | 74.64 | 91.05 |
Ⅳ | 40 | 6 | 50 | 71.54 | 93.62 |
①酒石酸的作用是___________。
②温度升高钕浸出率降低,可能原因是___________。
(2)“沉钕”过程中,草酸用量对钕回收的影响如图所示,当草酸实际用量与理论计算量比值n大于1.5时,沉钕率和沉淀纯度均下降,其原因是___________;“沉钕”后的滤液可导入___________操作再利用(填操作单元的名称);“沉钕”后的晶体在空气中充分煅烧的化学方程式为___________。
(3)“净化”时需先加入的试剂为___________(填化学式),再用氨水调溶液的pH,则pH的理论最小值为___________(当溶液中某离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全):“碳化“过程的离子方程式为___________。
(4)利用膜电解技术(装置如图所示),以溶液为原料制备,电解时通过膜的离子主要为___________。
八、实验题
18.三苯甲醇 []是一种重要的有机合成中间体,制备流程如下:
已知:Ⅰ.(R-表示烃基)能与水、二氧化碳、氧气、卤代烃、酮反应。如: RMgBr+R′Br→R-R′+MgBr2
Ⅱ.
Ⅲ.几种物质的物理性质如下表:(*表示溴苯与水形成的共沸物沸点)
物质 | 熔点(℃) | 沸点(℃) | 溶解性 |
三苯甲醇 | 164.2 | 380 | 不溶于水,易溶于乙醇 |
乙醚 | -116.3 | 34.6 | 微溶于水 |
溴苯 | -30.7 | 156.2(92.8*) | 不溶于水,易溶于乙醚 |
实验装置如下(加热及夹持装置略)。
回答下列问题:
(1)装置A中的试剂为___________。
(2)制备时,乙醚除作溶剂外,另一个作用是___________;若溴苯-乙醚混合液滴加过快,生成的主要副产物为___________(写结构简式)。
(3)用饱和溶液代替水与中间产物反应,能避免产生难溶的,加入饱和溶液反应的离子方程式为___________。
(4)水蒸气蒸馏过程中若出现堵塞,长导管中液面上升,应进行的操作是___________。
(5)当___________(填实验现象)时,表明水蒸气蒸馏完成;装置B中的物质经___________(填操作名称)分离出产品,再向产品中加入___________进行重结晶进一步提纯(填标号)。
A.溶液 B.水 C.稀盐酸 D.乙醇
(6)计算产率:反应中投加0.10mol溴苯、0.08mol二苯酮,经纯化、干燥后得13.0g产品[M(三苯甲醇)],则三苯甲醇的产率为___________。
九、有机推断题
19.平喘药富马酸福莫特罗中间体K的合成路线如下:
已知:
Ⅰ.
Ⅱ.
Ⅲ. (R=烃基)
回答下列问题:
(1)A的结构简式为___________;符合下列条件的A的同分异构体有___________种。
①有 ②能与按物质的量之比1∶4发生反应
(2)写出反应②的化学方程式___________。
(3)反应④的目的是___________,反应⑥的反应类型为___________。
(4)H中含氧官能团有___________种,Ⅰ的结构简式为___________。
(5)综合上述信息,写出由间硝基苯乙烯和制备的合成路线。___________
十、原理综合题
20.氢能将在实现“双碳”目标中起到重要作用,乙醇与水催化重整制氢发生以下反应。
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
回答下列问题:
(1)___________
(2)压强为,的平衡产率与温度、起始时的关系如图甲所示,每条曲线表示相同的平衡产率。
①产率:B点___________C点(填>、=或<)
②A、B两点产率相等的原因是___________
(3)压强为下,和投料比1∶3发生上述反应,平衡时和的选择性、乙醇的转化率随温度的变化曲线如图乙所示[已知:的选择性]
①表示选择性的曲线是___________(填标号);
②时,生成氢气的体积分数为___________(保留2位有效数字,下同);
③时,反应Ⅱ的标准平衡常数,其中为标准压强,、、和为各组分的平衡分压,则___________。(已知:分压=总压×该组分物质的量分数)
(4)已知,向重整体系中加入适量多孔,该做法的优点是___________。
参考答案:
1.B
2.A
3.D
4.C
5.B
6.A
7.B
8.D
9.D
10.C
11.A
12.D
13.BD
14.D
15.B
16.(1) 3 D
(2)Na+的半径大于Li+,在三维通道中传输困难
(3) PCl sp3
(4)H3PO4分子间存在较强的分子间氢键使溶液粘度很大,升高温度,一部分分子间氢键被破坏,粘度减小
(5) 4 (0, ,0) (, ,)
17.(1) 抑制Fe元素的浸出,提高Nd元素的浸出率 盐酸易挥发,温度升高,溶质挥发,导致盐酸溶液浓度下降,导致铁、钕浸出率降低
(2) 钕离子可与生成可溶性配合物 酸浸
(3) H2O2 2.8
(4)Nd3+
18.(1)碱石灰
(2) 挥发生成的乙醚蒸气,可以排除装置内的空气,防止与水、二氧化碳、氧气反应
(3)
(4)打开活塞K,撤去热源
(5) 无油状液体蒸出时 过滤(或抽滤) D
(6)
19.(1) 6
(2)+Br2+HBr
(3) 保护氨基 还原反应
(4) 2 HCOOH
(5)
20.(1)+173.3kJ/mol
(2) > B点温度高于A点,升高温度,反应Ⅱ逆向移动消耗氢气的量与反应Ⅰ、Ⅲ正向移动产生H2的量相等
(3) a 53% 14
(4)多孔CaO与CO2接触面积大,吸收CO2速率快,使得反应Ⅱ和Ⅲ正向进行,提高氢气的产率同时为反应提供热能
山东省淄博市部分学校2023届高三下学期二模化学试题: 这是一份山东省淄博市部分学校2023届高三下学期二模化学试题,共24页。试卷主要包含了单选题,不定项选择题,非选择题等内容,欢迎下载使用。
2023届山东省淄博市部分学校高考二模化学试题(含答案): 这是一份2023届山东省淄博市部分学校高考二模化学试题(含答案),文件包含2023届山东省淄博市部分学校高三下学期二模化学试题pdf、2023淄博二模化学试题及参考答案_auto_PMjlvn6g_试卷pdf等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
2023辽宁省部分学校高三下学期二模化学试题含答案: 这是一份2023辽宁省部分学校高三下学期二模化学试题含答案,文件包含辽宁省部分学校2023届高三下学期二模化学试卷无答案docx、二模答案定稿pdf等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。












