
2022-2023年江苏省南京市中考化学模拟试题汇编-实验题
展开
这是一份2022-2023年江苏省南京市中考化学模拟试题汇编-实验题,共16页。试卷主要包含了实验题等内容,欢迎下载使用。
(2022-2023年)南京市中考化学模拟试题汇编
实验题
一、实验题
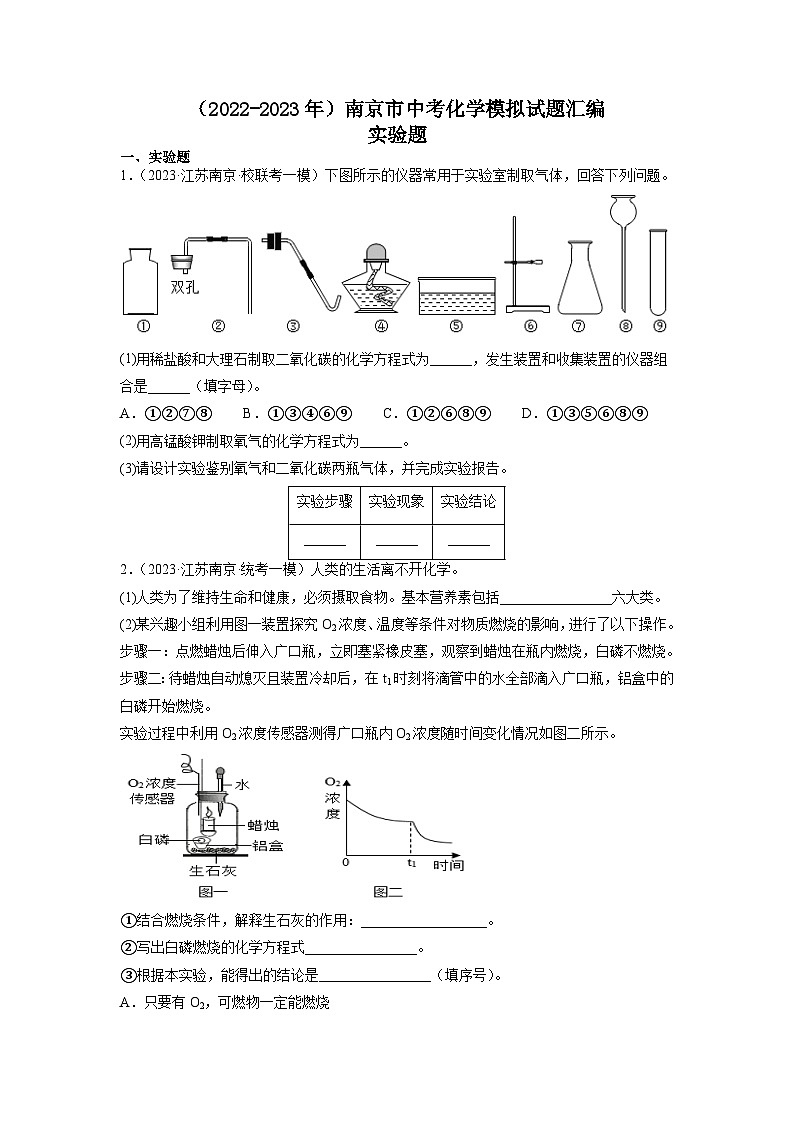
1.(2023·江苏南京·校联考一模)下图所示的仪器常用于实验室制取气体,回答下列问题。
(1)用稀盐酸和大理石制取二氧化碳的化学方程式为______,发生装置和收集装置的仪器组合是______(填字母)。
A.①②⑦⑧ B.①③④⑥⑨ C.①②⑥⑧⑨ D.①③⑤⑥⑧⑨
(2)用高锰酸钾制取氧气的化学方程式为______。
(3)请设计实验鉴别氧气和二氧化碳两瓶气体,并完成实验报告。
实验步骤
实验现象
实验结论
______
______
______
2.(2023·江苏南京·统考一模)人类的生活离不开化学。
(1)人类为了维持生命和健康,必须摄取食物。基本营养素包括________________六大类。
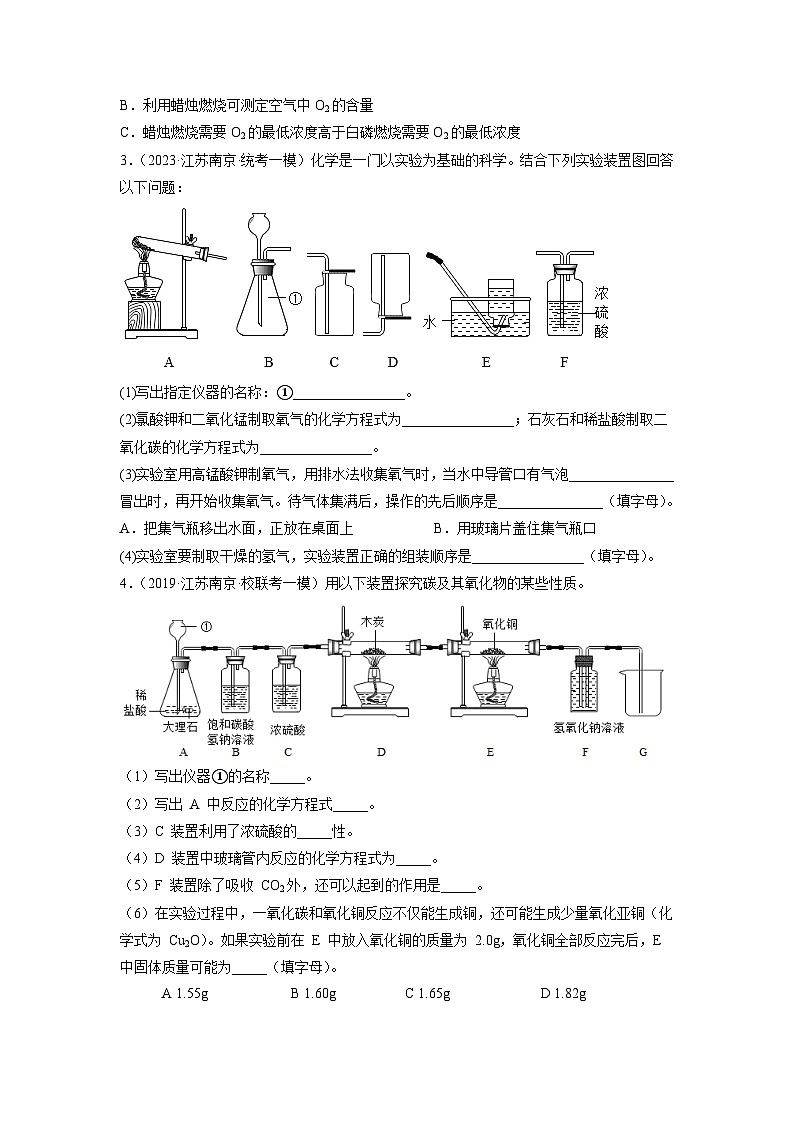
(2)某兴趣小组利用图一装置探究O2浓度、温度等条件对物质燃烧的影响,进行了以下操作。
步骤一:点燃蜡烛后伸入广口瓶,立即塞紧橡皮塞,观察到蜡烛在瓶内燃烧,白磷不燃烧。
步骤二:待蜡烛自动熄灭且装置冷却后,在t1时刻将滴管中的水全部滴入广口瓶,铝盒中的白磷开始燃烧。
实验过程中利用O2浓度传感器测得广口瓶内O2浓度随时间变化情况如图二所示。
①结合燃烧条件,解释生石灰的作用:__________________。
②写出白磷燃烧的化学方程式________________。
③根据本实验,能得出的结论是________________(填序号)。
A.只要有O2,可燃物一定能燃烧
B.利用蜡烛燃烧可测定空气中O2的含量
C.蜡烛燃烧需要O2的最低浓度高于白磷燃烧需要O2的最低浓度
3.(2023·江苏南京·统考一模)化学是一门以实验为基础的科学。结合下列实验装置图回答以下问题:
(1)写出指定仪器的名称:①________________。
(2)氯酸钾和二氧化锰制取氧气的化学方程式为________________;石灰石和稀盐酸制取二氧化碳的化学方程式为________________。
(3)实验室用高锰酸钾制氧气,用排水法收集氧气时,当水中导管口有气泡_______________冒出时,再开始收集氧气。待气体集满后,操作的先后顺序是_______________(填字母)。
A.把集气瓶移出水面,正放在桌面上 B.用玻璃片盖住集气瓶口
(4)实验室要制取干燥的氢气,实验装置正确的组装顺序是________________(填字母)。
4.(2019·江苏南京·校联考一模)用以下装置探究碳及其氧化物的某些性质。
(1)写出仪器①的名称_____。
(2)写出 A 中反应的化学方程式_____。
(3)C 装置利用了浓硫酸的_____性。
(4)D 装置中玻璃管内反应的化学方程式为_____。
(5)F 装置除了吸收 CO2外,还可以起到的作用是_____。
(6)在实验过程中,一氧化碳和氧化铜反应不仅能生成铜,还可能生成少量氧化亚铜(化 学式为 Cu2O)。如果实验前在 E 中放入氧化铜的质量为 2.0g,氧化铜全部反应完后,E 中固体质量可能为_____(填字母)。
A 1.55g B 1.60g C 1.65g D 1.82g
5.(2022·江苏南京·统考二模)化学是一门以实验为基础的科学。
(1)写出实验室用高锰酸钾制取氧气的化学方程式______,可选用的发生装置是______(填字母);氧气可用排水法收集的原因是______。
(2)实验室可用A、D装置来制取二氧化碳并进行“喷泉”实验。将A装置的导管和D装置的导管a连接,打开导管a、c上的活塞,关闭导管b上的弹簧夹,可收集CO2,检验集气瓶中已收集满CO2气体的方法是______;收集满CO2后,关闭导管a、c上的活塞,打开导管b上的弹簧夹,用热毛巾捂住集气瓶,一段时间后观察到氢氧化钠溶液进入集气瓶内,形成了“喷泉”,请写出集气瓶中发生反应的化学方程式______。
(3)实验室常用C装置制备气体,C装置与A装置相比具有的优点是______。
6.(2022·江苏·统考二模)硫酸铜是一种重要物质。
(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。
①写出生石灰与水生成熟石灰后,再与硫酸铜反应的两个化学方程式:______、______。
②果蔬表面残留的波尔多液不易用水洗去,浸泡时可在水中加点______(填字母)浸泡除去。
A、食醋 B、食盐 C、纯碱 D、植物油
(2)兴趣小组同学在做硫酸铜和氢氧化钠反应的实验时,发现滴加试剂的顺序不同会产生不同的现象。
【查阅资料】Ⅰ、NaOH和CuSO4溶液混合可生成Cu(OH)2、Cux(OH)y(SO4)z等多种产物。
Ⅱ、68℃时,Cu(OH)2发生分解;300℃左右Cux(OH)y(SO4)z发生分解。
【思考交流】实验一中加热时发生反应的化学方程式为______。
【实验探究】将实验二反应后的物质过滤、洗涤、低温干燥得浅蓝绿色固体样品。小组同学称取27.6g样品,在老师的指导下进行实验。
①装配好装置后,装药品前要进行的操作是______。
②控制温度为68℃,对样品进行热分解,至固体质量不再减少,再通一段时间N2。冷却后测得装置B增重1.8g。
A、再通一段时间N2的目的是______。
B、样品中Cu(OH)2的质量为______。
③取出装置A中加热后的剩余固体,溶于适量稀盐酸完全溶解后,再向溶液中加入过量BaCl2溶液,得11.65g沉淀;继续加入过量NaOH溶液,沉淀质量增加了24.5g。则Cux(OH)y(SO4)z中x:y:z=______。
【拓展延伸】在烧杯中放入20mL某硫酸铜溶液,逐滴加入某浓度的氢氧化钡溶液,测定混合液pH随滴入Ba(OH)2溶液体积的变化,结果如图。下列说法正确的是______(填字母)。
A、硫酸铜溶液呈酸性 B、a点烧杯内溶液中溶质是硫酸铜
C、b点烧杯内物质几乎不导电 D、bc段烧杯内沉淀质量不断增加
7.(2022·江苏南京·统考二模)某校同学就九年级化学课本上的相关实验开展研究性学习。
I.实验活动:溶液酸碱性的检验。
(1)同学们在校园里取少量土壤样品,将土壤样品与蒸馏水按1:5的质量比在烧杯中混合,充分搅拌后静置,用pH试纸测澄清液体的酸碱度。具体操作是________,由此得出,该土样pH>7,呈______(填“酸性”或“碱性”)。
(2)同学们经查阅资料获知:校园内土壤的酸碱度可能受城市建筑石灰性充填物的影响。据《本草图经》中记载:“石灰,今所在近山处皆有之,①此烧青石为灰也。…②以水沃之,则热蒸而解,力差劣。”文中的“青石”又名石灰石。请分别写出文中所述转化①和转化②的化学方程式:①_______②________。
II.课外实验:自制汽水。
下图是家庭自制汽水的操作,请回答下列问题:
(3)从气体溶解度的角度解释:步骤②中使用凉开水制汽水的原因:_________。步骤③中瓶盖旋紧后,为什么汽水中的气泡会由多变少直至不再冒出:_______。
(4)为证明柠檬酸溶液中有H+,可选用下列物质中的_______(填字母)进行验证。
A.酚酞溶液 B.镁条 C.铜片 D.鸡蛋壳 E.二氧化碳 F.食盐
(5)请设计实验证明上述自制汽水中含有二氧化碳,并完成实验报告。
实验操作
实验现象
实验结论
_________
________
该自制汽水中含有二氧化碳
8.(2022·江苏南京·统考二模)化学是一门以实验为基础的学科。
(1)请根据下列装置图,回答有关问题。
①实验室用高锰酸钾制取氧气的化学方程式为___________;可选用的发生装置是___________(填字母)。
②图中某装置既可用于收集氧气,又可用于收集氢气,组成该装置的仪器包括玻璃导管、___________。
(2)已知:白磷的着火点为40°C,红磷的着火点为240°C.甲、乙两位同学分别利用如图装置验证可燃物的燃烧条件。
甲同学:挤压滴管1,一段时间后,加热燃烧管至260°C,观察现象。
乙同学:挤压滴管2,一段时间后,加热燃烧管至某温度T,观察现象。
①挤压滴管1,稀盐酸与石灰石接触后发生反应的化学方程式为___________。
②挤压滴管2,过氧化氢溶液与二氧化锰接触后发生反应的化学方程式为___________。
③甲同学观察到红磷、白磷均未燃烧,请从燃烧条件的角度回答红磷、白磷的未燃烧的原因:___________。
④乙同学观察到红磷未燃烧,白磷迅速燃烧,T可能是___________(填字母)。
A.25°C B.80°C C.260°C
9.(2022·江苏南京·统考一模)通过海水晒盐可得到粗盐。下图是化学兴趣小组为了除去粗盐中难溶性杂质,进行的三步操作:
(1)三步操作的正确顺序是_________(填字母)。
(2)上述A、B操作中均使用了玻璃棒进行搅拌,其目的分别是:A:_________。B:_________。
(3)经过C操作后,发现滤液仍浑浊,可能的原因是_________(只写一条)。
(4)现有一瓶蒸馏水和一瓶稀氯化钠溶液,请用适当的化学方法把它们鉴别开,并完成实验报告。
实验步骤
实验现象
实验结论
_________。
_________。
_________。
10.(2022·江苏南京·统考一模)实验室常用溶质质量分数为6%的H2O2溶液(MnO2作催化剂)制取氧气。
(1)配制质量分数为6%的H2O2溶液。
①计算:配制150g质量分数为6%的H2O2溶液,需要质量分数为30%(密度为1.1g/cm3)的H2O2溶液体积为______mL(计算结果保留一位小数),水为______g。
②量取:用量筒量取所需H2O2溶液和水,倒入烧杯中。用量筒量取液体时,视线应与______。
③混匀:…。
(2)制取氧气(可能用到的部分装置如图)。
①实验室用氯酸钾(MnO2作催化剂)制取干燥的氧气,选择的发生装置和收集装置为______(填字母),反应的化学方程式为______。
②实验室用发生装置B制取氧气的化学方程式为______。
(3)实验反思。
①若其他操作正确,量取水时俯视读数,则配制的H2O2溶液溶质质量分数______6%(填“>”、“7,显碱性;
(2)
转化①为碳酸钙高温煅烧生成氧化钙和二氧化碳,该反应的化学方程式为:;
转化②为氧化钙和水反应生成氢氧化钙,该反应的化学方程式为:;
(3)
气体的溶解度随温度的升高而减小,使用凉开水,温度低,气体的溶解度较大,故步骤②中使用凉开水制汽水;
步骤③中瓶盖旋紧后,小苏打和柠檬酸反应生成二氧化碳,气体增多,压强增大,气体的溶解度增大;
(4)
A、无色酚酞试液在中性和酸性溶液中不变色,无法验证是否含氢离子,不符合题意;
B、镁能与氢离子反应生成氢气,产生气泡,可以验证,符合题意;
C、铜与氢离子不反应,无明显现象,无法验证,不符合题意;
D、鸡蛋壳中含碳酸钙,碳酸钙能与氢离子反应生成二氧化碳,产生气泡,可以验证,符合题意;
E、二氧化碳和氢离子不反应,无明显现象,无法验证,不符合题意;
F、食盐和氢离子不反应,无明显现象,无法验证,不符合题意。
故选BD;
(5)
通常用澄清石灰水检验二氧化碳,故振荡汽水瓶,将产生的气体通入澄清石灰水中,澄清石灰水变浑浊,说明该自制汽水中含有二氧化碳。
8.(1)
A 水槽、集气瓶
(2)
没有与氧气接触 B
【详解】(1)①实验室用高锰酸钾制取氧气,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气,反应条件是加热,所以反应的化学方程式为:;反应物为固体,反应条件是加热,所以应选用的发生装置是固固加热型为A;
②收集氧气可用排水法和向上排空气法,收集氢气可用排水法和向下排空气法,E装置既可用于收集氧气,又可用于收集氢气,组成该装置的仪器包括玻璃导管、水槽、集气瓶。
(2)①石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:;
②过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:;
③二氧化碳不燃烧、也不支持燃烧,所以甲同学实验中白磷和红磷均不燃烧,因为缺少氧气;
④乙同学实验证明可燃物燃烧需要温度达到着火点时,需要白磷燃烧而红磷不燃烧,所以温度应低于红磷的着火点,高于白磷的着火点,所以T应为80℃,故为B。
9.(1)ACB
(2) 搅拌,加快溶解速率 搅拌,防止局部温度过高,造成液滴飞溅
(3)滤纸破损(或接滤液的烧杯不干净等)
(4) 各取两种溶液少许进行蒸干 一种有少量白色残留固体,另一种无残留固体 有固体残留的是氯化钠,无固体残留的是蒸馏水
【分析】根据粗盐中难溶性杂质的步骤及注意事项进行分析。
【详解】(1)粗盐中难溶性杂质的操作步骤:取一定量的粗盐进行称量、溶解、过滤、蒸发及计算产率,故图示操作的正确顺序是ACB;
(2)A操作是溶解,玻璃棒的作用是搅拌,加快溶解速率;B操作是蒸发,玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅;
(3)过滤后,滤液仍浑浊的原因可能是滤纸破损(或接滤液的烧杯不干净等)
(4)蒸馏水是纯净物,稀氯化钠溶液是混合物,故鉴别蒸馏水和稀氯化钠溶液可以采取蒸发的方法进行鉴别,实验步骤:各取两种溶液少许进行蒸干,实验现象:一种有少量白色残留固体,另一种无残留固体,实验结论:有固体残留的是氯化钠,无固体残留的是蒸馏水。
【点睛】本题考查粗盐中难溶性杂质的步骤、注意事项及物质的鉴别,要熟练掌握粗盐中难溶性杂质的步骤,在鉴别物质时,要分析物质的性质,然后选择合适的试剂,出现不同的现象即可鉴别。
10.(1) 27.3 120 液体凹液面的最低处保持水平
(2) AD/DA
(3) > 150
【详解】(1)①加水稀释前后,溶液中的溶质质量不变,由于溶质质量=溶液质量×溶质质量分数,设需要质量分数为30%的H2O2溶液的质量为x,则: ,x=30g,体积为,即所需要质量分数为30%的H2O2溶液的体积为27.3mL,水为150g-30g=120g;
②用量筒量取液体时,视线应与液体凹液面的最低处保持水平。
(2)①用氯酸钾制取氧气时,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,反应物是固体,反应条件是加热,故发生装置为A,若想收集较干燥的氧气,应选用排空气法,又由于氧气的密度比空气大,则收集装置为D;反应的化学方程式为;
②发生装置B为固液常温装置,实验室用发生装置B制取氧气时,选用的药品为过氧化氢和二氧化猛,原理为。
(3)①量取水时俯视读数,则量取的水的体积偏小,则配制的H2O2溶液溶质质量分数>6%;
②若用E装置收集一瓶(容积为200mL)体积分数为80%的氧气,设预先应用量筒量取水的体积为x,由于空气中氧气约占空气体积的五分之一,则,则x=150mL。
11.(1) 炭 腐蚀 糖类
(2) 100 混匀
如果将水注入浓硫酸,由于水的密度较小,水会浮在浓硫酸上面,溶解时放出的热能使水立刻沸腾,使硫酸液滴向四周飞溅 a 向废液中加入足量的锌粒 锌粒周围产生气泡后消失
【详解】(1)由于浓硫酸具有强烈的腐蚀性,它能夺取蔗糖里的水分,生成黑色的炭,所以将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀:然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体。
六大基本营养素包括蛋白质、糖类、油脂、维生素、无机盐、水等。蔗糖属于六大基本营养素中的糖类。
(2)设:体积比1:4的硫酸中98%的硫酸质量为x,加水的质量为y。
所以
所以,体积比1:4的硫酸溶液的溶质质量分数=
设:配制该稀硫酸584克需浓硫酸体积为v。
所以,584g×31%=v×1.84g/cm3×98%
v=100cm3=100mL
第三步的操作为混匀,要注意稀释浓硫酸时把量筒中的浓硫酸沿烧杯壁慢慢注入水里,并用玻璃棒不断搅拌。切不可将水注入浓硫酸。如果将水注入浓硫酸,由于水的密度较小,水会浮在浓硫酸上面,溶解时放出的热能使水立刻沸腾,使硫酸液滴向四周飞溅。
由于氢气密度比空气小,所以制取氢气。如用图2装置收集氢气时,发生装置应该与导管a相连接。
若要除去废液中残余的H2SO4:得到硫酸锌溶液,实验步骤是向废液中加入足量的锌粒,现象是锌粒周围产生气泡后消失。说明锌与稀硫酸反应生成硫酸锌和氢气,化学方程式。
相关试卷
这是一份2022-2023年江苏省南京市中考化学模拟试题汇编-推断题,共15页。试卷主要包含了推断题等内容,欢迎下载使用。
这是一份江苏省常州市三年(2020-2022)中考化学模拟题分题型分层汇编-44实验题(化学实验),共15页。试卷主要包含了实验题等内容,欢迎下载使用。
这是一份广西各地区2022年中考化学模拟试题汇编-实验题(提升题),共16页。试卷主要包含了实验题等内容,欢迎下载使用。










