
所属成套资源:北京市高考化学三年(2020-2022)模拟题分类汇编
北京市高考化学三年(2020-2022)模拟题分类汇编18氧化还原反应(6)
展开
这是一份北京市高考化学三年(2020-2022)模拟题分类汇编18氧化还原反应(6),共30页。试卷主要包含了单选题,多选题,工业流程题,实验题等内容,欢迎下载使用。
北京市高考化学三年(2020-2022)模拟题分类汇编18氧化还原反应(6)
一、单选题
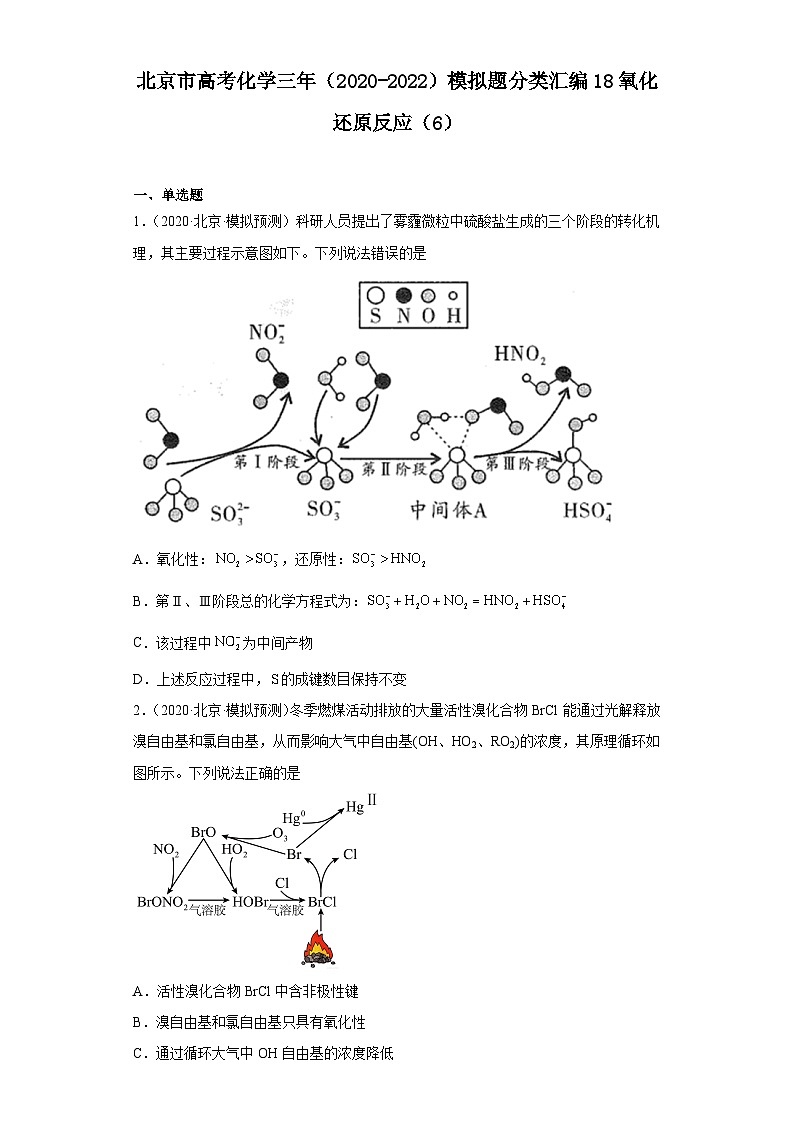
1.(2020·北京·模拟预测)科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如下。下列说法错误的是
A.氧化性:,还原性:
B.第Ⅱ、Ⅲ阶段总的化学方程式为:
C.该过程中为中间产物
D.上述反应过程中,的成键数目保持不变
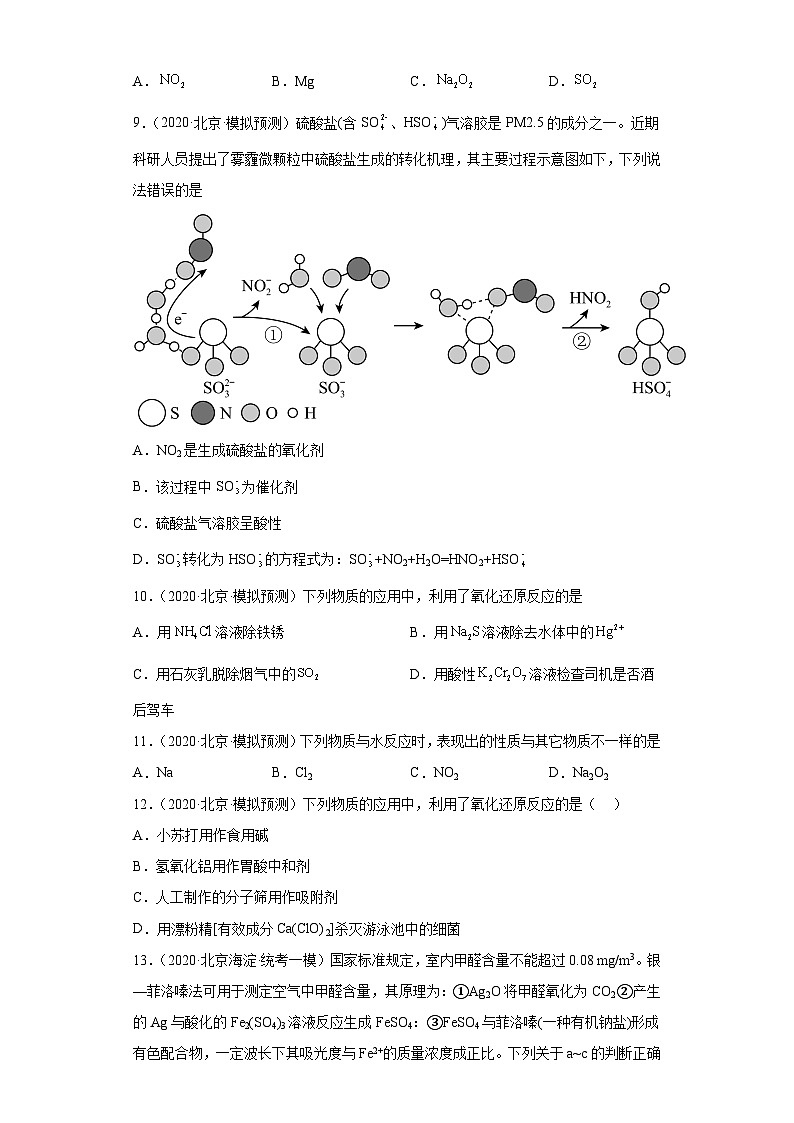
2.(2020·北京·模拟预测)冬季燃煤活动排放的大量活性溴化合物BrCl能通过光解释放溴自由基和氯自由基,从而影响大气中自由基(OH、HO2、RO2)的浓度,其原理循环如图所示。下列说法正确的是
A.活性溴化合物BrCl中含非极性键
B.溴自由基和氯自由基只具有氧化性
C.通过循环大气中OH自由基的浓度降低
D.BrCl的排放会造成臭氧含量减少、水中汞含量超标等
3.(2020·北京·模拟预测)下列物质的应用中,利用了氧化还原反应的是
A.双氧水作消毒剂 B.生石灰作干燥剂
C.碳酸氢钠作膨松剂 D.氧化铁作红色颜料
4.(2020·北京·模拟预测)下列方程式与所给事实不相符的是
A.向酸性溶液中滴加溶液,溶液褪色:
B.向沸水中滴加饱和溶液,胶体:
C.向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜:
D.用作潜水艇供氧剂:;
5.(2020·北京西城·统考二模)探究甲醛与新制Cu(OH)2的反应:①向6 mL 6mol/L NaOH溶液中滴加8滴2% CuSO4溶液,振荡,加入0.5 mL 15%甲醛溶液,混合均匀,水浴加热,迅速产生红色沉淀,产生无色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液与新制Cu(OH)2共热,未观察到明显现象;已知:,甲醛是具有强还原性的气体,下列说法正确的是
A.红色沉淀的主要成分不是Cu2O,可能是Cu
B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
C.从甲醛的结构推测,其氧化产物可能为碳酸()因此实验中得到的无色气体中大量含有CO2
D.含有-CHO的有机物都可以被新制Cu(OH)2氧化
6.(2020·北京·模拟预测)水与下列物质反应时,水表现出氧化性的是
A.Fe B. C. D.
7.(2020·北京·模拟预测)下列叙述不涉及氧化还原反应的是
A.根瘤菌固氮 B.84消毒液久置失效
C.用植物秸秆制造酒精 D.用石灰乳脱除烟气中的
8.(2020·北京·模拟预测)水与下列物质反应时,水表现出氧化性的是
A. B.Mg C. D.
9.(2020·北京·模拟预测)硫酸盐(含SO、HSO)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下,下列说法错误的是
A.NO2是生成硫酸盐的氧化剂
B.该过程中SO为催化剂
C.硫酸盐气溶胶呈酸性
D.SO转化为HSO的方程式为:SO+NO2+H2O=HNO2+HSO
10.(2020·北京·模拟预测)下列物质的应用中,利用了氧化还原反应的是
A.用溶液除铁锈 B.用溶液除去水体中的
C.用石灰乳脱除烟气中的 D.用酸性溶液检查司机是否酒后驾车
11.(2020·北京·模拟预测)下列物质与水反应时,表现出的性质与其它物质不一样的是
A.Na B.Cl2 C.NO2 D.Na2O2
12.(2020·北京·模拟预测)下列物质的应用中,利用了氧化还原反应的是( )
A.小苏打用作食用碱
B.氢氧化铝用作胃酸中和剂
C.人工制作的分子筛用作吸附剂
D.用漂粉精[有效成分Ca(ClO)2]杀灭游泳池中的细菌
13.(2020·北京海淀·统考一模)国家标准规定,室内甲醛含量不能超过0.08 mg/m3。银—菲洛嗪法可用于测定空气中甲醛含量,其原理为:①Ag2O将甲醛氧化为CO2②产生的Ag与酸化的Fe2(SO4)3溶液反应生成FeSO4:③FeSO4与菲洛嗪(一种有机钠盐)形成有色配合物,一定波长下其吸光度与Fe2+的质量浓度成正比。下列关于a~c的判断正确的是
a.反应①的化学方程式为HCHO+2Ag2O =CO2+ 4Ag↓+H2O
b.理论上吸收的HCHO与消耗的Fe3+的物质的量比为1:4
c. 取1m3空气,经上述实验后共得到Fe2+ 1.12mg,室内甲醛含量达标
A.全部正确 B.a、b正确,c错误
C.b、c正确,a错误 D.a正确,b、c错误
14.(2020·北京·模拟预测)水与下列物质反应时,水表现出还原性的是
A.Na B.F2 C.Na2O D.NO2
15.(2020·北京·模拟预测)硫酸盐(含、)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
下列说法不正确的是
A.①②过程中硫元素均被氧化 B.NO2是生成硫酸盐的催化剂
C.硫酸盐气溶胶呈酸性 D.该过程中有氧氢键断裂
16.(2020·北京西城·统考二模)已知由一种阳离子与两种酸根阴离子组成的盐称为混盐。向混盐CaOCl2中加入足量浓硫酸,发生反应:CaOCl2+H2SO4(浓)=CaSO4+Cl2↑+H2O。下列说法不正确的是
A.CaOCl2中的两种酸根阴离子分别为Cl-和ClO-
B.CaOCl2和Cl2中均含有非极性共价键
C.在上述反应中,浓硫酸不体现氧化性
D.每产生标准状况下2.24 L Cl2,转移电子的数目约为6.02×1022
17.(2020·北京·模拟预测)研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是
A.反应Ⅰ、反应Ⅱ均属于氧化还原反应 B.整个过程中O3作催化剂
C.光化学烟雾中含甲醛、乙醛等刺激性物质 D.反应Ⅲ的方程式为O2+ O = O3
18.(2020·北京西城·统考一模)海水提溴过程中发生反应:3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3,下列说法正确的是
A.标准状况下 2 mol H2O的体积约为 44.8 L
B.1L 0.1 mol·L− 1Na2CO3 溶液中 CO32−的物质的量为 0.1 mol
C.反应中消耗 3 mol Br2 转移的电子数约为 5×6.02×1023
D.反应中氧化产物和还原产物的物质的量之比为 5∶1
19.(2020·北京平谷·统考一模)利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的过程如图所示,H+、O2、等共存物会影响修复效果。下列说法错误的是( )
A.反应①②③④均为还原反应
B.1 mol 三氯乙烯完全脱Cl时,电子转移为3 mol
C.④的电极反应式为+10H++8e-=+3H2O
D.修复过程中可能产生Fe (OH)3
20.(2020·北京·模拟预测)水与下列物质反应时,水表现出氧化性的是
A.Na B.Cl2 C.NO2 D.Na2O
二、多选题
21.(2020·北京·模拟预测)高铁酸钾是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
下列叙述不正确的是( )
A.用作水处理剂时,既能杀菌消毒又能净化水
B.反应Ⅰ中尾气可用溶液吸收再利用
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为
D.该条件下,物质的溶解性:
22.(2020·北京大兴·统考一模)煤燃烧排放的烟气含有SO2和NOx,是大气的重要污染源之一。用Ca(ClO)2溶液对烟气[n(SO2)∶n(NO) =3∶2]同时脱硫脱硝(分别生成SO、NO),得到NO、SO2脱除率如图,下列说法错误的是
A.酸性环境下脱除NO的反应:2NO+3ClO-+H2O=2H++2NO+3Cl-
B.SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
C.依据图中信息,在80 min时,吸收液中n(NO)∶n(Cl-)=2∶3
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
三、工业流程题
23.(2020·北京·模拟预测)硝酸铁是一种工业和医药行业常用的原料,用作媒染剂、铜着色剂等。Fe(NO3)3∙9H2O是浅紫色晶体,易溶于水、乙醇和丙酮。
Ⅰ. 利用稀硝酸和铁屑制备硝酸铁。目前常见的生产流程如图所示。
(1)反应釜中原料是稀硝酸和细铁屑,反应的离子方程式是_______。硝酸需要过量,原因是_______。
(2)会污染空气,不能随意排放,浓缩池中也会产生,请用化学用语解释产生的原因_______。
(3)冷却结晶后的硝酸铁晶体,最适宜用下列哪种试剂进行洗涤_______。
A.水 B.四氯化碳 C.20%稀硝酸 D.乙醇
Ⅱ. 利用工业废水制备硝酸铁。不锈钢酸洗废液中含有大量、、等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
已知:①Cr(OH)3是两性氢氧化物。
②各金属离子沉淀的范围如下表所示:
开始沉淀
1.5
4.6
6.7
完全沉淀
3.2
6.9
9.5
(4)分离出适宜的范围是_______。
(5)请设计实验,继续从废液中分别分离出Cr元素和Ni元素_______。
24.(2020·北京·模拟预测)过氧化钙在水中能缓慢放出氧气,是一种用途广泛的供氧剂,可用于鱼塘养殖。
(1)中所含化学键的类型是___________、___________。
(2)与水反应的化学方程式是___________。
(3)由电石渣(主要成分为氢氧化钙)制备过氧化钙可实现工业废渣的资源化,其制备流程如下:
①滤液Y可循环使用,其主要溶质的质量与反应前的加入量几乎没有变化,该溶质是___________。解释其质量不变的原因:___________(用化学方程式表示)。
②Ⅰ和Ⅱ的反应装置均需置于冰水浴中,解释Ⅱ中冰水浴的作用:___________(答出一点即可)。
(4)样品纯度测定
ⅰ.按上图连接装置(夹持和加热装置均略去),从水准管口加入适量水,并检查气密性;
ⅱ.准确称量样品加入试管,并使其在试管底部均匀铺成薄层;
ⅲ.上下移动水准管,使水准管中液面与量气管中液面平齐;读取量气管中液面对应的刻度,记为;
ⅳ.加热发生反应:,充分反应至不再有气体产生,停止加热,___________;再次读取量气管中液面对应的刻度,记为;
Ⅴ.计算样品中的纯度。
①补全ⅳ中操作:___________。
②该实验条件下,气体摩尔体积为,样品中的纯度为___________(用质量分数表示)。
25.(2020·北京·模拟预测)镀镍废件是一种宝贵的可再生资源,可用于制备重要的化工原料NiSO4。将镀镍废件处理后得到废液(含大量的H+、SO、Ni2+以及少量的Zn2+、Cu2+、Fe2+、Fe3+等),采用如图工艺流程回收其中的镍制备NiSO4晶体。
资料:
P2O4为磷酸二异辛酯(可用HA表示),不溶于水,是一种弱酸性萃取剂。其酸根离子(A-)可与某些金属离子发生反应。
(1)写出H2O2的电子式________。
(2)加入H2O2溶液发生反应的离子方程式为______。
(3)加石灰乳的作用是________。
(4)在萃取过程中,若溶液酸度过高,会导致萃取效率变低,其原因是__。
(5)在结晶过程中,需要加浓硫酸调pH至2~4,再进行__,过滤出的固体洗涤、干燥,得NiSO4晶体。
NiSO4在不同温度下的溶解度
温度/℃
20
30
40
60
80
90
100
溶解度/g
44.4
46.6
49.2
55.6
64.5
70.1
76.7
(6)NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式__。
26.(2020·北京·模拟预测)重铬酸钾在工业中有广泛的应用,可用铬铁矿为原料制备。以铬铁矿(主要成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3、Fe2O3等杂质)制备重铬酸钾(K2Cr2O7)固体的工艺流程如下:
资料:① NaFeO2遇水强烈水解。
②。
(1)K2Cr2O7中Cr元素的化合价是______。
(2)步骤①发生多个反应,补全下列化学方程式___:
___FeO·Cr2O3 + ___Na2CO3 +___KClO3 =12Na2CrO4 +___Fe2O3 +___CO2 + _KCl
(3)熔块的主要成分为Na2CrO4、NaFeO2、Na2SiO3和NaAlO2等可溶性盐,滤渣1为红褐色固体,写出步骤②NaFeO2水解的离子方程式______。
(4)结合化学用语解释步骤④调pH的目的______。
(5)重铬酸钾纯度测定
称取重铬酸钾试样2.9400 g配成250 mL溶液,取出25.00 mL于锥形瓶中,加入10 mL 2 mol/L H2SO4和足量碘化钾(Cr2O的还原产物为Cr3+),放于暗处5 min,然后加入100 mL水和淀粉指示剂,用0.1200 mol/L Na2S2O3标准溶液滴定(I2 + 2S2O= 2I- + S4O)。
①滴定终点的颜色变化是______。
②若实验共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度是______(滴定过程中其它杂质不参与反应)。
27.(2020·北京·模拟预测)门捷列夫在研究周期表时预言了“类硅”元素锗和“类铝”元素镓等11种元素。锗及其化合物应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:
已知:ⅰ.GeO2与碱反应生成Na2GeO3.ⅱ.GeCl4极易水解,GeCl4沸点86.6℃。
ⅲ.As位于同主族P的下一周期,As2O3+2NaOH = 2NaAsO2+H2O。
(1)Ge位于同主族Si的下一周期,则Ge在周期表中的位置是_______。
(2)从原子结构角度解释Ge和Si金属性递变的原因_______。
(3)“氧化”过程是将NaAsO2氧化为Na3AsO4,其离子方程式为_______。
(4)加盐酸蒸馏生成GeCl4,反应的化学方程式为_______。
(5)高纯二氧化锗的含量采用碘酸钾滴定法进行测定。称取ag高纯二氧化锗样品,加入氢氧化钠在电炉溶解,用次亚磷酸钠还原为Ge2+,以淀粉为指示剂,用bmol/L的碘酸钾标准溶液滴定,消耗碘酸钾的体积为V mL。(20℃以下,次亚磷酸钠不会被碘酸钾和碘氧化)
资料:3Ge2++IO+6H+ = 3Ge4++I-+3H2O,IO+5I-+6H+ = 3I2+3H2O。
此样品中二氧化锗的质量分数是_______(用表达式表示)。
28.(2020·北京·模拟预测)用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
已知:①浓硝酸不能单独将Au溶解。②HAuCl4=H++AuCl
(1)酸溶后经____操作,将混合物分离。
(2)浓、稀HNO3均可作酸溶试剂。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:____。
(3)HNO3-NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3溶金原理相同。
①将溶金反应的化学方程式补充完整:
Au+____NaCl+____HNO3=HAuCl4+____+____+____NaNO3
②关于溶金的下列说法正确的是____。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1molHAuCl4完全还原,则参加反应的Zn的物质的量是____mol。
(5)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。
试剂1是____,物质2是____。
四、实验题
29.(2020·北京·模拟预测)某实验小组研究KI和酸性KMnO4溶液的反应。
实验序号
Ⅰ
Ⅱ
实验操作
实验现象
KMnO4溶液的紫色褪去,溶液变为棕黄色
KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀消失,溶液变为棕黄色
资料:i.MnO在酸性条件下最终被还原为Mn2+
ii.酸性条件下氧化性:KMnO4>KIO3>I2
(1)实验Ⅰ中溶液呈棕黄色,推测生成了___________;
(2)实验小组继续对实验Ⅱ反应中初始阶段的产物成分进行探究:
①经检验,实验Ⅱ初始阶段I-的氧化产物不是I2,则“实验现象a”为___________;
②黑色固体是___________;
③经检验,在“紫色清液”中存在,写出生成的离子方程式___________;下列实验方案中,可用于检验“紫色清液"中的是___________(填字母);
A.用洁净的玻璃棒蘸取“紫色清液”滴在淀粉一碘化钾试纸上,观察试纸是否变蓝色。
B.取少量“紫色清液”于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变蓝色。
C.取少量“紫色清液”于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
(3)探究实验Ⅱ中棕褐色沉淀消失的原因。
用离子方程式解释实验Ⅱ中棕褐色沉淀消失的原因:___________;
(4)实验后的反思:导致实验Ⅰ和实验Ⅱ中KI和酸性KMnO4溶液反应产物变化的因素是(写出两点):___________、___________。
30.(2020·北京·模拟预测)探究Na2SO3固体的热分解产物。
资料:①4Na2SO3Na2S+3Na2SO4②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。③BaS易溶于水。
隔绝空气条件下,加热无水Na2SO3固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到浊液,放置得无色溶液B。
(1)检验分解产物Na2S:取少量溶液B,向其中滴加CuSO4溶液,产生黑色沉淀,证实有S2-。反应的离子方程式是____。
(2)检验分解产物Na2SO4:取少量溶液B,滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(H2S),由于沉淀增多对检验造成干扰,另取少量溶液B,加入足量盐酸,离心沉降(固液分离)后,____(填操作和现象),可证实分解产物中含有SO。
(3)探究(2)中S的来源。
来源1:固体A中有未分解的Na2SO3,在酸性条件下与Na2S反应生成S。
来源2:溶液B中有Na2Sx,加酸反应生成S。
针对来源1进行如图实验:
①实验可证实来源1不成立。实验证据是____。
②不能用盐酸代替硫酸的原因是____。
③写出来源2产生S的反应的离子方程式:____。
(4)实验证明Na2SO3固体热分解有Na2S,Na2SO4和S产生。运用氧化还原反应规律分析产物中S产生的合理性:____。
参考答案:
1.D
【详解】A.根据方程式和可得氧化性:,还原性:,A正确;
B.根据图示可知:在第Ⅱ阶段,、在存在条件反应产生、。在第Ⅲ阶段,结合变为,结合变为,故第Ⅱ、Ⅲ阶段总的化学方程式为:,B正确;
C.根据图示的转化过程知该过程中→→,为中间产物,C正确;
D.由题图可知由,最终生成,的成健数目由3变为4,D错误。
故答案选D。
2.D
【详解】A.BrCl之间是不同原子形成的共价键,属于极性键,故A错误;
B.溴自由基和氯自由基处于低价,Br和O3反应生成BrO,具有还原性,故B错误;
C.BrO+HO2=HOBr+O2,Cl+HOBr=BrCl+OH,循环大气中OH自由基的浓度升高,故C错误;
D.BrCl的循环中自由基Br和臭氧结合生成BrO而造成臭氧含量减小,自由基Br结合Hg0生成HgII,造成水中汞含量超标,故D正确;
故选:D。
3.A
【详解】A.双氧水作消毒剂利用了过氧化氢的强氧化性使蛋白质变性,故A符合题意;
B.生石灰作干燥剂是利用了生石灰与水反应生成熟石灰,与氧化还原反应无关,故B不符合题意;
C.碳酸氢钠作膨松剂是利用碳酸氢钠和酸反应产生二氧化碳,使物质蓬松,与氧化还原反应无关,故C不符合题意;
D.氧化铁作红色颜料是利用氧化铁的颜色,与氧化还原反应无关,故D不符合题意;
故答案为:A
4.B
【详解】A. 酸性溶液与溶液反应生成二氧化碳、Mn2+和水,则离子方程式为:,A正确;
B. 向沸水中滴加饱和溶液得到胶体:则,B不正确;
C.银氨溶液与乙醛经水浴加热,得到乙酸铵、银、氨气和水:,C正确;
D. 能分别与水、二氧化碳反应生成氧气,可作供氧剂:;,D正确;
答案选B。
5.A
【解析】向6 mL 6 mol·L−1 NaOH溶液中滴加8滴2%CuSO4溶液,配制成新制的Cu(OH)2,加入0.5 mL15%甲醛溶液,混合均匀,水浴加热,甲醛具有强还原性,与新制的Cu(OH)2发生氧化还原反应,迅速产生红色沉淀,产生无色气体。将所得沉淀洗净后加入浓盐酸,不溶解,根据已知信息:Cu2O 浓盐酸[CuCl2]−,可知,红色沉淀不是Cu2O,可能是Cu。甲醛被氧化,根据甲醛中碳元素的化合价为+2价,可知氧化产物不可能为CO,可能是碳酸盐,由于水浴加热,甲醛具有挥发性,生成的无色气体中混有甲醛气体,据此分析解答。
【详解】A.根据已知信息,Cu2O [CuCl2]−,实验操作②中,红色沉淀洗净后加入浓盐酸,不溶解,则可以确定红色沉淀的主要成分不是Cu2O,可能是Cu,故A正确;
B.甲醛是具有强还原性的气体,甲醛具有挥发性,生成的无色气体中混有甲醛气体,可将灼热的CuO还原为铜单质,得到红色固体,所以不能证明气体中含有CO,故B错误;
C.配制新制氢氧化铜悬浊液时,NaOH是过量的,在碱性溶液中不可能产生二氧化碳,故C错误;
D.根据实验操作③,甲酸钠中也含有醛基,与新制的Cu(OH)2反应,未观察到明显现象,含有-CHO的甲酸钠没有被新制Cu(OH)2氧化,故D错误;
答案选A。
【点睛】2015年第6期77页《化学教学》上有一篇文章,通过探究了甲酸和新制氢氧化铜的反应,实验结论是适量甲醛和新制氢氧化铜反应生成的是Cu2O和甲酸钠,过量的甲醛和新制氢氧化铜反应生成的是铜和甲酸钠,副反应中有氢气生成。
6.A
【详解】A.Fe和水蒸气反应生成四氧化三铁和氢气,水中氢元素化合价降低,得到电子,被还原,水表现出氧化性,A符合;
B.和水反应生成盐酸和次氯酸,水中元素的化合价均不发生变化,水不是氧化剂也不是还原剂,B不符合;
C.和水反应生成氢氧化钠,不是氧化还原反应,C不符合;
D.和水反应生成硝酸和NO,水中元素的化合价均不发生变化,水不是氧化剂也不是还原剂,D不符合;
答案选A。
7.D
【详解】A.根瘤菌有固氮作用,能将空气中的N2转化为NH3,此过程涉及氧化还原反应,故A不符合题意;
B.84消毒液的主要成分是NaClO,它与空气中的二氧化碳和水反应能产生具有强氧化性的次氯酸,次氯酸不稳定易分解成HCl和O2,此过程涉及到氧化还原反应,故B不符合题意;
C.用植物秸秆制造酒精涉及到反应:(C6H10O5)n+nH2O→nC6H12O6,C6H12O6→2C2H5OH+2CO2↑,此过程涉及到氧化还原反应,故B不符合题意;
D.是酸性氧化物,可与碱反应,用石灰乳脱除烟气中的时,与氢氧化钙反应生成亚硫酸钙或者亚硫酸氢钙,反应过程中无元素化合价改变,不涉及氧化还原反应,故D符合题意;
故答案为D。
8.B
【详解】A.3NO2+H2O=2HNO3+NO,H2O中的元素没有发生化合价的变化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故A错误;
B.2Mg+2H2O=Mg(OH)2+H2↑,H2O中H元素化合价由+1降为0价,得电子被还原,作氧化剂,在反应中表现出氧化性,故B正确;
C.2Na2O2+2H2O=4NaOH+O2↑,H2O中的元素没有发生化合价的变化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故C错误;
D.SO2+H2OH2SO3,该反应没有元素化合价变化,不是氧化还原反应,水在反应中既不表现氧化性也不表现还原性,故D错误;
故选B。
9.B
【详解】A. 根据图示的转化过程,NO2转化为HNO2,N元素的化合价由+4价变为+3价,化合价降低,得电子被还原,做氧化剂,则NO2的是生成硫酸盐的氧化剂,故A正确;
B. SO是反应物,参与了反应,不是催化剂,故B错误;
C. 硫酸盐(含SO、HSO)气溶胶中含有HSO,转化过程有水参与,则HSO在水中可电离生成H+和SO,则硫酸盐气溶胶呈酸性,故C正确;
D. 由图可知,SO转化为HSO的过程中还有HNO2和HSO生成,离子方程式为:SO+NO2+H2O=HNO2+HSO,故D正确;
故选B。
10.D
【详解】A.溶液水解显酸性,氢离子与氧化铁反应生成铁离子和水,可除去铁锈,与氧化还原反应无关,A不符合题意;
B.S2-可与Hg2+反应生成HgS,因此可用溶液除去水体中的,与氧化还原反应无关,B不符合题意;
C.石灰乳的主要成分为Ca(OH)2,可与烟气中的发生复分解反应,与氧化还原反应无关,C不符合题意;
D.乙醇具有还原性,可与橙色的酸性重铬酸钾发生氧化还原反应,生成绿色的铬酸钾,因此用酸性溶液检查司机是否酒后驾车与氧化还原反应有关,D符合题意;
答案选D。
11.A
【详解】A. Na与水反应生成NaOH和H2,Na元素的化合价升高,Na作还原剂;
B. Cl2与水反应生成HCl和HClO,Cl元素的化合价既升高又降低,Cl2既是氧化剂又是还原剂;
C. NO2与水反应生成HNO3和NO,N元素的化合价既升高又降低,NO2既是氧化剂又是还原剂;
D. Na2O2与水反应生成NaOH和O2,Na2O2中的O元素化合价既升高又降低,Na2O2既是氧化剂又是还原剂;
根据以上分析可知,在与水反应时,Na是还原剂,Cl2、NO2、Na2O2都既是氧化剂又是还原剂,答案选A。
12.D
【详解】A.小苏打用作食用碱时,主要是与酸发生非氧化还原反应产生二氧化碳,受热体积膨胀,从而使面团变得松软,A不合题意;
B.氢氧化铝能与胃酸(盐酸)反应为复分解反应,不涉及氧化还原反应,B不合题意;
C.人工制作的分子筛表面积大,具有很强的吸附能力,常用作吸附剂,不涉及氧化还原反应,C不合题意;
D.漂粉精[有效成分Ca(ClO)2]具有强氧化性,能杀灭游泳池中的细菌,涉及氧化还原反应,D符合题意;
故选D。
13.B
【详解】a.由题干可知,HCHO与Ag2O反应,产物为CO2和Ag,故化学方程式为HCHO+2Ag2O =CO2+ 4Ag↓+H2O,故a项正确;
b.由题干可知:n(HCHO)~4n(Ag)~4n(Fe3+),所以理论上吸收的HCHO与消耗的Fe3+的物质的量比为1:4,故b项正确。
c.1.12mg Fe2+物质的量为0.02mmol,因为n(HCHO)~4n(Ag)~4n(Fe3+)~n(Fe2+),故HCHO的物质的量为0.005mmol,故m(HCHO)=0.005mmol×30g/mol=0.15mg,取1m3空气,故甲醛含量为0.15mg/m3,超过国家标准,所以室内甲醛含量超标,故c项错误。
故答案为:B。
14.B
【详解】A.Na与生成氢气,中H的化合价降低被还原,表现出氧化性,故A不选;
B.与F2反应生成O2和HF,中O的化合价升高被氧化,表现出还原性,故选B;
C.与Na2O反应生成NaOH,中没有元素化合价发生变化,则即没体现还原性又没体现氧化性,故C不选 ;
D.与NO2反应生成HNO3和NO,中没有元素化合价发生变化,则即没体现还原性又没体现氧化性,故D不选。
答案选B
15.B
【分析】图中过程①表示和NO2反应生成和,过程②表示和NO2加入一个水分子转化为HNO2和,由此分析。
【详解】A.转化为,硫元素从+4转化为+5价,转化为,硫元素由+5价转化为+6价,硫元素的化合价升高,①②过程中硫元素均被氧化,故A正确;
B.根据图示的转化过程,NO2转化为HNO2,N元素的化合价由+4价变为+3价,化合价降低,得电子被还原,做氧化剂,则NO2的是生成硫酸盐的氧化剂,故B错误;
C.硫酸盐(含、)气溶胶中含有,转化过程有水参与,则在水中可电离生成H+和,则硫酸盐气溶胶呈酸性,故C正确;
D.根据图示转化过程中,由转化为,根据图示对照,有水分子中的氧氢键的断裂,故D正确;
答案选B。
16.B
【分析】由化学反应方程式CaOCl2+H2SO4(浓)=CaSO4+Cl2↑+H2O可知,反应中混盐含有的阴离子为Cl-和ClO-,CaOCl2自身既是氧化剂又是还原剂,反应中C1-失电子,C1O-得电子,发生归中反应。以此分析。
【详解】A.根据上述分析可知:CaOCl2中的两种酸根阴离子分别为Cl-和ClO-,故A正确;
B.CaOCl2中没有非极性共价键,故B错误;
C.在CaOCl2+H2SO4(浓)=CaSO4+Cl2↑+H2O反应中,浓硫酸中没有化合价变化,不体现氧化性,故C正确;
D.标准状况下2.24 L Cl2为0.1mol,根据反应中C1-失电子,C1O-得电子,可知发生归中反应生成Cl2,所以转移电子的数目约为6.02×1022,故D正确;
故答案:B。
17.B
【分析】在紫外线作用下,NO2分解生成NO和O,O2与O发生反应Ⅲ生成O3,O3与NO发生反应I生成NO2,丙烯与O3发生反应Ⅱ生成甲醛和乙醛,据此分析解答。
【详解】A. 反应Ⅰ为O3+3NO=3NO2,反应Ⅱ为丙烯与O3发生反应生成甲醛和乙醛,均存在化合价的变化,均属于氧化还原反应,故A正确;
B. 整个过程中O3属于中间产物,故B错误;
C. 由分析知,反应Ⅱ中丙烯与O3发生反应生成甲醛和乙醛,故光化学烟雾中含甲醛、乙醛等刺激性物质,故C正确;
D. 由分析知,反应Ⅲ的方程式为O2+ O = O3,故D正确;
故选B。
18.C
【分析】反应3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3中,Br2一部分被还原成NaBr,一部分被氧化成NaBrO3,Br2既是氧化剂又是还原剂。
【详解】A.标准状况下H2O不是气体,不能用22.4L/mol计算2mol水的体积,A错误;
B.CO32-在溶液中会水解,导致其物质的量小于0.1mol,B错误;
C.每消耗3 mol Br2,其中有0.5 mol Br2被氧化成NaBrO3,有2.5 mol Br2被还原成NaBr,整个过程中转移电子的物质的量为5 mol,数目约为 5×6.02×1023,C正确;
D.氧化产物是NaBrO3,还原产物是NaBr,由化学计量数可知氧化产物与还原产物物质的量之比为1:5,D错误;
答案选C。
【点睛】标准状况下H2O、SO3、CCl4、HF等不是气体,不能用22.4L/mol计算已知体积的这些物质的物质的量。
19.B
【详解】A.由修复过程示意图中反应前后元素化合价变化可知,反应①②③④均为化合价降低得电子的反应,所以均为还原反应,A说法正确;
B.三氯乙烯C2HCl3中C原子化合价为+1价,乙烯中C原子化合价为−2价,则1mol三氯乙烯完全脱Cl时,即转化为1molC2H4时,得到6mol电子,B说法错误;
C.由示意图及N元素的化合价变化可写出如下转化+8e-=,生成物中有生成,则应用H+和H2O来配平该反应,所以④的电极反应式为+10H++8e-=+3H2O,C说法正确;
D.由修复过程示意图可知,生成的二价铁、氧气与氢氧根离子反应,能生成Fe(OH)3,D说法正确;
答案为B。
20.A
【详解】A.2Na+2H2O=2NaOH+H2↑,H2O中H元素化合价由+1降为0价,得电子被还原,做氧化剂,在反应中表现出氧化性,故A符合题意;
B.Cl2+H2OHCl+HClO,H2O中的元素没有发生化合价的变化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故B不符合题意;
C.3NO2+H2O=2HNO3+NO,H2O中的元素没有发生化合价的变化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故C不符合题意;
D.Na2O + H2O = 2NaOH,该反应没有元素化合价变化,不是氧化还原反应,水在反应中既不表现氧化性也不表现还原性,故D不符合题意;
答案选A。
21.CD
【分析】铁与氯气反应生成氯化铁,加入NaClO、NaOH,次氯酸钠将铁离子在碱性条件下氧化成Na2FeO4,加入饱和KOH溶液可析出高铁酸钾(K2FeO4),分离得到粗K2FeO4,采用重结晶、洗涤、低温烘干将其提纯,以此解答该题。
【详解】A. K2FeO4具有强氧化性,可用于杀菌消毒,生成的铁离子可水解生成具有吸附性的氢氧化铁胶体,可用于净水,故A正确;
B. 尾气含有氯气,可与氯化亚铁反应生成氯化铁,可再利用,故B正确;
C. 反应中Cl元素化合价由+1价降低为−1价,Fe元素化合价由+3价升高到+6价,则氧化剂与还原剂的物质的量之比为3:2,故C错误;
D. 结晶过程中加入浓KOH溶液,增大了K+浓度,该温度下,高铁酸钾的溶解度比高铁酸钠的溶解度小,有利于K2FeO4晶体的析出,故D错误;
故选:CD。
22.AC
【详解】A.次氯酸钙溶液应显碱性,且酸性环境下会生成弱电解质HClO,HClO不能写成离子形式,故A错误;
B.SO2在水中的溶解度大于NO,更多的二氧化硫溶于水中被氧化,会使得SO2脱除率高于NO,故B正确;
C.脱除反应的化学原理分别为:2NO+3ClO-+H2O=2H++2NO+3Cl-;SO2+ClO-+H2O=2H++2SO+Cl-;已知n(SO2)∶n(NO)=3∶2;依据图中信息及得:在80min时,NO脱除率80%,即反应的NO为:2mol×80%=1.6mol,1.6molNO生成1.6mol NO和2.4molCl-;SO2脱除率100%,即3molSO2全部反应生,成3molCl-,所以Cl-共3mol+2.4mol=5.4mol;吸收液中n(NO)∶n(Cl-)=1.6:5.4=8:27,故C错误;
D.脱除反应的化学原理分别为:2NO+3ClO-+H2O=2H++2NO+3Cl-;SO2+ClO-+H2O=2H++2SO+Cl-,生成大量H+,使H+浓度增大,pH减小;所以吸收剂溶液的pH逐渐减小,故D正确;
综上所述答案为AC。
23.(1) Fe+4H++=Fe3++NO↑+2H2O 防止生成,抑制水解
(2)4HNO34NO2↑+2H2O+O2↑
(3)C
(4)
(5)加入过量NaOH,Cr3++4OH-=+2H2O,Ni2++2OH-=Ni(OH)2↓,过滤后滤渣中可得Ni元素;再向滤液中加入稀盐酸,调节至pH=7-8,,过滤,滤渣中可得元素
【分析】反应釜中稀硝酸和Fe反应,方程式为4HNO3+Fe=Fe(NO3)3+NO↑+2H2O,NO可以与O2反应生成NO2,2NO+O2=2NO2,NO与NO2通入碱液中吸收;Fe(NO3)3溶液在120℃下浓缩,加入Fe(NO3)3晶种后结晶,经过离心分离得到Fe(NO3)3∙9H2O。
【详解】(1)根据分析,稀硝酸和Fe反应生成Fe(NO3)3、NO和H2O,离子方程式为Fe+4H++=Fe3++NO↑+2H2O;硝酸具有强氧化性,硝酸过量可以将Fe2+完全氧化为Fe3+,而且酸过量可以抑制Fe3+的水解;
(2)浓缩池中有过量的硝酸,受热分解,方程式为4HNO34NO2↑+2H2O+O2↑;
(3)A.硝酸铁晶体溶于水,不能用水洗涤,A不符合题意;
B.CCl4不溶于水,因此无法洗涤,B不符合题意;
C.20%稀硝酸可以洗去硝酸铁表面较浓的硝酸,也可以抑制Fe3+的水解,C符合题意;
D.乙醇可以洗去水,但不能抑制Fe3+的水解,D不符合题意;
故选C。
(4)调pH需要Fe3+完全沉淀,Cr3+不能沉淀,因此pH的反应是3.2≤pH
相关试卷
这是一份北京市高考化学三年(2020-2022)模拟题分类汇编20氧化还原反应(8),共48页。试卷主要包含了单选题,原理综合题,工业流程题,实验题,元素或物质推断题,填空题等内容,欢迎下载使用。
这是一份北京市高考化学三年(2020-2022)模拟题分类汇编19氧化还原反应(7),共42页。试卷主要包含了单选题,填空题,原理综合题,工业流程题,实验题等内容,欢迎下载使用。
这是一份北京市高考化学三年(2020-2022)模拟题分类汇编16氧化还原反应(4),共37页。试卷主要包含了单选题,实验题,填空题,工业流程题,原理综合题等内容,欢迎下载使用。









