





所属成套资源:2023年7月广东省普通高中学业水平合格性考试化学模拟卷
2023年7月广东省普通高中学业水平合格性考试化学模拟卷01
展开
这是一份2023年7月广东省普通高中学业水平合格性考试化学模拟卷01,文件包含2023年7月广东省普通高中学业水平合格性考试化学模拟卷01解析版docx、2023年7月广东省普通高中学业水平合格性考试化学模拟卷01考试版docx、2023年7月广东省普通高中学业水平合格性考试化学模拟卷01参考答案docx等3份试卷配套教学资源,其中试卷共29页, 欢迎下载使用。
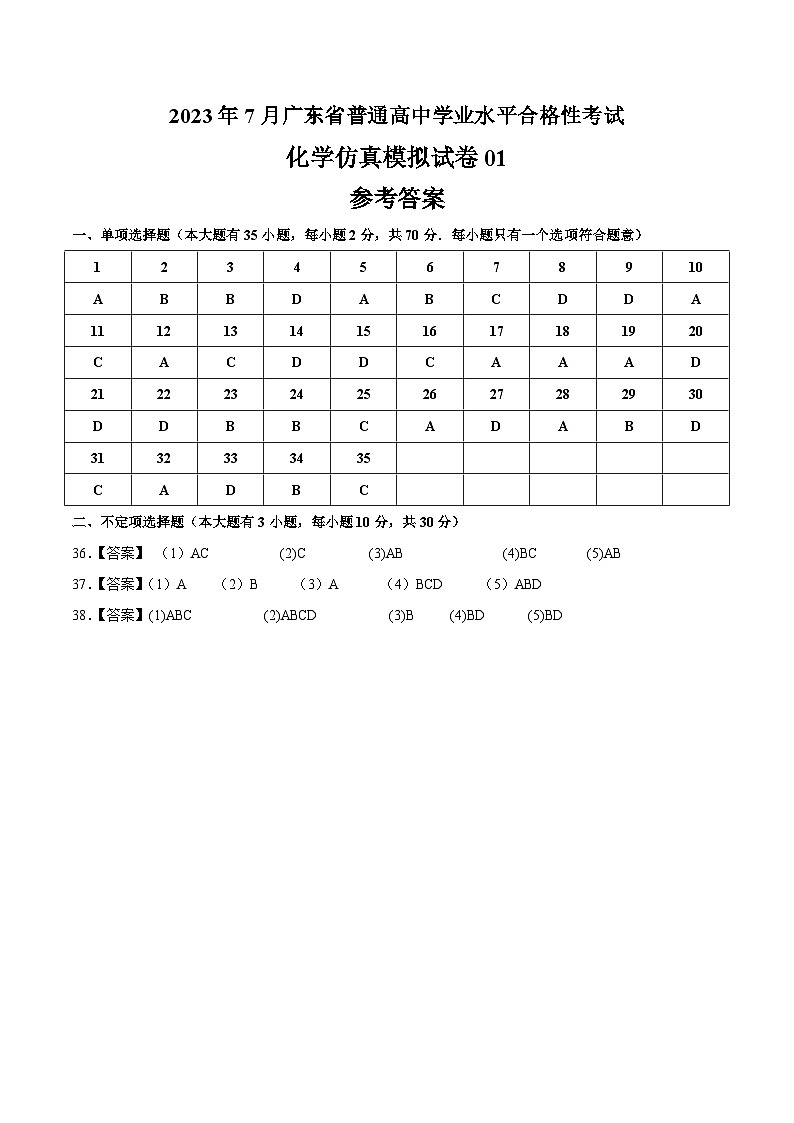
2023年7月广东省普通高中学业水平合格性考试
化学仿真模拟试卷01
(考试时间:60分钟;满分:100分)
一、单项选择题(本大题有35小题,每小题2分,共70分.每小题只有一个选项符合题意)
1.某些食品的包装袋中放置有半透明的颗粒状干燥剂,其成分可能是
A.硅胶 B.铁粉 C.小苏打 D.苏打
【答案】A
【详解】
A.硅胶干燥剂的主要成分是二氧化硅,由天然矿物经提纯加工成透明颗粒状,A正确;
B.铁粉是黑色的,且不适合作为食品的干燥剂,B错误;
C.小苏打是碳酸氢钠,作为发酵粉,C错误;
D.苏打是碳酸钠,白色粉末,在空气中吸收水分而结成硬块,D错误;
答案选A。
2.生活是化学的源泉。下列叙述错误的是
A.浓度为75%的酒精、含氯消毒剂、双氧水均可以有效灭活新型冠状病毒
B.煤、石油、太阳能、风能等均属于新能源
C.许多食品包装盒里用小袋包装的铁粉来防止食品氧化变质
D.节日里燃放的焰火与电子的跃迁有关
【答案】B
【详解】A.75%的酒精、含氯消毒剂、双氧水均能使蛋白质发生变性,能有效杀死病毒,故A正确;
B.煤和石油属于化石能源,不是新能源,故B错误;
C.铁具有较强的还原性,能优先与氧气发生反应,可防止食品被氧化,故C正确;
D.燃放焰火涉及金属的焰色反应,是电子从高能轨道向低能轨道跃迁时释放能量导致,故D正确;
故选:B。
3.目前世界上用量最大、用途最广的合金是
A.青铜 B.钢材 C.铝合金 D.钛合金
【答案】B
【详解】铁与其他元素形成的合金称为铁合金,包括生铁和钢,钢包括低碳钢、中碳钢和高碳钢、合金钢。铁合金是使用最广泛,用量最大的合金,故选:B。
4.下列各组物质,若不加指示剂则不能确定是否发生了反应的一组是
A.锌粒和盐酸 B.锈铁钉和稀硫酸
C.二氧化碳气体和石灰水 D.盐酸和氢氧化钠溶液
【答案】D
【详解】A.锌和盐酸反应会有气体产生,所以不用指示剂就能确定反应发生了,A不符合题意;
B.铁锈和硫酸反应溶液变浅黄色,不用指示剂也能确定反应发生,B不符合题意;
C.二氧化碳和氢氧化钙反应式生成碳酸钙沉淀和水,所以不用指示剂就能确定反应发生,C不符合题意;
D.盐酸和氢氧化钠反应没有明显现象,不用指示剂不能确定其是否反应,D符合题意;
故选D。
5.下列物质中属于强电解质,但在给定条件下不能导电的是( )
A.液态溴化氢 B.蔗糖
C.铝 D.醋酸
【答案】A
【分析】强电解质是在水溶液中或熔融状态中(几乎)完全发生电离的电解质。
【详解】A. 液态溴化氢中没有水,不是水溶液,所以不能导电,但溴化氢是强电解质,A项正确;
B. 蔗糖属于非电解质,B项错误;
C. 铝是单质,既不属于电解质也不属于非电解质,C项错误;
D. 醋酸属于弱电解质,不符合题意,D项错误;
答案选A。
6.磷酸盐氧同位素技术在土壤磷循环中有重要应用。关于的说法正确的是
A.中子数为8
B.与O互为同位素
C.质量数为16
D.核外电子数为10
【答案】B
【分析】原子符号左下角为质子数,左上角为质量数,质量数等于质子数与中子数的和,据此分析解答。
【详解】A.的质子数是8,质量数是18,则其中子数是18-8=10,A错误;
B.与O质子数相同,而中子数不相同,因此二者互为同位素,B正确;
C.的质量数是18,C错误;
D.的质子数是8,由于原子核外电子数等于原子核内质子数,故其核外电子数为8,D错误;
故合理选项是B。
7.苯是重要的化工原料,其分子结构具有对称美,下列说法正确的是( )
A.苯分子中只含有碳碳单键 B.苯能与溴水发生取代反应
C.苯分子中所有原子位于同一平面 D.苯能使KMnO4溶液褪色
【答案】C
【详解】
A.苯分子中6个碳碳键完全相同,是介于碳碳单键和碳碳双键之间的一种独特的化学键,既不是碳碳单键也不是碳碳双键,A错误;
B.苯能与溴水发生萃取,属于物理变化,苯中不含碳碳双键,不能与溴水发生取代反应,苯在有催化剂的条件下可以与纯液溴发生取代反应,B错误;
C.苯分子是平面型分子,分子中所有原子在同一平面上,C正确;
D.苯中不含碳碳双键,不能使KMnO4溶液褪色,D错误。
答案选C。
8.原电池的应用促进了人类社会的发展,某种铜锌原电池示意图如图,关于该原电池的说法正确的是( )
A.铜是负极 B.锌发生还原反应
C.溶液中H+发生氧化反应 D.接通时,电子由锌电极经导线流向铜电极
【答案】D
【详解】
A.活泼金属做负极,故锌是负极,铜做正极,A错误;
B.锌失去电子,发生氧化反应,B错误;
C.溶液中H+得电子,发生还原反应,C错误;
D.电子由负极经导线流向正极,则电子由锌电极经导线流向铜电极,D正确。
答案选D。
9.元素周期表揭示了元素间的内在联系,制出了第一张元素周期表的科学家是
A.张青莲
B.汤姆孙
C.侯德榜
D.门捷列夫
【答案】D
【详解】俄国化学家门捷列夫总结了元素间的内在联系,制出了第一张元素周期表,故D正确;
故选:D。
10.“当晨曦投向街头的雾霾,一道道光束清晰可见”,这句现代诗中描述的“雾霾”应属于胶体,下列关于胶体的叙述中错误的是( )
A.能否发生丁达尔效应是溶液和胶体的本质区别 B.胶体粒子的大小应介于 1-100nm 之间
C.有些胶体能发生电泳现象,但所有胶体均不带电 D.河流入海口形成的三角洲与胶体的聚沉现象有关
【答案】A
【详解】A.溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,分散质微粒直径在10-9~10-7m之间的分散系属于胶体,故A错误;
B.分散质微粒直径在10-9~10-7m即1-100nm之间的分散系属于胶体,故B正确;
C.胶体不带电,胶粒带电,可以发生电泳现象,故C正确;
D.河水是胶体,而海水是电解质溶液,故河流在入海口发生胶体的聚沉,形成三角洲,和胶体的性质有关,故D正确;
综上所述答案为A。
11.食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
品名
×××蔬菜苏打饼
配料
面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁
保质期
12个月
生产日期
2019年1月20日
对上表中各种配料的成分的理解不正确的是( )
A.富含蛋白质的是鸡蛋 B.富含维生素的是脱水青菜和橙汁
C.富含糖类的物质只有白砂糖 D.富含油脂的是精炼食用植物油和奶油
【答案】C
【详解】A.鲜鸡蛋中富含蛋白质,A项正确;
B.脱水青菜或橙汁中富含维生素,B项正确;
C.面粉和白砂糖富含糖类,C项错误;
D.植物油或奶油中富含油脂,D项正确.
答案选C。
【点睛】糖类包括单糖如葡萄糖和果糖等,二糖如蔗糖和麦芽糖等,还有多糖如淀粉、纤维素。
12.若中含有x个原子,则阿伏加德罗常数是
A.7x B.14 x C. x /14 D. x /7
【答案】A
【详解】,则,含有个原子,则;
故选A。
13.下列不属于酸性氧化物的是
A.CO2 B.SO2 C.NO2 D.Mn2O7
【答案】C
【详解】能和碱反应只生成盐和水的氧化物是酸性氧化物,能和酸反应只生成盐和水的氧化物是碱性氧化物,据此分析解题:
A.二氧化碳和NaOH溶液反应生成碳酸钠和水,所以只生成盐和水,为酸性氧化物, A不合题意;
B.二氧化硫和过量NaOH溶液反应生成亚硫酸钠和水,所以只生成盐和水,为酸性氧化物, B不合题意;
C.二氧化氮和碱反应生成盐、水,但由于没有一种含N的含氧酸与NO2中N的化合价相同,故NO2不是酸性氧化物,C符合题意;
D.Mn2O7和强碱溶液反应只生成盐和水,所以为酸性氧化物,D不合题意;
故答案为:C。
14.下列说法中,正确的是
A.浓硫酸稀释时,应将水沿器壁慢慢倒入浓硫酸中,并不断用玻璃棒搅拌
B.浓硫酸不分解,不挥发,所以可以敞口放置于空气中
C.浓硫酸具有氧化性,稀硫酸无氧化性
D.可以用铁罐或铝槽车来运输冷的浓硫酸、浓硝酸
【答案】D
【详解】A.浓硫酸稀释的正确方法为:将浓硫酸沿着烧杯壁缓缓注入水中,同时用玻璃棒不断搅拌,故A错误;
B.浓硫酸具有吸水性,所以放置浓硫酸应密封保存,故B错误;
C.硫酸中氢、硫元素都处于最高价态,所以浓硫酸、稀硫酸都具有氧化性,故C错误;
D.浓硫酸、浓硝酸具有强的氧化性,常温下能够使铁、铝钝化生成致密的氧化膜,所以可以用铁罐或铝槽车来运输冷的浓硫酸、浓硝酸,故D正确;
故答案选D。
15.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图, 它属于
A.无机物 B.烃 C.聚合物 D.烃的衍生物
【答案】D
【详解】A.无机物不含有C=C不饱和键,故A错误;
B.除碳氢元素还含有硫元素,不属于烃,故B错误;
C.该物质相对分子质量较小,不是聚合物,故C错误;
D.该化合物除碳氢元素还含有硫元素,属于烃的衍生物,故D正确。
故答案选D。
16.下列离子能在溶液中大量共存的是
A.Na+、Ca2+、、 B.Na+、、、Mg2+
C.、、K+、Cu2+ D.、K+、H+、
【答案】C
【详解】A.Ca2++=CaCO3↓,A不合题意;
B.+=+H2O,2+Mg2+=Mg(OH)2↓,B不合题意;
C.、、K+、Cu2+ 各离子间均不能发生反应,C符合题意;
D.+ H+=H2O,D不合题意;
故答案为:C。
17.以人为本,注意安全。下列与实验有关的图标中,与其名称相匹配的是
A.洗手: B.用电:
C.热烫: D.排风:
【答案】A
【详解】A.该图标为离开实验室前,要洗手的图标,A正确;
B.该图标为佩戴护目镜,保护眼睛,B错误;
C.该图标为实验中会用到电器的图标,C错误;
D.该图标表示,实验中需要加热操作,D错误;
故选A。
18.有关酯化反应的说法不正确的是
A.酯化反应的产物只有酯
B.浓硫酸可作酯化反应的催化剂
C.除去乙酸乙酯中残留的乙酸可以用饱和的碳酸钠溶液
D.反应加热的目的是加快反应速率
【答案】A
【详解】A.酯化反应除了生成酯之外还生成水,A错误;
B.浓硫酸在酯化反应中做催化剂、吸水剂,B正确;
C.乙酸可以与Na2CO3反应,2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑,乙酸乙酯不与Na2CO3反应,故可以除去乙酸乙酯中残留的乙酸,C正确;
D.升温可以加快反应速率,减少反应时间,D正确;
故选A。
19.根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
实验结论
A
向某溶液中加入NaOH溶液并加热,产生能使湿润红色石蕊试纸变蓝的气体
该溶液中一定含有
B
向某白色粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体
该粉末一定是碳酸盐
C
向CuSO4溶液中加入铁粉,有红色固体析出
氧化性∶Fe2+>Cu2+
D
用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色
该溶液中一定不含K+
【答案】A
【详解】A.能使湿润的红色石蕊试纸变蓝的气体是氨气,向某溶液中加入NaOH溶液并加热,产生能使湿润红色石蕊试纸变蓝的气体,证明该溶液中一定含有 ,故A正确;
B.CO2、SO2都能使澄清石灰水变浑浊,向某白色粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,该粉末可能是碳酸盐或亚硫酸盐,故B错误;
C.向CuSO4溶液中加入铁粉,有红色固体析出,发生了反应:Fe+Cu2+=Cu+Fe2+,根据氧化还原反应规律,氧化剂的氧化性强于氧化产物的氧化性,氧化性:Cu2+>Fe2+,故C错误;
D.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,说明溶液中含有Na+,由于没有透过蓝色钴玻璃,所以不能确定该溶液中是否含有K+,故D错误;
故选A。
20.下列关于硅及其化合物的说法不正确的是
A.高温下石英坩埚会被烧碱腐蚀 B.玻璃、陶瓷和水泥都是传统硅酸盐材料
C.硅元素是构成岩石的核心元素 D.太阳能电池板主要成分为SiO2
【答案】D
【详解】A.石英的主要成分是SiO2,烧碱是NaOH,二者将发生反应:2NaOH+SiO2=Na2SiO3+H2O,故高温下石英坩埚会被烧碱腐蚀,A正确;
B.玻璃、陶瓷和水泥的主要成分均为硅酸盐,都是传统硅酸盐材料,B正确;
C.硅在地壳中的含量高,在自然界中硅主要以化合物二氧化硅、硅酸盐等的形式存在,二氧化硅、硅酸盐等硅的化合物是构成岩石和许多矿物的主要成分,可以说硅是构成岩石和许多矿物的核心元素,C正确;
D.太阳能电池板主要成分为晶体硅,可实现光-电转换,D错误;
答案选D。
21.下列关于试剂存放的叙述正确的是( )
A.硝酸银溶液存放在无色试剂瓶中
B.金属钠保存在CCl4中(钠的密度小于CCl4)
C.氢氧化钠溶液保存在带玻璃塞的玻璃瓶中
D.浓硫酸的装运包装箱应贴上如图所示的标识
【答案】D
【详解】A.硝酸银见光易分解生成银、二氧化氮和氧气,所以要保存在棕色试剂瓶中,故A错误;
B.钠和四氯化碳不反应,但钠的密度小于四氯化碳的密度,钠会浮在四氯化碳液面上,不能隔绝空气,所以不能用四氯化碳保存,故B错误;
C.玻璃中含有二氧化硅,二氧化硅和氢氧化钠反应生成粘性的硅酸钠,导致玻璃塞和玻璃瓶粘结在一起,所以氢氧化钠溶液不能保存在带玻璃塞的玻璃瓶中,应该选用橡皮塞,故C错误;
D.浓硫酸是强腐蚀性的药品,所以浓硫酸的装运包装箱应贴上腐蚀性标签,故D正确;
故选D。
22.物质的性质与用途说法正确,且有因果关系的是
选项
性质
用途
A
Al与浓硫酸不反应
用铝槽盛放浓硫酸
B
SiO2与NaOH溶液不反应
用磨砂玻璃瓶长期存放NaOH溶液
C
FeCl3在沸水中能形成胶体
用FeCl3溶液作为铜电路板刻蚀液
D
Na2O2与CO2反应生成O2
用Na2O2作防毒面具供氧剂
【答案】D
【详解】
A.A1与浓硫酸发生钝化,在铝表面形成致密的氧化膜,钝化是化学反应,A不符题意;
B.SiO2与NaOH溶液能反应,反应的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O,反应生成的硅酸钠有粘性,能粘住磨砂玻璃瓶口,不能长期存放NaOH 溶液,B不符题意;
C.FeCl3溶液可作为铜电路刻蚀液,发生反应为;2Fe3++Cu=2Fe2++Cu2+,FeCl3溶液可作为铜电路刻蚀液与FeCl3在沸水中能形成胶体无关,C不符题意;
D.过氧化钠与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,可作为防毒面具供氧剂,D符合题意。
答案选D。
23.我国谚语与古籍中,有许多关于化学变化的记载。例如,谚语“雷雨发庄稼”;《淮南万毕术》中记载“曾青得铁则化为铜”,以上例子不涉及的反应是( )
A.N2+O22NO B.Zn+Fe2+=Zn2++Fe
C.Fe+Cu2+=Fe2++Cu D.3NO2+H2O=2HNO3+NO
【答案】B
【详解】
谚语“雷雨发庄稼”涉及的反应:氮气在放电条件下与O2反应,N2+O22NO,NO在常温下易与空气的O2反应生成NO2,2NO+O2=2NO2;二氧化氮易与水反应生成硝酸,3NO2+H2O=2HNO3+NO。
“曾青得铁则化为铜”中曾青就是胆矾,即五水硫酸铜,意思是向胆矾中加铁就可以得到铜,有关反应为:Fe+CuSO4=FeSO4+Cu,离子方程式:Fe+Cu2+=Fe2++Cu。所以以上例子不涉及的反应是B。
答案选B。
24.科学使用消毒液是阻断病毒传播的有效方式之一、下列关于“84”消毒液(有效成分是NaClO)的说法,错误的是
A.应在阴凉处密闭保存
B.最好与浓盐酸混合使用
C.能杀菌消毒,利用的是HClO的强氧化性
D.制备原理为Cl2+2NaOH=NaClO+NaCl+H2O
【答案】B
【详解】A.84消毒液中的次氯酸钠可以和水、二氧化碳反应生成的次氯酸见光易分解,应放在阴凉处密封保存,A正确;
B.84消毒液中的次氯酸钠可以和盐酸反应生成氯气,不能混用,B错误;
C.氯酸钠和水、二氧化碳反应生成的次氯酸具有强氧化性,可以杀菌消毒,C正确;
D.氯气和氢氧化钠反应生成84消毒液,方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,D正确;
故选B。
25.元素化合价和物质类别是研究物质性质的两个重要维度。图为氮元素的部分价类二维图。下列推断错误的是
A.空气中a点所示物质体积分数最高
B.b点所示物质遇空气变为红棕色
C.c点所示物质为硝酸
D.d点所示物质可能是一种复合肥料
【答案】C
【分析】根据元素化合价和物质类别分析得到a为氮气,b为NO,c为亚硝酸,d为硝酸盐。
【详解】A.空气中a点所示物质体积分数最高,达到约为78%,故A正确;
B.NO与空气中氧气反应生成二氧化氮,二氧化氮是红棕色气体,因此b点所示物质遇空气变为红棕色,故B正确;
C.c点所示物质为亚硝酸,故C错误;
D.复合肥料是指含有氮磷钾中两种或两种以上营养元素的化肥,d点所示物质可能为硝酸钾,是一种复合肥料,故D正确。
综上所述,答案为C。
26.“共享单车”,低碳环保,有益健身,方便出行。“最后一公里”,下列关于单车的制造材料说法正确的是
A.制造车轮钢圈的材料是合金 B.铝合金制造的车架较钢制造的重
C.制造轮胎用的橡胶有固定的熔点 D.制作反光板的有机玻璃属于硅酸盐
【答案】A
【详解】
A.钢圈含有Fe、C等,是合金,A正确;
B.铝的密度较小,用铝合金制造的车架较钢的更轻,B错误;
C.制轮胎用的橡胶是高分子化合物制成的,属于混合物,无固定熔点,C错误;
D.有机玻璃是有机高分子材料,不是硅酸盐,D错误;
答案选A。
27.实验小组设计如图所示实验,探究Fe与稀硝酸、稀硫酸的反应。实验过程①、③管口处产生红棕色气体,经检验③中反应无产生。
下列说法正确的是
A.①中反应产生,③中反应产生
B.②中存在大量阳离子和
C.③中一定既含有,又含有
D.实验结论:稀硝酸的氧化性强于稀硫酸
【答案】D
【详解】A.①③中都是铁和稀硝酸反应,反应都产生,故A错误;
B.②中铁粉有剩余,所以不可能存在大量,故B错误;
C.硝酸能把铁氧化为,铁又能把还原为,所以③中可能既含有又含有,故C错误;
D.③中反应生成,不生成,所以稀硝酸的氧化性强于稀硫酸,故D正确;
选D。
28.下列反应的离子方程式书写正确的是
A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
B.稀HNO3与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化钡溶液与稀H2SO4反应:Ba2++ OH-+ H++=BaSO4↓+H2O
D.碳酸钙与醋酸反应:+2H+=H2O+CO2↑
【答案】A
【详解】A.氯化铜溶液与铁粉反应发生置换反应生成铜和氯化亚铁,离子方程式为Cu2++Fe=Fe2++Cu ,A正确;
B.稀HNO3与Fe反应不放出氢气,B错误;
C.氢氧化钡溶液中钡离子和氢氧根的个数比为1:2,稀H2SO4中氢离子和硫酸根的个数比为2:1,二者反应的离子方程式为Ba2++2OH-+ 2H+ +=BaSO4↓+2H2O,C错误;
D.醋酸是弱酸,用化学式表示,碳酸钙难溶,用化学式表示,二者反应的离子方程式为CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,D错误。
答案选A。
29.NA代表阿伏伽德罗常数,下列说法正确的是
A.常温常压下,中含有共价键数为4NA
B.和含有电子数均为10NA
C.含有质子数为NA
D.铁在足量氯气中充分燃烧转移电子数为0.2NA
【答案】B
【详解】A.常温常压下,气体摩尔体积不是22.4L/mol,故A错误;
B.和的物质的量均为1mol,均含有10mol电子,含有电子数均为10NA,故B正确;
C.中还原11个质子,含有质子数为1.1NA,故C错误;
D.5.6g铁的物质的量为=0.1mol,而铁在氯气中燃烧变为+3价,故0.1mol铁燃烧后转移0.3NA个电子,故D错误;
故选B。
30.一定条件下,反应2SO2(g)+O2(g)2SO3(g)的正反应反应速或速率(v正)和逆反应速率(v逆)随反应时间(t)变化的曲线如图。其中,处于化学平衡状态的时刻是
A.t1 B.t2 C.t3 D.t4
【答案】D
【详解】当可逆反应达到平衡状态时,用同一物质表示的正、逆反应速率相等。根据图示可知处于化学平衡状态的时刻是t4时刻,故合理选项是D。
31.下列反应中,氧化剂是非金属单质的是( )
A. B.
C. D.Cu + 4HNO3(浓) = Cu(NO3)2+ 2NO2↑+ 2H2O
【答案】C
【详解】
A.反应中,H2O是氧化剂,属于氧化物,故A不符合题意;
B.反应中,HClO既是氧化剂又是还原剂,属于酸,故B不符合题意;
C.反应中,Cl2是氧化剂,属于非金属单质,故C符合题意;
D.反应Cu + 4HNO3(浓) = Cu(NO3)2+ 2NO2↑+ 2H2O中,浓硝酸是氧化剂,属于酸,故D不符合题意;
故选C。
32.旅途中,处处蓝天白云,空气清新,近年来环境治理卓有成效。有关环境污染防治措施与目的不对应的是( )
A.降低CO2排放,以减少酸雨形成
B.使用不含铅的汽油,以减少重金属污染
C.开发利用太阳能,以减少化石能源使用对大气的污染
D.有机化工厂加装尾气处理装置,以减少挥发性有机物对大气的污染
【答案】A
【详解】
A.降低CO2排放能减少温室气体的排放,不能减少酸雨的形成;减少氮的氧化物硫的氧化物的排放才能减少酸雨的形成,故选A;
B.铅属于重金属,对环境会造成污染,所以使用不含铅的汽油,以减少重金属污染,故B不选;
C.利用开发太阳能等新能源能减少对化石能源的开发使用,以减少对大气的污染,故C不选;
D.大部分的有机化合物都具有挥发性,所以有机化工厂加装尾气处理装置,以减少挥发性有机物对大气的污染,故D不选。
答案选A。
33.2007年诺贝尔化学奖授予了合成氨研究领域的科学家。关于合成氨的说法正确的是( )
A.该反应为吸热反应
B.原料N2主要来源于化石燃料
C.合成氨工业生产在常温常压下进行
D.合成氨工业生产通常会使用催化剂来加快反应速率
【答案】D
【详解】
A.合成氨反应为放热反应,故A不选;
B.原料N2主要来源于空气,故B不选;
C.合成氨工业生产需要在高温高压以及催化剂存在的条件下进行,故C不选;
D.由C分析可知合成氨工业生产通常会使用催化剂来加快反应速率,符合题意,故选D。
答案选D
34.中华文明源远流长,劳动人民创造和使用的许多技术彰显了中华智慧。下列技术不涉及化学变化的是
A.古代湿法冶金技术
B.打磨磁石制指南针
C.用铁矿石冶炼钢铁
D.用黏土烧制陶瓷
【答案】B
【详解】A.湿法冶金指Fe与CuSO4发生置换反应生成Cu和FeSO4,属于化学变化,A不符合题意;
B.打磨磁石制指南针过程中只是物体的形状发生改变,没有新物质生成,属于物理变化,B符合题意;
C.铁矿石冶炼钢铁是用还原剂将铁还原出来,属于化学变化,C不符合题意;
D.黏土烧制陶瓷涉及二氧化硅变为硅酸盐的过程,属于化学变化,D不符合题意;
故答案选B。
35.为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶解于水,然后进行以下操作:①过滤 ②加过量NaOH溶液 ③加入适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。正确的操作顺序是( )
A.④①③⑤② B.①④③⑤② C.⑤②④①③ D.③④①②⑤
【答案】C
【详解】除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,NaOH可除去镁离子,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子及钙离子,所以④碳酸钠溶液必须放在⑤氯化钡溶液之后,盐酸要放在最后,则合理的顺序为⑤②④①③,C项正确,
答案选C。
【点睛】粗盐提纯过程中要思考过量的除杂剂应该如何处理,理解为什么碳酸钠要放在氯化钡之后进行除杂,盐酸要放在过滤之后是解题的突破口。
二、不定项选择题(本大题有3小题,每小题10分,共30分)
36.如图所示,实验室用铜与浓硫酸加热的方法来制备SO2,并探究其化学性质。
(1)试管①中反应的化学方程式或离子方程式为_______。
A. Cu+2H2SO4(浓)CuSO4+SO2↑+H2O B. Cu+H2SO4CuSO4+H2↑
C.Cu+2H2SO4(浓)Cu2++SO42-+SO2↑+H2O D.Cu+SO42-Cu2++SO2↑+H2O
(2)若试管②中盛放品红试液,可以验证的SO2的性质是_______。
A.还原性 B.氧化性 C.漂白性 D.酸性
(3)若要验证SO2的还原性,试管②中应盛放_______溶液。
A.酸性高锰酸钾溶液 B.溴水溶液
C.乙醇溶液 D.H2S溶液
(4)试管③的试剂和用途分别是_____________。
A.防倒吸 B.处理SO2尾气 C.NaOH溶液 D.水
(5)SO2 是唯一在葡萄酒生产中普遍应用的添加剂,在葡萄酒工艺中加入SO2的主要目的是__________。
A.选择性杀菌 B.抗氧化作用
C.提高酸度 D.增加口感
【答案】 (1)AC (2)C (3)AB (4)BC (5)AB
【分析】试管①产生SO2,试管②验证SO2的性质,则试管③用来除去多余的SO2,据此分析。
【详解】用铜与浓硫酸加热条件下,反应会生成硫酸铜,二氧化硫和水,故试管①中反应的化学方程式为:Cu+2H2SO4(浓)CuSO4+SO2↑+H2O,离子方程式为Cu+2H2SO4(浓)Cu2++SO42-+SO2↑+H2O ;试管②中盛放品红溶液,可以验证SO2的漂白性。若要验证SO2的还原性,试管②中盛放酸性高锰酸钾溶液或溴水溶液。二氧化硫有毒,需要尾气处理,则试管③中应盛放氢氧化钠溶液。SO2 是唯一在葡萄酒生产中普遍应用的添加剂,在葡萄酒工艺中加入SO2的主要目的是选择性杀菌和抗氧化。
37.有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B的单质充分反应可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)上述ABCD四种元素分别为_______________
A. 碳 氧 钠 硫 B. 氮 氧 钠 硫
C. 氢 氮 钠 氯 D. 碳 氧 镁 硫
(2)D元素位于周期表__________________。
A.第二周期VIA B.第三周期VIA
C第二周期VA D.第三周期VA
(3) A元素的简单氢化物的空间结构为_____________
A. 正四面体 B.直线形 C.V形 D.三角锥
(4) C2B2的化学性质有______________________
A. 可与二氧化碳反应生成氢气 B.可与二氧化碳反应生成氧气
C.可与水反应生成氧气 D.可做漂白剂
(5)下列说法正确的是________________
A.用电子式表示C2D的形成过程:
B.AB2的电子为
C.D的氧化物只有一种
D.D的最高价氧化物对应水化物的酸性大于A的最高价氧化物对应水化物的酸性
【答案】 (1)A (2)B (3)A (4)BCD (5) ABD
【分析】C燃烧时使火焰呈现黄色,由焰色反应可知C为钠元素,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物E,则B为氧元素,生成Na2O2、D为硫元素; A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,应为碳元素,D单质为黄色,应为硫元素,据此分析;
【详解】(1)据以上分析可知,A为碳元素,B为氧元素,C为钠元素,D为硫元素;
(2) D为硫元素,原子核外有3个电子层,最外层电子数为6,应位于周期表第三周期第VIA族;
(3) CH4的空间结构为正四面体形;
(4) C2B2为Na2O2,具有的化学性质是可以与二氧化碳反应生成氧气,可与水反应生成氧气,可做漂白剂;
(3)C2D为Na2S,电子式表示形成过程可为 , AB2为CO2,为共价化合物,电子式为,D的氧化物有二氧化硫和三氧化硫两种,D的最高价氧化物对应水化物为硫酸,A的最高价氧化物对应水化物为碳酸,硫酸酸性大于碳酸。
38.基于自然界可再生资源获得石油化工产品,是绿色化学的研究热点。一定条件下,以纤维素和淀粉为原料,制备对二甲苯 (PX) 的合成路线如下:
(1)下列关于纤维素、淀粉和葡萄糖的说法,正确的是_________
A.葡萄糖属于单糖
B.葡萄糖可发生银镜反应
C.稀酸催化下,纤维素和淀粉都能发生水解反应
D.人体不能吸收纤维素,因此不宜食用含纤维素的食物
(2)乳酸的某些性质类似于乙醇和乙酸。下列关于乳酸的说法,正确的是_________
A.分子式为C3H6O3
B.能与NaOH反应
C.能与CH3CH2OH发生酯化反应
D.能与CH3COOH发生酯化反应
(3)化合物 的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物,该反应类型为_________
A.取代反应 B.加成反应 C.氧化反应 D.水解反应
(4)丙烯酸能通过原子利用率 100% 的加聚反应生成高分子化合物。下列化合物中,也能发生原子利用率100%的加聚反应的是_________
A.乙烷 B.乙烯 C.乙醇 D.氯乙烯
(5)化合物PX属于_________
A.烷烃 B.芳香烃 C.链状烃 D.不饱和烃
【答案】(1)ABC (2)ABCD (3)B (4)BD (5)BD
【详解】(1)A.葡萄糖属于单糖,A正确;B.葡萄糖中含有醛基,可以发生银镜反应,B正确;
C.纤维素和淀粉在酸性条件下可以发生水解反应,C正确;D.纤维素可以促进大肠蠕动,从而促进消化吸收其他营养物质,所以纤维素在防止便秘方面是有利的,D错误;故选BC;
(2)A.根据乳酸的结构简式可知,其分子式为:C3H6O3,A正确;B.乳酸中含有羧基,可以跟氢氧化钠反应,B正确;C.乳酸中含有羧基,可以和羟基发生酯化反应,C正确;D.乳酸中含有羟基,可以和羧基发生酯化反应,D正确;故选ABCD;
(3)中含有碳碳双键,可以和氢气发生加成反应,生成;
故选B;
(4)A.乙烷中没有碳碳双键,不能发生加聚反应,A错误;B.乙烯中含有碳碳双键,可以发生加聚反应,B正确;C.乙醇中没有碳碳双键,不能发生加聚反应,C错误;D.氯乙烯含有碳碳双键,可以发生加聚反应,D正确;故选BD;
(5)A.化合物PX中含有苯环,不是烷烃,A错误;B.化合物PX中,含有苯环,属于芳香烃,B正确;
C.化合物PX中,含有苯环,不是链状烃,C错误;D.化合物PX中,含有苯环,属于不饱和烃,D正确;
故选BD。
相关试卷
这是一份卷01—2023年普通高中学业水平合格性考试化学模拟卷(广东专用),文件包含卷012023年普通高中学业水平合格性考试化学模拟卷解析版广东专用docx、卷012023年普通高中学业水平合格性考试化学模拟卷原卷版广东专用docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
这是一份2023年北京第二次普通高中学业水平合格性考试化学模拟卷01,文件包含2023年6月北京市普通高中学业水平合格性考试化学模拟卷01解析版docx、2023年6月北京市普通高中学业水平合格性考试化学模拟卷01考试版docx、2023年6月北京市普通高中学业水平合格性考试化学模拟卷01参考答案docx等3份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
这是一份2023年7月浙江省普通高中学业水平合格性考试化学模拟卷01,文件包含2023年7月浙江省普通高中学业水平合格性考试化学模拟卷01解析版docx、2023年7月浙江省普通高中学业水平合格性考试化学模拟卷01考试版docx、2023年7月浙江省普通高中学业水平合格性考试化学模拟卷01参考答案docx等3份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。









