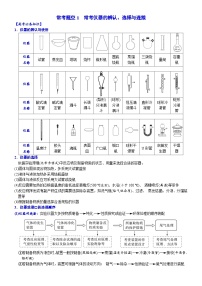
04 常考题空4 晶体化学式及粒子数确定 (附答案解析)-备战高考化学大题逐空突破系列(全国通用)
展开
这是一份04 常考题空4 晶体化学式及粒子数确定 (附答案解析)-备战高考化学大题逐空突破系列(全国通用),共9页。
常考题空4 晶体化学式及粒子数确定【高考必备知识】1.晶胞中微粒数目的计算方法——均摊法(1)原则:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额就是(2)方法:①长方体(正方体)晶胞中不同位置的粒子数的计算a.处于顶点上的粒子,同时为8个晶胞所共有,每个粒子有属于该晶胞b.处于棱边上的粒子,同时为4个晶胞所共有,每个粒子有属于该晶胞c.处于晶面上的粒子,同时为2个晶胞所共有,每个粒子有属于该晶胞d.处于晶胞内部的粒子,则完全属于该晶胞②非长方体晶胞中粒子视具体情况而定三棱柱六棱柱平面型石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三个六边形共有,每个六边形占2.熟记几种常见的晶胞结构及晶胞含有的粒子数目晶体NaClCsClZnSCaF2金刚石晶体结构粒子数目 4个Na+,4个Cl- 1个Cs+,1个Cl- 4个S2-,4个Zn2+ 4个Ca2+,8个F-8个C 晶体简单立方体心立方面心立方氮化硼干冰晶体结构粒子数目1个原子2个原子4个原子4个B,4个N4个CO2 【题组集训】1.利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,如图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为________,该功能陶瓷的化学式为________2.石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为________,该材料的化学式为________3.一个Cu2O晶胞如图所示,Cu原子的数目为______4.某FexNy的晶胞如图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如题图-2 所示,其中更稳定的Cu替代型产物的化学式为___________5.碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为_________ 6.某镍白铜合金的立方晶胞结构如图所示,晶胞中铜原子与镍原子的数量比为________7.某晶体的一部分如图所示,这种晶体中A、B、C三种粒子数之比是________8.最近发现一种钛原子和碳原子构成的气态团簇分子,如图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式为________9.已知镧镍合金LaNin的晶胞结构如下图,则LaNin中n=________10.如图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为________11.Cu元素与H元素可形成一种红色化合物,其晶体结构单元如右图所示。则该化合物的化学式为_______ 12.科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示。该化合物中的K原子和C60分子的个数比为________13.已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为__________,其配位数为__________14.砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图,砷化镓的化学式为______,镓原子的配位数为______15.一种铜金合金晶体具有面心立方最密堆积的结构.在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________16.随着科学的发展和大型实验装置(如同步辐射和中子源)的建成,高压技术在物质研究中发挥越来越重要的作用。高压不仅会引发物质的相变,也会导致新类型化学键的形成。近年来就有多个关于超高压下新型晶体的形成与结构的研究报道。NaCl 晶体在50~300GPa 的高压下和Na 或Cl2反应,可以形成不同组成、不同结构的晶体。下图给出其中三种晶体的晶胞(大球为氯原子,小球为钠原子)。写出A、B、C 的化学式。A________; B________; C________17.某离子晶体的晶体结构中最小重复单元如图所示。A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为________18.最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性,因这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为________19.钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。钛酸钡晶胞结构示意图如图所示,它的化学式是________20.如图是Mn和Bi形成的某种晶体的晶胞结构示意图,则该晶体的化学式可表示为________21.钒(V)的某种氧化物的晶胞结构如图所示。该晶体的化学式为( ) 22.硼普遍存在于蔬菜水果中,是维持骨骼健康和钙、磷、镁正常代谢所需要的微量元素之一。晶体硼的基本结构单元是由硼原子组成的正二十面体(如右图),其中含有20个等边三角形和一定数目的顶角,每个顶角上各有1个硼原子。请观察图形后回答:这个基本结构单元由 个硼原子组成,键角是 ,共含有 个B—B键23.元素铜的一种氯化物晶体的晶胞结构如右图所示,该氯化物的化学式是 24.硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为________25.已知如图所示晶体的硬度很可能比金刚石大,且原子间以单键结合,则根据图确定该晶体的化学式为_______26.131I2晶体的晶胞结构如图甲所示,该晶胞中含有_______个131I2分子;KI的晶胞结构如图乙所示,每个K+紧邻________个I-27.钡钛矿的晶体结构如图所示,Ba2+的O2-配位数是________,Ti4+的O2-配位数是________,O2-的Ba2+配位数是________,Ti4+的Ba2+配位数是________28.以Zn为顶点的ZnGeP2晶胞结构如图所示。Zn的配位数为__________,以Ge为顶点的晶胞中,Zn原子位于_________29.天然硅酸盐组成复杂,阴离子的基本结构单元是SiO四面体,如图(a),通过共用顶角氧离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中Si与O的原子数之比为________,化学式为________(用n代表聚合度)30.在硼酸盐中,阴离子有链状、环状等多种结构形式。如图是一种链状结构的多硼酸根,则多硼酸根离子符号为________31.V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为________;也可以得到偏钒酸钠,其阴离子呈如图d所示的无限链状结构,则偏钒酸钠的化学式为________32.磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如图所示,由图推知该多磷酸钙盐的通式为________33.NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示,这类磷酸根离子的化学式可用通式表示为________(用n代表P原子数)34.磷酸通过分子间脱水缩合形成多磷酸,如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为________【常考题空4 晶体化学式及粒子数确定】答案1.2 BN解析:的个数:1+8×=2;的个数:1+4×=2,所以每个晶胞中含有B原子、N原子的个数均为2,其化学式为BN。2.12 M3C60解析:由晶胞结构图可知,位于棱上的M原子数为12,内部M原子数为9,晶胞中M原子数共12×+9=12;C60位于顶点8个,面心6个,晶胞中含C60数共8×+6×=4。M原子与C60微粒数之比为3∶1,因而化学式为M3C60。3.44.Fe3CuN5.K3C60 6.3∶17.1∶4∶2 8.Ti14C13 解析:由题意知该物质是气态团簇分子,题图所示应是该物质的一个完整的分子,由14个钛原子和13个碳原子构成9.5解析:La:2×+12×=3,Ni:12×+6×+6=15,所以n=510.+3价解析:R:8×+1=2,G:8×+8×+4×+2=8,Q:8×+2=4,R、G、Q的个数之比为1∶4∶2,则其化学式为RQ2G4。由于R为+2价,G为-2价,所以Q为+3价。11.CuH解析:根据晶胞结构可以判断:Cu():2×+12×+3=6;H():6×+1+3=6,所以化学式为CuH。12.3∶1解析:根据晶胞结构可以判断C60:8×+1=2,K:2×6×=6,所以K原子与C60分子的个数之比为3∶1。13.+2 614.GaAs 4 15.1:316.A:NaCl3 B:Na3Cl C:Na2Cl 17.BA2 解析:A:8,B:8×+6×=4。18.MgCNi3 解析:该晶体的结构单元中含镁原子个数为8×=1;含镍原子个数为6×=3;含碳原子个数为1。B项符合题目要求。19.BaTiO320.MnBi 解析:由晶胞的结构图可知,锰原子分布在正六棱柱的顶点、上下底面的面心上、棱边的中点上和体心上,所以锰原子的个数为:12×+2×+6×+1=6,铋原子分布在六棱柱的体内,数目为6,所以锰原子和铋原子的个数比为6:6=1:1,所以化学式为MnBi,故选C。21.VO2 解析:由晶胞图可知,V位于晶胞的顶点和体心,V的个数为1+8×=2,有4个O位于晶胞面上,2个O位于晶胞内部,则O的个数为4×+2=4,则该晶体的化学式为VO2。22.12 60° 3023.CuCl 24.MgB2。解析 (1)每个Mg周围有6个B,而每个B周围有3个Mg,所以其化学式为MgB2。25.B3A426.4 6解析:由131I2晶胞结构图可知,碘分子位于晶胞的8个顶角和6个面上,故一个晶胞中含有4个131I2分子;KI晶胞与NaCl晶胞结构相似,每个K+紧邻6个I-,同层有4个,上下各1个。27.12 6 4 828.4 面心(底心)、棱心29.2∶5.5 [Si4O11]。解析:n个SiO2通过共用顶点氧离子可形成双链结构,找出重复的结构单元,如图:,由于是双链,其中顶点氧占,Si原子数为4,O原子数为4×+6×+4+2=11,其中Si与O的原子数之比为2∶5.5,化学式为[Si4O11]。30.BO。解析:从图可看出,每个单元中,都有一个B和一个O完全属于这个单元,剩余的2个O分别被两个结构单元共用,所以B∶O=1∶(1+2/2)=1∶2,化学式为BO。31.正四面体形 NaVO332.(CaP2O6)n33.(PnO3n+1)(n+2)-34.PnO
相关试卷
这是一份03 常考题空3 等电子体、成键方式、晶体类型的判断 (附答案解析)-备战高考化学大题逐空突破系列(全国通用),共7页。
这是一份04 常考题空4 工艺流程中的答题规范 (附答案解析)-备战高考化学大题逐空突破系列(全国通用),共12页。
这是一份04 常考题空4 实验简答题的精准描述 (附答案解析)-备战高考化学大题逐空突破系列(全国通用),共18页。