
_2018年内蒙古乌兰察布市中考化学真题及答案
展开2018年内蒙古乌兰察布市中考化学真题及答案
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 S-32 C1-35.5 K-39 Ca-40
一、选择题
1. 物质的下列用途主要利用其化学性质的是
A.液氧(支持燃烧) | B.金属铜(制电线) | C.活性炭(做防毒面具的吸附剂) | D.不锈钢(做水壶) |
A. A B. B C. C D. D
【答案】A
2. 分类法是学习和研究物质的一种重要方法,下列分类正确的是
A. 生铁、黄金、金刚石——合金 B. 纯碱、烧碱、熟石灰——碱
C. 氮气、红磷、铝—— 单质 D. 水、干冰、氯酸钾——氧化物
【答案】C
3. 下列有关说法正确的是
A. 氧气、二氧化碳和过氧化氢三种物质中都含有氧分子
B. 表示的粒子都是阴离子
C. 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
D. 硝酸钾、氯化钠和硫酸铵三种物质在pH=10的溶液中能大量共存
【答案】B
4. 下列有关叙述正确的是
A. 分离Zn和Fe的固体混合物,加适量的FeSO4溶液后过滤
B. 除去CO2气体中混有的HCl气体,依次通过足量的NaOH溶液和浓硫酸
C. 配制50g质量分数为6%的NaOH溶液,将NaOH固体放到纸上称量,再用50mL量简量取水
D. 鉴别NaOH溶液、Ca(OH)2溶液和稀硫酸,可用一种试剂一次鉴别
【答案】D
5. 有一不纯的Na2CO3样品,杂质可能是K2CO3、CaCO3、FeCl3和NaCl中的一种或几种,取该样品10.6g,加入足量稀盐酸完全反应后得到无色容液,同时产生4.48气体,下列判断正确的是
A. 杂质一定有FeCl3和CaCO3
B. 杂质一定没有NaCl
C. 杂质可能是K2CO3、CaCO3、NaCl组成的
D. 杂质可能是K2CO3和NaCl组成的
【答案】C
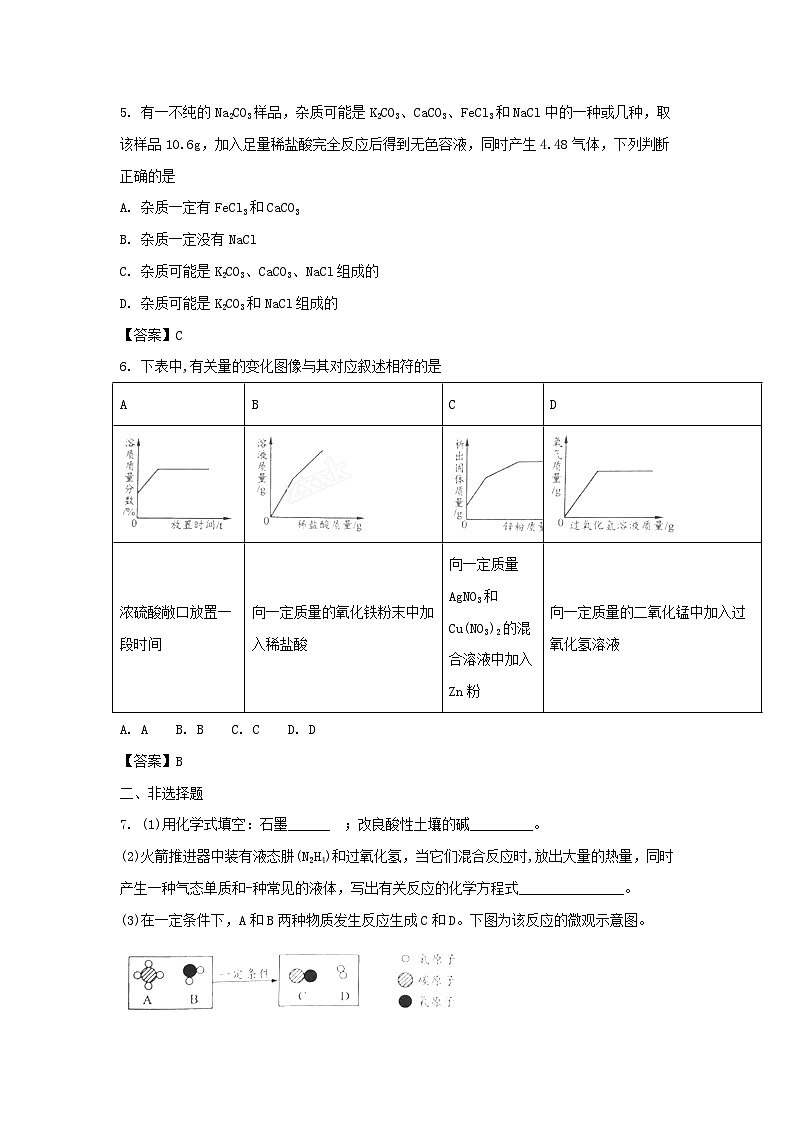
6. 下表中,有关量的变化图像与其对应叙述相符的是
A | B | C | D |
浓硫酸敞口放置一段时间 | 向一定质量的氧化铁粉末中加入稀盐酸 | 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉 | 向一定质量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
【答案】B
二、非选择题
7. (1)用化学式填空:石墨______ ;改良酸性土壤的碱_________。
(2)火箭推进器中装有液态肼(N2H4)和过氧化氢,当它们混合反应时,放出大量的热量,同时产生一种气态单质和-种常见的液体,写出有关反应的化学方程式_______________。
(3)在一定条件下,A和B两种物质发生反应生成C和D。下图为该反应的微观示意图。
①从微观角度分析该反应的实质是______________。
②该反应中,生成C和D的质量比是___________。
(4)在托盘天平(灵敏度极高)两边各放盛有等质量、等质量分数足量稀硫酸的烧杯,天平平衡。向左烧杯中加入一定质量的金属M,同时向右烧杯中加入相同质量的金属N,观察到从反应开始至结束天平指针始终偏向右边(注:反应中都生成十2价的硫酸盐)。则:
①M、N两种金属的活动性由强到弱的顺序为____________。
②M、N两种金属的相对原子质量由大到小的顺序为__________。
【答案】 (1). C (2). Ca(OH)2 (3). N2H4+2H2O2=N2↑+4H2O (4). 在化学变化中分子可分,原子不可再分 (5). 14: 3 (6). M N (7). N M
8. 根据下图回答问题:
(1)实验室用高锰酸钾制取并收集较纯净的氧气,应选用的装置是________(填字母)。向气体发生装置内加入药品前应进行的操作是____________。
(2)实验室用石灰石和稀盐酸反应制取二氧化碳时,可选用发生装置A或G,G与A相比较,其优点是_________;若用F 装置收集二氧化碳,检验二氧化碳已收集满的方法是______。如果要证明制取二氧化碳实验后的废液呈酸性,可选用的试剂是_______(填字母)。
a.紫色石蕊溶液 b.石灰石 c.氢氧化钠溶液 d.硝酸银溶液 e.铜
【答案】 (1). BE (2). 检查装置的气密性 (3). 可控制反应的发生与停止 (4). 将燃着的木条放在b导管ロ处,若木条熄火,证明巳收集满 (5). ab
9. 有一包固体,可能含有NaCl、NaOH、Na2CO3、Na2SO4、MgCl2中的一种或几种。为确定其组成,取少量固体加足量水溶解得到无色溶液M,进行下图实验。
试推断:
(1)白色沉淀B是______ (填化学式)。
(2)原固体中一定含有的物质是_______。
(3)无色滤液2中一定含有的阳离子是__________(填离子符号)。
(4)通过上述实验可知还有一种物质不能确定是否存在,为进-步确定,应采用的方法是____。
【答案】 (1). AgCl (2). NaOH、Na2SO4 (3). Na+、H+、Ba2+ (4). 方法一:将上述实验中的稀盐酸改成稀硝酸
方法二:取原固体少量加足量水溶解,先加过量的稀硝酸,再加过量的Ba(NO3)2溶液,过滤,取滤液滴加适量的AgNO3溶液,如果产生白色沉淀,证明有NaCl
10. 为探究CuO和稀硫酸反应后溶液中溶质的成分,同学们设计了实验、歩驟如下:
(1)取少量CuO粉末于试管中,滴加稀硫酸,粉末全部溶解,得到溶液A。
(2)向歩驟(1)的試管中滴加BaCl2溶液,有白色況淀生成。得出结论:A中溶质只有CuSO4。有同学认为该结论不合理,继续迸行实验。
(3)向歩驟(2)的武管中滴加NaOH溶液,产生沉淀质量随加入NaOH溶液貭量的変化关系如图。回答下列问题:
①A中的溶质有_____(填化学式),b~c之间的沉淀是___________。
②c点对应溶液中溶质的可能组成有_________(填化学式)。
③由以上实验总结出:在分析化学反应后溶液中溶质的成分时,除了考虑生成物外,还需要考虑____________。
【答案】 (1). CuSO4、H2SO4 (2). BaSO4、Cu(OH)2 (3). NaCl或NaCl、Na2SO4或NaCl、BaCl2 (4). 反座物是否有剩余
11. 某兴趣小組为测定石灰石中碳酸钙的貭量分数,取12g石灰石样品加入烧杯中,将120g稀盐酸平均分四次加入,充分反应后(杂质不溶于水也不与稀盐酸反应),测得实验数据如下:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸的质量/g | 30 | 30 | 30 | 30 |
剩余固体的质量/g | 9 | 6 | 3 | 2 |
分析数据计算(結果精碩到0.1%):
(1)该祥品中碳酸钙的质量分数为__________。
(2)所用稀盐酸的溶质貭量分数为__________。
(3)12g样品中的碳酸钙恰好完全反应时所得溶液的溶貭貭量分数为__________。
【答案】 (1). 83.3% (2). 7.3% (3). 10.5%
_2022年内蒙古呼伦贝尔中考化学真题及答案: 这是一份_2022年内蒙古呼伦贝尔中考化学真题及答案,共15页。试卷主要包含了选择题,填空与简答题,实验与探究题,计算与分析题等内容,欢迎下载使用。
_2022年内蒙古呼和浩特中考化学真题及答案: 这是一份_2022年内蒙古呼和浩特中考化学真题及答案,共14页。试卷主要包含了选择题,填空题,实验题,计算题等内容,欢迎下载使用。
_2018年内蒙古兴安盟中考化学真题及答案: 这是一份_2018年内蒙古兴安盟中考化学真题及答案,共5页。试卷主要包含了 选择题, 填空与简答题, 实验与探究题, 计算与分析题等内容,欢迎下载使用。












