2023年四川省成都市锦江区中考二模化学试题(含答案)
展开2023年四川省成都市锦江区中考二模化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
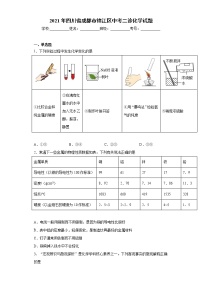
1.下列劳动项目所涉及的化学知识正确的是
选项 | 劳动项目 | 化学知识 |
A | 用石灰浆刷墙 | 氢氧化钙能与氧气反应 |
B | 利用明矾来净化鱼缸内的水 | 明矾能作净水的絮凝剂 |
C | 用生石灰制作发热包 | CaO与水反应吸收热量 |
D | 用含NaOH的炉具清洁剂去除油污 | NaOH能乳化油污 |
A.A B.B C.C D.D
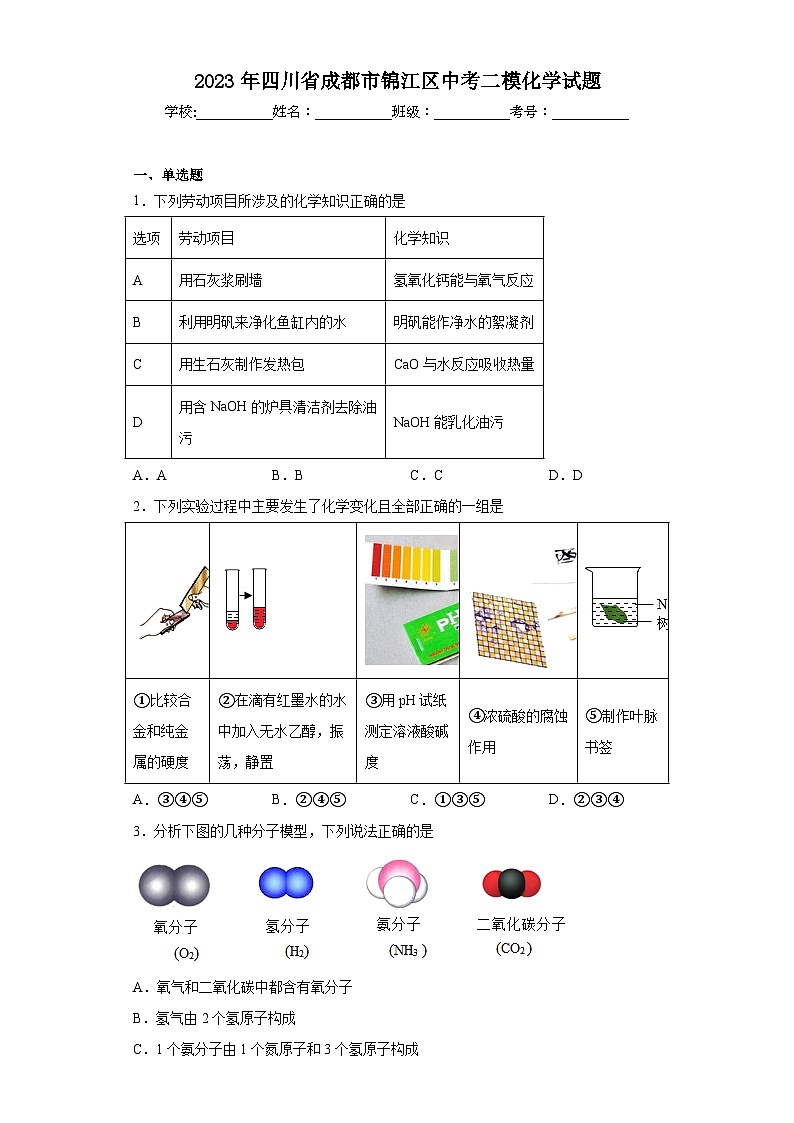
2.下列实验过程中主要发生了化学变化且全部正确的一组是
①比较合金和纯金属的硬度 | ②在滴有红墨水的水中加入无水乙醇,振荡,静置 | ③用pH试纸测定溶液酸碱度 | ④浓硫酸的腐蚀作用 | ⑤制作叶脉书签 |
A.③④⑤ B.②④⑤ C.①③⑤ D.②③④
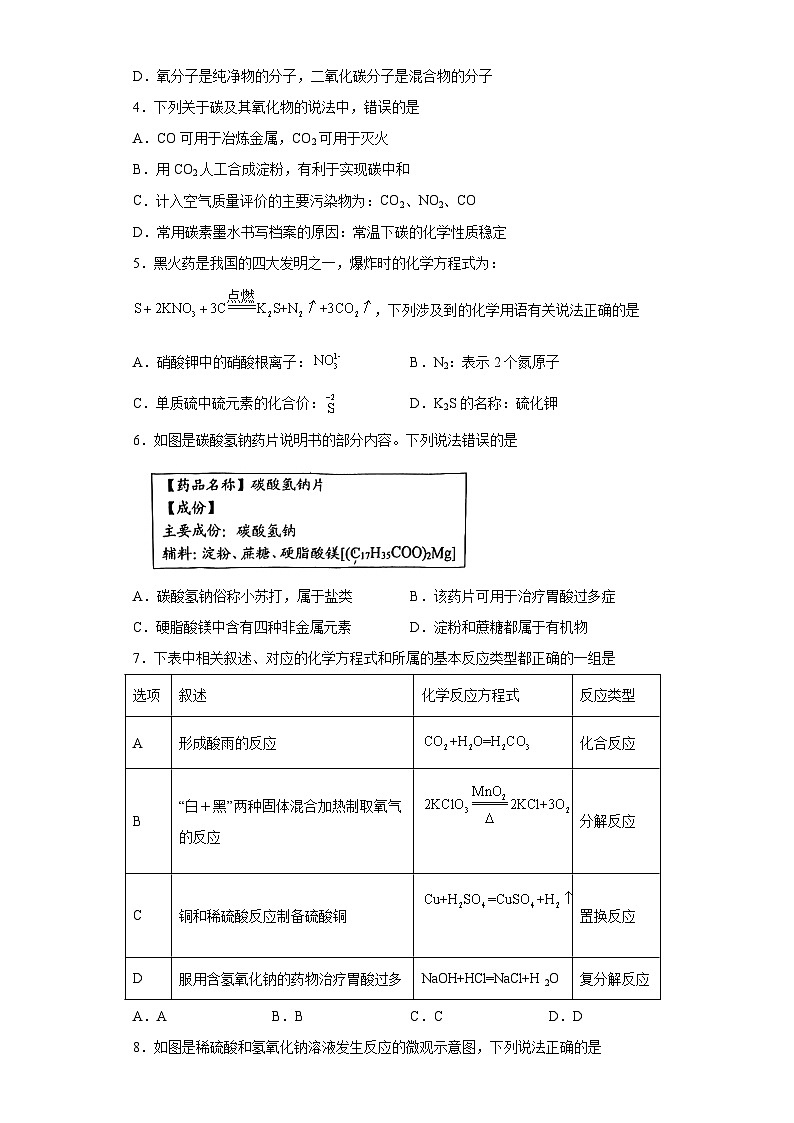
3.分析下图的几种分子模型,下列说法正确的是
A.氧气和二氧化碳中都含有氧分子
B.氢气由2个氢原子构成
C.1个氨分子由1个氮原子和3个氢原子构成
D.氧分子是纯净物的分子,二氧化碳分子是混合物的分子
4.下列关于碳及其氧化物的说法中,错误的是
A.CO可用于冶炼金属,CO2可用于灭火
B.用CO2人工合成淀粉,有利于实现碳中和
C.计入空气质量评价的主要污染物为:CO2、NO2、CO
D.常用碳素墨水书写档案的原因:常温下碳的化学性质稳定
5.黑火药是我国的四大发明之一,爆炸时的化学方程式为:,下列涉及到的化学用语有关说法正确的是
A.硝酸钾中的硝酸根离子: B.N2:表示2个氮原子
C.单质硫中硫元素的化合价: D.K2S的名称:硫化钾
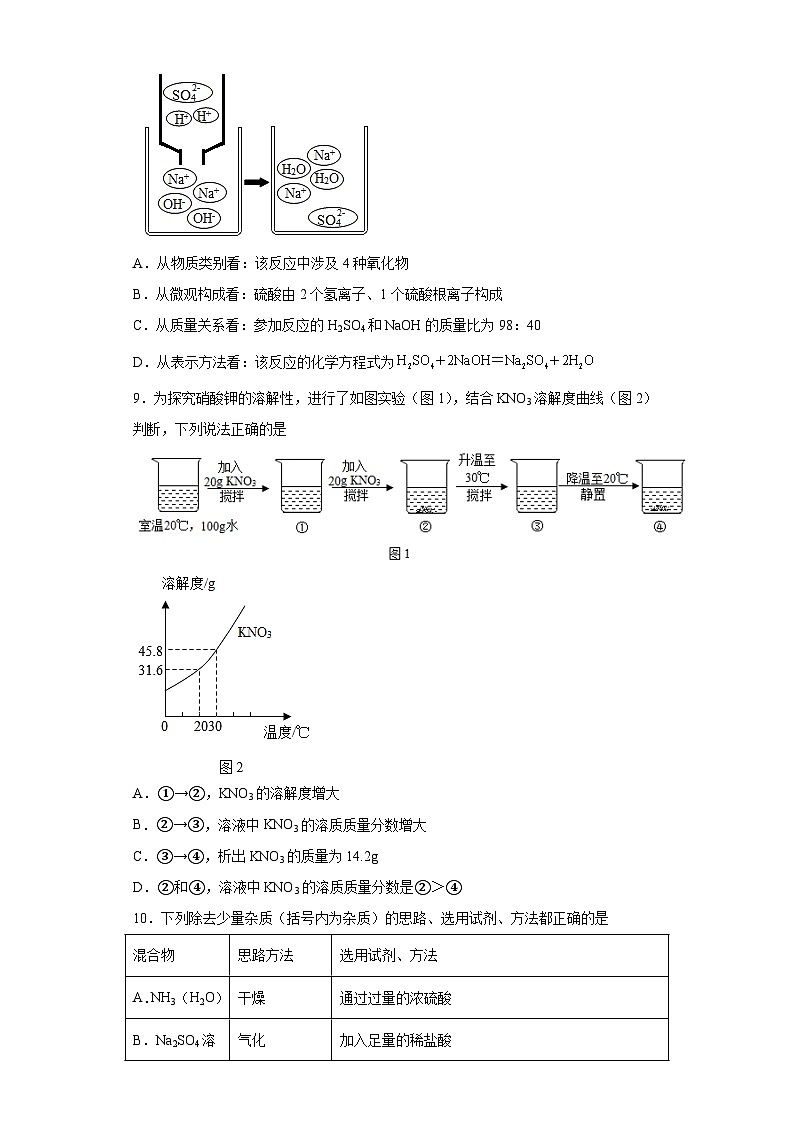
6.如图是碳酸氢钠药片说明书的部分内容。下列说法错误的是
A.碳酸氢钠俗称小苏打,属于盐类 B.该药片可用于治疗胃酸过多症
C.硬脂酸镁中含有四种非金属元素 D.淀粉和蔗糖都属于有机物
7.下表中相关叙述、对应的化学方程式和所属的基本反应类型都正确的一组是
选项 | 叙述 | 化学反应方程式 | 反应类型 |
A | 形成酸雨的反应 | 化合反应 | |
B | “白+黑”两种固体混合加热制取氧气的反应 | 分解反应 | |
C | 铜和稀硫酸反应制备硫酸铜 | 置换反应 | |
D | 服用含氢氧化钠的药物治疗胃酸过多 | NaOH+HCl=NaCl+H2O | 复分解反应 |
A.A B.B C.C D.D
8.如图是稀硫酸和氢氧化钠溶液发生反应的微观示意图,下列说法正确的是
A.从物质类别看:该反应中涉及4种氧化物
B.从微观构成看:硫酸由2个氢离子、1个硫酸根离子构成
C.从质量关系看:参加反应的H2SO4和NaOH的质量比为98:40
D.从表示方法看:该反应的化学方程式为
9.为探究硝酸钾的溶解性,进行了如图实验(图1),结合KNO3溶解度曲线(图2)判断,下列说法正确的是
A.①→②,KNO3的溶解度增大
B.②→③,溶液中KNO3的溶质质量分数增大
C.③→④,析出KNO3的质量为14.2g
D.②和④,溶液中KNO3的溶质质量分数是②>④
10.下列除去少量杂质(括号内为杂质)的思路、选用试剂、方法都正确的是
混合物 | 思路方法 | 选用试剂、方法 |
A.NH3(H2O) | 干燥 | 通过过量的浓硫酸 |
B.Na2SO4溶液(Na2CO3) | 气化 | 加入足量的稀盐酸 |
C.CaCl2溶液(HCl) | 转化、过滤 | 加入过量CaO后过滤 |
D.NaCl溶液(MgCl2) | 沉淀、过滤、转化 | 加入过量的NaOH溶液,过滤,向滤液中加适量的稀盐酸,调至pH=7 |
A.A B.B C.C D.D
11.下列实验设计能到达相应实验目的的是
选项 | A | B | C | D |
实验 设计 | ||||
实验 目的 | 探究质量守恒定律 | 探究空气是铁生锈的必要条件 | 探究同种物质在不同溶剂中的溶解能力 | 探究CO2与NaOH溶液能否发生反应 |
A.A B.B C.C D.D
12.向盛有等质量等浓度稀盐酸的四个烧杯中,分别逐渐加入金属锌、Fe2O3粉末、Ca(OH)2粉末、Na2CO3粉末至过量。下列四个实验对应的变化关系图像中,正确的是
实验 | 实验1 | 实验2 | 实验3 | 实验4 |
对应变化关系 | ||||
选项 | A | B | C | D |
A.A B.B C.C D.D
13.结构化总结可大大提高学习效率。有很多不同类别的物质之间反应都能生成盐(其他生成物省略),如图所示。下列有关说法错误的是
A.若盐是硫酸钾,则①中的反应物应为KOH和H2SO4
B.图中⑤处应补充的文字一定是:金属氧化物+酸
C.若盐是氯化亚铁,则在已显示的变化中可以通过④、⑥的置换反应来实现
D.若盐是硝酸铜,由⑦来实现的化学方程式可能是:
14.CO、H2还原Fe2O3的过程相似,大致分为三个阶段。向4.8gFe2O3中不断通入H2,不断加热,实验测得固体残留率(固体残留率=×100%)随温度的变化曲线如图所示。下列叙述错误的是
A.d点对应固体为Fe,其质量为3.36g
B.从a到d点,固体中的含氧量逐渐变小
C.从a到d点,固体减少的质量等于生成的水的质量
D.bc段发生反应的方程式为Fe3O4+H23FeO+H2O
二、填空题
15.在金属材料中,铝是目前最经济实用的材料之一。
(1)铝具有很好的抗腐蚀性,原因是_______。铝原子的结构示意图为_______;位于元素周期表第______周期。
(2)由铝制成的铝箔厚度仅为0.01mm,广泛用于食品包装等,铝能制成铝箔,主要利用铝的______性。将铝箔在酒精灯上加热,发现铝箔逐渐变软,中间有液体被外面的固体包裹住。由此可以推测氧化铝的熔点比金属铝_______(填“高”或“低”)。
(3)将铝片和稀盐酸放在密闭容器中,用传感器探究反应容器内的温度随时间变化如下图,50s时溶液中的溶质为_______(填化学式);50s后温度升高的主要原因是_______。
16.第31届“世界大学生夏季运动会”将于2023年7月28日在成都开幕。
(1)大运会的火炬“蓉火”使用丙烷(C3H8)作燃料,C3H8完全燃烧的化学方程式为_____。
(2)成都制造的碲化镉发电玻璃将成为绿色和科技办大运的创新点。元素周期表中镉、碲的相关信息如上图。镉的相对原子质量为______。碲有多种氧化物,Te2O5中碲元素的化合价为_______。
(3)碲化镉(CdTe)可由H2Te溶液和CdSO4溶液通过复分解反应制得,其化学方程式为_______。当太阳光照射到碲化镉发电玻璃后,会在光电薄膜层中产生电子运动,从而完成发电,实现______转化为电能。
三、计算题
17.硫氧粉(Na2SO3)可用作漂染脱氧剂,常因氧化变质生成Na2SO4。向20g可能已被氧化的样品中,加入质量分数为10%的稀硫酸至恰好不再产生气泡为止(假设气体全部逸出),共消耗稀硫酸98g。已知:
(1)根据化学式判断Na2SO4和Na2SO3中钠元素的质量分数较小的是______。
(2)若用5g质量分数为98%的浓硫酸配制10%的稀硫酸,所需加水______g。稀释浓硫酸时,一定要把_______,并不断搅拌。
(3)利用化学方程式计算,20g样品中含有Na2SO3的质量是多少?(写出计算过程)
(4)20g样品中Na2SO3的质量分数为______%。
四、流程题
18.若一个区域在一定时间范围内,通过各种方式消减的CO2与排放的CO2等量,就称这个区域实现了“碳中和”。我国已向世界承诺在2060年实现“碳中和”。某工厂为实现本厂“碳中和”目标,设计了一种“捕捉”CO2的减排方案,流程如下:
(1)“捕捉室”中发生反应的化学方程式为______。
(2)在“转化、沉淀室”发生的反应中,属于复分解反应的化学方程式为______。
(3)“操作a”的名称是______;在“循环Ⅱ”中循环的物质是______。将“储存室”中的产品降温固化,所得固体可用于______(回答一条)。
(4)工厂要实施这一流程,还需设计向“固体热解室”零排放供热的配套方案。下列方案中可以选用的是______(填编号)。
A.燃煤供热 B.燃油供热 C.聚集太阳能供热 D.电供热
(5)实验室用澄清石灰水检验CO2也是“捕捉”CO2的过程。工厂却不宜采用澄清石灰水“捕捉”CO2的减排方案,原因______。
五、实验题
19.下图是实验室常用的气体发生装置和收集装置,请回答下列问题:
发生装置 | 收集装置 |
(1)某同学欲用高锰酸钾制取并收集O2进行铁丝燃烧实验,要在集气瓶内预留一些水的作用是______。他应选用_____装置组合(填字母序号)进行制取,该反应的化学方程式为_______。
(2)D图中①仪器的用途是_______;D装置与C装置比较,具有的优点是_______。
(3)下图甲中的活塞k处于关闭状态,据图判断装置甲______(填“漏气”或“不漏气”)。甲中长颈漏斗下端管口应处于塑料板之下的理由是________。
(4)用上图乙制取氢气,使反应发生的操作方法是_______;反应的化学方程式为_______。若选择H装置收集氢气,则应从导管_______(填“a”或“b”)端通入。
六、科学探究题
20.打开碳酸饮料瓶盖时,会有大量含有二氧化碳气体的气泡逸出。某项目学习小组对二氧化碳溶解能力进行了如下实验探究。
【查阅资料】通常状况下,1体积水约能溶解1体积二氧化碳,所得饱和溶液pH约为5.6。
I.探究通常状况下,二氧化碳在水中溶解的体积
实验1:
(1)如图1,进行实验前需先将甲装置中的空气排尽,其操作是:打开弹簧夹K1,关闭其余弹簧夹;打开活塞,滴加稀盐酸至空气排尽。甲中发生反应的化学方程式为______;检验甲中空气已排尽的方法是________。
(2)关闭K1,打开K2,K3。待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH计测得如下数据:
物质 | 丁装置中溶液 | 丙装置中溶液 |
pH | 6.50 | 5.60 |
分析可知,在丙和丁装置中所溶解二氧化碳的体积_________(填“大于”“小于”“等于”)丙和丁装置中溶液的总体积。
(3)实验1说明,通常状况下,在生成较大量二氧化碳时,可以用______收集二氧化碳气体。
II.比较二氧化碳在不同物质中的溶解能力
实验2:
四个烧瓶中收集250mL的气体,分别加入50mL不同液体,通过压强传感器测定瓶中压强变化(实验前烧瓶内压强为104.20kPa,实验过程中保持温度恒定)。
实验操作 | 实验序号 | 烧瓶中气体 | 注射器中物质 | 实验后瓶内压强 |
实验① | 空气 | 水 | 130.25kPa | |
实验② | CO2 | 水 | 104.98kPa | |
实验③ | CO2 | 盐酸 | 106.67kPa | |
实验④ | CO2 | 小苏打的水溶液 | 103.40kPa |
【解释与结论】
(4)实验①的作用是______。实验后瓶内的压强,实验②小于实验①的原因是_______。
(5)比较实验②、③、④的数据,可得出CO2在三种液体中溶解能力的关系是________。
III.探究实验的废液处理
项目小组完成探究实验后,产生大量废液。经理论分析和实验确定废液中含NaCl、CaCl2和HCl。小组决定用Na2CO3除去废液中CaCl2和HCl后再利用,如何估算Na2CO3固体的用量?
实验3:
取100mL废液样品于烧杯中,逐滴滴加5.3%的Na2CO3溶液,用pH传感器测定滴加过程中溶液的pH。实验结果如20—图2所示。
【讨论与交流】
(6)a→b阶段,观察到烧杯中的现象是______。
(7)b点后曲线平缓阶段,对应的化学方程式为______。
(8)c点时,取少量烧杯中的清液于试管中,滴加CaCl2溶液,有白色沉淀生成,说明处理100mL废液,所需5.3%的Na2CO3溶液的体积______120mL(填“大于”、“等于”或“小于”)。
(9)将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g。那么,处理项目组800mL的废液,理论上需要Na2CO3固体______g。(实验所用5.3%Na2CO3溶液的密度近似看做1g/mL)
参考答案:
1.B
2.A
3.C
4.C
5.D
6.C
7.B
8.D
9.B
10.D
11.D
12.A
13.B
14.C
15.(1) 铝在空气中与氧气反应生成一层致密的氧化铝薄膜,阻止铝进一步氧化 三/3
(2) 延展 高
(3) AlCl3、HCl Al与稀盐酸反应放热,使容器内温度升高
16.(1)
(2) 112.4 +5
(3) 太阳能
17.(1)硫酸钠/Na2SO4
(2) 44 浓硫酸沿容器壁缓慢注入水中
(3)解:设20g样品中Na2SO3的质量为x
解得x=12.6g
答:20g样品中Na2SO3的质量为12.6g。
(4)63
18.(1)
(2)
(3) 过滤 CaO 制冷(或人工降雨等)
(4)CD
(5)澄清石灰水浓度太小,“捕捉”效率低
19.(1) 防止高温熔融物溅落下来,炸裂瓶底(其他合理答案均可) AE/EA
(2) 便于添加液体药品 可随时控制反应的发生和停止(其他合理答案均可)
(3) 不漏气 形成液封,避免生成的气体从长颈漏斗口逸出(其他合理答案均可)
(4) 倾斜试管,使固液接触(或“添加稀硫酸”或“加水”或“加密度大于稀硫酸且不溶于水的液体:如四氯化碳”)(其他合理答案均可) b
20.(1) 在K1左侧的导管口,用燃着的木条检验,木条立即熄灭,证明空气已排尽(其他合理答案均可)
(2)小于
(3)排水法
(4) 作为空白实验,与其他三组实验作对比(其他合理答案均可) 因为CO2溶于水且与水发生反应,气体减少,使瓶内压强明显降低。(其他合理答案均可)
(5)其他条件相同时,CO2在盐酸、水、小苏打的水溶液中溶解能力依次增大(其他合理答案均可)(或其他条件相同时,CO2在小苏打的水溶液、水、盐酸中溶解性依次减小)
(6)产生大量气泡
(7)
(8)小于
(9)33.92
2023年四川省成都市青羊区中考二模化学试题: 这是一份2023年四川省成都市青羊区中考二模化学试题,共11页。
2023年四川省成都市高新区中考二模化学试题(含答案): 这是一份2023年四川省成都市高新区中考二模化学试题(含答案),共9页。试卷主要包含了 本试卷分为第Ⅰ卷第Ⅱ卷两部分, 可能用到的相对原子质量, 下列实验操作正确的是, 化学与生活息息相关等内容,欢迎下载使用。
2023年四川省成都市锦江区嘉祥外国语学校中考化学模拟试题(含答案): 这是一份2023年四川省成都市锦江区嘉祥外国语学校中考化学模拟试题(含答案),共10页。试卷主要包含了62g,75等内容,欢迎下载使用。