










2024年高考化学一轮复习(新高考版) 第8章 热点强化18 多平衡体系平衡常数的计算
展开热点强化18 多平衡体系平衡常数的计算
类型一 连续反应
连续平衡是指有关的两个可逆反应有着关联,第一个反应的某一生成物,是第二个反应的反应物。解题时要注意如果该物质是第一个反应的生成物,第二个反应的反应物;则在第一个反应中,该物质的初始量为0,它的平衡量则为第二个反应中该物质的初始量(在计算第二个反应的转化率尤为重要)。
例1 [2021·辽宁,17(6)]苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
Ⅰ.主反应: (g)+3H2(g) (g) ΔH1<0
Ⅱ.副反应: (g)(g) ΔH2>0
回答下列问题:
恒压反应器中,按照n(H2)∶n(C6H6)=4∶1投料,发生Ⅰ、Ⅱ反应,总压为p0,平衡时苯的转化率为α,环己烷的分压为p,则反应Ⅰ的Kp=________(列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
答案
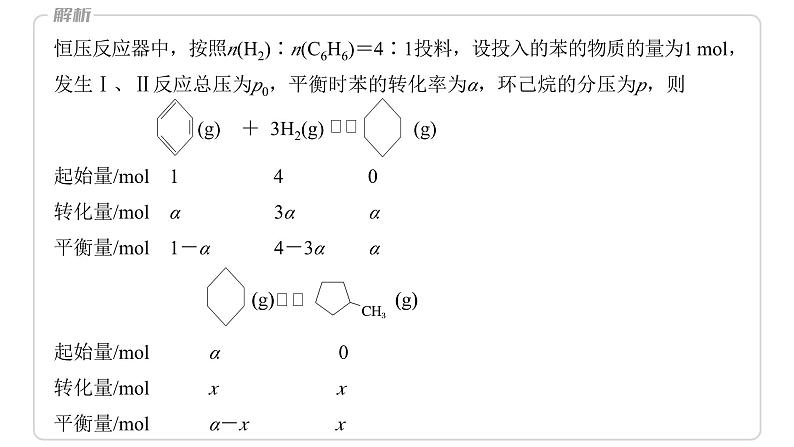
解析 恒压反应器中,按照n(H2)∶n(C6H6)=4∶1投料,设投入的苯的物质的量为1 mol,发生Ⅰ、Ⅱ反应总压为p0,平衡时苯的转化率为α,环己烷的分压为p,则
(g) + 3H2(g) (g)
起始量/mol 1 4 0
转化量/mol α 3α α
平衡量/mol 1-α 4-3α α
(g)(g)
起始量/mol α 0
转化量/mol x x
平衡量/mol α-x x
反应后平衡体系中总的物质的量为1-α+4-3α+α-x+x=5-3α,故平衡时,苯的分压为p0,H2的分压为p0,则反应Ⅰ的Kp==。
例2 二甲醚是一种清洁能源,用水煤气制取二甲醚的原理如下:
Ⅰ.CO(g)+2H2(g)CH3OH(g)
Ⅱ.2CH3OH(g)CH3OCH3(g)+H2O(g)
500 K时,在2 L密闭容器中充入4 mol CO和8 mol H2,4 min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3),则:
(1)0~4 min,反应Ⅰ的v(H2)=________。
(2)反应Ⅱ中CH3OH的转化率α=________,反应 Ⅰ的平衡常数K=________。
思路引导 利用C、H、O原子守恒计算平衡时各物质的物质的量,再求各物质的平衡浓度,代入平衡常数表达式计算。
答案 (1)0.8 mol·L-1·min-1 (2)80% 1.25
解析 (1)设平衡时CO为x mol,H2为y mol,CH3OH为z mol,则CH3OCH3为2z mol,H2O为2z mol,根据:
C守恒:x+z+2×2z=4
H守恒:2y+4z+6×2z+2×2z=2×8
O守恒:x+z+2z+2z=4
CO的转化率为=80%,解得x=0.8,y=1.6,z=0.64,v(H2)==0.8 mol·L-1·min-1。(2)反应Ⅰ中CO的转化率为80%,则生成的CH3OH的物质的量为4 mol×80%=3.2 mol,反应Ⅱ生成的CH3OCH3的物质的量为2z mol即2×0.64 mol=1.28 mol,则反应Ⅱ转化的CH3OH的物质的量为2×1.28 mol=2.56 mol,则反应Ⅱ中CH3OH的转化率α=×100%=80%。根据之前所解方程,可得平衡时:CH3OH、H2、CO的浓度分别为0.32 mol·L-1、0.8 mol·L-1、0.4 mol·L-1,反应Ⅰ的平衡常数K==1.25。
类型二 竞争反应(平行反应)
平行反应是指反应物能同时平行地进行两个或两个以上的不同反应,得出不同的产物。其中反应较快或产物在混合物中所占比率较高的称为主反应,其余称为副反应。解题时要注意如果一个物质是两个平行反应的反应物,则题目中所给初始量则是该物质在这两个反应中的初始量之和。
例3 2021年8月,我国第一套利用中国石油自主研发的乙烷裂解制乙烯技术建成的大型乙烯生产装置成功投料开车。其反应原理为①C2H6(g)C2H4(g)+H2(g),副反应为②2C2H6(g)C2H4(g)+2CH4(g)。
250 ℃时,在容积为1 L的密闭容器中,充入2 mol C2H6(g),发生反应①和②。反应达到平衡时,C2H6(g)的转化率为50%,H2的选择性(生成的H2占生成的CH4和H2总量的百分比)为80%,则该温度下反应②的平衡常数为________。
答案 0.036
解析 C2H6(g)的起始浓度为2 mol·L-1,设生成H2(g) x mol·L-1,生成CH4(g) y mol·L-1,反应①达平衡后再发生反应②,列三段式:
C2H6(g)C2H4(g)+H2(g)
起始浓度/(mol·L-1) 2 0 0
转化浓度/(mol·L-1) x x x
平衡浓度/(mol·L-1) 2-x x x
2C2H6(g)C2H4(g)+2CH4(g)
起始浓度/mol·L-1 2-x x 0
转化浓度/mol·L-1 y 0.5y y
平衡浓度/mol·L-1 2-x-y x+0.5y y
达到平衡时C2H6(g)的转化率为50%,则x+y=2×50%=1,H2(g)的选择性为80%,则×100%=80%,解得x=0.8,y=0.2,则该温度下,副反应的平衡常数K===0.036。
1.加热N2O5时,发生以下两个分解反应:①N2O5N2O3+O2,②N2O3N2O+O2,在2 L密闭容器中充入8 mol N2O5,加热到T ℃达到化学平衡时O2为9 mol,N2O3为3.4 mol,则在该温度下反应①的平衡常数为( )
A.8.5 B.9.6 C.10.2 D.10.7
答案 A
解析 假设①N2O5N2O3+O2生成N2O3的物质的量为x mol,②N2O3N2O+O2中消耗N2O3的物质的量为y mol,则有x-y=3.4,x+y=9,解得x=6.2,y=2.8。则反应达到平衡时,N2O5的物质的量为8 mol-6.2 mol=1.8 mol,该温度下反应①的平衡常数为=8.5,故选A。
2.[2020·山东,18(2)]探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)CH3OH(g)+H2O(g)
ΔH1=-49.5 kJ·mol-1
Ⅱ.CO(g)+2H2(g)CH3OH(g)
ΔH2=-90.4 kJ·mol-1
Ⅲ.CO2(g)+H2(g)CO(g)+H2O(g) ΔH3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为_______ mol·L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为__________。
答案
解析 由题给反应的化学方程式可知,对于反应Ⅰ,每生成1 mol甲醇的同时生成1 mol水;对于反应Ⅲ,每生成1 mol一氧化碳的同时生成1 mol水;对于反应Ⅱ,每消耗1 mol一氧化碳的同时生成1 mol甲醇;由此可知,生成的水的物质的量等于生成的甲醇和一氧化碳的物质的量之和,即生成水的物质的量为(a+b) mol,即水的浓度为 mol·L-1。由C原子个数守恒可知,平衡时混合气体中CO2的物质的量为(1-a-b) mol,由H原子个数守恒可知,平衡时混合气体中H2的物质的量为[3-2a-(a+b)] mol,因此平衡常数K=。
3.[2019·天津,7(5)]在1 L真空密闭容器中加入a mol PH4I固体,t ℃时发生如下反应:
PH4I(s)PH3(g)+HI(g) ①
4PH3(g)P4(g)+6H2(g) ②
2HI(g)H2(g)+I2(g) ③
达平衡时,体系中n(HI)=b mol,n(I2)=c mol,n(H2)=d mol,则t ℃时反应①的平衡常数K值为________(用字母表示)。
答案 (b+)b
解析 反应①生成的n(HI)=体系中n(HI)+2×体系中n(I2)=(b+2c) mol,反应②中生成的n(H2)=体系中n(H2)-反应③中生成的n(H2)=(d-c) mol,体系中n(PH3)=反应①生成的n(PH3)-反应②中转化的n(PH3)=[b+2c-(d-c)] mol=(b+) mol,反应①的平衡常数K=c(PH3)·c(HI)=(b+)b。
(1)有关多平衡体系平衡常数的计算,如何确定多个反应相关联物质在平衡时量的多少是解题的关键点。若用常规的三段式计算,对反应过程分析要求高,容易出错。但无论多少个反应,反应进行的程度如何,反应前后的原子总数是不变的,因而解答这类问题可用原子守恒法,可规避对反应过程的分析。
(2)原子守恒法解题基本思路:
2024年高考化学一轮复习课件(鲁科版)第8章 热点强化23 有关水溶液中平衡常数关系计算: 这是一份2024年高考化学一轮复习课件(鲁科版)第8章 热点强化23 有关水溶液中平衡常数关系计算,文件包含第8章热点强化23有关水溶液中平衡常数关系计算pptx、第8章热点强化23有关水溶液中平衡常数关系计算docx等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
高考化学一轮复习课件18.化学平衡状态和化学平衡常数(含解析): 这是一份高考化学一轮复习课件18.化学平衡状态和化学平衡常数(含解析),共27页。PPT课件主要包含了化学平衡,可逆反应,同一条件,随堂练习,不再改变,正反应,逆反应,动态平衡,Ⅰ直接标志,逆反应方向必须对立等内容,欢迎下载使用。
2024年高考化学一轮复习(新高考版) 第9章 热点强化23 有关水溶液中平衡常数关系计算: 这是一份2024年高考化学一轮复习(新高考版) 第9章 热点强化23 有关水溶液中平衡常数关系计算,文件包含2024年高考化学一轮复习新高考版第9章热点强化23有关水溶液中平衡常数关系计算pptx、2024年高考化学一轮复习新高考版第9章热点强化23有关水溶液中平衡常数关系计算docx、第9章热点强化23有关水溶液中平衡常数关系计算docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。












